 去看看
去看看


流行病学
葡萄膜黑色素瘤(uveal melanoma,UM)是成人最常见的原发性眼内恶性肿瘤。UM可起源于眼球壁的中层葡萄膜(虹膜、睫状体和脉络膜)但其中超过90%的是脉络膜肿瘤[1]。尽管从构成比看眼部黑色素瘤仅占全部黑色素瘤的5%,但它是继皮肤黑色素瘤之后的第二大常见的黑色素瘤[2]。
文献报道UM的发病率为4.3/100万~10.9/100万。美国国立卫生研究所(NIH)所属SEER指出:UM总体平均发病率为4.3/100万,男性(4.9/100万)高于女性(3.7/100万)[3]。据Kivela估计[4] ,全世界每年有6679~7095例UM新发病例。UM更多地发生于浅肤色的人群中。有研究报道UM发病率分别为(每百万人):黑种人为0.31,亚洲人为0.38,西班牙人为1.67,非西班牙白种人为6.02[5]。UM在中国人中的发病率目前尚无统计数据。
生物学行为特点
UM与皮肤黑色素瘤在临床特征和生物学行为方面迥然不同[6]。例如,UM主要经血行转移,不同于皮肤黑色素瘤普遍经淋巴管转移。大约一半的UM患者最终发生血行转移,肝脏转移最为常见。发生转移的患者如不治疗大多在短期内(6~8个月)死亡[7]。COMS(眼黑色素瘤协作研究:由北美43个临床眼科中心参与的一项多中心研究)的大样本数据显示:确诊为转移的UM患者中位生存期仅为3.6个月,5年累计生存率仅为1%[8]。
UM较多见的细胞遗传学异常表现为部分染色体缺失或获得,如3号染色体单体缺失,8号染色体获得等[9,10],UM典型的分子异常是GNAQ/11突变[11-13],但很少有BRAF和NRAS突变,而皮肤黑色素瘤中最为突出的分子异常是BRAF、CKIT和NRAS突变[14,15]。
诊断与分期
综合运用间接眼底镜、超声、MRI可以对UM做出准确率较高的临床诊断。COMS报道UM临床诊断的准确率高于99%[16]。COMS根据肿瘤的最大基底直径和高度将UM分为小型、中型和大型(图1)[17,18]。
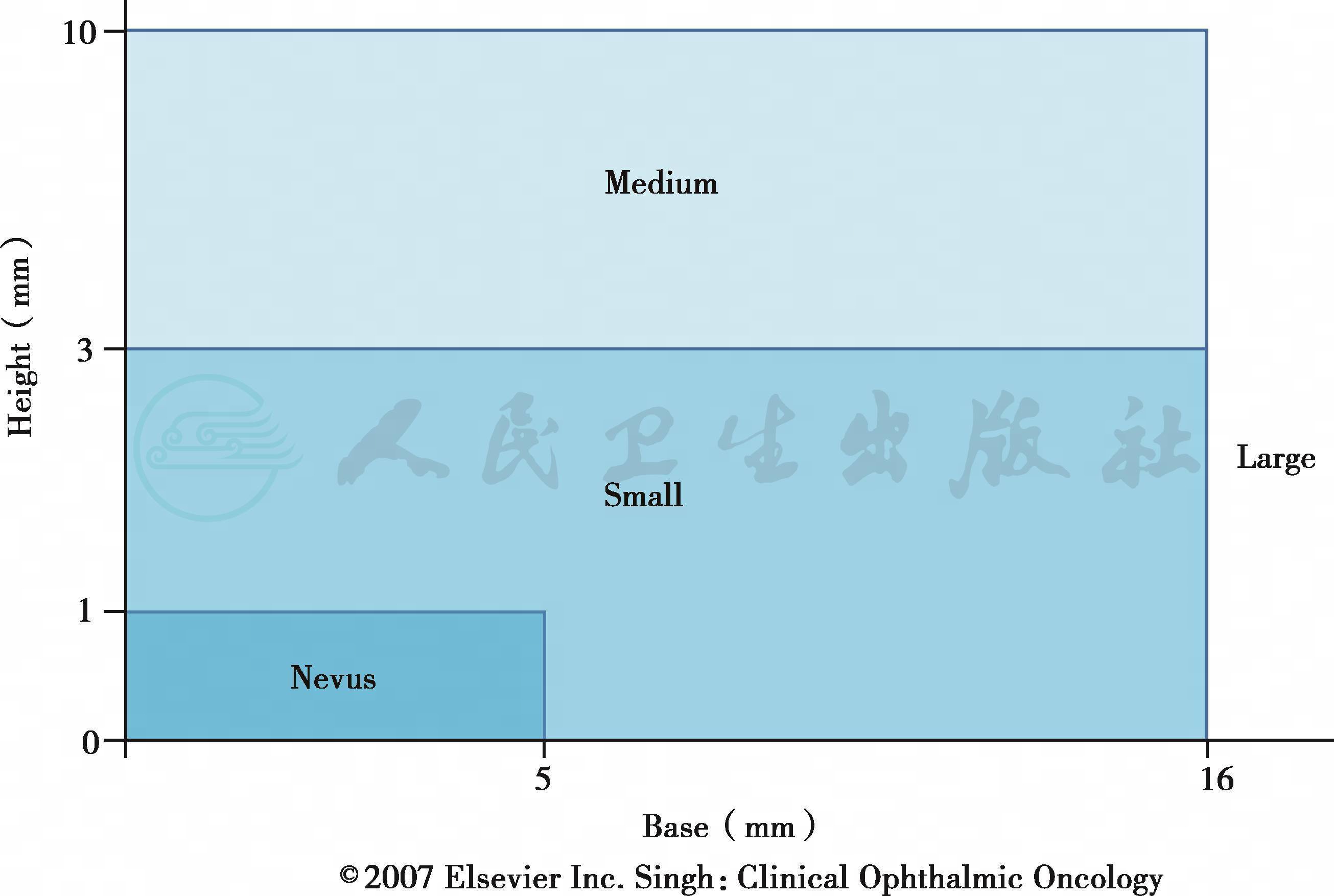
图1 COMS的UM分类标准[18]
1990年12月,中型肿瘤高度标准由3mm降为2.5mm
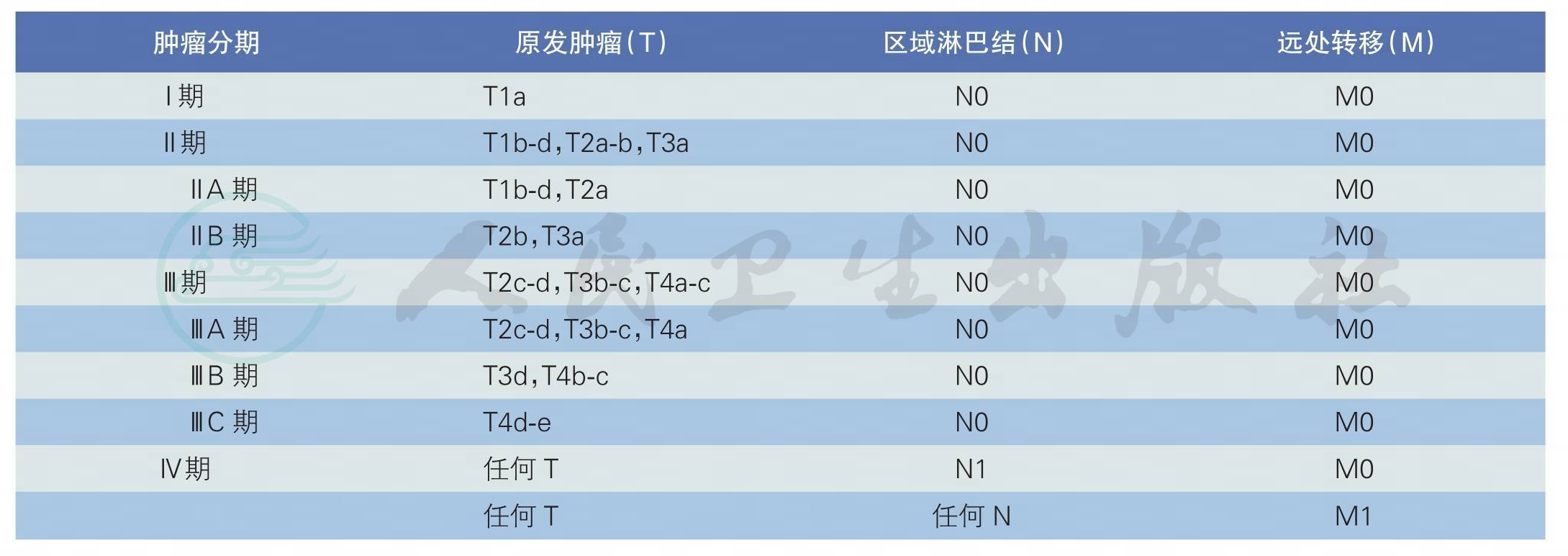
AJCC(第7版)后部UM的分期详见表1和表2。以AJCCⅠ期UM为基准,Ⅱ期患者转移/死亡率是Ⅰ期的3倍,Ⅲ期是Ⅰ期的9~10倍,Ⅳ期更甚[19-21]。
表1 AJCC(第7版)后部葡萄膜黑色素瘤原发肿瘤大小分类[19]
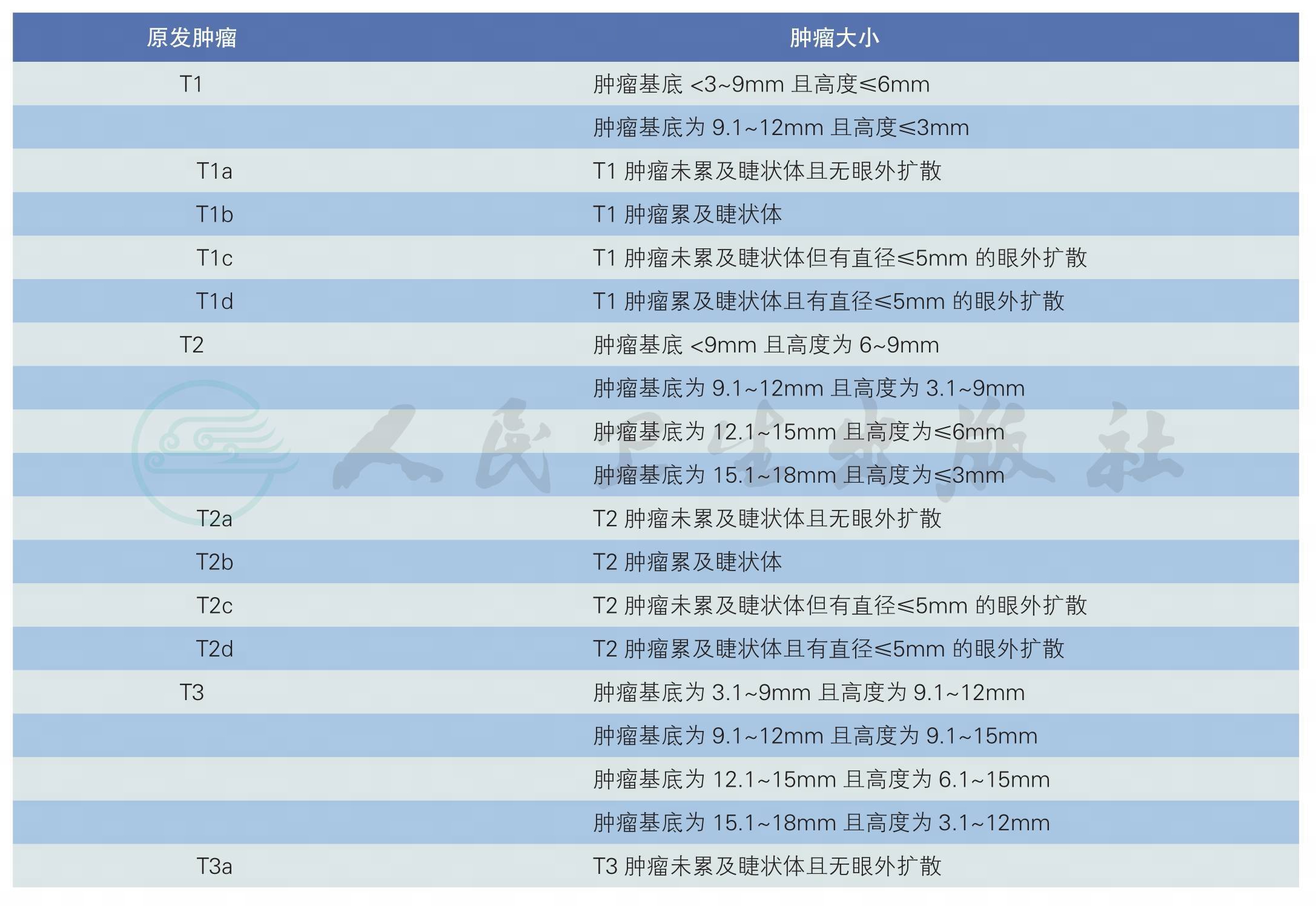
续表
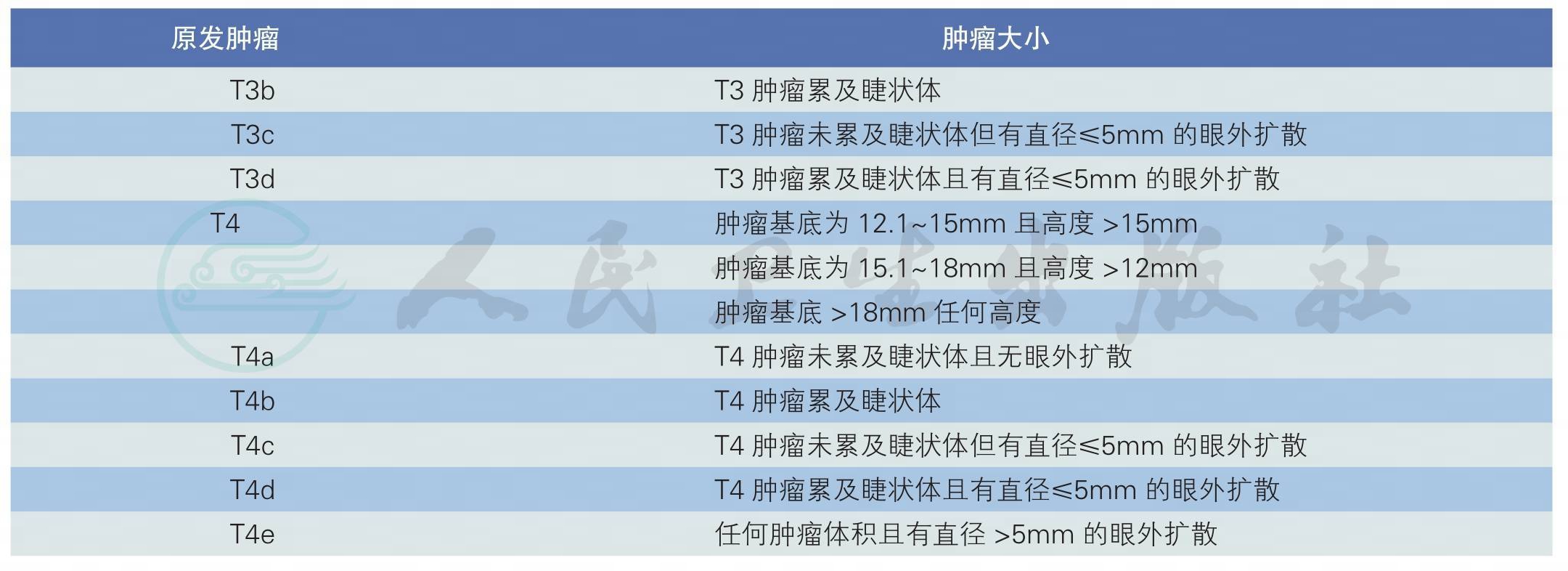
表2 AJCC(第7版)后部葡萄膜黑色素瘤分期[19]
预后指标
在UM肿瘤组织中检测单体型染色体3和通过基因表达谱(GEP)对肿瘤分型,已经成为国际上较为公认的评价UM预后的方法。
细胞遗传学检测:50%的具有单倍体型染色体3的患者将会在3年内死亡。具有二倍体型染色体3的患者如果伴有染色体8q扩增则预后会很差[9,10]。
分子遗传学检测:GEP分析可以辨别出两类在转移潜能方面显著不同的肿瘤。1类细胞很少发生转移(<5%),2类细胞却有超过90%的转移风险[22-24]。
对于具有高转移风险的患者,需要进行密切的全身查体,以期早期发现微小的转移灶,争取局部切除的机会,甚或可以加入新药的临床试验。对于具有低转移风险的患者,则无需过度频繁体检,从而可以提高患者的生活质量。
治疗
1. 眼局部治疗
COMS研究结果表明:中型UM患者随机接受敷贴放射治疗或眼球摘除,其生存率并没有显著不同,非校正5年生存率分别为81%和82%,并且经组织病理学证实分别有11%和9%的黑色素瘤发生转移[25]。该研究奠定了UM眼局部治疗的重要依据。据此可根据肿瘤大小及部位来选择治疗方法,在不影响生存率的前提下尽量保存眼球甚或有用视力。
(1) 巩膜表面敷贴器放射治疗
国外大多数眼科中心的首选疗法,这属于一种近距离放疗,具体方法是在局部巩膜表面放置一个含125I或106Ru放射性粒子的金属盘。建议小型和中型肿瘤采用敷贴放射治疗。
(2) 眼球摘除
肿瘤局限于眼球内时可考虑采用。建议大型肿瘤、疼痛无视力的或无光感的眼球采用眼球摘除。
(3) 眶内容剜除术
适宜于较大范围的肿瘤穿出眼球扩散至眼眶的病例。
(4) 其他治疗
包括质子束放疗、立体定向放疗、肿瘤局部切除术等。
2. 全身治疗
目前尚无大型随机对照临床研究结果能够证实可以延长转移性UM的总生存期。化学治疗、肝动脉化疗栓塞、免疫治疗、免疫靶向治疗、个体化分子靶向治疗已经对发生转移的UM进行了尝试,但大多数报道为非随机无对照的小样本研究或Ⅰ、Ⅱ期临床试验[26,27]。发生转移的UM患者亟需新的更为有效的治疗方法。入组临床试验是目前治疗转移性UM的首选。
(1) MEK抑制剂
基于UM中较为普遍的GNAQ/11突变以及其直接导致的MAPK通路激活,MEK抑制剂治疗UM被认为很有希望并引起广泛关注。2014年Carvajal等报道一项随机、开放的多中心(美国和加拿大共15个临床肿瘤中心)Ⅱ期临床试验在120例转移的UM患者中比较了Selumetinib(司美替尼)与Dacarbazine(达卡巴嗪)的治疗效果。结果显示:中位PFS在Dacarbazine组为7周,在Selumetinib组为15.9周。中位OS在Dacarbazine组为9.1个月,在Selumetinib组为11.8个月。Dacarbazine组无客观反应,Selumetinib组客观反应率为49%。结论是:Selumetinib与Dacarbazine相比,在提高PFS和反应率方面有一定的作用,但并没有提高OS[28]。进一步评价Selumetinib联合Dacarbazine治疗转移UM的多中心、随机、双盲Ⅲ期临床试验正在进行中[29]。
(2) Ipilimumab
2015年DeCOG报道的多中心Ⅱ期临床试验中,转移UM患者以3mg/kg剂量服用4周期Ipilimumab后,中位OS为6.8个月 (95% CI:3.7~8.1),中位PFS为2.8 个月 (95% CI:2.5~2.9)。结论是:Ipilimumab对于转移UM的临床疗效非常有限[30]。
(3) PD-1
目前临床试验尚在进行中,结果值得期待。
1. Egan KM,Seddon JM,Glynn RJ,et al. Epidemiologic aspects of uveal melanoma. Surv Ophthalmol,1998,32(4):239-251.
2. Singh AD,Topham A. Incidence of uveal melanoma in the United States:1973-1997. Ophthalmology,2003,110(5):956-961.
3. Reis L,Eisner MP,Kosary CL,et al. SEER Cancer Statistics Review. 1973-2000. Bethesda,MD:National Cancer Institute,2003.
4. KivelT. The epidemiological challenge of the most frequent eye cancer:retinoblastoma,an issue of birth and death. Br J Ophthalmol.,2009,93(9):1129-1131.
5. Hu DN,Yu GP,McCormick SA,et al. Population-based incidence of uveal melanoma in various races and ethnic groups. Am J Ophthalmol,2005,140(4):612-617.
6. Hurst EA,Harbour JW,Cornelius LA. Ocular melanoma:a review and the relationship to cutaneous melanoma. Arch Dermatol,2003,139(8):1067-1073.
7. Rietschel P,Panageas KS,Hanlon C,et al. Variates of survival in metastatic uveal melanoma. J Clin Oncol. 2005,23(31):8076-8080.
8. Diener-West M,Reynolds SM,Agugliaro DJ,et al. Development of metastatic disease after enrollment in the COMS trials for treatment of choroidal melanoma:Collaborative Ocular Melanoma Study Group Report No. 26. Arch Ophthalmol,2005,123(12):1639-1643.
9. Prescher G,Bornfeld N,Hirche H,et al. Prognostic implications of monosomy 3 in uveal melanoma. Lancet. 1996,347(9010):1222-1225.
10. Lake SL,Coupland SE,Taktak AF,et al. Whole-genome microarray detects deletions and loss of heterozygosity of chromosome 3 occurring exclusively in metastasizing uveal melanoma. Invest Ophthalmol Vis Sci,2010,51(10):4884-4891.
11. Van Raamsdonk CD,Bezrookove V,Green G,et al. Frequent somatic mutations of GNAQ in uvealmelanoma and blue naevi. Nature,2009,457(7229):599-602.
12. Van Raamsdonk CD,Griewank KG,Crosby MB,et al. Mutations in GNA11 in uveal melanoma. N Engl J Med,2010,363(23):2191-2199.
13. Xu X,Wei W,Xu X,et al. Oncogenic GNAQ and GNA11 mutations in uveal melanoma in Chinese. PLoS One,2014,9(10):e109699.
14. Brose MS,Volpe P,Feldman M,et al. BRAF and RAS mutations in human lung cancer and melanoma. Cancer Res,2002,62(23):6997-7000.
15. Pollock PM,Meltzer PS. A genome-based strategy uncovers frequent BRAF mutations in melanoma. Cancer Cell,2002,2(1):5-7.
16. Group COMS. Histopathologic characteristics of uveal melanomas in eyes enucleated from the Collaborative Ocular Melanoma Study. COMS report no. 6. Am J Ophthalmol,1999,125(6):745-766.
17. Group COMS. COMS Manual of Procedures:accession no. PBS 179 693. Springfield,VA:National Technical Information Service,1995.
18. Uveal malignant melanoma:COMS results//singh AD,Damato BE,Pe′er J,et al. Clinical Ophthalmic Oncology. Philadelphia: Saunders Elsevier,2007:268.
19. Malignant melanoma of the uvea//Edge DB,Byrd DR,Compton CC,et al. AJCC Cancer Staging Manual. 7th ed. New York,NY:Springer,2010:547-559.
20. Shields CL,Kaliki S,Furuta M,et al. American Joint Committee on Cancer Classification of Uveal Melanoma (Anatomic Stage) Predicts Prognosis in 7731 Patients:The 2013 Zimmerman Lecture. Ophthalmology,2015,122(6):1180-1186.
21. AJCC Ophthalmic Oncology Task Force. International Validation of the American Joint Committee on Cancer’s 7th Edition Classification of Uveal Melanoma. JAMA Ophthalmol,2015,133(4):376-383.
22. Onken MD,Worley LA,Ehlers JP,et al. Gene expression profiling in uveal melanomareveals two molecular classes and predicts metastatic death. Cancer Res,2004,64(20):7205-7209.
23. Tschentscher F,Husing J,Holter T,et al. Tumor classification based on gene expression profiling shows that uveal melanomas with and without monosomy 3 represent two distinct entities. Cancer Res,2003,63(10):2578-2584.
24. Onken MD,Worley LA,Char DH,et al. Collaborative Ocular Oncology Group report number:prospective validation of a multi-gene prognostic assay in uveal melanoma. Ophthalmology,2012,119(8):1596-1603.
25. Diener-West M,Earle JD,Fine SL,et al. Collaborative Ocular Melanoma Study Group. The COMS randomized trial of iodine 125 brachytherapy for choroidal melanoma,Ⅲ:initial mortality findings. COMS Report No. 18. Arch Ophthalmol,2001,119(7):969-982.
26. Patel M,Smyth E,Chapman PB,et al. Therapeutic implications of the emerging molecular biology of uveal melanoma. Clin Cancer Res,2011,17(8),2087-2100.
27. Harbour JW,Chao DL. A molecular revolution in uveal melanoma:implications for patient care and targeted therapy. Ophthalmology,2014,121(6):1281-1288.
28. Carvajal RD,Sosman JA,Quevedo JF,et al. Effect of selumetinibvs chemotherapy on progression-free survival in uveal melanoma:a randomized clinical trial. JAMA,2014,311(23):2397-2405.
29. Carvajal RD,Schwartz GK,Mann H,et al. Study design and rationale for a randomised,placebo-controlled,double-blind study to assess the efficacy ofselumetinib (AZD6244;ARRY-142886) in combination with dacarbazine in patients with metastatic uveal melanoma (SUMIT). BMC Cancer,2015,15:467.
30. Zimmer L,Vaubel J,Mohr P,et al. Phase Ⅱ DeCOG-study of ipilimumab in pretreated and treatment-naïve patients with metastatic uveal melanoma. PLoS One,2015,10(3):e0118564.