中文别名 :弥漫性间质性肺病;间质性肺疾病
弥漫性肺疾病又称弥漫性间质性肺疾病(diffuse interstitial lung disease,DILD)、间质性肺疾病(interstitial lung disease,ILD),是一组以肺泡单位的炎症和间质纤维化为基本病变的异质性非肿瘤非感染性肺部疾病的总称。它不仅累及位于肺泡-毛细血管膜之间的肺间质,同时也累及细支气管、肺泡实质、血管、淋巴管和胸膜。其临床主要表现为活动后呼吸困难、干咳等,由于这类疾病具有相似的临床、放射影像学表现、生理或病理表现,故将这类疾病归在一起讨论。
2002年美国胸科学会((ATS)和欧洲呼吸学会(ERS)提出了简明的ILD分类框架:①已知病因:职业、环境、放射性、药物及结缔组织疾病;②肉芽肿性病:结节病和过敏性肺炎等;③未知病因:如LAM、PLCH和PAP等;④特发性间质性肺炎(idiopathic interstitial pneumonia,IIP)。
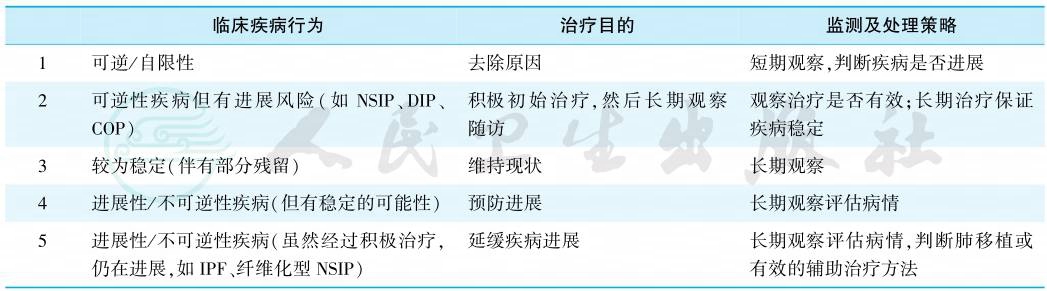
2013年ATS/ERS发布了特发性间质性肺炎国际多学科分类更新,将IIP细分为3类:①主要的IIP:包括慢性致纤维化性间质性肺炎[包括特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)和非特异性间质性肺炎(nonspecific interstitial pneumonia,NSIP)]、急性/亚急性 IIP(包括隐源性机化性肺炎和急性间质性肺炎)、吸烟相关性间质性肺炎(包括呼吸性细支气管炎并间质性肺炎和脱屑性间质性肺炎);②罕见的IIP:包括淋巴细胞性间质性肺炎和特发性胸膜肺弹力纤维增生症;③不能分类的IIP:包括急性纤维素性机化性肺炎和呼吸道中心型间质性肺炎(图1)。在此基础上,还增加了IIP疾病行为的分类及临床监测和处理策略(表1)。该分类系统提出了相应的临床诊断途径,有其独特和新颖之处,目前已被多数临床医师和研究者接受。
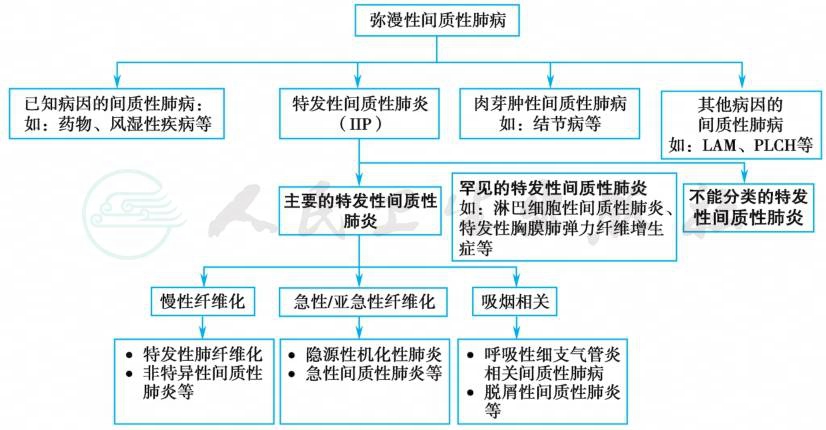
图1 ATS/ERS对弥漫性间质性肺病的分类
表1 特发性间质性肺炎(IIP)的疾病行为及处理策略
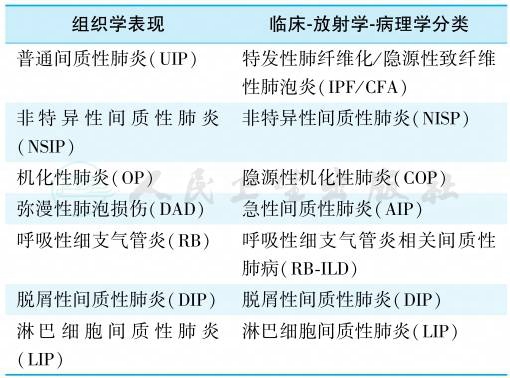
间质性肺疾病是以间质增生、炎细胞浸润为主要病理改变的一组异质性疾病,2002年ATS/ERS将特发性间质性肺炎的病理诊断升级为“临床-影像-病理诊断”(表2),进一步强调了该类疾病中的某些病例需要通过多学科讨论来共同诊断。间质性肺疾病的主要病理为:①纤维组织增生:如肺间质纤维组织增生、间质胶原化和蜂窝肺形成;②炎细胞浸润:肺泡隔和小气道周围大量炎症细胞浸润,多为淋巴细胞和浆细胞等;③肺泡腔和小气道充填各种物质,如细胞和组织成分等;④肺血管病变:小动/静脉血管壁弹力纤维的破坏,纤维素性坏死、慢性炎症细胞浸润;⑤肉芽肿性病变:病理为类上皮样组织细胞、纤维母细胞,伴/不伴多核巨细胞形成的结节。
表2 ILD组织学和临床-放射学-病理学分类对照
1.实验室检查
血常规和一般生化检查对于ILD的诊断、病情严重度及活动性判断并无重要意义。对临床怀疑存在风湿性疾病的患者,需进行相关血清学检查,如ANA、抗双链DNA抗体及抗可提取性核抗原抗体、抗合成酶抗体(如Jo-1)、肌酸激酶和醛缩酶、抗中性粒细胞胞质抗体(ANCA)。对于存在肺出血表现的患者,尚需检测抗肾小球基底膜抗体、抗磷脂抗体等。
另外,目前已研究了许多ILD的血清标志物,其中KL-6(Ⅱ型肺泡上皮细胞表达的一种循环高分子量糖蛋白)的一项研究表明,它检测ILD的敏感性、特异性及诊断准确性分别为94%、96%和94%。
2.胸部影像学
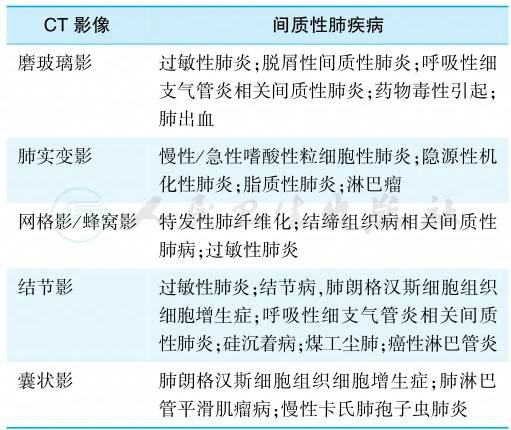
运用HRCT可发现早期肺泡充盈与间质改变。典型的影像改变为线条或网格影、结节或囊状影、磨玻璃影。线条或网格影多见于双肺底(如IPF、结缔组织病、石棉沉着病、细胞毒性药物诱发的肺炎)。蜂窝肺是指外围分布为主的多发囊状影聚集成蜂窝状,囊壁厚度为1~3mm。结节影提示不同的肉芽肿性肺病如结节病、硅沉着病、过敏性肺炎等。磨玻璃影为肺密度增高影,但尚未掩盖肺血管轮廓和支气管壁,它可为肺泡部分充填,也可为间质炎性浸润。出现磨玻璃影的ILD有NSIP、呼吸性细支气管炎相关间质性肺病(RBILD)、脱屑性间质性肺炎(DIP)、药物诱导性肺炎、肺泡蛋白沉着症、急性间质性肺炎等(表3)。
表3 间质性肺疾病的CT影像特征及其疾病举例
3.肺功能
早期肺功能可正常,随病情进展,可出现典型的限制性通气障碍。表现为肺活量和肺总量降低,弥散功能减低,肺顺应性降低。动脉血气分析示低氧血症,但PaCO2大多降低。肺泡-动脉血氧分压差增大。心肺运动试验显示最大运动负荷和最大氧耗量减低,还可发现静息状态下不能检出的弥散功能障碍。
病变若累及呼吸道,如肺淋巴管平滑肌瘤和晚期结节病可显示混合性或阻塞性通气功能障碍。
4.支气管肺泡灌洗(bronchoalveolar lavage,BAL)
是一种微创性操作,于支气管镜检查过程中获取肺泡细胞样本,可以分析细胞数量、成分,微生物学涂片及培养,通过BAL可了解免疫性、炎症性、肿瘤性及感染性病变情况。通过BAL主要排除感染性、肿瘤性和提示具有特征性灌洗成分的间质性疾病,如肺孢子虫病、肺泡蛋白沉着症和嗜酸性粒细胞性肺炎。BAL中矿物颗粒、石棉小体及吞噬粉尘的巨噬细胞有助于尘肺的诊断。富含有脂肪颗粒的巨噬细胞提示微量吸入引起的类脂质肺炎,CD1a+的朗格汉斯细胞比例增高提示肺朗格汉斯细胞组织细胞增生症。另外,BAL中某种炎症细胞比例增高有助于缩小鉴别诊断的范围,例如中性粒细胞显著升高,可考虑急性间质性肺炎、IPF和肺部感染性疾病;淋巴细胞明显增高,见于过敏性肺炎、结节病早期、淋巴细胞性间质性肺炎和肺淋巴瘤;嗜酸性粒细胞明显增高,见于嗜酸性粒细胞性肺炎、嗜酸性肉芽肿性血管炎等(表4)。
表4 BAL中细胞成分分析及代表性疾病
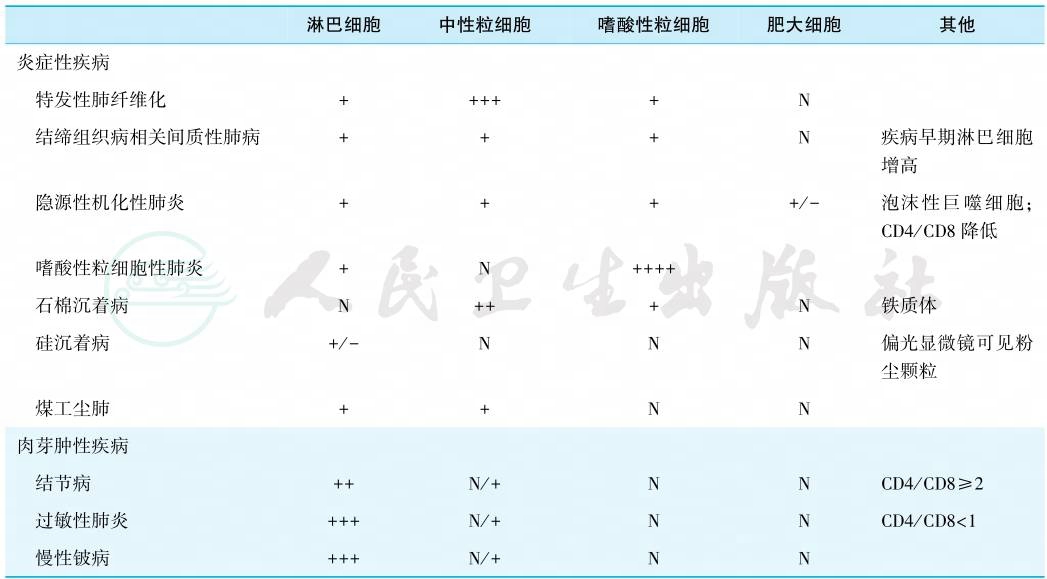
注:N正常;+轻度增高;++中度增高;+++明显增高。
5.超声心动图
用于以下情况,如心电图异常、弥散功能(DLCO,肺一氧化碳弥散量)中到重度降低而不能用肺疾病来解释,此类患者可能合并肺高压。6分钟步行测试(6MWT)后1分钟心率未降至正常,也提示潜在的肺高压。另外,患者进行外科肺活检前需利用超声心动图排除隐匿性心力衰竭的可能性。
6.肺活检
对症状、体征及影像学轻微异常的患者,倾向于定期复查肺功能和HRCT,而非立即进行肺活检。对症状和体征不典型或呈进行性发展、临床恶化者,可考虑肺活检;需排除肿瘤性及感染性疾病的患者,可进行肺活检。若无创评估的结果出现相互矛盾,例如心肺运动试验提示可能的ILD,但其HRCT仅显示极小的间质变化,这类患者可建议肺活检。活检采取的方式有经支气管镜肺活检(TBLB)、经支气管镜冷冻肺活检(cyo-TBB)。手术肺活检包括胸腔镜肺活检或开胸肺活检。













