甲状腺结节是正常甲状腺组织中出现的局限性肿块,它可以是无功能性的(“冷结节”),也可以是有功能的(自主结节),不伴有(“热结节”)或伴有甲状腺激素分泌增多(毒性结节)。甲状腺结节是最常见的甲状腺疾病之一。流行病学数据依筛选方法和入选人群的不同而变化,目前常用筛选方法为体表触诊检查法和超声检查法,但结节发现率的高低受检查者水平和经验的影响。流行病学调查显示:碘充足地区触诊患病率女性5%,男性1%。也有报道成人可触及甲状腺结节的患病率为4%~8%,尸检病理学为50%。甲状腺癌的发生率逐年递增,以美国为例,2009年甲状腺癌的新发病例数和死亡病例数分别是37 200例和1630例。虽然有的学者指出这种现象可能是因为筛查和检测手段的提高可以发现早期的患者。但是近年的研究报告显示甲状腺结节和甲状腺癌的发生率的确在升高,而并非单纯归因于早期筛查和检测手段的提高。至于是否结节单发多于多发,尚未确定。
良性疾病
(一)单纯性甲状腺肿伴结节
为引起结节性甲状腺肿最常见的病因。病史一般较长,往往在不知不觉中渐渐长大,而于体检时偶然被发现。结节是腺体在增生和代偿过程中发展而成的,大多数呈多结节性甲状腺肿,少数为单个结节性。大部分结节为胶性,其中有因发生出血、坏死而形成囊肿者;久病者部分区域内可有较多纤维化或钙化,甚至骨化。由于结节的病理性质不同,它们的大小、坚度、外形不一。甲状腺出血往往有骤发肿痛史,触诊腺体内有囊性肿块感;有胶性结节者,质地较硬;有钙化及骨化者,质地坚硬。
(二)甲状腺炎伴结节
1.亚急性甲状腺炎
结节的大小视病变范围而定,质地可较硬。有典型的病史,包括起病较急,有发热、咽痛及显著甲状腺区疼痛和压痛等表现。急性期,显像多呈“冷结节”,甲状腺摄131I率降低,血清T3和T4升高,呈“分离”现象,有助于诊断。
2.慢性淋巴细胞性甲状腺炎
为对称弥漫性甲状腺肿,有时由于肿大不对称和表面有分叶,可状似结节,硬如橡皮,无压痛。此病多起病缓慢,呈慢性发展过程,但与甲状腺癌可同时并发,临床上不易作出鉴别,须引起注意。抗甲状腺球蛋白和微粒体抗体及抗甲状腺过氧化物酶抗体滴度常升高。甲状腺细针穿刺细胞学检查有助诊断。
3.侵袭性纤维性甲状腺炎
结节坚硬且与腺体外邻近组织粘连固定。起病和发展过程缓慢,可有局部隐痛和压痛,伴以明显压迫症状,其临床表现如甲状腺癌,但局部淋巴结不大,摄131I率正常或偏低。
(三)甲状腺腺瘤
可发生于任何年龄,女性多见。腺瘤在大小和组织学特征各不相同,一般有完整的包膜,分三种主要类型:乳头状、滤泡性和Hurthle细胞性。根据滤泡的大小又将滤泡性腺瘤分为巨滤泡性或胶质性,胎儿性或小滤泡性及胚胎性,还有非典型腺瘤。乳头状瘤较少见,多呈囊性,又称乳头状囊腺瘤。滤泡性腺瘤最常见,组织高度分化接近正常组织。有些腺瘤不能浓聚99mTc或131I,甲状腺核素显像为功能丧失或“冷结节”,可致误诊为癌。事实上起初怀疑为癌的冷结节大部分为低功能腺瘤、出血性腺瘤和腺瘤囊肿变。临床上除触及颈部肿块外并无特殊表现。极少数较大的腺瘤可压迫气管,但罕见喉返神经受损。部分腺瘤可有浓聚碘的功能,扫描示“温结节”。血清甲状腺激素和TSH水平正常。随着时间的推移,结节进一步增大,释放甲状腺激素增加并足以抑制垂体TSH分泌,结节外甲状腺组织萎缩。显像时在结节区有放射性99mTc 或131I的浓聚呈“热结节”,其中部分患者可能有甲亢表现,称高功能或毒性腺瘤。高功能腺瘤极少癌变。治疗一般做手术摘除腺瘤。对高功能腺瘤也可予131I治疗,剂量较一般甲亢者大。但有时腺瘤由于出血、坏死、囊性变,可致功能部分或全部丧失。
(四)甲状腺囊肿
囊肿内含血液或清澈液体,与周围甲状腺组织分界清楚,可相当坚硬,直径很少>3~4cm,一般无压痛,无摄131I或摄99mTc能力,故在甲状腺显像图上系一种“冷”的结节,超声波检查常有助于诊断。临床上除甲状腺肿大和结节外,大多无功能方面的改变。
恶性肿瘤
(一)甲状腺腺癌
可发生在任何年龄,多见于年长者,高峰年龄出现于49~69岁的阶段,但年轻女性也不少见,女性发病数比男性高约3倍。恶性程度高的甲状腺癌少见于<40岁的人,但年龄>40岁后,甲状腺癌发生转移和死亡数上升。在单结节中远比多结节性甲状腺肿多见。根据形态分以下几种。
1.乳头状癌
从生物学特性的相似而言,此类肿瘤包括单纯性乳头状癌和混合性甲状腺癌。临床最常见,恶性程度也最低,大约占甲状腺癌的50%~70%,此外作为隐性癌,在尸检中亦屡发现,占尸检的6%~13%。任何年龄均可发病,但多见于儿童和年轻女性患者(40岁前)。男女之比为1∶2~1∶3。部分年轻患者在儿童时期曾有颈部X线治疗病史。乳头状癌生长缓慢,可在甲状腺内局限数年。病灶可经腺体内淋巴管扩散至腺体的其他部位或局部淋巴结。有时颈部淋巴结转移掩盖了原发病灶,故易忽视其性质。血行转移较少,如有则以肺转移为主;次为骨转移。随着年龄的增大,肿瘤恶性程度增高,偶可转为未分化癌,预后差。有时患者在甲状腺癌切除后,对侧腺体在若干年后出现复发癌。病理上可见分化良好的柱状上皮,呈乳头状突起,核清晰伴嗜酸性胞质(hurthle cell),常可见同心圆的钙盐沉积。有时伴有滤泡癌成分。甚至占较大比重。但只要查见磨砂玻璃样核的乳头状癌结构,不论其所占成分多少均应诊断为乳头状癌。临床上除扪及甲状腺结节及局部淋巴结肿大外,症状很少,有时甚至摸不到结节。乳头状癌可由TSH的刺激而生长。用甲状腺素可使之缩小。手术如包膜完整而无转移者,预后较好。如有血管侵犯,10年存活率约1/3。
2.滤泡细胞癌
占甲状腺癌的10%~15%,多见于40岁以上患者,女性2~3倍于男性,儿童极少见。滤泡细胞癌很少从淋巴转移,一般通过血行远处扩散。特别扩散至骨骼、肺、肝等脏器。给予治疗剂量的甲状腺素可以抑制其扩散。病理所见可各处表现不一,有的部位组织几乎正常,有的部位则仅见有核分裂,也可见有Hurthle细胞,常可见到血管和附近组织的侵蚀,年老者更为显著。侵袭范围和程度决定滤泡细胞癌的预后。甲状腺滤泡细胞癌,多数伴乳头状癌夹杂而成混合类型。早期的滤泡细胞癌易与滤泡性腺瘤混淆,须镜检鉴别,部分滤泡细胞癌有转变成间变癌的可能。临床上患者主要有结节性甲状腺肿大,单结节多见,质硬如石,有时可累及整叶,后期可出现邻近组织侵蚀、疼痛以及远处的转移。滤泡细胞癌及其转移灶有摄碘功能,偶尔可引起甲亢。
3.未分化癌
占所有甲状腺癌的5%~10%,通常见于55岁以后,女∶男为1.3∶1到1.5∶1。恶性程度高,可分为几个亚型,以小细胞癌和巨细胞癌为最重要。常可迅速侵蚀毗邻组织和全身广泛转移,如皮肤、血管、食管、肺等。病理所见主要为含有许多核分裂的不典型细胞和多核巨细胞,恶性程度最大。有时以小细胞为主,不易与淋巴瘤区别。有些呈肉瘤样结构的癌,光镜下很难与肉瘤鉴别。电镜有助于鉴别。有时可见乳头状癌或滤泡状癌的成分,提示部分未分化癌是乳头状或滤泡状癌的退行性变(间变)。临床上患者常诉甲状腺肿块迅速增大、疼痛。侵及邻近组织,引起嘶哑、呼吸窘迫和吞咽困难。肿块大而压痛,与周围组织相固定,在吞咽时活动度差,质地硬如石,局部淋巴结肿大,也可向远处转移。一般情况下,未分化癌无浓聚碘的功能,扫描呈“冷结节”。治疗方面尽管原发病灶可被切除,但由于已有远处转移,总的效果欠佳。巨细胞腺癌多在诊断6个月内死亡。小细胞癌5年生存率约为20%~25%。
4.甲状腺滤泡旁细胞癌
又称甲状腺髓样癌,约占甲状腺癌的2%~3%。常在50岁以上患者中发病,女性略多。恶性程度较滤泡腺癌为高。甲状腺髓样癌一般分为散发型和家族型。散发型约占80%,家族型占20%。癌肿甚易侵蚀腺体内淋巴管,扩散至腺体其他部分及局部淋巴结,也同样可自血行扩散至远处。髓样癌一般无包膜。病理所见细胞形态和排列不一。细胞可为未分化,有核分裂,但无坏死或多核细胞浸润。以淀粉样沉淀为常见。腺体的其他部位也可见到癌性病灶,有血管侵蚀。肿瘤及受累的淋巴结钙化是诊断的重要线索。临床上一般先有甲状腺坚硬结节或局部淋巴结肿大,有时也可发现远处转移灶。结节不摄碘,扫描时呈“冷结节”,肿瘤可分泌降钙素,故血中常可检出降钙素浓度增高,但血钙一般不低。甲状腺滤泡旁细胞属于APUD细胞系统。因此,肿瘤可以分泌血清素和ACTH,表现有类癌瘤症状和库欣综合征。亦可分泌前列腺素、肾素和血管活性肠肽引起相应症状。20%~30%有腹泻,原因不明,可能与5-羟色胺或前列腺素E2及F2α有关。也可以多发性内分泌腺综合征Ⅱa型或Ⅱb型发病,即同时伴有单侧或双侧嗜铬细胞瘤,甲状旁腺瘤及黏膜神经瘤。合并甲旁亢较常见。可有高钙症状、肾结石或肾钙质沉着,测定肿瘤细胞的DNA倍体、降钙素免疫活性和淀粉样染色,用以估计患者的预后。晚近,人们已用ret基因突变分析来诊断本病,并筛选家族成员中的高危对象。
(二)甲状腺淋巴瘤
甲状腺淋巴瘤罕见,占甲状腺癌1%~2%,男∶女为1∶3。可在桥本甲状腺炎基础上发病。是淋巴瘤中唯一女性发病为主的肿瘤。这与桥本甲状腺炎多发生于女性有关。病理间质内异型淋巴细胞呈弥漫性浸润,淋巴滤泡生发中心萎缩消失,淋巴细胞成堆或环状浸润,甲状腺滤泡上皮呈瘤样损害,在滤泡腔内血管壁浸润,尤其在肌层小血管壁淋巴细胞浸润。临床上桥本甲状腺炎或甲亢患者有迅速增大的甲状腺肿块,甲状腺扫描呈“冷结节”,免疫球蛋白标记为轻链单克隆者要考虑是否本瘤可能,进一步检查明确诊断。甲状腺淋巴瘤易与以小细胞为主的未分化癌混淆,须镜检病理鉴别。
甲状腺结节恶变的高危因素
1.有甲状腺癌的近亲家族史。
2.儿童时期有头颈部放射性外照射病史。
3.儿童时期或青少年时期有辐射照射史。
4.年龄<20岁或>70岁。
5.结节明显增大。
6.在既往甲状腺手术史中曾有甲状腺癌的病理诊断。
7.18FDG-PET显像有明显浓聚18FDG的甲状腺结节。
8.有甲状腺癌或多种内分泌肿瘤家族史(multiple endocrine neoplasia type 2,MEN2),或者家族性甲状腺髓样癌相关的RET突变,或降钙素大于100pg/ml。
9.颈部有异常淋巴结。
(一)B超检查
超声技术的快速发展,以及超声检查具有良好的分辨率和血供观察能力,且方法简便经济,使得超声检查已成为临床甲状腺结节诊断应用最广的影像学检查。高频线阵式探头的应用,使超声对甲状腺肿瘤的诊断取得了显著的效果,能够清晰显示病灶形态结构、大小、边界、有无包膜、内部回声、钙化和后方声影等。恶性病变多表现为结构致密的低回声区或结节,且形态不规整、边界不清晰或毛糙不规则,可对周围组织产生挤压。超声检查结节中微钙化诊断甲状腺癌的特异性为85%~95%;结节边界不规则或不清楚诊断恶性的特异性为83%~85%;结节内部血管紊乱诊断的特异性为81%。但是上述征象的敏感性不高,分别只有29%~59.2%,55.1%~77.5%,74.2%,因此在临床实践中必须注意各个征象相结合,而非依靠某一征象。
1.彩色多普勒血流显像(CDFI)
绝大多数的恶性肿瘤用CDFI可探及血流信号,并以内部血流为主,一般而言结节越大、血流信号越丰富,且分布凌乱。近几年应用的新技术三维能量血管成像(3D-CPA)对甲状腺癌血流分布情况的显示明显高于二维彩色血流,其可以清楚显示肿瘤内明显增多、增粗的动脉及大量粗细不均、迂回紊乱的新生血管。临床实践中彩色多普勒血流显像必须与灰阶超声共同使用以诊断甲状腺结节性质。
2.超声造影检查
分析造影剂通过组织的时间和研究它们的时间-强度曲线可提供定量和客观的信息。时间-强度曲线的形态可反映造影剂在灌注相和清除相的动力学状况。恶性肿瘤可能由于动-静脉短路和血流速度加快,所以显影时间早。甲状腺癌显影时间早,其峰值时间也早。
3.超声引导下的细针抽吸细胞学检查(US-FNA)
由于其实时且可较为准确地到达所要抽吸的结节部位,在临床诊断中愈来愈受到重视。US-FNA的主要指征有:①直径大于10mm的实性低回声结节;②超声检查怀疑囊外生长或颈部淋巴结转移的任何大小的甲状腺结节;③儿童或青春期有颈部放射线接触史的患者;甲状腺乳头状癌(PTC)、甲状腺髓样癌(MTC)或多发性内分泌肿瘤2型(MEN2)患者的一级亲属;有甲状腺癌手术史者;在无任何干扰因素的情况下所测降钙素水平升高者;④直径虽小于10mm,但超声检查发现有与恶性病变相关征象[低回声和(或)边界不规则、呈细长形、有微小钙化或结节内血流信号紊乱]的结节。
对于多结节性甲状腺肿:①当结节符合上述超声检查恶性征象时,须行FNA活检的结节极少需要超过2个;②当同位素扫描显示为“热”结节时,不行FNA活检;③若存在可疑淋巴结病时,应同时对肿大的淋巴结和可疑结节行FNA活检。对于混合性(囊实性)甲状腺结节:①对其中的实性部分行UGFNA活检;②同时将FNA活检样本和吸取的液体标本行细胞学检查。
FNA的优点是方便、安全,但需要专门的细胞病理学医师参与。超声引导下的细针穿刺是诊断甲状腺癌的有用手段,但对滤泡状癌不能作出明确诊断,因为只有通过外科切除标本的组织学检查才能发现包膜和血管浸润。需要指出的是甲状腺结节超声检查的高检出率,就是在可触诊出的结节中恶性肿瘤的发生率也只有5.0%~6.5%,因此US-FNA的临床使用必须严格掌握指征,尤其是须认真解读结节的超声影像学特征以判断结节恶性可能的高低。
鉴于超声对甲状腺癌的高度敏感性和特异性,临床医师已将超声检查列为体检和偶然发现甲状腺结节鉴别诊断的首选方法。但超声检查取决于操作者经验、技术熟练和精细程度、探头选择及检查时手法等众多因素。另外对于特殊病例结节性质难以明确的病变采用超声引导下的细针穿刺细胞学检查或手术探查应由临床医师根据病例具体情况衡量利弊合理选择。
(二)核素显像
甲状腺癌99m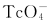 和131I显像多表现为冷结节,其反映了结节的功能状态,但仅根据99m
和131I显像多表现为冷结节,其反映了结节的功能状态,但仅根据99m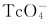 和131I显像估计肿瘤的良、恶性是非常局限的,这是因为显像为“冷”结节中只有5%~15%为恶性可能,因此“冷”结节中恶性的预测值非常低。近几年应用111In、99mTc标记生长抑素类似物奥曲肽(octreotide)显像,对于诊断甲状腺髓样癌和不摄取131I的DTC取得较好的效果。需要指出的是,无论哪一种甲状腺亲肿瘤显像剂均有局限性,主要是少数良性病变亦呈部分浓聚(例如慢性淋巴细胞性甲状腺炎、腺瘤等),另外值得指出,核素显像的空间分辨率按目前仪器的水平为平均10mm左右,近年推出的SPECT/CT有利于形态与功能融合显像,除核素信息外,亦可获得相关CT诊断信息。因此当出现阳性结果时一定要结合其他影像学表现和血清Tg、降钙素等指标综合分析。
和131I显像估计肿瘤的良、恶性是非常局限的,这是因为显像为“冷”结节中只有5%~15%为恶性可能,因此“冷”结节中恶性的预测值非常低。近几年应用111In、99mTc标记生长抑素类似物奥曲肽(octreotide)显像,对于诊断甲状腺髓样癌和不摄取131I的DTC取得较好的效果。需要指出的是,无论哪一种甲状腺亲肿瘤显像剂均有局限性,主要是少数良性病变亦呈部分浓聚(例如慢性淋巴细胞性甲状腺炎、腺瘤等),另外值得指出,核素显像的空间分辨率按目前仪器的水平为平均10mm左右,近年推出的SPECT/CT有利于形态与功能融合显像,除核素信息外,亦可获得相关CT诊断信息。因此当出现阳性结果时一定要结合其他影像学表现和血清Tg、降钙素等指标综合分析。
131I全身显像对甲状腺癌转移的探测可检查转移病灶有无摄取131I功能。如只见残余正常甲状腺有摄131I功能,而转移灶无摄131I功能,则进一步可用131I消除残余正常甲状腺。用131I量可根据摄131I功能和显像所见残余正常甲状腺的多少来估计,如有摄131I功能的残余甲状腺,则需用131I摧毁之后每月显像一次以观察转移灶是否有摄131I功能,直至转移灶出现摄131I功能方可行131I治疗。
18F脱氧葡萄糖(18FDG)为葡萄糖的类似物,18F可发出正电子,是葡萄糖代谢的示踪剂。血液中的18FDG也经细胞膜上葡萄糖转运体(GLUT)进入细胞,在细胞内通过己糖激酶的作用生成6-磷酸脱氧葡萄糖(DG-6-P)。后者不被细胞内的酶进一步代谢,因此在细胞内堆积,其数量与病灶细胞对葡萄糖摄取和利用能力相一致,恶性肿瘤的这种能力通常增高,因此18 FDG可作为示踪剂进行PET显像,通过观察18FDG-6-P在细胞内浓集的多少,判断肿瘤的良、恶性质。
131I全身显像可以评价是否存在完整的钠/碘转运泵,对高分化、低度恶性的肿瘤诊断阳性率较高,而18FDG-PET对低分化、高度恶性的肿瘤敏感性高,因此,18FDG-PET不能完全取代131I全身显像。部分甲状腺良性病变可以浓集18FDG,特别是甲状腺腺瘤,可以表现很高的18 FDG摄取,标准摄取值(SUV值)达到3.0~6.0以上(通常SUV=2.5作为良、恶性病变的诊断界限,SUV>3.0通常考虑为恶性病变)。延时显像有助于鉴别诊断。部分Graves病甲亢和桥本甲状腺炎患者其甲状腺FDG摄取弥漫性增加。甲状腺18FDG-PET的假阴性主要见于生长慢、分化好的病灶或过小的原发或转移灶。一般不主张常规使用18FDGPET诊断原发甲状腺癌,尤其是分化好的甲状腺滤泡癌和甲状腺乳头状癌,但对于未分化癌、髓样癌,18FDG-PET检查有意义。18FDG-PET在甲状腺癌术后复发和转移灶的检测可作为131I全身显像的补充,适用于:①血清Tg水平升高,但131I全身显像阴性而疑有甲状腺癌复发和远处转移癌灶者。②甲状腺髓样癌术后血清降钙素水平升高患者转移病灶的探测。③131I全身显像已发现肿瘤复发或转移,18FDG-PET有可能发现更多的转移病灶。重组人促甲状腺激素(rhTSH)可刺激DTC对FDG的摄取,从而提高18FDG-PET诊断的准确性。总之,18FDG-PET显像不是诊断甲状腺癌和转移病灶的第一线方法,但对探测甲状腺癌的微小转移病灶有优势,并有助于治疗方案的确定。
(三)CT和MRI
CT可清楚显示甲状腺的解剖形态,判断甲状腺病变对邻近器官的影响,明确肿瘤有无邻近淋巴结、血管或胸腔上部侵犯转移等方面具有较高的临床价值,但有一点须注意的就是碘增强剂对甲状腺疾病的影响。多层螺旋CT因其无运动伪影、可在任意层面重组影像等优势增强了CT的诊断价值。CT灌注显像可在显示形态学变化的同时反映生理功能,以了解肿瘤间质血管分布情况,并能定量地了解肿瘤微血管功能状态。
MRI具有软组织对比度佳及区分不同来源组织能力强的特点,但MRI对局灶性病变的诊断敏感性欠佳,在确定钙化方面有一定的不足。MRI技术发展迅速,功能性MRI显像技术如弥散加权成像技术(DWI)与灌注加权成像(PWI)、磁共振波谱分析(MRS)用于甲状腺结节的诊断和鉴别诊断。个别单位虽积累一些经验,但目前国内临床上尚未列入一线常规检查。
各种新的甲状腺成像技术必将不断涌现,它们在不断丰富临床医师的检查手段的同时,也带来了如何合理运用的新问题。了解各种成像的机制,掌握各种检查的信息含义,明确各种检查在甲状腺疾病诊断中所处的地位和作用。遵照循证医学的原则,充分发挥各自的特长,一定会把甲状腺结节的诊断和鉴别诊断提高至一个新水平。
甲状腺癌确诊后,一般均需手术治疗。术前用甲状腺激素进行抑制性治疗,使手术操作变得容易,也可减少肿瘤扩散的可能。手术中应行冰冻切片,以决定是否作根治手术,术后应作石蜡切片以求准确病理结果。甲状腺癌肿患者应进行甲状腺全切除及其他根治手术,并在术后4周时,行131I全身扫描在甲状腺及转移病灶中搜索放射性活性。手术治疗后的处理主要是放射性碘和甲状腺激素抑制治疗。对于疑似肿瘤而又不能或不愿做活检者,则可使用甲状腺激素抑制肿瘤3个月。肿瘤中结节缩小,则应长期继续用药;如结节未缩小或更增大,应即考虑手术治疗。如结节有功能,虽无恶性证据,也应手术治疗。
全切除术后,血清甲状腺球蛋白仍增高,提示有残余癌组织。如发现甲状腺部位尚有具吸碘功能的病变残留,即可使用大量放射性碘以去除残余甲状腺组织。按病灶情况,一般剂量在50~150mCi,次日继以甲状腺激素充分抑制治疗,使血清TSH降至测不出水平。甲状腺素每天需用300μg以上,或甲状腺干制剂每天120~240mg。患者每2~3个月详细检查一次,包括甲状腺球蛋白测定及全身131I扫描,因为接受抑制治疗的患者血清甲状腺球蛋白值升高表示存在转移灶。如无转移灶发现,继续甲状腺激素治疗,直至下一次131I扫描检查前4周,改用三碘甲状腺原氨酸,后者在扫描前10天停用。如有复发,则需再用较前更大剂量的放射性碘,总剂量宜在500mCi左右。有些患者,131I扫描没有可证明的病灶转移,但血清甲状腺球蛋白升高,有条件者可用18FDG-PET扫描检查以查明分泌甲状腺球蛋白的转移癌的部位。













