患者女性,50岁。因“进行性肢体麻木2年,行走不稳2个月””于2016年1月29日入院。
现病史
患者2年前无明显诱因出现左足𧿹趾麻木,活动无异常。1年前出现双手指尖麻木,逐渐向上进展至腕部,伴前臂发凉感,同时左足𧿹趾麻木逐渐向上进展至左小腿麻木。当地医院按“颈椎病”或“腰椎病”物理治疗,症状未见好转。2个月前逐渐出现右足、右小腿麻木,伴行走不稳,自觉行走时踩棉花感、需注视地面,夜间行走不稳症状加重,自觉足底增厚,曾诉“脚上穿鞋却不自知”;双手活动欠灵活,使用筷子、系纽扣、拿笔费力,双手接触冷水有过电感。当地医院行肌电图(EMG)检查显示多发性神经损害,轴索损害为主;头部MRI显示脑白质轻微脱髓鞘改变;颈椎MRI显示颈椎骨质增生,T2椎体异常信号(可疑血管瘤),椎间盘退行性变,表现为C2~3、C3~4椎间盘向左后突出,C4~5、C5~6和C6~7椎间盘向后突出,继发相应椎管狭窄。临床诊断为“周围神经病,颈椎病”。予针灸和营养神经、改善循环治疗(具体方案不详),自觉症状改善不明显。为求进一步诊断与治疗,遂至我院就诊。
患者自发病以来,精神、睡眠、饮食可,大小便正常,体重无明显变化;自觉近3~4个月偶有眼干,否认皮疹、关节痛、光过敏、口腔和生殖器溃疡等其他免疫性疾病。
既往史、个人史及家族史
无特殊。
体格检查
体温36.2℃,脉搏106次/min,呼吸18次/min,血压152/90mmHg。神志清楚,语言流利,对答切题,粗测高级智能活动正常。脑神经检查未见明显异常。四肢无肌萎缩,双上肢近端肌力5级,远端对指、并指、握拳肌力5-级,尤以左侧显著,双下肢肌力5级,四肢肌张力均正常。双侧肱二头肌反射未引出,双侧肱三头肌反射、桡骨膜反射对称减低,双侧膝腱、跟腱反射未引出,病理征阴性。双上肢腕部以远、左下肢膝部以下、右下肢踝部以下针刺觉减退,双侧T8~10平面以下、双上肢肩关节以下音叉振动觉减退,双肘以下、双足关节位置觉减退;双手实物辨别觉、双下肢皮质复合觉减退。快复轮替动作笨拙,双侧指鼻试验和跟-膝-胫试验睁眼可、闭眼欠稳准。行走时蹒跚步态,需注视地面,足尖足跟站立、行走可,蹲起正常,直线行走欠平稳,Romberg征阳性。脑膜刺激征阴性。
辅助检查
实验室检查,血、尿、粪便常规、肝、肾功能试验、凝血功能均于正常值范围;血清甘油三酯(TG)2.26mmol/L;感染免疫检测四项、红细胞沉降率(ESR)、超敏C反应蛋白(hs-CRP)均于正常水平;空腹血糖4.50mmol/L,甲状腺功能试验、血清铜蓝蛋白、血清叶酸和维生素B12、同型半胱氨酸(Hcy)均于正常值范围;抗核抗体(ANA)谱:ANA阳性(滴度1:160,斑点型),抗干燥综合征A型抗体(SSA)强阳性,抗Ro52抗体强阳性;抗可提取性核抗原(ENA)抗体谱:抗SSA抗体滴度1:4(双扩散法);类风湿因子(RF)113.40IU/ml(10~20IU/ml);抗中性粒细胞胞质抗体(ANCA),免疫球蛋白 IgG、IgM和IgA,补体C3和C4均呈阴性;狼疮抗凝物、抗心磷脂抗体(ACA)、抗β2糖蛋白1抗体均呈阴性;血清女性肿瘤标志物均于正常参考值范围;血清抗Hu、Yo、Ri抗体阴性。腰椎穿刺脑脊液外观清亮、透明,压力115mmH2O,白细胞计数2×106/L,细胞学未见异常,生化正常,抗酸染色、墨汁染色、细菌和真菌涂片、抗水通道蛋白4(AQP4)抗体IgG、髓鞘碱性蛋白(MBP)均呈阴性,寡克隆区带(OB)阳性,抗Hu、Yo、Ri抗体阴性。影像学检查:胸、腹、盆腔CT增强扫描未见明显异常。颈椎MRI显示颈椎退行性变:C3~4、C4~5、C5~6和C6~7椎间盘突出,继发相应椎管狭窄;C5~T1水平后索异常高信号影。头部MRI显示,右侧额叶少量斑点状异常高信号,考虑为慢性缺血所致。神经传导速度(NCV)和肌电图:四肢周围神经源性损害(感觉纤维),运动神经传导速度(MNCV)和波幅正常,多条感觉神经动作电位(SNAP)波幅明显下降甚至未引出(表1,表2)。四肢皮肤交感反应(SSR)未见异常;瞬目反射未见异常(图1)。
表1 运动及感觉神经传导
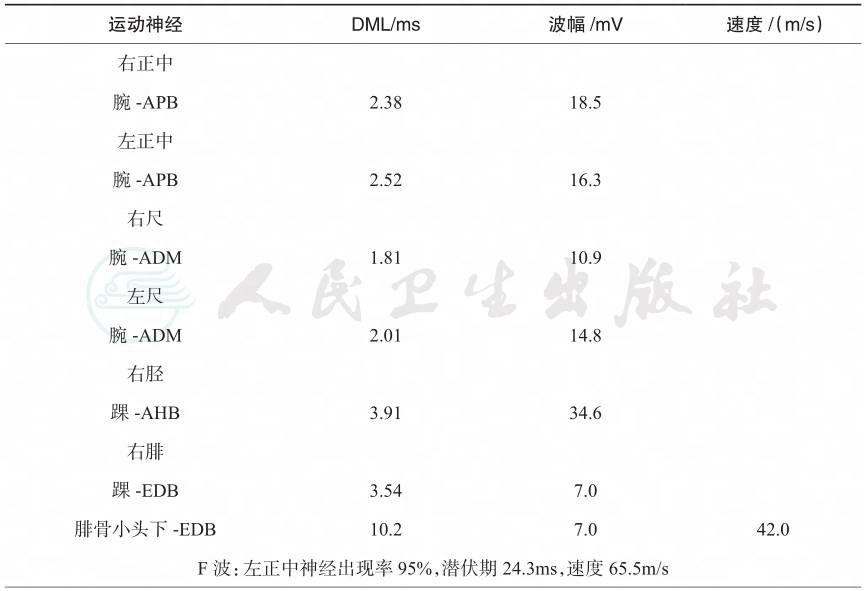
续表
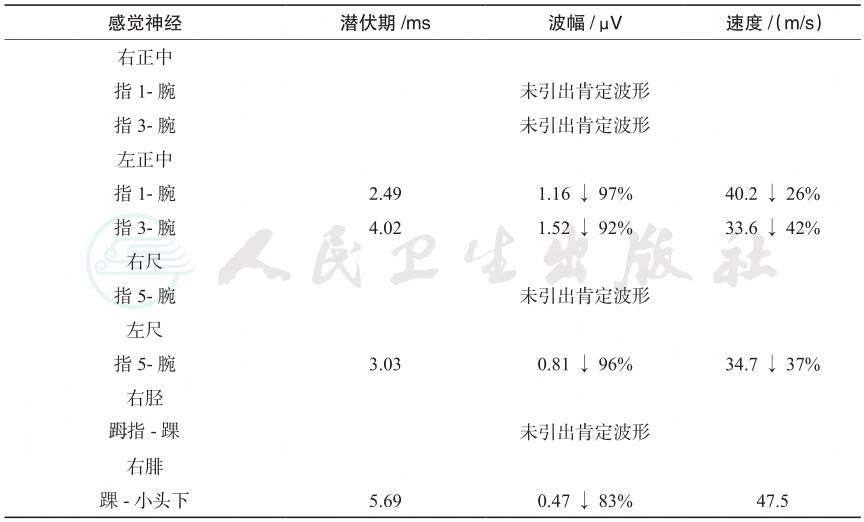
DML:运动末梢潜伏期;APB:拇短展肌;ADM:小指展肌;AHB: 𧿹短展肌;EDB:趾短伸肌
表2 针电极肌电图

MUAP:运动单位动作电位
肌肉 安静 MUAP/ms 波幅/μV 多相/% 大力/mV |
左小指展肌 P++F+ 12.8↑16% 621↑69% 23.1 混合相2.7 左胫前肌 P++++ 17.1↑25% 599↑38% 22.2 混合相2.5 |
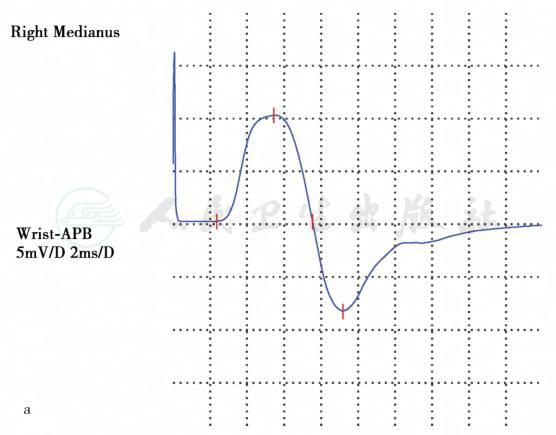
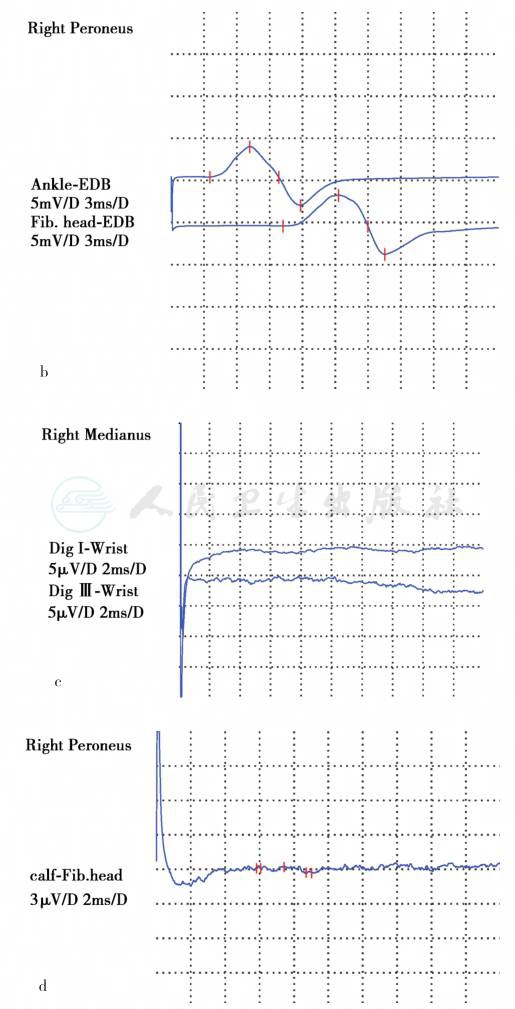
患者运动神经传导测定
图1 a~d.上、下肢运动末端潜伏期及波幅正常(a、b),感觉神经传导显示感觉神经动作电位波幅明显降低(c、d),提示上、下肢周围神经源性损害,以感觉纤维受累为主
诊断与治疗经过
患者抗SSA抗体阳性,完善干燥综合征相关检查。请眼科会诊:泪膜破裂时间(TBUT)右眼为5s、左眼5s(>10s),Schirmer试验右眼为 20mm/5min、左眼9mm/5min(>5mm/5min),角膜染色阴性。请口腔科会诊:唾液流速0.02ml/min(>1.50ml/15min),腮腺造影显示主导管正常,分支导管不显影,末梢导管点球状扩张,排空延迟。进一步行唇腺组织活检术,病理学显示(唇腺)小涎腺组织,局灶性腺泡萎缩,可见小导管扩张,腺泡周围灶性或团状浆细胞、淋巴细胞浸润,淋巴细胞灶>4灶(4mm2组织内至少有50个淋巴细胞聚集于唇腺间质为1灶)。
神经科主治医师
患者中年女性,慢性发病,病情缓慢并呈进行性加重,病史2年。临床主要表现为:①不对称性起病,进行性加重的四肢远端感觉异常。②近2~3个月出现步态异常,行走时踩棉花感,并出现双手活动欠灵活。近3~4个月有眼干症状,自发病以来体重无明显下降,大小便无异常,既往无糖尿病病史、毒物接触史和特殊药物应用史。定位诊断:患者以四肢远端感觉异常为突出表现,同时有行走不稳,行走时踩棉花感;体格检查深浅感觉减退,浅感觉减退呈不对称性“手套-袜套”样分布,深感觉减退平面更高,上肢在肩关节以下、躯干和下肢在T8~T10平面以下,四肢腱反射减低;神经传导速度显示部分感觉神经动作电位波幅明显下降甚至未引出,运动神经传导未见异常;颈椎MRI显示颈髓后索异常信号,定位于感觉性周围神经、后根和后索,综合定位于后根神经节感觉神经元。定性诊断:患者中年女性,病史2年,病情逐渐进展,近3个月进展相对较快,临床主要以四肢感觉异常和感觉性共济失调为突出表现,肌电图显示多条感觉神经动作电位波幅明显下降甚至未引出,颈椎MRI可见颈髓后索异常信号,定性诊断考虑同时累及后索和感觉性周围神经的感觉神经元神经病可能大。病因方面,首先考虑系统性自身免疫性疾病,多种自身免疫性疾病可以累及后根神经节,包括干燥综合征、系统性红斑狼疮、类风湿性关节炎等,尤以干燥综合征最为常见。干燥综合征是一种主要累及外分泌腺的慢性炎症性自身免疫性疾病,除涎腺和泪腺受累出现口干、眼干症状外,尚有其他外分泌腺和腺体外器官受累出现多系统损害症状,如周围神经系统,可以引起单神经病、多发性单神经病、感觉神经病、自主神经病等。该例患者近3~4个月有眼干症状,应高度怀疑干燥综合征,完善相关实验室检查和眼科、口腔科检查,以明确诊断:血清ANA阳性(滴度1:160,斑点型),抗SSA抗体和抗Ro52抗体强阳性,抗SSA抗体滴度1:4(双扩散法),类风湿因子113.40IU/ml,泪膜破裂时间、唾液流速、腮腺造影均呈阳性,唇腺组织活检符合干燥综合征组织病理学表现,根据中华医学会风湿病学分会2010年发布的《干燥综合征诊断及治疗指南》,原发性干燥综合征诊断明确,考虑为干燥综合征合并感觉神经元神经病。鉴别诊断主要是累及后根神经节和同时累及后索和感觉性周围神经的疾病。①副肿瘤综合征(PNS):副肿瘤性感觉神经元神经病最常见于小细胞肺癌,呈亚急性或慢性发病,感觉神经元神经病可出现于肿瘤症状出现前数月,部分患者血清和/或脑脊液抗Hu抗体阳性。该例患者完善胸、腹、盆腔CT增强扫描,血清肿瘤标志物筛查,抗Hu、Yo、Ri抗体检查,均无明显异常,故不予考虑。②感染:如人类嗜T细胞病毒Ⅰ型(HTLV-1)感染、梅毒螺旋体(TP)感染等。前者多以锥体束征临床常见,表现为痉挛性截瘫,该例患者无锥体束征表现,故不支持诊断;后者可以累及后索和后根,出现深感觉障碍和根性疼痛,该例患者的“手套-袜套”样浅感觉减退较少见于梅毒且无相关病史,梅毒螺旋体抗体相关检测均呈阴性,故可以排除诊断。③代谢性疾病:应考虑脊髓亚急性联合变性(SCD)、铜缺乏性脊髓病等,两者临床表现相似,后索、侧索和周围神经均可受累,前者是维生素B12缺乏所致,后者是铜缺乏所致。该例患者锥体束征阴性,侧索未见明显受累,周围神经损害局限于感觉纤维,血清维生素B12和铜蓝蛋白于正常值范围,均不支持脊髓亚急性联合变性和铜缺乏性脊髓病的诊断。④药物、中毒性因素:主要与化疗药物(尤其是铂)和维生素B6过量有关,该例患者无相关药物接触史,故暂不考虑。
神经科教授
患者中年女性,慢性病程,临床主要表现为四肢远端不对称性感觉异常和行走不稳,体格检查深浅感觉减退、感觉性共济失调,结合神经传导速度显示多条感觉神经动作电位波幅明显下降甚至未引出、运动神经传导无明显异常,颈椎MRI显示颈髓后索异常信号,后根神经节感觉神经元病变相对明确。该例患者血清免疫学指标、口腔科和眼科检查、唇腺组织活检病理学检查均支持干燥综合征,同时未发现副肿瘤综合征相关证据,故考虑为干燥综合征合并感觉神经元神经病。治疗方面,针对原发病,予泼尼松、环磷酰胺和羟氯喹治疗;针对周围神经病变,予甲钴胺、维生素B1营养神经治疗,同时密切关注药物不良反应。注意应告知患者及其家属该病缺乏可监测的指标,需长期治疗。
诊治经过
结合临床表现和上述辅助检查结果,干燥综合征诊断明确,考虑为干燥综合征合并感觉神经元神经病。请风湿免疫科会诊,予泼尼松1mg/(kg·d)口服,连续治疗4周后减量,每周减5mg直至0.5mg/(kg·d),然后每周减2.5mg直至停药;环磷酰胺100mg(隔日1次)和羟氯喹0.2g(2次/d)口服,定期监测血常规和肝肾功能。患者共住院32日,出院时四肢麻木、行走不稳较前改善。
1.感觉神经元神经病(sensory neuronopathy)
2.干燥综合征(Sjögren syndrome,SS)
干燥综合征(Sjögren syndrome,SS)是主要累及外分泌腺的慢性自身免疫性疾病,除涎腺和泪腺等外分泌腺受累出现口干、眼干症状外,还有其他外分泌腺和腺体外器官受累出现多系统损害症状。国内关于干燥综合征的诊断指南主要是中华医学会风湿病学分会2010年发布的《干燥综合征诊断及治疗指南》,国际关于干燥综合征的最新指南为美国风湿病学会(ACR)2012年发布的诊断标准。无论是参照中华医学会风湿病学分会2010年版指南还是美国风湿病学会2012年版指南,该例患者干燥综合征诊断明确。
干燥综合征可以累及中枢神经系统和/或周围神经系统,尤以周围神经系统常见,可以累及周围神经系统任何部分,包括运动神经、感觉神经、自主神经或兼而有之。临床表现为感觉神经病(感觉轴索性神经病、感觉神经元神经病、感觉神经小纤维病)、感觉运动神经病(感觉运动轴索性神经病、脱髓鞘性多发性神经根神经病、单神经病、多发性单神经病)和自主神经病等。由于诊断标准的演变、纳入标准的差异、回顾性研究的局限性等因素,不同临床研究中干燥综合征合并周围神经病的发病率明显不同。Pavlakis等统计1988—2010年的15项病例研究,发现干燥综合征合并周围神经病的发病率为1.8%~64.0%。不同研究中周围神经病在干燥综合征病程中的出现时间差异较大:有研究显示周围神经病可出现于干燥综合征之前;亦有研究显示干燥综合征病程后期方出现神经系统症状。这种差异性可能与患者就诊科室不同有关。
该例患者临床表现以感觉症状突出,体格检查提示感觉性共济失调和“手套-袜套”样深浅感觉减退,无运动系统受累,故主要考虑感觉神经病变,包括感觉神经元神经病和/或感觉神经病。肌电图显示运动神经复合肌肉动作电位(CMAP)正常,多条感觉神经动作电位波幅明显下降甚至未引出;颈椎MRI显示颈髓后索异常信号,因此,临床考虑后根神经节损害可能性大,即感觉神经元神经病,亦称感觉神经节神经病(sensory ganglionopathy)。感觉神经元神经病最早由Denny-Brown于1948年描述,由于后根神经节受累,感觉神经元缺失,导致其周围突和中枢突均受累变性,前者主要表现为非长度依赖性感觉神经病,后者表现为后柱(索)病变。感觉神经元神经病的最常见病因为副肿瘤综合征和自身免疫性疾病(如干燥综合征),其次为获得性免疫缺陷综合征(AIDS)、人类嗜T细胞病毒Ⅰ型感染、维生素B6中毒和药物化疗(主要是铂)等。干燥综合征合并感觉神经元神经病多呈亚急性或慢性发病,也有呈急性发病的文献报道。疾病早期感觉障碍多为不对称性,随着疾病进展,感觉缺失分布可融合、对称;多表现为深感觉性行走不稳,可逐渐加重直至丧失行走能力,部分患者上肢远端可见假性手足徐动。体格检查深感觉减退、Romberg征阳性和腱反射消失。神经电生理学检查,感觉神经动作电位波幅下降或消失。部分患者影像学可见T2WI后索高信号影,与后索传入纤维变性有关。综合该例患者临床表现和辅助检查结果,符合感觉神经元神经病。
关于干燥综合征合并感觉神经元神经病的治疗尚缺乏大样本的临床研究。目前主要采用免疫治疗,包括静脉注射免疫球蛋白(IVIg)、血浆置换(PE)疗法、糖皮质激素、硫唑嘌呤、环磷酰胺等。尽管有研究显示静脉注射免疫蛋白、血浆置换疗法可使部分患者临床症状改善,但总体疗效尚不确定。该例患者予泼尼松、环磷酰胺和羟氯喹治疗,出院后2个月随访时自觉行走不稳较前略有好转,长期疗效尚待进一步观察。
[1]MoriK,IijimaM,KoikeH,et al.The wide spectrum of clinical manifestations in Sjögren's syndrome-associated neuropathy. Brain,2005,128 (Pt11):2518-2534.
[2]DelalandeS,deSezeJ,FauchaisAL,et al.Neurologic manifestations in primary Sjögren syndrome:a study of 82 patients.Medicine (Baltimore),2004,83 (5):280-291.
[3]Kuntzer T,Antoine JC,Steck AJ.Clinical features and pathophysiological basis of sensory neuronopathies (ganglionopathies).Muscle Nerve,2004,30 (3):255-268.
[4]SghirlanzoniA,PareysonD,LauriaG.Sensory neuron diseases.Lancet Neurol,2005,4 (6):349-361.
[5]Souayah N,Chong PS,Cros D.Acute sensory neuronopathy as the presenting symptom of Sjögren's syndrome.J ClinNeurosci,2006,13 (8):862-865.
[6]Camdessanché JP,Jousserand G,Ferraud K,et al.The pattern and diagnostic criteria of sensory neuronopathy:a case-control study.Brain,2009,132 (Pt 7):1723-1733.
[7]张君怡,朱以诚,崔丽英,等.反复腹痛四肢无力呼吸困难.中国现代神经疾病杂志,2013,13 (4):354-357.













