患者,男性,80岁。因“反复劳力后胸痛3年,加重2个月”入院。半月前于外院行冠脉造影及PCI术,处理了前降支至左主干,手术耗时4小时,术后症状好转。
心血管病危险因素:高血压史20年;吸烟1包/天×50年。
心电图:窦性心律。
心脏超声心动图:LVEDD 52mm,LVEF 66%。
实验室检查:血肌钙蛋白(-)。
冠状动脉造影结果
选用右侧桡动脉径路,6F血管鞘。造影发现:右优势型,右冠状动脉(RCA)起源异常位于前壁,近端完全闭塞,可见自身桥侧支供应远端循环(图1、图2);前降支近段至左主干中段支架通畅,支架远端60%狭窄;回旋支开口起完全闭塞(图3、图4)。
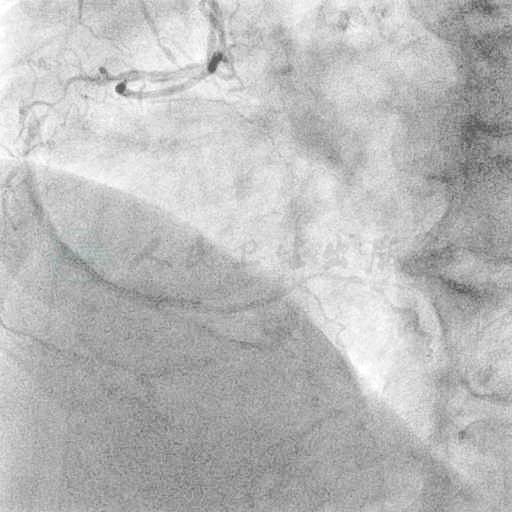
图1 造影示RCA起源异常位于前壁,近端完全闭塞,可见自身桥侧支供应远端循环
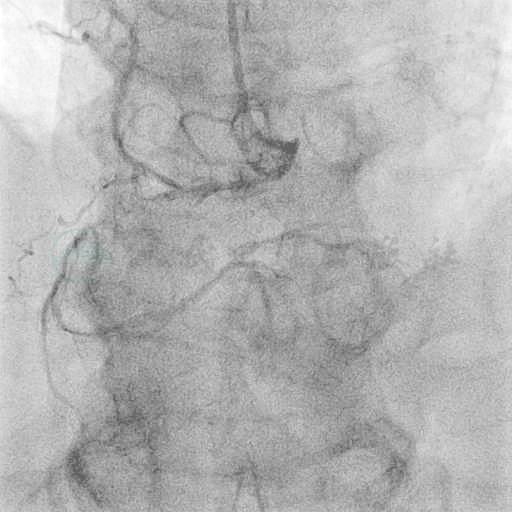
图2 头位造影结果
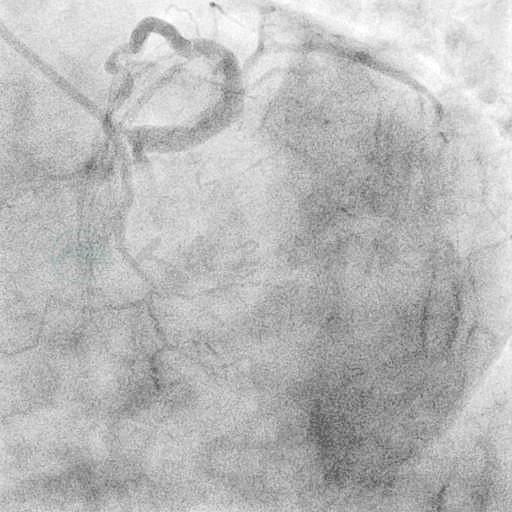
图3 左冠蜘蛛位造影提示前降支近段至左主干中段支架通畅,回旋支开口起完全闭塞
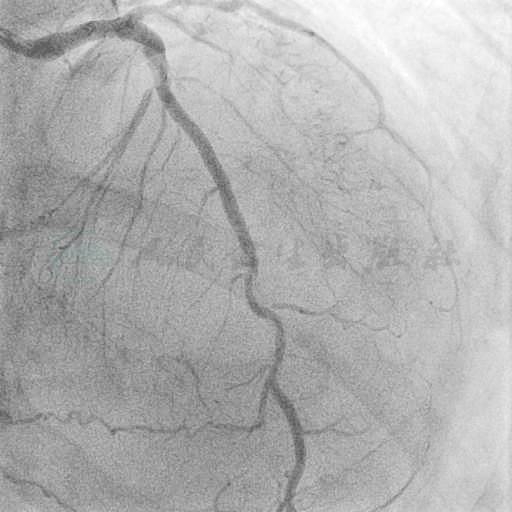
图4 头位造影示前降支近段至左主干中段支架通畅,支架远端60%狭窄
PCI过程
因为本例右冠起源于前壁且为CTO病变,故选择6F AL1.5指引导管以期获得较强的支撑,在Finecross微导管的支撑下,先后尝试Fielder XT、Crosswire NT导丝容易进入桥侧支及夹层(图5、图6),重新仔细调整Fielder XT导丝通过闭塞段进入远端真腔(图7),因为右冠起源于前壁,AL 1.5指引导管同轴性欠佳故支撑不够,Finecross微导管、Sprinter 1.25mm球囊不能通过病变。使用边支球囊锚定、双导丝斑块挤压技术,Sprinter 1.25mm球囊仍不能通过病变(图8、图9)。接延长导丝后,Tornus导管仍不能通过病变(图10)。因手术时间较长,决定结束手术,择期股动脉入路用8F指引导管再次尝试PCI。
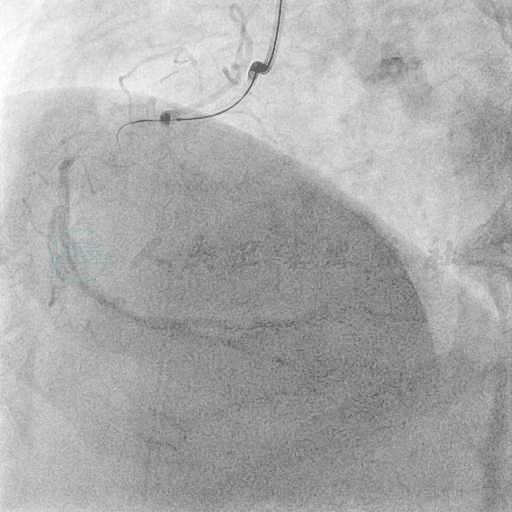
图5 Fielder XT在Finecross微导管支撑下容易进入桥侧支及夹层
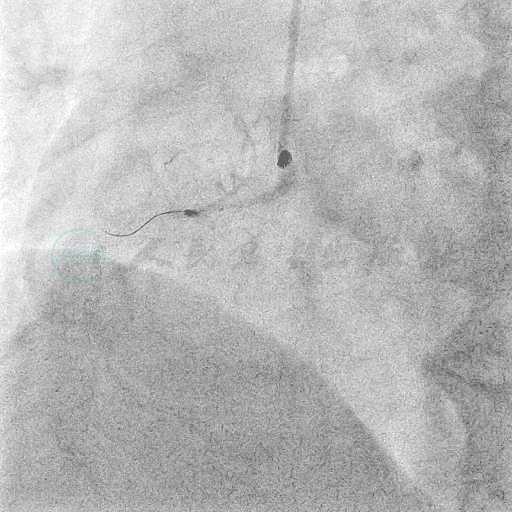
图6 Crosswire NT导丝仍在夹层
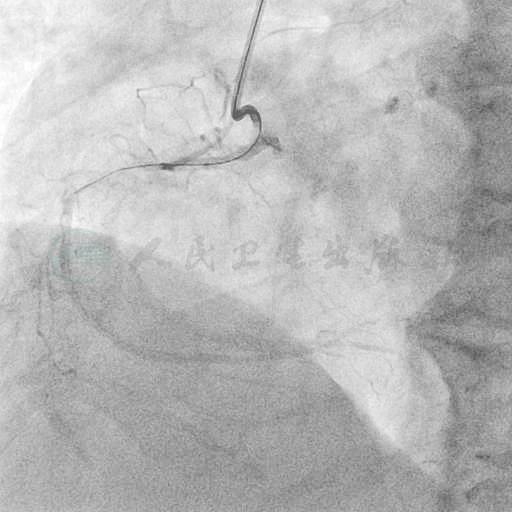
图7 Fielder XT导丝重新调整后进入远端真腔
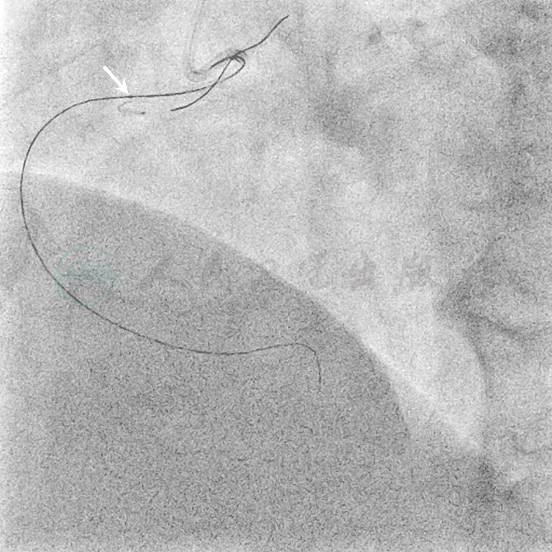
图8 边支球囊锚定后,Sprinter 1.25mm球囊(白箭头所指)仍不能通过病变
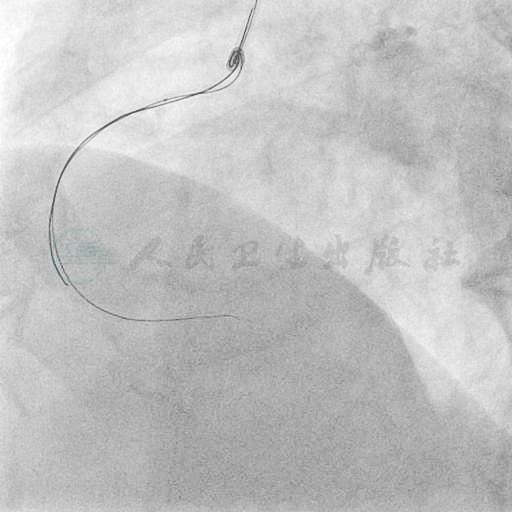
图9 使用双导丝斑块挤压技术,Sprinter 1.25mm球囊仍不能通过病变
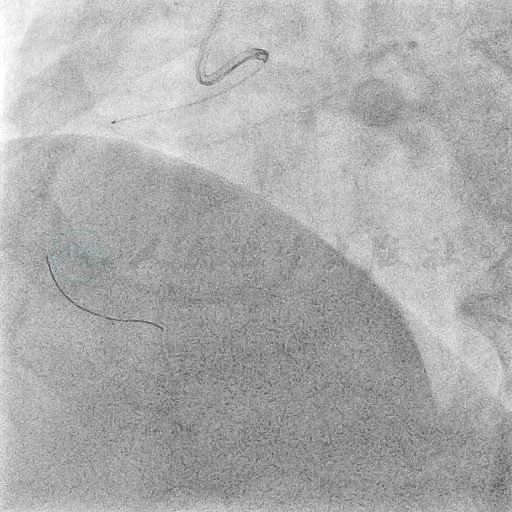
图10 Tornus导管仍不能通过病变
半个月后再次尝试处理RCA病变,采取右侧股动脉径路,8F血管鞘,8F AL1.5指引导管,在Finecross微导管的支撑下,Fielder FC导丝容易通过闭塞段进入远端真腔,但Sprinter 1.25mm球囊即使在病变近端反复扩张后仍不能通过病变(图11),接延长导丝后Tornus导管仍不能通过病变(图12)。考虑原因有两个:一是病变为坚硬的纤维斑块或伴内膜钙化;二是RCA起源于前壁,导致指引导管同轴不佳,支撑不够。因为已经使用了8F AL1.5指引导管,再尝试5进6子母导管、边支锚定等辅助加强支撑技术估计也不能解决问题,最后剩下一个方法即旋磨术。0.009英寸RotaWire旋磨导丝在Finecross微导管支撑下顺利通过病变进入远端真腔(图13),1.25mm旋磨头反复打磨后通过病变,但旋磨头前进时阻力仍然很大,可见指引导管脱离冠脉口(图14);再以1.5mm磨头进一步进行斑块改良(图15),旋磨完成后造影可见前向血流恢复(图16)。2.5mm×15mm Sprinter球囊预扩后顺利植入Promus Element 3.0mm×28mm、3.5mm×28mm支架各一枚,并以Quantum Maverick 3.5mm×15mm进行高压后扩,最后造影结果满意(图17~图22)。
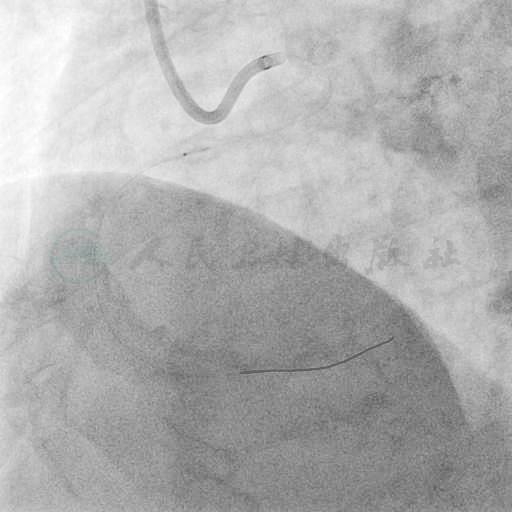
图11 8F AL1.5指引导管支撑下,Sprinter 1.25mm球囊在病变近端反复扩张后仍不能通过病变
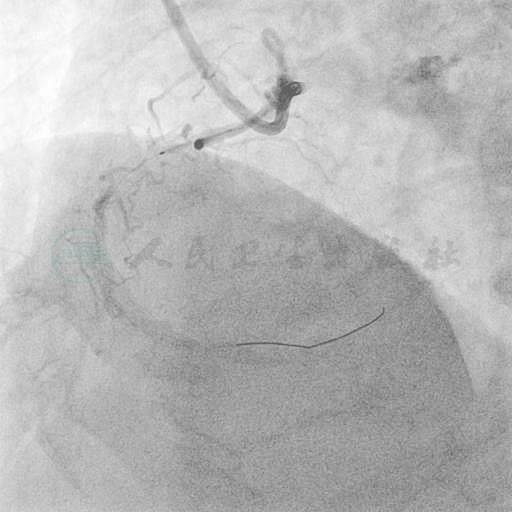
图12 Tornus导管仍不能通过病变
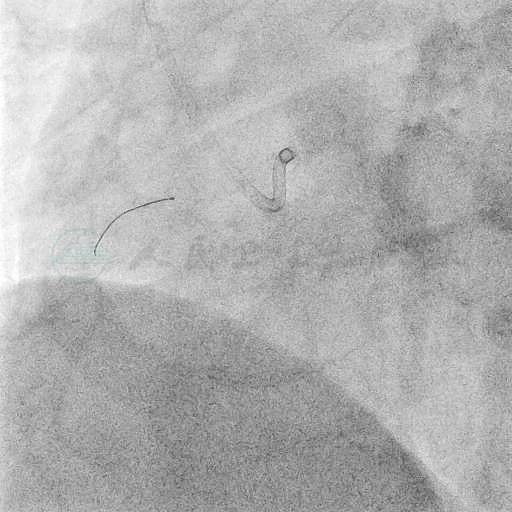
图13 旋磨导丝在Finecross微导管支撑下顺利通过病变进入远端真腔
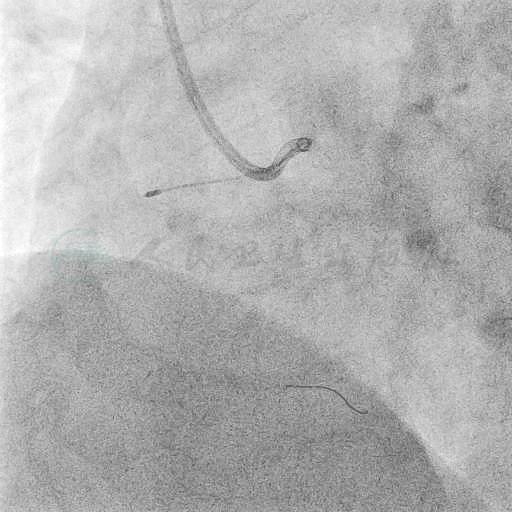
图14 1.25mm旋磨头前进时阻力仍然很大,可见指引导管脱离冠脉口,多次旋磨后通过病变
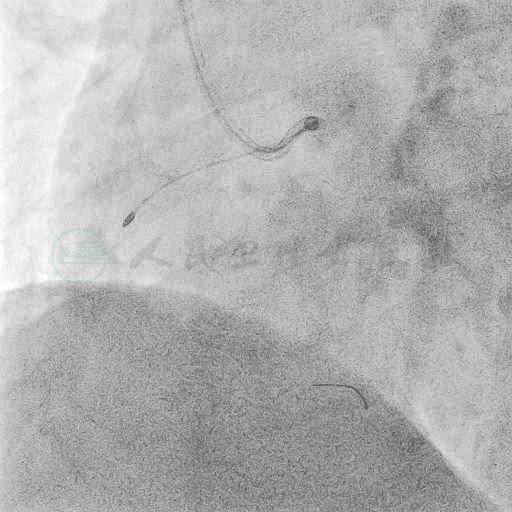
图15 1.5mm磨头进一步进行斑块改良
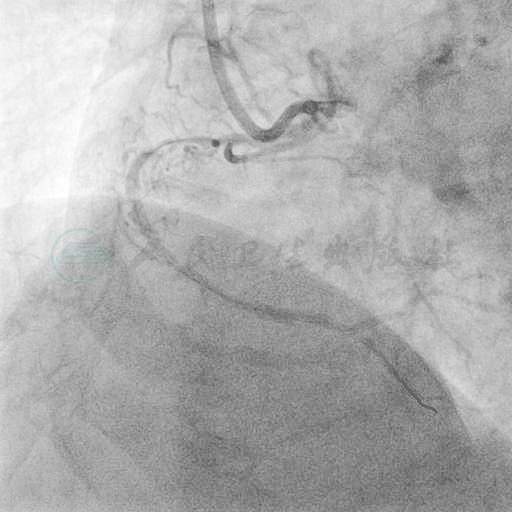
图16 旋磨后造影可见前向血流恢复
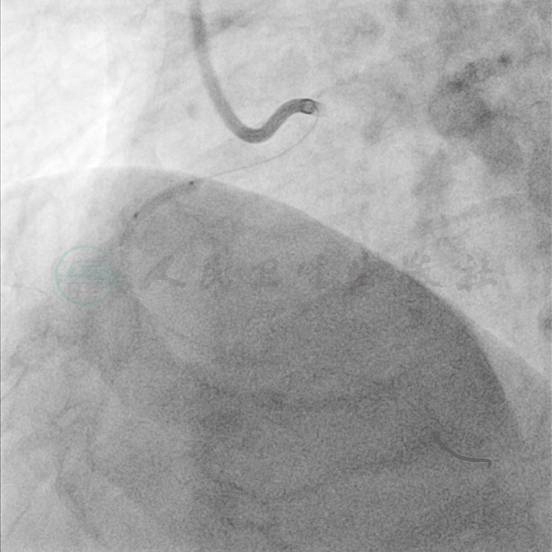
图17 2.5mm×15mm Sprinter球囊预扩
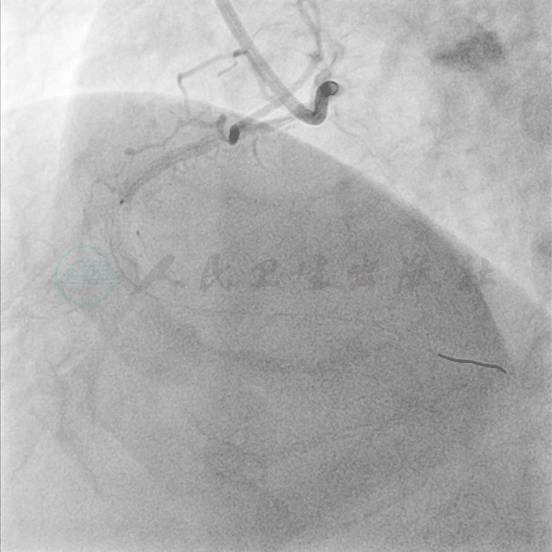
图18 植入Promus Element 3.0mm×28mm支架
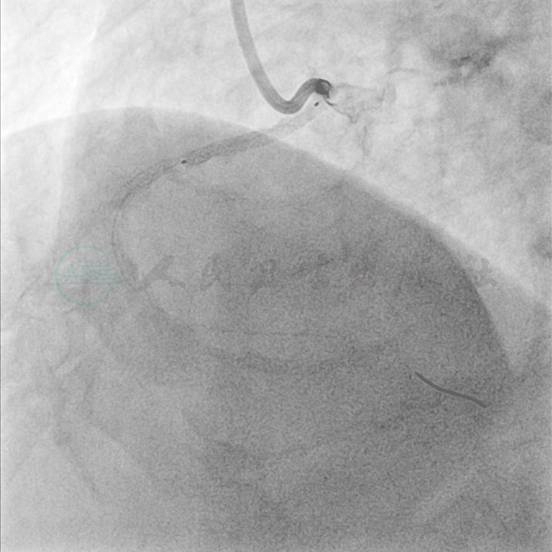
图19 植入Promus Element 3.5mm×28mm支架
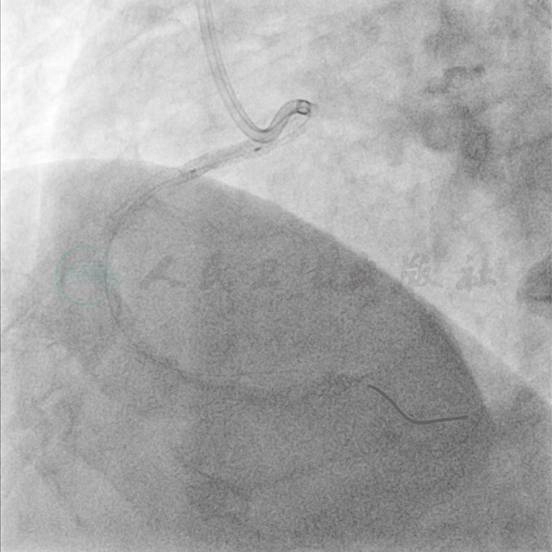
图20 Quantum Maverick 3.5mm×15mm球囊高压后扩
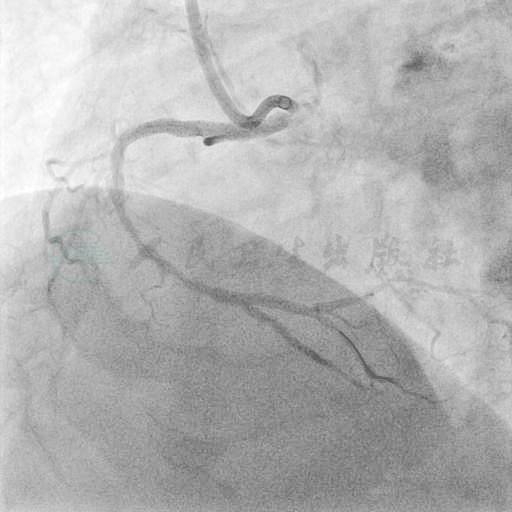
图21 左前斜位造影示最终结果满意
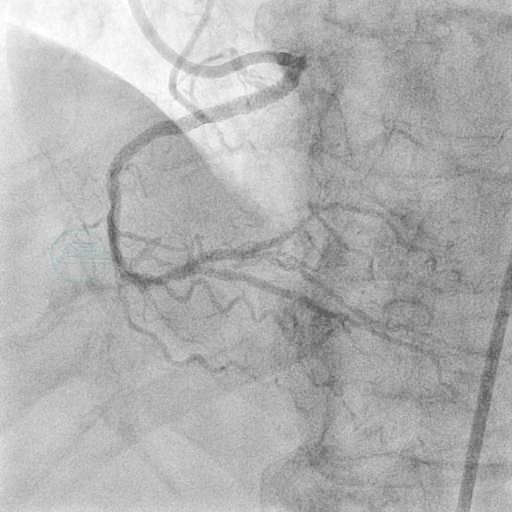
图22 左前头位造影结果













