患者,男性,41岁。因“活动后胸痛2年,加重6个月”入院。1年前曾于当地医院行冠状动脉造影并植入1枚支架,出院后未复查造影。
心血管病危险因素:高血压史3年。
心电图:窦性心律、心肌缺血。
心脏超声心动图:LVEDD 47mm,LVEF 60%。
实验室检查:未见明显异常。
入院后给予阿司匹林及氯吡格雷治疗后行冠状动脉造影。
冠状动脉造影结果
造影选用右侧桡动脉径路,6F血管鞘。造影结果显示:左主干未见明显狭窄,前降支近中段30%左右狭窄,回旋支未见明显狭窄,远端向右冠状动脉远端形成逆向灌注,右冠状动脉近段完全闭塞,中段可见支架影(图1~图3)。
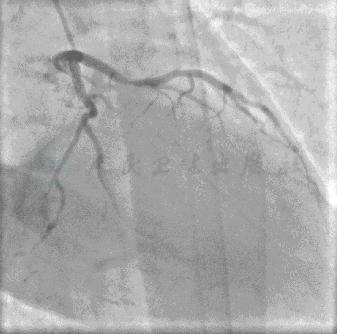
图1 回旋支未见明显狭窄,远端向右冠状动脉远端形成逆向灌注
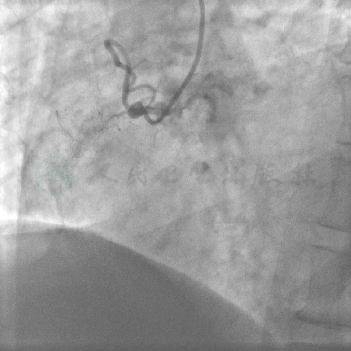
图2 右冠状动脉近段完全闭塞,中段可见支架影
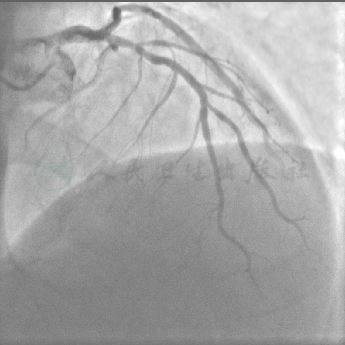
图3 左主干未见明显狭窄,前降支近中段30%左右狭窄
PCI过程
考虑患者病变时间长,闭塞段较长,病变较硬,我们选择支撑力较强的6F AL0.75SH指引导管,在微导管的支持下选择Cross-it 200导丝尝试刺破闭塞段起始(图4、图5)。导丝走行似乎较顺利,最终将导丝送入远端,正向造影无法确认导丝是否走行于血管真腔内,进行对侧造影(图6)。穿刺右侧股动脉,置入6F血管鞘,应用6F JL4造影导管行左冠状动脉造影。造影结果显示:导丝头端并未走行于真腔内(图7)。将导丝撤回至血管中段,重新调整导丝方向,再次反复向前推进,尝试进入血管真腔。但反复尝试经对侧造影显示导丝均未走行于血管真腔(图8、图9)。至此手术遇到瓶颈。
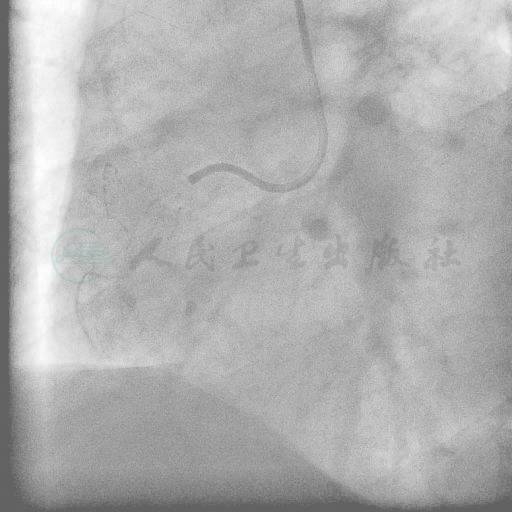
图4 选择 6F AL0.75SH指引导管,在微导管的支持下选择Cross-it 200导丝
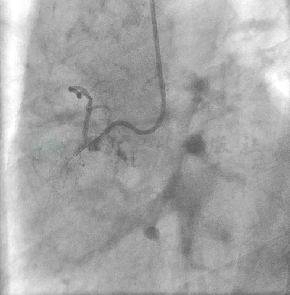
图5 Cross-it 200导丝尝试刺破闭塞段起始
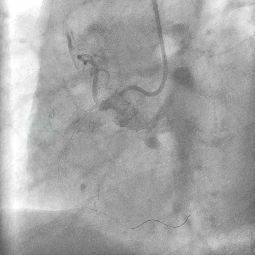
图6 Cross-it 200导丝送入远端,正向造影无法确认导丝是否走行于血管真腔内
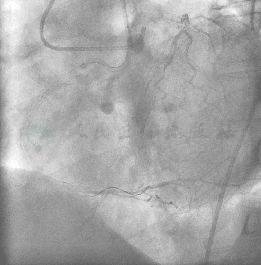
图7 对侧造影显示导丝头端并未走行于真腔内
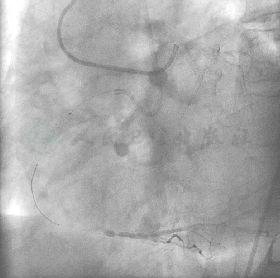
图8 反复尝试经对侧造影显示导丝均未走行于血管真腔
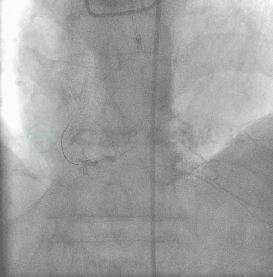
图9 反复尝试经对侧造影显示导丝均未走行于血管真腔
患者目前一般状况良好,无不适主诉,血流动力学稳定。对于下一步的处理策略选择:①终止手术,患者药物治疗,经一段时间修复血管内夹层后再重新尝试开通;②改为应用逆向导丝技术,尝试通过回旋支的侧支循环逆向通过闭塞段;③更换导丝,继续尝试前向进入远端血管真腔内。我们分析,患者目前血流动力学稳定,无不适,手术进行时间不长,造影剂未过量,目前尚无必须立即终止手术的征象,且从造影结果来看远端管腔并未受到过多累及,可继续尝试。此外,患者回旋支至右冠的侧支迂曲而细小,且逆向灌注走行短,闭塞段长,应用逆向导丝技术并不一定能顺利通过闭塞段,反而增加风险,故我们决定继续尝试前向开通。
我们更换导丝为Conquest Pro,重新进入闭塞病变,经过反复尝试后到达血管远端,期间反复行对侧造影,最终证实导丝进入远端血管真腔内(图10、图11)。
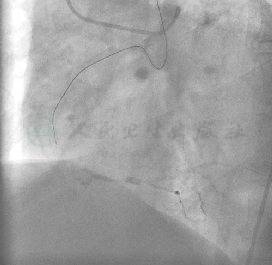
图10 更换导丝为Conquest-Pro到达血管远端
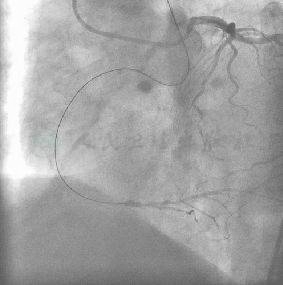
图11 对侧造影证实导丝进入远端血管真腔内
经交换导丝撤出微导管。选择Sprinter 1.25mm×15mm的球囊反复尝试无法通过中段病变(图12),考虑既往支架段球囊难以通过,决定采用锚定技术。送入Rinato导丝至窦房结支,送入Sprinter 1.5mm×15mm 球囊,随后主支送入 Apex 1.5mm×8mm的球囊,将分支球囊以8个大气压打开锚定后,主支球囊顺利通过右冠病变到达远端,由远端至近端扩张病变(图13、图14)。撤出球囊,再次送入微导管至远端,利用Rinato导丝交换Conquest Pro导丝。撤出微导管,选用Braun 2.0mm×20mm的球囊送入右冠内再次扩张病变后(图15~图17)。由远端至近端分别植入BuMa 3.0mm×35mm支架、BuMa 3.0mm×35mm支架、BuMa 3.5mm×35mm支架(图18~图20)。选用Dura Star 3.0mm×20mm的后扩张球囊扩张支架接头(图21、图22)。最后造影结果见图23、图24。
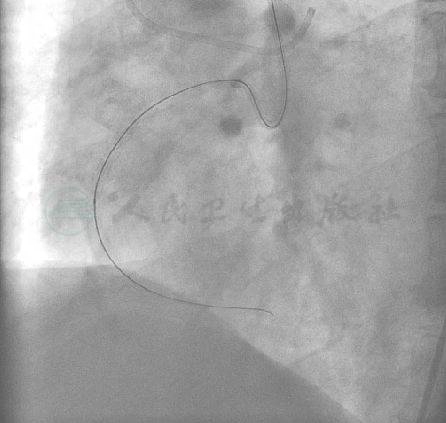
图12 选择Sprinter 1.25mm×15mm的球囊反复尝试无法通过中段病变
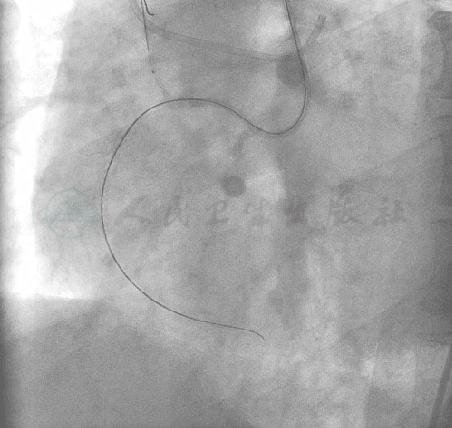
图13 采用锚定技术
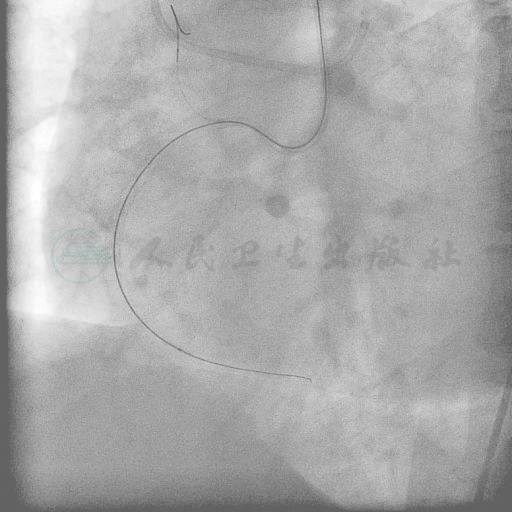
图14 主支球囊顺利通过右冠病变到达远端
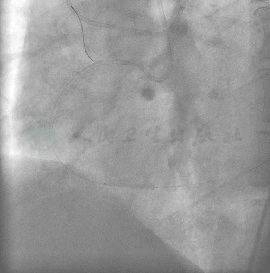
图15 撤出球囊,再次送入微导管至远端,利用Rinato导丝交换Conquest-Pro导丝
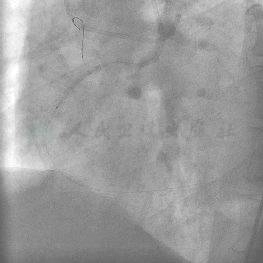
图16 撤出微导管,选用Braun 2.0mm× 20mm的球囊送入右冠内再次扩张病变
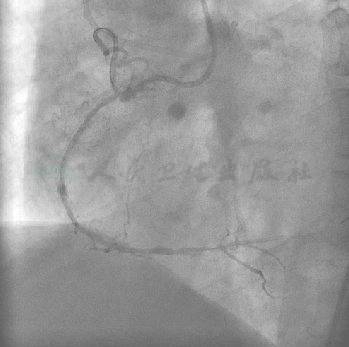
图17 球囊扩张后造影
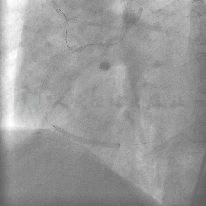
图18 RCA远端植入BuMa 3.0mm×35mm支架
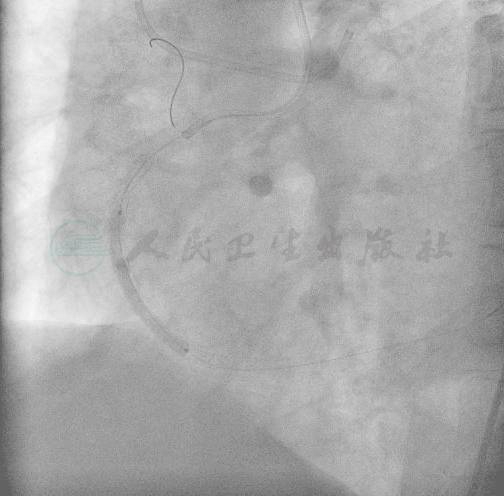
图19 RCA中段植入BuMa 3.0mm×35mm支架
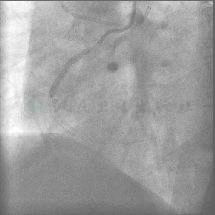
图20 RCA近端植入BuMa 3.5mm×35mm支架
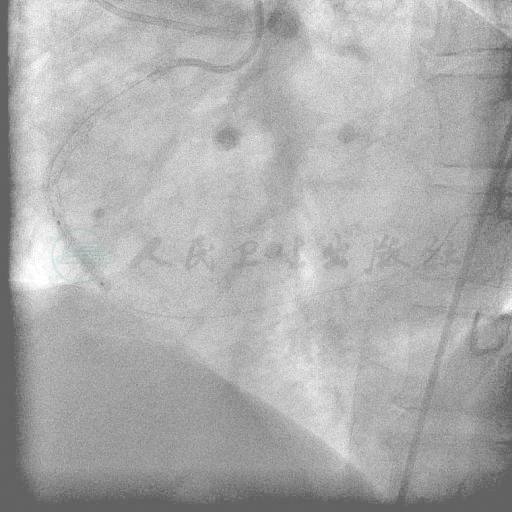
图21 Dura Star 3.0mm×20mm的后扩张球囊扩张支架接头
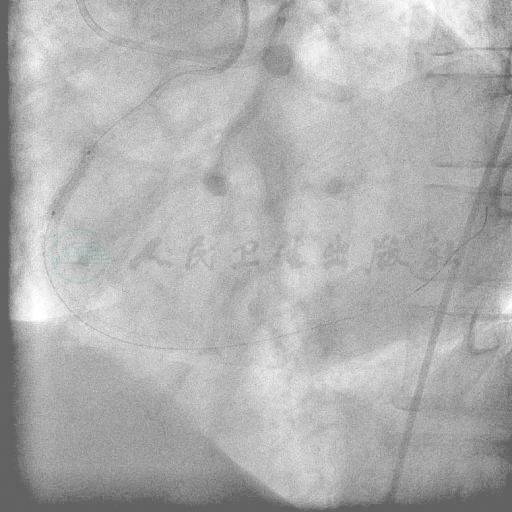
图22 Dura Star 3.0mm×20mm的后扩张球囊扩张支架接头
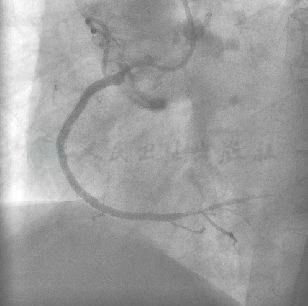
图23 最终结果
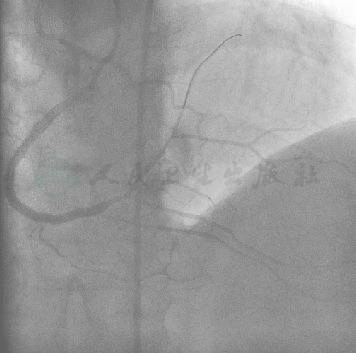
图24 最终结果













