 去看看
去看看


导鞘内部装有可防止漏血的单向活瓣,穿刺动脉成功后经导丝将导鞘送入血管,拔出鞘芯,即在皮肤表面和血管腔之间建立了一条安全的过渡通道,保证在进行随后的造影和腔内操作时避免无谓的血液丢失,而且减少了导管和导丝交换时对血管壁损伤。导鞘适用于几乎所有造影及腔内治疗操作。
导鞘的大小取决于腔内治疗的方案和相应通过器械的直径。一般来说,导鞘直径从4F到10F不等(3F=1mm),在进行主动脉腔内修复术时,由于支架血管直径粗大,常需要应用20F甚至更粗的导鞘。通常情况下,导鞘长度大都在15cm左右。有时,导鞘长度可以达到60cm,甚至90cm,这就是所谓的长鞘。长鞘的作用是可以将弯曲的动脉(如髂股动脉)拉直,还可以减少反复交换导管等器械时对血管壁的损伤,便于球囊导管和支架的传输,使腔内操作更加安全快捷。长鞘适合应用于颈动脉、锁骨下动脉、肾动脉及对侧下肢动脉的腔内治疗操作。
导丝可以分为多种类型,主要根据直径、长度、尖端形状、内芯硬度、防摩擦外涂层等不同来区分(图1)。但所有导丝共同的基本作用是可以通过各种不同情况的血管,包括扭曲、狭窄甚至闭塞的血管,从而辅助导管及其他腔内治疗器械进入目标血管,因此导丝在血管腔内治疗中发挥着至关重要的作用。

图1 各种不同类型导丝
各种导丝均至少由两层结构组成,内部芯轴和外套。内部芯轴保证导丝的整体硬度和旋转操控性。内芯自导丝主体至尖端逐渐移行变细,因此导丝尖端比主干柔软。有些导丝的内芯可以抽出,以此来调整导丝的强度,或者从中心腔内注射药物。导丝外套大多为细不锈钢丝绕成的弹簧状套管,使导丝具有一定的柔顺度和减少摩擦。有些导丝外表面有一层亲水性涂层,如聚四氟乙烯(TEFLON)等,可以进一步减少摩擦。所有导丝的尖端3~20cm较柔软,可以避免推进时损伤血管。
导丝直径一般有0.038英寸(1英寸=2.54厘米)、0.035英寸,0.025英寸,0.018英寸和0.014英寸等型号。其中0.035英寸最常用,可适用于大多数造影及腔内治疗需要,直径小于0.018英寸的一般被称为微导丝,适合于处理一些直径细小动脉的严重狭窄甚病变。一般来说,标准的球囊导管或支架都可以通过0.035英寸以上导丝,而适用于小血管的腔内治疗器械,只能通过0.018英寸甚至0.014英寸的微导丝。
导丝长度一般分为150cm,180cm,260cm和300cm等型号,绝大多数部位的动脉造影都可以采用180cm以内的导丝来完成,但如果需要应用球囊或支架进行腔内治疗时,往往需要应用260cm甚至300cm的长导丝。除非目标血管距入路穿刺点在30~40cm左右,或是应用快速交换型球囊或支架,此时也可以使用短导丝来进行器械的交换,从而完成腔内治疗。
根据尖端形状不同,导丝可以分为柔软型、直头和弯头等类型。一般来说,初始造影和病变血管评估时选用弯头的J形导丝,可以减少损伤血管的可能。在经过造影,明确病变部位和特点后,可以更换为柔软型、直头或尖端塑形的导丝通过病变。
根据内芯硬度不同,导丝又可以分为标准型、加硬型和超硬型等。在导丝通过病变后,可以提供内支撑力,保证随后的球囊导管及支架等器械的通过。导丝的硬度决定了随后跟进的腔内器械的容易程度,特别是需要通过严重狭窄或扭曲的病变血管,或是需要跟进直径比较大的球囊、支架或支架血管时,常常需要高硬度的导丝作为支撑。如果单纯依靠导丝仍不能提供足够的内支撑力,通常需要导引导管(guiding catheter)或长鞘来提供和加强外支撑力,从而便于腔内器械到达目标血管。
【应用导丝技巧】
1.在操作过程中,随时用肝素盐水擦洗、湿润导丝,可以减少摩擦力,提高导丝的通过性,尤其是对于表面附有亲水涂层的导丝。亲水性导丝在通过穿刺针时,外涂层很容易划伤,因此在穿刺时尽量使用导鞘配带的导丝。
2.导丝在前进时一定要在透视下进行,注意观察导丝尖端的形状,尤其在处理动脉硬化狭窄的血管时。导丝前方有阻力时切不可强行通过,防止损伤血管壁形成夹层或动脉破裂。
3.在导丝通过严重硬化狭窄病变时,为防止导丝尖端引起夹层,可以将导丝尖端形成一个回弯,待通过狭窄病变恢复原状。
4.导丝一旦到达目标位置,一定保证导丝位置不动,直到所有检查和治疗完成。交换导管时助手扶住导丝,如果导丝在体外过长,为防止导丝尾部易位被污染,可以用无菌单压住导丝。一旦导丝污染,需要重新更换。
导管的作用是提供一个进入目标血管的通道,便于下一步进行造影或腔内治疗。导管一般长度在65cm和150cm之间,短者用于腹主动脉近端内脏分支或分叉处病变的造影,长者可以用于远距离的头臂动脉分支或对侧下肢远端血管到达。与导鞘不同,导管有外径和内径两个参数。导管用外径表示其粗细,单位也用F,一般在4F和6F之间,6F导管可以通过6F导鞘或指引导管;内径用英寸表示,表明容许通过的导丝直径,如0.038英寸或0.035英寸。微导管外径一般只有2F或3F,可以通过普通的4F导管内部,用于进行分支血管的超选择性操作。
导管种类繁多,主要根据尖端不同形状、长度、硬度及顶端是否有侧孔等分类。其中,导管头端形状是在选择各种导管时最重要的参数(图2)。
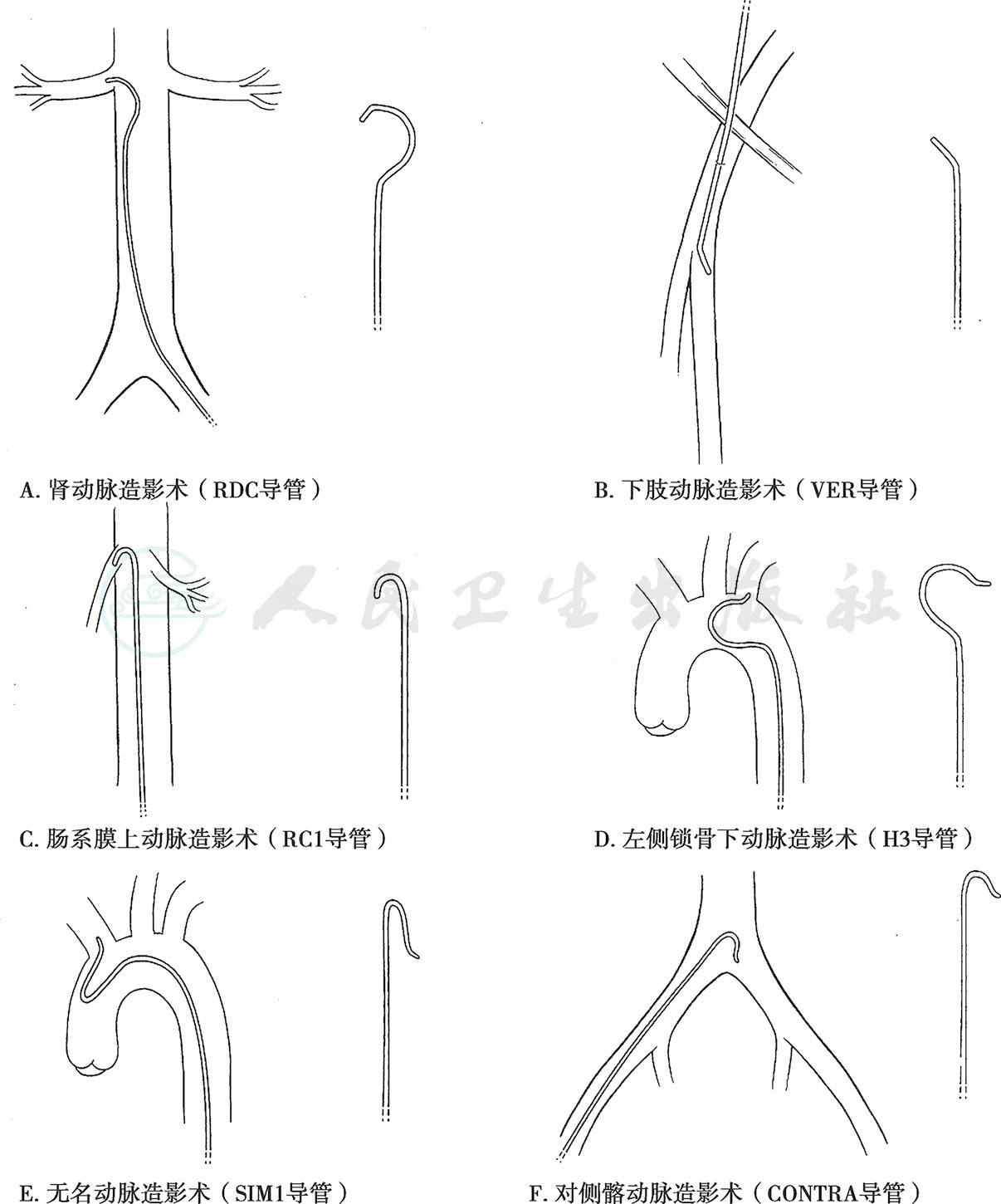
图2 各种不同类型导管
导管按其用途不同可以分为三类:诊断性导管、选择性导管和指引导管。
(1) 诊断性导管:通常置于大血管内进行血管造影,材料一般为尼龙,可以承受高压。导管头端有一个端孔和多个侧孔,这样对比剂可以向各个方向散开,大动脉血流速快,局部可以形成对比剂高浓度区域,显影效果好,而且减少对血管损伤,可以用于高压注射器造影。最常用的诊断性导管有猪尾导管和腔静脉导管等。猪尾导管头端卷曲呈猪尾样,一般用于各主动脉等大动脉造影,有时也可以用于髂总动脉等中等血管造影,此时由于血管直径小,导管尖端没有完全弯曲成形。腔静脉导管头端为直型,适用于上、下腔静脉的造影。
(2) 选择性导管的头端形状各异,只有一个端孔,可以协助导丝选择进入血管及其分支,也可以用来进行节段性测压、局部取血或注射各种药物等。材料一般为聚乙烯,因此更加柔软,便于配合导丝前进和后退。目前常用的有椎动脉导管( VER)、眼镜蛇导管( COBRA)、席梦思导管(SIMMONS)、多功能导管(MPA)等。
(3) 指引导管:是一类特殊的导管,与其他造影导管相比,管腔内径至少增大一倍,管壁支撑力强,可提供一个固定管腔用于导丝导管的交换和其他腔内治疗器械的通过,其作用与长鞘类似。尤其适用于对内脏动脉及头臂动脉等分支动脉病变腔内治疗时,应用指引导管可以简化操作,减少反复交换器械的阻力,避免可能造成的血管损伤。指引导管长度一般为45~100cm,内径为 6~9F。
【应用导管技巧】
1.导管在前进和后撤时必须在导丝指引下进行,以防止导管尖端损伤血管壁。
2.导管在前进和后撤时一定要控制住导丝,防止导丝移动。助手应不断用盐水擦洗导丝,减少其阻力。每次用导管前要用肝素盐水冲洗管腔,撤回的导管也要将内外积血冲洗干净。
3.在将导管连接至高压注射器造影前,应该用普通注射器手推少量对比剂以确认导管头端位置,确保在血管腔内。如果导管尖端顶住血管壁,在高压造影时可能会导致血管壁损伤。
4.造影时尽量将导管靠近目标血管,一方面可以减少其他血管的干扰,使目标血管显影更加清楚;另一方面,也可以减少对比剂的应用。
5.在腔内治疗过程中,需要保持导丝通过病变血管,直到确认治疗结束,期间需要反复造影,明确球囊和支架的位置,此时,指引导管可以发挥重要作用。
6.在处理肾动脉等成角大的分支病变时,由于跨病变导丝长度短,无法为随后的球囊和支架等腔内器材提供足够的内支撑力,此时指引导管可以提供很好的外支撑力。
7.与长鞘不同,指引导管头端没有渐细的扩张器,因此前进时需要在X线引导下小心进行,防止对血管壁的损伤;另外,指引导管也没有止血阀,因此尾端需要加装Y型头,从而减少出血,便于造影。
8.应用席梦思(SIMMONS)等“∩”形头端的导管时,由于主动脉直径小,有时头端难以塑形。此时可以利用髂动脉或锁骨下动脉等分支,把导管尖端挂住分支,然后前进导管主体,从而完成头端折叠塑形。但是这种塑形方法有可能会造成斑块脱落,远端栓塞风险,最安全的塑形方法还是把导管前进到升主动脉,此处主动脉直径宽,一般可以成功塑形(图3、图4)。
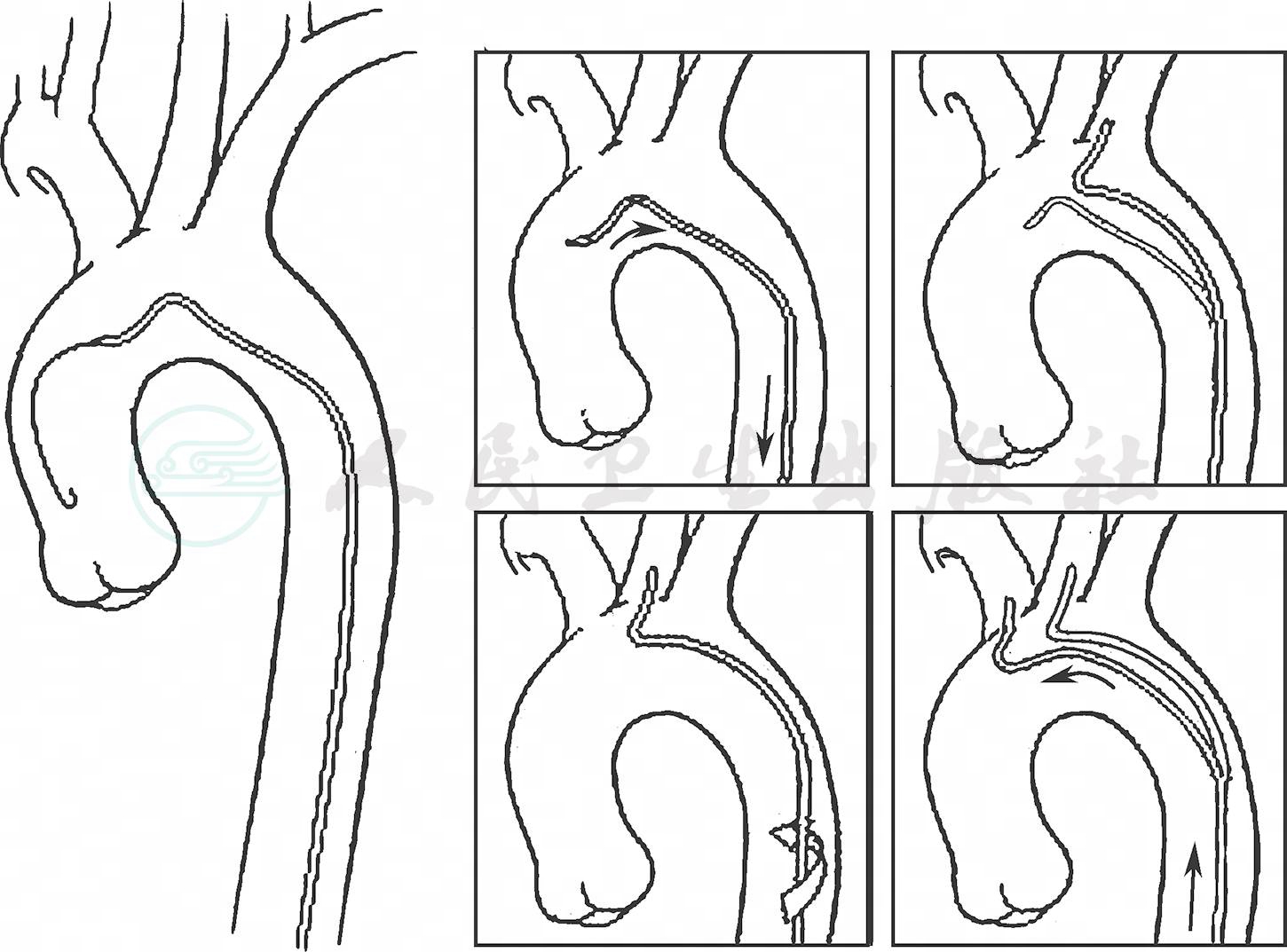
图3 SIMMONS导管于左侧锁骨下动脉开口塑形
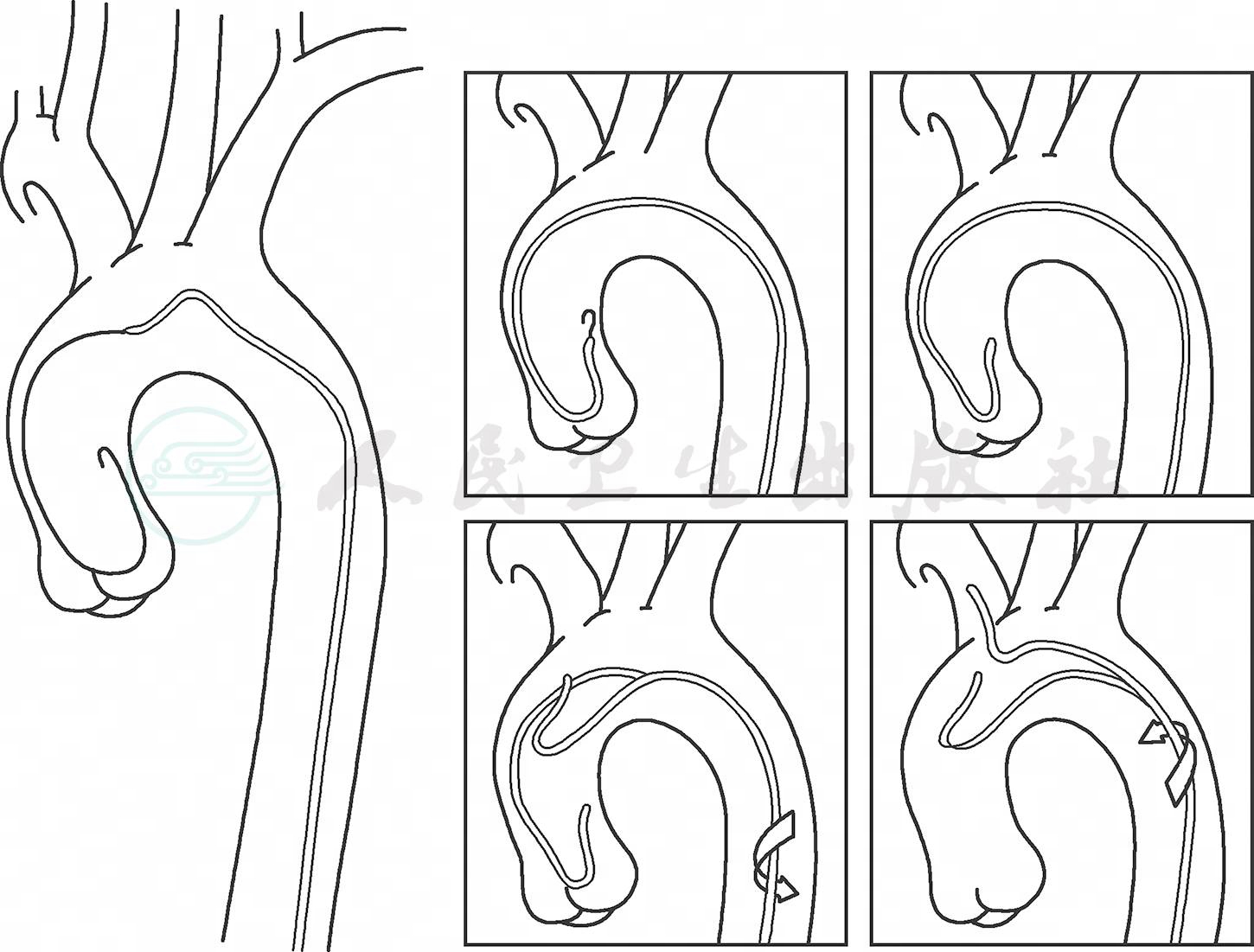
图4 SIMMONS导管于升主动脉塑形
球囊导管是腔内治疗中应用很广泛的器械,其作用是将狭窄或闭塞的动脉扩张成形,重新恢复动脉管腔的通畅性。理想的球囊导管都有一个重要特性,即在设定的压力下球囊可以膨胀达到规定的直径。
球囊导管可以分为顺应性球囊和非顺应性球囊两大类。顺应性球囊由普通弹性材料制成,球囊在压力作用下会不断膨胀增大,当遇到阻力时,球囊会发生变形,向阻力小处扩张,导致对周围作用压力减少,而且容易损伤到正常血管壁,因此限制了其应用。目前主要用于主动脉腔内修复术后扩张支架型血管,使其与血管壁贴合更紧密。非顺应性球囊由聚对苯二甲酸乙二醇酯等合成材料制成,可以承受很高的压力。当球囊在压力作用下膨胀达到设定直径后不会继续增大,因此可以保持对周围狭窄部位施以较高的压力,这对于治疗严重钙化狭窄的外周动脉病变是十分必要的。目前临床应用的绝大部分腔内治疗球囊都是非顺应性球囊。
一般来说,球囊导管有如下一些常用参数:扩张后球囊的直径(mm)与长度(cm);球囊推送杆主体长度(cm);可以通过的导鞘直径(F);允许通过的最粗导丝(英寸);球囊容许最大爆破压(atm)等。
球囊直径的选择是通过造影后测量病变段动脉附近正常动脉直径来决定,可以选择2~25mm不等。一般直径超过参考血管直径的10%~20%。球囊的长度根据病变长度来选择,应该完全覆盖动脉病变段。为增加可通过性,绝大多数球囊外表面有亲水涂层,但对于球囊扩张型支架,为了防止支架中途脱落,外表面则无亲水涂层(表1)。
球囊推送杆的长度在60~150cm不等,一般根据病变距离远近来选择。应该尽量选用推送杆短的球囊导管,这样便于交换和输送。长推送杆的球囊,由于推送阻力大,交换时需要应用质硬导丝加强内支撑,或应用长鞘或指引导管作为外支撑。
切割球囊是一类特殊的球囊导管,其球囊表面有三到四条刀片沿长轴纵行分布,主要应用于一些顽固性质硬动脉病变,此时应用普通球囊无法扩张成形,比如支架内再狭窄或移植物再狭窄等。切割球囊有时也可以应用于一些细小血管病变,不适宜放置支架时,如胫腓动脉等处的病变。应用切割球囊时需要注意,不能过度扩张,防止血管破裂;也不能应用于闭塞病变,防止血管破裂;由于球囊质硬,扩张和回缩时要缓慢,减少对血管壁的损伤,压力一定不能超过爆破压力。
表1 不同部位血管的球囊选择
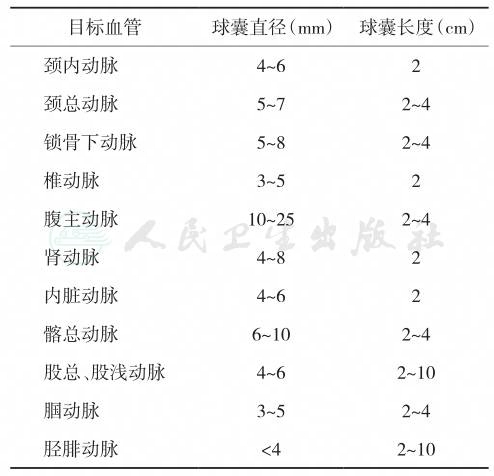
| 目标血管 球囊直径(mm) 球囊长度(cm) |
| 颈内动脉 4~6 2 颈总动脉 5~7 2~4 锁骨下动脉 5~8 2~4 椎动脉 3~5 2 腹主动脉 10~25 2~4 肾动脉 4~8 2 内脏动脉 4~6 2 髂总动脉 6~10 2~4 股总、股浅动脉 4~6 2~10 腘动脉 3~5 2~4 胫腓动脉 <4 2~10 |
【应用球囊导管的技巧】
1.在完全覆盖病变的前提下尽量选用短球囊,球囊刻度两端“肩部(shoulder)”应尽量短,以减少对正常血管的损伤。
2.在对动脉分叉处病变扩张时,为避免影响其他分支动脉,可以在两分支动脉内同时应用球囊扩张,这称为“对吻”球囊(kissing balloon)技术。
3.球囊扩张时应逐渐增加压力,扩张时间一般为30秒~3分钟,以减少对血管壁的损伤。各型号球囊的最大爆破压不同,应注意不要超过限定压力,避免球囊破裂。
4.对长病变段血管扩张时,尽量选用长球囊一次扩张,避免用短球囊反复扩张,以减少远端栓塞的可能性和血流阻断时间。但是在处理髂外动脉等迂曲血管病变时,可以选用短球囊扩张,防止长球囊拉伸血管导致的血管壁损伤。
单纯行球囊扩张血管成形术容易产生一系列问题,如血管弹性回缩、形成夹层和术后再狭窄等。为了解决这些问题,血管内支架应运而生。所有血管支架的共同特点是都对血管腔有支撑和扩大的作用,因此可以防止血管回缩,提高血管远期通畅率。
目前临床应用的支架分类很多,按照制作材料不同,支架可以分为不锈钢支架和镍钛合金支架。按照制作方式分为编织型、激光镂刻型和弹簧圈型支架。按照表面涂层不同,可以分为裸支架和药物涂层支架。
最具有临床意义的是按照释放方式不同将支架分为自膨式支架和球囊扩张式支架(图5、图6)。自膨式支架特点是柔顺度高,不容易发生晚期支架变形,但定位欠佳,存在释放后短缩现象。适用较迂曲的血管,主要用于治疗髂动脉、股动脉和颈动脉的病变。影响自膨式支架膨胀性的因素有支架结构和材料,目前常用材料为不锈钢和镍钛合金。早期的支架皆为不锈钢材料,最具代表性的是Wallstent TM(BOSTON),但后期的大部分支架都采用常温记忆金属―镍钛合金。这种镍钛合金支架当温度降低时可以变形,压缩到很小的推送杆内,在体内定位释放后,在常温下会自动塑形为支架形状。不锈钢编织支架的优点是,当释放部分小于85%时,可以回收支架,重新定位释放,这是即使到目前大多数支架都没有的优点。不锈钢编织支架的缺点是体内释放后长度回缩大,即回缩比大,因此定位不准确;而且支架两端径向支撑力小于镍钛合金支架。镍钛合金支架为激光镂刻制成,其显著优点是回缩比小,因此其释放定位比较准确,适用于一些重要分支血管病变的治疗。

图5 自膨式支架释放过程
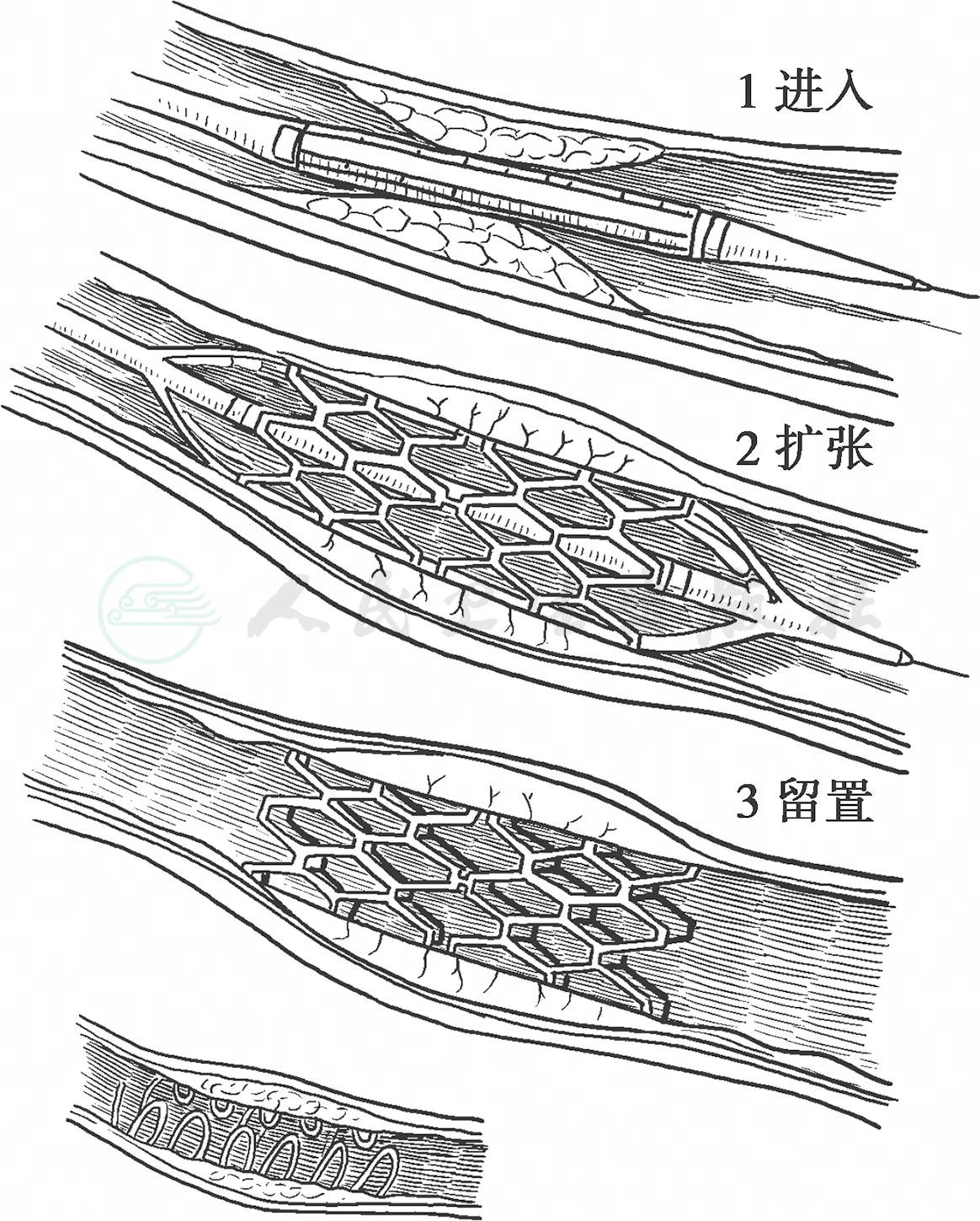
图6 球囊扩张式支架释放过程
球囊扩张式支架特点是定位非常准确,支撑力强。球囊膨胀的直径不同,决定了支架的最后直径大小,如果预估直径过小,可以再次扩张。球囊扩张式支架缺点首先是直径固定,因此不能用于跨过动脉分支等直径改变的血管,比如髂总动脉、髂外动脉,或颈总动脉、颈内动脉。另外,由于球囊扩张式支架弹性差,在动脉壁长期压力下可能会发生不可逆变形,因此不能用于迂曲血管病变。球囊扩张式支架一般适用于肾动脉、内脏动脉和椎动脉等动脉开口处病变。PALMAZ支架是最早的球囊扩张式支架,目前第五代产品Genesis TM(CORDIS)已经在临床应用,其支架网格趋向更小,架构趋向更薄,而径向支撑力保持不变。
另外,腘动脉等关节处适合应用柔顺性更高的弹簧圈型支架,如IntracoilTM(EV3)支架。对于膝下动脉等细小分支动脉,可以应用药物洗脱支架,来抑制血管内皮过度增生,从而提高血管远期通畅率。药物洗脱支架代表了支架治疗领域的最新进展,主要着力于解决支架术后再狭窄的问题。外涂层药物包括抑制细胞增生、免疫抑制和促进内皮细胞修复等几类。目前最常用的药物有西罗莫司和紫杉醇,前者是一种大环内酯类抗生素,还具有免疫抑制的作用。后者是一种抗肿瘤药物,可以有效抑制细胞的分裂和增殖。外涂于支架表面的药物通过孔隙缓慢释放于周围血管壁组织,可以抑制局部的体液免疫,从而避免由此诱发的炎症因子和生长因子的活化。临床循证医学证实,药物洗脱支架可以明显降低冠脉支架术后的再狭窄率,但是可以应用于外周动脉的药物洗脱支架仍在临床试验中(表2)。
表2 血管腔内治疗常用支架类型
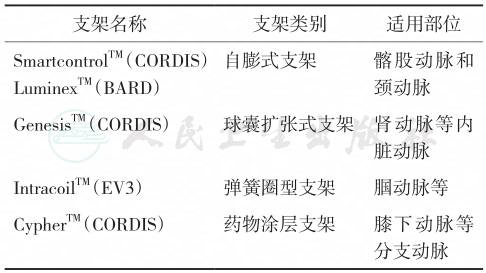
| 支架名称 支架类别 适用部位 |
| SmartcontrolTM(CORDIS) LuminexTM(BARD) 自膨式支架 髂股动脉和 颈动脉 GenesisTM(CORDIS) 球囊扩张式支架 肾动脉等内 脏动脉 IntracoilTM(EV3) 弹簧圈型支架 腘动脉等 CypherTM(CORDIS) 药物涂层支架 膝下动脉等 分支动脉 |
在应用支架时,需要注意以下一些常用参数:支架直径(mm)与长度(cm);释放系统推送杆长度(cm);可以通过的导鞘或指引导管内径(F);允许通过的导丝(英寸)。选择支架的直径和长度的测量方法和应用球囊的方法基本相同,但选择支架时一般应该比使用的球囊长1~2cm,以保证球囊扩张时被破坏的血管内皮层能够得到完全覆盖。大部分支架可以通过6~8F的导鞘,还要根据病变血管离穿刺点距离选择适合的推送杆。
【应用支架的注意事项】
1.应用球扩式支架时,在通过迂曲狭窄的病变血管时,支架容易发生脱落,这点和自膨式支架不同,因为自膨式支架一般有外鞘保护。预防方法是,应用长鞘或指引导管作为外保护,同时可以减少支架传输过程中的阻力。
2.应用自膨式支架时,一般比目标血管直径稍大1~2mm,如果测量值过小,会导致支架贴壁不好,即使用球囊后扩张也无法完全贴壁,除非在内部再放置一个直径更大的支架作为支撑,这点和球囊扩张式支架不同。
支架血管是将血管内支架和外科旁路移植术相结合的产物,它是把血管移植物外衬或内附于血管支架上,用来治疗血管疾病(图7)。目前,支架血管已经广泛用于动脉瘤、动脉夹层或破裂、动静脉瘘等疾病的治疗。还有人将支架型血管用于长段的下肢动脉闭塞,但其远期通畅率有待进一步观察。与裸支架相比,由于有血管移植物的存在,其输送器直径更粗,一般需要8F以上的导鞘。当输送器直径超过10F时,往往需要行入路动脉切开。

图7 支架血管治疗胸主动脉瘤
目前,在国内上市的应用于周围动脉的支架血管 主 要 有 WallgraftTM(Boston),和 Fluency TM(BARD)等。Wallgraft被覆的是涤纶血管,而Fluency被覆的是ePTFE血管。应用于大动脉的支架血管主要有进口的 TalentTM(Medtronic)和 ZenithTM(Cook),国产的有Ancura TM(深圳先健)和 Microport TM(上海微创)。
血管缝合装置主要用于血管的腔内治疗结束后,在动脉导鞘撤出时对动脉穿刺点进行封堵止血。一般认为,穿刺动脉导鞘小于6F时可以通过压迫止血,而导鞘在6F以上的则需要应用血管缝合装置,尤其是当腔内治疗过程中应用了大量抗凝药物时也需要考虑应用血管缝合装置。目前临床应用比较广泛的经皮血管缝合装置有:利用胶原塞压迫动脉外壁达到止血的AngioSealTM(St.Jude);还有通过缝合动脉穿刺点进行止血的PercloseTM(Abbott)等,可以应用于绝大多数6F~8F的动脉穿刺点封闭。
【常见并发症及防治】
1.穿刺点出血、血肿、假性动脉瘤和动静脉瘘形成
这是血管腔内操作最常见的并发症。主要原因为穿刺点压迫止血不充分,肝素用量过大,或凝血机制障碍等。其防治有下列几方面措施:
(1) 腔内操作后,穿刺点压迫止血时间应足够,一般4F动脉鞘压迫时间不小于10分钟,导管鞘较粗时应适当延长压迫时间。使用肝素剂量较大时可以带动脉鞘回病房,等肝素代谢完后再拔管。如导管鞘>10F、患者局部皮下脂肪较厚无法有效压迫止血或患者有凝血机制障碍时,尽量采用直视下血管切开导入。
(2) 患者术后应该用沙袋压迫穿刺点,卧床制动24小时(视导管鞘粗细而定),避免剧烈咳嗽等增加腹压行为。
(3) 一旦发生该并发症,应立即给予加压包扎,停用抗凝药物,患肢固定36~48小时,然后随访局部肿块大小和彩超。如果血肿或假性动脉瘤持续增大时,应及时手术切开行血肿清除及血管破口修补。
2.急性动脉血栓形成和远端动脉栓塞
主要原因:动脉壁损伤、动脉持久痉挛、操作时间过长导管鞘及导管促血栓形成、动脉附壁血栓及动脉硬化斑块向远端脱落等。这些均可诱发动脉血栓或栓塞,造成肢体远端缺血,甚至坏死。
治疗策略:症状轻者,可用溶栓、抗凝、扩血管等保守治疗;如肢体严重缺血应尽早手术取栓并修复损伤的动脉,必要时可能需要动脉旁路或人工血管移植。
3.动脉夹层形成
主要原因:血管扭曲、硬化、狭窄,致使导丝导管前进困难,如果操作手法不当,过于暴力,可能使导丝导管插破动脉内膜,形成夹层。若此时在夹层内进行高速对比剂注射或注入过量对比剂,可能导致血管破裂。此外,夹层形成还会导致远端动脉管腔闭塞引起急性缺血。
治疗策略:在操作中前进导丝时需轻柔仔细,造影前仔细了解导管头端位置,切忌在动脉夹层内进行造影。一旦夹层形成,导致远端动脉管腔闭塞引起急性缺血,有条件者可以置入支架把夹层内膜片固定,重新开放管腔,否则需要手术把局部夹层破口切除,行血管重建。
4.动脉穿孔出血
当患者血管扭曲、硬化严重时,如果操作过于暴力,可能会发生血管穿孔和破裂。穿孔较小时,会发生局部出血和血肿,穿孔较大时,可致大量出血,甚至出现休克和死亡。如果系导丝引起的小穿孔,回撤导丝后再次造影,一般可以自行愈合。如果为大的穿孔,需要立即紧急处理,原则同上述发生夹层时的策略。
5.腔内治疗器械折断
原因:如导丝或导管多次使用,反复塑形,会导致磨损乃至老化;或在前进后退时导丝或导管弯曲,操作过于暴力,有可能导致导丝导管的折断。
处理策略:可用血管抓捕器及时取出,必要时切开血管取出。
6.中枢神经损伤
原因:在进行全脑造影时,如果大剂量、高浓度对比剂通过颈动脉到达大脑时,可能破坏血-脑屏障,损伤脑组织,患者可出现头痛、烦躁不安、一过性失明,重者可引起昏迷或癫痫样抽搐。在进行主动脉或其他分支动脉造影时,如导管头端恰巧对准脊髓动脉开口,高浓度对比剂可造成脊髓损伤,轻者会发生感觉运动功能减退,重者可引起截瘫。
预防措施:应尽量选用与血浆等渗或低渗的非离子型对比剂,并在不影响诊断的前提下,尽可能减少对比剂的用量及降低对比剂浓度。在进行主动脉或其他分支动脉造影时,应确认导管尖端的位置,确保导管头端不应置于脊髓动脉开口。