SSTR是G蛋白偶联受体,在神经内分泌肿瘤细胞的广泛表达使其成为功能显像和治疗的理想靶点。肽受体放射性核素药物通常由多肽、螯合剂[如1,4,7,10-四氮杂环十二烷-1,4,7,10-四羧酸(1,4,7,10-tetraazacyclododecane-1,4,7,10-tetraaceticacid,DOTA)]和放射性核素(表1)三部分组成。
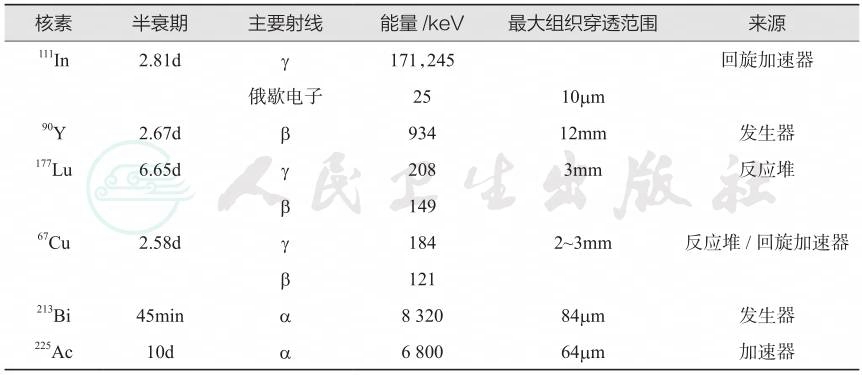
表1 可能适用于肽受体放射性核素治疗治疗的放射性核素
引自:专科技能培训教程.医学影像与介入分册.第1版.ISBN:978-7-117-32594-3.主编:
铟-111(111Indium,111In)发射γ射线,1990年,Krenning的团队与Sandoz研究所成功开发了111In-喷曲肽[Indium(111In)Pentetreotide]用于NET影像诊断,并成为NEN诊断“金标准”,该放射性药物于1994年获得FDA批准。1992年,Erasmus小组使用大剂量111In-喷曲肽治疗了1例胰岛素瘤患者,发现临床症状缓解。但后续研究表明,接受111In-喷曲肽治疗的患者病情缓解不佳,血液学毒性大,故该治疗未得到广泛推广。
目前,临床最常用的核素为90Y和177Lu,前者发射纯β射线,组织最大穿透范围为12mm,适合治疗较大的病灶;后者组织最大穿透范围为3mm,适合小病灶。177Lu发射γ和β两种射线,治疗后SPECT/CT探测γ射线评估体内放射性聚集,进行个性化剂量学研究,并预测疗效。68Ga-DOTATATE(NETSPOT)于2016年5月被FDA批准用于NET的诊断研究;177Lu-DOTATATE作为NET的放射性治疗药物,于2018年1月被FDA批准用于晚期NET治疗(图1)。
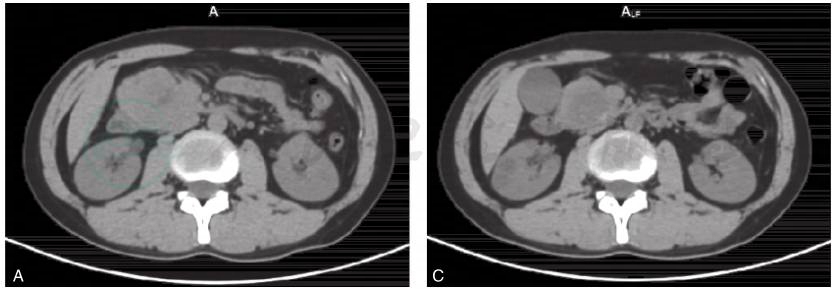
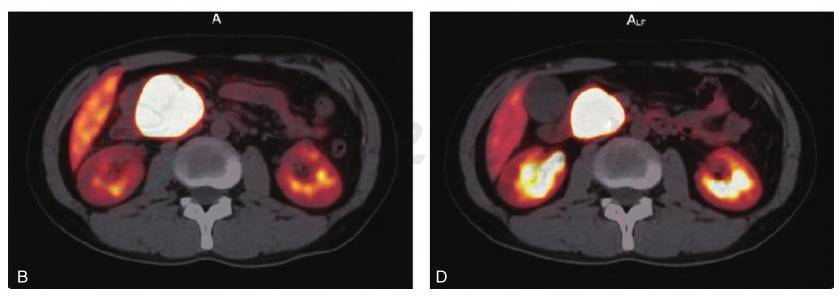
图1 68Ga-DOTA-NOC PET/CT评价(肽受体放射性核素治疗PRRT疗效)
患者,男,25岁。胰腺神经内分泌肿瘤。经过4次PRRT后,肿瘤原发病灶缩小50%,症状基本消失,肿块中央有部分坏死。分别为治疗前CT图(A)、治疗前PET/CT融合图(B)、4次PRRT治疗后CT图(C)和4次PRRT治疗后PET/CT融合图(D)。
引自:专科技能培训教程.医学影像与介入分册.第1版.ISBN:978-7-117-32594-3.主编:
213Bi和225Ac具有α射线,其特征在于高线性能量传递(LET),每微米可产生2000~7000个离子对,导致成簇的双链DNA断裂,使肿瘤细胞快速死亡。相比之下,发射β射线的核素通常仅导致单链DNA断裂,杀伤力较小。213Bi发射的α射线不仅具有更高的能量,对周围正常组织的伤害较小,无明显骨髓毒性反应,对90Y和177Lu标记药物产生耐药性的NET患者提供更有效的疗法。
1.经组织病理学证实的NE。
2.生长抑素受体显像阳性或免疫组化证实SSTR受体高表达。
3.卡氏评分>60分或ECOG评分>2分。
4.G1~G2患者,尤其是Ki-67指数< 20%。
5.有无法手术切除的原发灶或转移灶。
6.经多学科联合会诊共同讨论。
1.绝对禁忌证
(1)妊娠妇女。
(2)严重的急性伴发疾病。
(3)严重的无法控制的精神障碍。
2.相对禁忌证
(1)哺乳期妇女。
(2)严重的肾功能损害。
(3)严重骨髓抑制:治疗前应输血、升高白细胞、升高血小板对症治疗。建议当血常规各项低于以下参考值时对症处理:①白细胞计数< 3.0×109/L,中性粒细胞计数< 1.0×109/L;②拟接受177Lu-DOTATATE治疗,血小板计数< 7.5×109/L或拟接受90Y-DOTATOC治疗,血小板计数< 9.0×109/L;红细胞计数< 3.0×1012/L。
(4)即使无明确的骨髓抑制,在4周内接受过放疗或化疗患者慎用。
PRRT最常见的3~4级不良反应(≥ 4%,发病率较高)为淋巴细胞减少、γ-谷氨酰转肽酶升高、呕吐、恶心、谷丙转氨酶升高、谷草转氨酶升高、高血糖和低钾血症。













