 去看看
去看看


肌肉衰减综合征又称“老年性骨骼肌减少症”、“骨骼肌减少症”等,严重影响老年人健康寿命和生活品质。肌肉衰减症发病原因复杂多样,目前认为与衰老有直接关系,同时与营养不良和少动有关,其机制尚未完全明确,营养和运动是治疗的主要方法。
肌肉衰减综合征(sarcopenia)是与增龄相关的进行性骨骼肌量减少、伴有肌肉力量的或肌肉功能减退的综合征。1989年,Rosenberg第一次提出了“Sarcopenia”的概念。具体来说,肌肉衰减综合征是一种随着年龄增加,以肌肉流失、丢失、衰退、衰减为表现形式,以骨骼肌细胞体积和数量减少、肌力下降、结缔组织和脂肪增多而导致躯体功能减低、跌倒、虚弱及不同程度残疾为特征的临床综合征,又称为年龄相关性肌肉减少症。2016年10月,肌少症被正式纳入国际疾病分类ICD-10疾病编码中,肌少症是老年人衰弱的生理基础,是造成成年人跌倒风险、降低活动能力的重要原因之一,是衡量老年人衰弱的标志。
根据发病原因,欧洲老人肌肉减少症工作组(the European Working Group on Sarcopenia in Older People,EWGSOP)将肌肉衰减综合征分为原发性、继发性和营养相关性三类。原发性肌肉衰减综合征除明显老化,没有其他任何原因。继发性肌肉衰减综合征包括活动相关性和疾病相关性肌肉衰减综合征。活动相关性肌肉衰减综合征可能是由于长期卧床,久坐的生活方式,或零重力条件所引起。疾病相关性肌肉衰减综合征即由合并心、肺、肝、肾、脑等器官功能衰竭,炎症性疾病,或内分泌疾病等引起。营养相关性肌肉衰减综合征主要由于能量和/或蛋白质摄入不足,胃肠功能紊乱,消化吸收障碍或服用药物,造成厌食等引起。
肌肉衰减综合征的发病率受多种因素影响,流行病学研究显示,人体骨骼肌随年龄增加不断衰减,50岁以后,骨骼肌量平均每年减少1%~2%;60岁以上慢性肌肉丢失估计30%;80岁以上约丢失50%。青壮年时男性的四肢骨骼肌比女性发达,但是随着年龄的增长,男性骨骼肌衰减的速率比女性快。肌肉减少30%将影响肌肉的正常功能。西方国家的研究数据提示,60~70岁的老年人中肌肉衰减综合征发生率5%~13%,在80岁以上的人群中发生率达11%~50%。亚洲地区中,日本65岁以上老年人中男性和女性肌肉衰减综合征的发生率分别为11.3%和10.7%。国内上海地区的研究发现在≥70岁的健康老年人中,女性肌肉衰减综合征的发生率为4.8%,而男性的发生率为13.2%,但上述的上海研究并不是根据目前最为推荐的欧洲老年人肌肉衰减综合征工作组提出的诊断方法,仅测定肌肉的含量,未进行肌肉力量和躯体功能测试。我国人群发病率资料多来自于台湾和香港地区,男、女性发病率分别为6.7%~8.4%、0.4%~2.6%。有研究对中国城市与农村老年人群进行筛查显示,60岁以上人群总体发病率为9.8%,男性6.7%,女性12.0%;农村发病率为13.1%,城市为7.0%。在中国的西部地区,农村老年人较城市老年人更易患肌肉衰减综合征。
美国与欧洲报道,老年人肌肉组织的增龄性流失,常伴发脂肪组织的蓄积或增加,称之为“肌肉衰减性肥胖”(sarcopenic obesity,SO)。将显著增加代谢综合征等慢性病危险。韩国一项新近研究,用四肢骨骼肌量及内脏脂肪面积评定健康老年人SO,结果显示:男性高达35.1%、女性高达48.1%,而且患代谢综合征的危险性高于单纯肥胖及单纯肌肉衰减综合征者。
伴随着我国人口老龄化的日益加剧,老年人的健康问题越来越受到社会的关注,而肌肉衰减综合征已经成为老年常见疾病,能够引起骨质疏松、关节炎、跌倒损伤,并增加糖尿病等疾病的发病风险,已经成为严重影响中老年人正常生活和自理能力的一个突出问题,目前已成为老年医学的研究热点之一。
肌肉衰减综合征的发病机制尚未完全明确,已知众多因素与其发生和发展密切相关,其中个体内在因素包括老龄化、内分泌系统功能变化、骨骼肌去神经支配、体力活动量下降、营养失衡与基因遗传等,外在因素则包括各种原发疾病和全身慢性炎症,各种因素间相互影响,共同促进疾病的进展。
(一)内因
最重要的影响是老年人体内合成代谢的激素减少,如睾酮、雌激素、生长激素、胰岛素样生长因子-1,使肌肉蛋白的合成减少;肌纤维凋亡活性增强,促炎症因子增加,特别是肿瘤坏死因子-α、白介素-6,自由基积聚引起的氧化应激,肌细胞线粒体功能的改变和α-运动神经元数目的减少,均造成肌细胞蛋白分解增加,最终导致分解代谢大于合成代谢。
(二)外因
蛋白质营养不良是最主要的因素之一,维生素D摄入减少或合成能力不足均会导致肌肉质量的减少和功能的下降,引起跌倒和骨折。同时,由于老年人味觉嗅觉减退、牙齿残缺、抑郁、胃肠功能紊乱、消化吸收障碍或服用药物等因素,极易造成食欲缺乏甚至厌食等,引起能量营养素摄入不足和吸收率下降。而安静久坐的生活方式、长期卧床休息或零重力条件也可引起肌肉蛋白的丢失。不可忽视的是,老年人还可能因合并有心、肺、肝、肾、脑等器官功能衰竭、炎症性疾病、恶性肿瘤或内分泌疾病等,从而进一步加剧肌肉容积的减少。
(三)病理
老年性肌肉衰减在解剖学上的表现是肌肉量与横断面积下降、脂肪与结缔组织渗入肌肉、快肌纤维(Ⅱ型)与慢肌纤维(Ⅰ型)数量均减少,但纤维面积只在Ⅱ型肌纤维有减少,提示老年肌肉强度减弱与肌肉纤维的变化有关。光镜下显示内核、破残肌纤维蓄积。电镜下显示肌丝与Z线紊乱、肌质网增殖、脂褐素与线性杆状结构畜积。肌电图显示,腰胝段脊髓的运动神经元数降低一半,导致具有最快运动单位的快肌纤维减少很多。此时的生化变化是肌肉蛋白质主要是肌球蛋白合成率降低约28%,导致肌肉量与收缩功能下降,但肌浆蛋白质不变。老年肌肉内糖酵途径的酶活力无变化,但线粒体标志酶活力降低,相应老年人肌肉的呼吸能力也降低。钙-ATP酶蛋白浓度下降35%,而钙通道释放蛋白却增加,这些变化导致老年性肌肉收缩变慢。
(四)发病机制
肌肉衰减综合征的发生是机体骨骼肌合成代谢和分解代谢失衡的结果。与年龄相关的性激素水平、线粒体功能下降、细胞凋亡、神经系统的退行性疾病、多种慢性疾病、体内炎症状态、运动减少以及营养不良等多种因素有关。其中多种因素是不可改变的,但可以进行运动和营养干预,锻炼时肌肉收缩可以释放肌肉生长因子如胰岛素样生长因子(insulin like growth factor,IGF)和机械生长因子(mechano growth factor),促进卫星细胞核蛋白质合成,从而促进肌肉再生。另外,肌肉衰减综合征也与低BMI、低体重有关。蛋白质、能量摄入不足,骨骼肌则分解代谢增加,充足的营养摄入也是保证肌肉质量的必需条件,并且衰老的机体存在合成代谢阻力(anabolic resistance),因此需要更多的蛋白质摄入才能促进机体的骨骼肌的蛋白质合成反应。
关于肌肉衰减综合征的发生机制,近年来从分子、细胞、组织、整体水平及行为生活方式等多方面进行了研究。概括起来,包括神经元数量及传导速度下降、肌纤维变化、兴奋-收缩偶联减少、氧化应激损伤、卫星细胞激活/增殖减少、收缩蛋白基因表达减少、收缩蛋白mRNA转录减少、肌肉分解代谢有关的细胞因子白介素-1(IL-1)、肿瘤坏死因子(tumor necrosis factor,TNF)增高,肌肉蛋白质分解产物3-甲基组氨酸(3-Me-His)从尿中排出、生长激素(growth hormone,GH)、类胰岛素样生长因子(IGF-1)、雌激素、睾酮、雄酮不能合成及组织对激素的反应下降、味觉嗅觉减退、牙齿不好、抑郁等形成老年性食欲不振,以致蛋白质摄入不足而致营养不良、负氮平衡、血清白蛋白下降,及失去活动能力等多种机制。
肌肉衰减综合征最主要的表现为四肢骨骼肌质量与功能的下降。部分患者出现呼吸肌群受累,特别是慢性阻塞性肺疾病、慢性充血性心力衰竭患者。除对骨骼肌结构与功能直接影响外,肌肉衰减综合征还可增加患者跌倒与骨折风险、降低体力活动表现、提高入院概率与次数、加重护理负担,甚至增加死亡风险等。
(一)跌倒
肌肉衰减综合征造成肌肉力量的下降,在日常生活中下肢抗重力肌表现尤为突出,踝背屈肌、股四头肌肌肉衰减30%即可明显增加跌倒风险,同时伴随肌容积的减少,下肢本体感觉减退、神经反应速度下降均使老年人无法很好应对变化的外周环境,进一步增加了跌倒的风险。
(二)骨折
肌容积的减少导致骨所受应力的下降,骨缺乏刺激,骨母细胞活动减少引起骨质疏松。同时在跌倒时,萎缩的肌肉对骨骼的保护不足也使骨折的风险增加。
(三)生活质量下降
主要表现为提重物、下肢负重、久行久站等活动受限,职业活动能力和日常生活活动能力逐渐减退,并导致生活质量的下降。
(四)增加死亡风险
老年人过快地出现严重的四肢肌肉减少,死亡率随之增加。最近在新英格兰医学上发表一项关于亚洲人BMI与死亡率的关系研究,对110万亚洲人群长达9.2年的队列研究表明,体重过低(BMI≤15)死亡率增加2.8倍。体重过低或过高都可增加死亡率,亚洲人BMI在22.6~27.5死亡率最低。
(一)肌肉质量评定
1.CT和MRI
是最常见的肌肉质量评定影像学手段,两者均能清晰地区分人体的不同组织成分,并通过合适的算法计算相应组织的体积与质量,是现有评定肌肉质量的“金标准”。但CT、MRI设备占地体积庞大,不能移动,费用高昂,不适用于社区人群筛查,且CT具有一定的辐射暴露,而MRI则不能应用于体内放置金属或电子设备如起搏器等个体,因此在实际应用中有一定的局限性。
2.双能X线吸收法(dual energy X-ray absorptiometry, DXA)
是另一种常用的肌肉质量评定影像学手段,具有放射暴露量低、清晰区分不同组织成分等优点,是CT、MRI理想的替代工具。但设备的不可移动性限制了其广泛应用,尤其是在社区大规模筛查时。
3.生物电阻抗分析(bio-impedance-analysis, BIA)
是近年来大规模筛查的常用方式,通过放置于体表不同位置的多个电极向检测对象发送微弱交流测量电流或电压,检测相应的电阻抗及其变化,通过各种算法,推算出个体的脂肪体积与全身肌肉质量。BIA具有无创、无害、廉价、操作简单、功能信息丰富及便携等优点,但其结果的精确性严重依赖于算法,而近年随着算法的不断完善,已经逐渐有取代其他测量评定手段的趋势。
(二)肌肉力量的评定
目前通用方法为采用电子握力计测量优势手的握力,界值标准为男性≤26kg,女性≤18kg。
(三)肌肉功能的评定
4m正常步速:从静止开始,步行4m,计算步速,≤0.8m/s为异常。
(一)筛查
对有以下情况的人群进行筛查:①社区人群:60岁及以上人群;合并慢性疾病如慢性心力衰竭、慢性阻塞性肺疾病、糖尿病、慢性肾功能不全、结缔组织病、结核菌感染及其他慢性消耗性疾病等;近期曾有入院史;长期卧床者。②疾病患者:日常步行速度≤1.0m/s者;营养不良者;近期出现跌倒者;合并抑郁状态或认知障碍者;1个月内不能察觉的体重下降超过5%者;近期出现临床可见的力量、体能或健康状态下降或受损者。
(二)诊断
1.诊断标准
肌肉衰减综合征的诊断标准目前国际尚无统一的肌肉衰减综合征的诊断标准,但以下几种方法较为常用。
(1)相对骨骼肌质量指数(relative skeletal muscle index, RSMI):
这是国际上提出的第一个诊断肌肉衰减综合征的方法,其使用与身高相关的四肢肌肉来诊断肌肉衰减综合征的程度,即四肢骨骼肌质量(appendicular skeletal muscle,ASM)与身高平方的比值,再乘以100%即可得出。可表示为RSMI=ASM(kg)/身高(m2)×100%。ASM可以通过DXA、BIA直接或间接测量。
(2)骨骼肌质量参数(skeletal mass index, SMI):
2002年,Janssen等人提出了SMI,使用的是总体重和瘦体重两个参数来评定老年人肌肉衰减综合征的程度,即SMI=100×骨骼肌质量/体重。他们当时采用的是BIA测量身体成分。该种测量方法还将肌肉衰减综合征进行了分级。如果某个体测量结果SMI值小于该种族同性别健康青壮年(18~39岁)SMI均值的1~2个标准差,则将诊断为患有Ⅰ级肌肉衰减综合征;同理,若小于2个及以上标准差,则诊断为患有Ⅱ级肌肉衰减综合征。
(3)残值法(residuals methods):
是Newman等人推荐使用一种新的诊断方法,这种方法以回归模型为基础。残值法利用男性和女性各自身高和脂肪的线性回归方程来推算相对应的ASM值,然后找出测量值比预测值高和低的个体,将分布在第20个百分残差数值作为cut-off值。这一方法优点是将身高和脂肪两个因素均考虑在内,而ASM经这两个因素校正后,与身体活动能力受限有着更强的相关性。因此部分研究中认为用残值法定义肌肉衰减综合征有一定的参考价值。
(4)基于肌肉质量和功能的综合诊断标准:
EWGSOP建议使用包含低水平的肌肉质量和肌肉功能(肌肉力量和身体活动能力)的指标综合诊断肌肉衰减综合征。该种诊断方法在近年来被更多的研究中采用,而且得到了部分学者的认可。认为EWGSOP定义的肌肉衰减综合征的方法实用性更强,临床诊断价值相对较高。
如前所述,肌肉质量与功能的下降与年龄、性别、种族等多种因素相关,因此,根据肌肉衰减综合征的定义,诊断肌肉衰减综合征需结合肌肉质量、肌肉力量及体能状况三者情况,具体诊断标准如表6-2-1,并按图6-2-1的流程进行确诊。
表6-2-1 肌肉衰减综合征诊断标准

注:DXA:双能X线吸收法;BIA:生物阻抗分析
| 指标 诊断标准 |
| 肌肉质量 低于同种族年轻成年人(低于35岁)骨骼肌质量平均值2个标准差或DXA法男性低于 7.0kg/m2、女性低于5.4kg/m2或BIA法男性低于7.0kg/m2、女性低于5.7kg/m2 握力 低于同种族年轻成年人(低于35岁)骨骼肌质量平均值2个标准差或男性低于26kg、女 性低于18kg 体能状况 日常步行速度≤0.8m/s |
引自:主编:.老年病康复指南.第1版.ISBN:978-7-117-30662-1
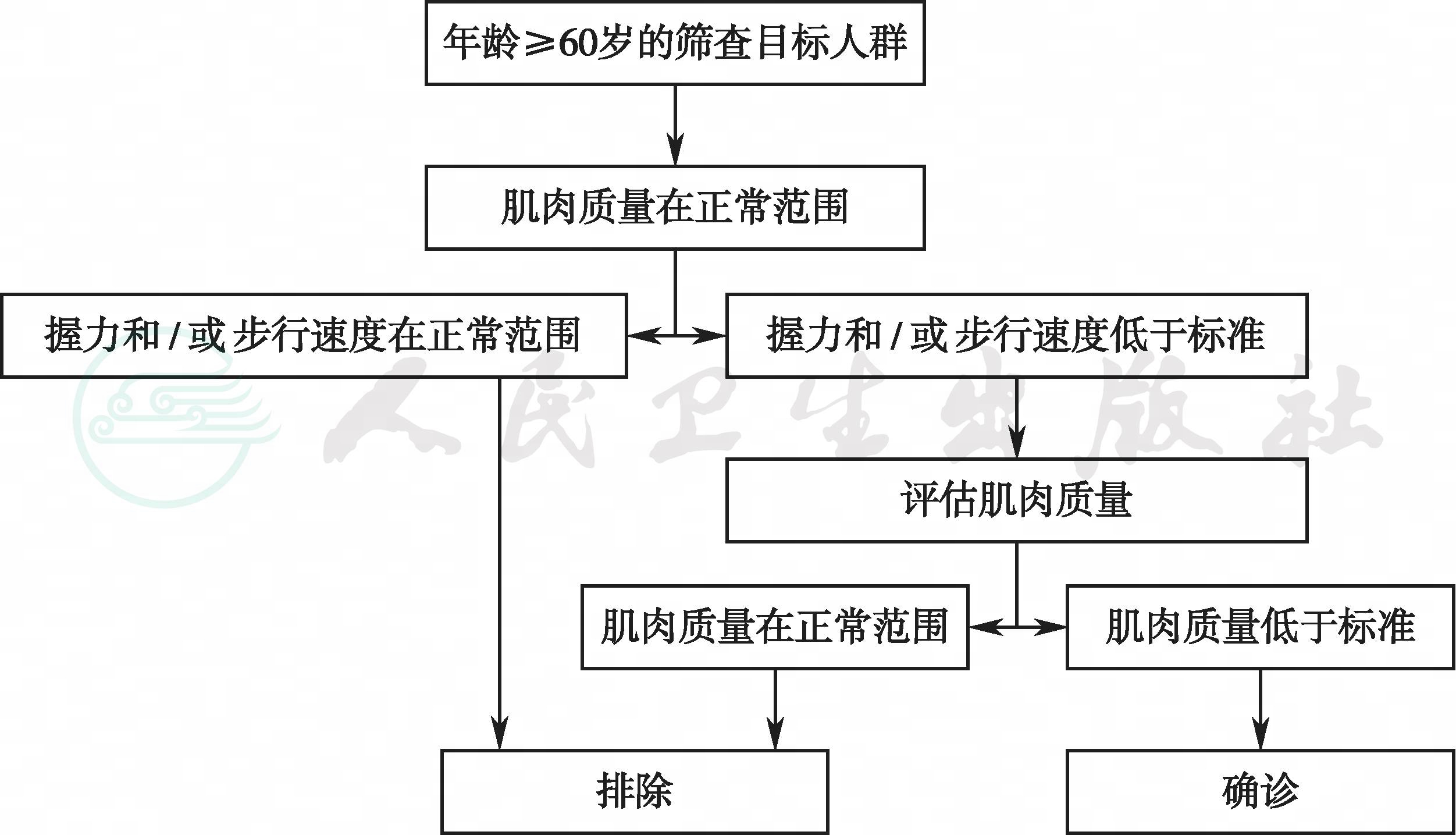
图6-2-1 肌肉衰减综合征诊断流程
引自:主编:.老年病康复指南.第1版.ISBN:978-7-117-30662-1
实际操作中,需要注意以下细节:首先,在参考人群的选择方面,需考虑到可能影响肌肉质量与功能的多种因素,如种族、性别、年龄、地理位置等,尽可能减少干预因素;此外,由于包括我国在内的亚洲国家老年人群倾向于传统的生活方式,而年轻人群的生活方式倾向于西方化,当采用当地年轻成年人的平均值作为参考标准值时,可能会造成老年人群肌肉力量、功能丧失程度的低估。其次,在个体化校正方法的选择方面,大部分基于中国人群的研究建议采用身高平方值校正法,因身高平方值校正后的结果与握力降低、体能下降、跌倒风险、活动困难及死亡率的相关性更好。
2.诊断分期
EWGSOP将肌肉衰减综合征进行了分级:①肌肉衰减综合征前期(pre-sarcopenia):指仅有肌肉质量减少,而肌肉力量和躯体功能尚正常。②肌肉衰减综合征:指有肌肉质量减少,伴有肌肉力量或躯体功能下降。③严重肌肉衰减综合征(severe sarcopenia):指肌肉质量、肌肉力量和躯体功能均有下降。
肌肉衰减综合征的发生与多种因素有关,其中很多因素是不可控的,常用干预方法有药物治疗、抗阻训练、饮食营养治疗。药物治疗主要是补充睾酮与生长激素等替代疗法,虽然补充睾酮等激素能逆转增龄性骨骼肌减少症,但激素替代疗法易导致红细胞增多、体液潴留乃至前列腺癌变等不良反应。而营养干预和抗阻训练是防治老年人肌肉衰减综合征的有效方法。
(一)预防和饮食治疗
临床工作中,我们需要常规对老年人进行营养风险评定,了解老年人的食欲、咀嚼功能、饮食习惯、食物摄入量和体重的变化,是否存在其他影响进食的疾病,以便早发现营养问题,早干预、避免不良预后,可以使用微营养评估表(Mini Nutritional Assessment,MNA)。目前,肌肉衰减综合征的营养治疗研究主要集中在蛋白质、肌酸、维生素D的补充。良好的营养,特别是充足的蛋白质和能量摄入,可以帮助限制以及治疗增龄性的肌肉质量、力量和功能能力下降。对有营养风险的老年人,予以针对性的干预,保证老年人有足够的能量摄入,具体如下:
1.蛋白质
越来越多的生物和临床证据证明,蛋白质补充可以改善老化肌肉中的卫星细胞功能。
蛋白质的摄入以及消化利用率会影响肌肉蛋白质的合成,有助于延缓和改善老年肌肉衰减综合征。蛋白质摄入不足将影响老年人的新陈代谢和生理调节能力,包括肌肉质量减少和肌力下降等。膳食蛋白质的摄入对肌肉蛋白质的合成非常重要。
(1)食物蛋白质能促进肌肉蛋白质的合成,有助于预防肌肉衰减综合征。
(2)老年人蛋白质的推荐摄入量应维持在1.0~1.5g/(kg·d),优质蛋白质比例最好能达到50%,并均衡分配到一日三餐中。
(3)富含亮氨酸等支链氨基酸的优质蛋白质,如乳清蛋白及其他动物蛋白,更有益于预防肌肉衰减综合征。
2.脂肪酸
补充脂肪酸对预防和延缓老年肌肉衰减综合征的发生。
(1)对于肌肉量丢失和肌肉功能减弱的老年人,在控制总脂肪摄入量的前提下,应增加深海鱼油、海产品等富含n-3多不饱和脂肪酸的食物摄入。
(2)推荐二十碳五烯酸(eicosapntemacnioc acid,EPA)+二十二碳六烯酸(docosahexaenic acid,DHA)的平均每日代谢率(average daily metabolic rate,ADMR)为0.25~2.00g/d。
3.维生素D
适量补充维生素D能够有效预防肌肉衰减,改善肌力,减少老年人跌倒风险。维生素D的补充可以通过基因组和非基因组效应通路参与肌肉功能,维生素D代谢物1,25(OH)2D可促成肌细胞的分化,增加肌肉量,有效的缓解老年人肌肉衰减。
(1)有必要检测所有肌肉衰减综合征老年人体内维生素D的水平,当老年人血清25(OH)D低于正常值范围时,应予补充。
(2)建议维生素D的补充剂量为15~20μg/d(600~800IU/d);维生素D2与维生素D3可以替换使用。
(3)增加户外活动有助于提高老年人血清维生素D水平,预防肌肉衰减综合征。
(4)适当增加海鱼、动物肝脏和蛋黄等维生素D含量较高的食物摄入。
4.抗氧化营养素
抗氧化营养素包括维生素C、维生素E、类胡萝卜素和硒等,通过补充抗氧化营养素可以改善老年人的身体状况,提高身体活动能力,改善肌肉功能。人体衰老细胞的线粒体代谢异常会产生过量的活性氧,造成体内氧化应激损伤,使骨骼肌代谢异常,从而导致负氮平衡。补充抗氧化营养素可以帮助老年人维持内环境稳态和线粒体功能,预防肌肉衰减综合征的发生和发展。
(1)鼓励增加深色蔬菜和水果以及豆类等富含抗氧化营养素食物的摄入,以减少肌肉有关的氧化应激损伤。
(2)适当补充含多种抗氧化营养素(维生素C、维生素E、类胡萝卜素、硒的膳食补充剂。
5.口服营养补充(oral nutritional supplements, ONS)
口服营养补充剂对于已经存在或可能发生营养不良或具有营养风险的老年人可以增加其能量和营养物质的摄入,有助于减少肌肉丢失、改善身体功能。
(1)口服营养补充有助预防虚弱老年人的肌肉衰减和改善肌肉衰减综合征患者的肌肉量、强度和身体组分。
(2)每天在餐间或锻炼后额外补充2次营养制剂,每次摄入15~20g富含必需氨基酸或亮氨酸的蛋白质及200kcal(836.8kJ)左右能量,有助于克服增龄相关的肌肉蛋白质合成抗性。
(二)药物治疗
药物对于治疗老年肌肉衰减综合征具有一定的疗效和积极作用。睾酮、雄激素、雌激素、生长激素等激素对于肌肉蛋白质的结构与功能均具有重要的调控作用。睾酮、雄激素可以促进肌肉蛋白质的合成从而增加肌肉质量。绝经后的中老年女性卵巢功能衰退,雌激素水平低,血钙水平低,对肌肉的结构和功能的维持极其不利,在肌肉衰减综合征的发生、发展中起着不可忽视的作用,雌激素替代治疗具有一定减缓肌肉衰减的作用。
老年人肌肉衰减综合征评定从肌肉力量、肌肉功能、体能评定和平衡功能评定等多个维度综合评定。
1.肌肉力量的测定
目前通用方法为采用电子握力计测量优势手的握力,界值标准为男性≤26kg,女性≤18kg。
2.肌肉功能的测定
4m正常步速:目前通用方法为从静止开始,步行4m,计算步速,≤0.8m/s为异常。
3.体能评定
体能状况量表(Short Physical Performance Battery,SPPB量表)是综合性测试工具,包含重复椅子站立测试(计算连续完成5组起立-坐下的时间)、平衡测试(包含10秒双脚左-右侧方站立、半前后脚站立、前后脚站立测试三个部分)、步行测试(以常规步行速度通过4m距离的时间)3个部分,以0~12表示个体的体能水平,分数越高,体能越好;6min步行测试是测试个体在6min内能达到的最大步行距离,主要测试老年人的有氧运动能力。
4.平衡功能评定
包括观察法、量表法、平衡仪测试法。
运动疗法是预防和治疗肌肉衰减综合征的有效手段,可不同程度地引起骨骼肌质量和力量的改变以及平衡能力的改善。近几年来,国内学者在肌肉衰减综合征运动疗法的基础和临床研究上取得了重要进展,并达成了专家共识。
(一)有氧训练
每周进行规律的有氧训练对肌肉衰减综合征的患者具有增加肌肉质量,改善肌肉功能等积极作用。
1.作用机制
有氧训练能改善线粒体功能,增加线粒体数量,改善整个机体的代谢调节,降低氧化应激水平,减轻慢性炎症,能减少身体脂肪比例,极大地降低代谢性疾病的危险因素,提高老年人心肺功能与活动功能,改善耐力,维持最佳的运动能力。
2.训练方法
有氧运动的特点是强度低,可以持续较长的时间,其实质就是反复多次的中小强度运动,如行走、慢跑、骑自行车、爬山、爬楼梯、游泳、舞蹈、太极拳以及一些小球类活动项目等,训练者可以根据自身情况和兴趣来选择。
(二)抗阻训练
抗阻训练促进骨骼肌生长的结果来源于肌纤维蛋白的增加,这种增加通常发生在运动后1小时并能持续24~48小时。除此之外,抗阻运动还能够诱导同化激素,如生长素、胰岛素样生长因子和睾酮水平改变,并抑制肌生成抑制素的生成,这些因素的改变对肌肉功能有着重要的影响。因此,抗阻运动是增强老年人肌肉力量和质量最佳的方式,可以有效预防肌肉衰减引起的身体功能下降、残疾,提高生活质量。
1.渐进性抗阻训练
渐进性抗阻运动指通过在训练过程中不断增加阻力负荷,使肌肉产生连续适应性刺激进而提高力量的方法,近几年来得到了广泛的运用。美国运动医学学会(American College Sports Medicine,ACSM)的运动处方指南指出,老年人在进行运动训练的过程中需要遵循循序渐进的原则,在低强度训练的基础上逐渐增加频率和时间更有益于健康。
(1)作用机制:
抗阻训练通过对线粒体介导的细胞凋亡等多条信号通路的影响,起到减缓肌肉衰减的发生,有效改善肌肉质量和力量,改善身体活动能力和功能,提高生活质量。
(2)训练方法:
以抗阻运动为基础的运动,如坐位抬腿、静力靠墙蹲、举哑铃、拉弹力带等,每天进行累计40~60min中-高强度运动,如快走、慢跑,其中抗阻运动20~30min,每周≥2天,对于肌肉衰减综合征患者需要更多的运动量。
2.快速抗阻力量训练
(1)作用机制:
由于衰老骨骼肌Ⅱ型肌纤维萎缩,快速抗阻力量训练对于维持Ⅱ型肌纤维和骨骼肌的整体功能水平很重要。老年人进行快速抗阻训练时募集到较多的Ⅱ型肌纤维运动单位,其快速力量显著性提高,因此,在为老年人设计运动方案时应适当考虑一些快速抗阻力量训练。
(2)训练方法:
快速抗阻力量训练是老年人提高快速力量的有效手段,在每次进行力量练习时,以尽可能快的速度进行向心收缩,然后以较慢的速度(2秒左右)进行离心收缩,老年人快速抗阻力量训练需要涉及多关节和单关节的力量训练,用轻到中等负荷的重量,30%~60%最大阻力,快速重复6~10次,每个练习做1~3组。
(三)柔韧性训练与平衡训练
平衡和柔韧性是老年人整体健康状态所不能缺少的,对老年人的活动能力具有非常重要的作用。积极进行柔韧性训练和平衡训练可以有效促进老年肌肉衰减综合征患者的骨骼肌功能和平衡能力。
柔韧性训练每周至少2天,每次进行10min,强度控制在5~6感知延伸率(the rate of perceived extension,RPE),包括颈、肩、肘、腕、髋、膝、踝关节;平衡训练需每周进行3次以上。柔韧性训练与平衡训练需循序渐进,长期坚持,量力而行,避免运动不当引起的损伤。
(四)血流限制训练
又称加压训练,是在上臂和大腿近端部位通过加压带施加压力,造成肢体远端肌肉缺血进行肌肉训练的方法。
以往研究表明,高强度并且大于70%1RM的抗阻运动能够有效的促进肌肉蛋白质的合成以及肌肉体积的增大,但近年来的研究证明,低强度的抗阻运动结合血流限制训练同样能够增加肌肉体积。对于进行高强度抗阻运动较困难的老年人来说,血流限制训练被证实能够显著增加肌肉体积,提高肌肉适应性,并且不会导致肌肉损伤。
(五)运动训练原则
1.运动锻炼 应该有一个推荐的体力活动水平的训练计划,依据运动强度、运动持续时间、运动频率,循序渐进地达到所建议的体力活动水平。
2.可以利用娱乐活动和闲暇活动、步行或骑车上下班、职业活动、家务、家庭和社区活动等进行有氧运动训练。
3.尽可能早地开始抗阻训练,以获得理想的抗阻训练效益。为老年人设计抗阻训练计划时,还应该适当涉及快速抗阻力量训练项目。
4.注意给予平衡和柔韧性训练。
(六)运动训练指南
运动训练指南详见表6-2-2。
表6-2-2 运动训练指南

| 运动方式 运动频率 运动强度 持续时间/组数 |
| 有氧运动 每周至少5次 中等强度的运 动或3次大强 度运动 中等强度,10分制的5~6分(呼 吸频率和心率有明显增加) 大强度,10分制的7~8分(呼吸频 率和心率有非常显著性的增加) 每天中等强度的体力活 动累计时间至少不低于 30min,每次体力活动 的时间不少于10min |
续表

| 运动方式 运动频率 运动强度 持续时间/组数 |
| 涉及大肌肉群的抗 阻运动(自由重量 或力量训练器械) 每周至少2次 60%~80%最大阻力重量,慢速 到中等速度 8~10个练习动作,每个 练习动作1~3组,每个 练习动作重复8~12次 (组间间歇时间1~3min) 快速力量练习仅在 抗阻练习后进行 每周2次 轻到中等负荷(30%~60%最大 阻力重量)高速度重复 每个练习动作1~3组, 重复6~10次 |
引自:主编:.老年病康复指南.第1版.ISBN:978-7-117-30662-1
蛋白质、脂肪酸、维生素D、抗氧化营养素、口服营养补充等营养物质的摄入既是治疗的措施也是重要的预防方式,此外,还需老年人每天进行适当运动,尤其是适当的抗阻力运动,减少静卧或静坐,增加日常活动量。
(郑洁皎 高 文 周媚媚)