 去看看
去看看


1 前言
侵袭性真菌病(invasive fungal disease,IFD)是指真菌侵入人体,在组织、器官或血液中生长、繁殖,并导致炎症反应及组织损伤的疾病[1]。在实体器官移植(solid organ transplant,SOT)受者中,IFD已成为致病和死亡的重要原因[2]。2009年,中华医学会器官移植学分会结合我国移植受者的临床特点,参考国内外相关指南,制订了《实体器官移植患者侵袭性真菌感染的诊断和治疗指南》[3-4]。
近年来,随着诊断和治疗水平不断提高,在SOT受者的IFD预防、评估和治疗方面,均取得巨大进步。然而由于新型免疫抑制剂及更新的预防策略的应用,SOT后真菌感染模式已发生显著变化[2],真菌的耐药性出现,标准化抗真菌治疗效果不明显,大大增加了临床治疗难度,严重影响了IFD患者的预后[5]。因此,中华医学会器官移植学分会和中国医师协会器官移植医师分会结合更新的国内外临床证据,并参考2013年中国侵袭性真菌感染工作组的《血液病/恶性肿瘤患者侵袭性真菌病的诊断标准与治疗原则(第四次修订版)》[1]、美国感染学会(IDSA)2016年《念珠菌感染临床实践指南》[6]、2010年《隐球菌感染临床实践指南》[7]、2008年《曲霉菌感染临床实践指南》[8]、2014年欧洲临床微生物与感染性疾病学会《实体器官移植受者中侵袭性真菌感染》[9]、2008年欧洲癌症研究和治疗组织侵袭性真菌感染协作组/美国国立变态反应和感染病研究院真菌病研究组(EORTC/MSG)《侵袭性真菌病修订定义》[10]等文件,对2009年版《实体器官移植患者侵袭性真菌感染的诊断和治疗指南》进行修订,以期为实体器官移植和相关学科的同道提供帮助。
在本版指南中,“侵袭性真菌病”的概念代替了此前的“侵袭性真菌感染(invasive fungal infection,IFI)”。“感染”着重描述的是病原菌与宿主的一种共存状态,而“病”则描述的是病原菌在体内侵袭、繁殖造成器官组织损伤的病理现象,更能反映一种病理状态[10]。
2 指南参照的推荐级别/证据水平标准
本指南按照“推荐分级的评估、制定与评价(GRADE)”系统[11]对证据等级和推荐意见强度进行分级。
2.1 证据等级
(1)高:以A表示,表明未来研究几乎不可能改变现有疗效评价结果的可信度;(2)中:以B表示,表明未来研究可能对现有疗效评估有重要影响,可能改变评价结果的可信度;(3)低:以C表示,表明未来研究很有可能对现有疗效评估有重要影响,改变评价结果可信度的可能性较大;(4)极低:以D表示,表明任何疗效的评估都很不确定。
2.2 推荐强度
(1)强推荐:
以1表示,明确显示干预措施利大于弊或弊大于利;(2)弱推荐:以2表示,利弊不确定,或干预的效果不明显。
3 SOT受者IFD的流行病学特点
3.1 SOT受者发生IFD的重要致病菌、发病率及死亡率
国内及欧美流行病学研究显示,IFD的发生率依据移植器官的种类和免疫抑制程度、各移植中心的环境以及预防性药物的使用情况等因素而不尽相同。两项国际多中心、大样本、前瞻性临床研究对SOT受者IFD特点进行了较全面的研究,结果表明SOT受者术后IFD病原以念珠菌最多见,其次为曲霉菌、隐球菌、非曲霉菌(除外接合菌)、地方性真菌、接合菌及卡氏肺囊虫等[12-13]。我国2014年发表的一篇流行病学结果也显示,肝移植受者的IFD发生率为18.8%,例次感染率为33.9%,其中白色念珠菌占55.2%,曲霉菌占18.4%,其他非白色念珠菌占36.4%,其中光滑念珠菌占10.5%[14]。
常见IFD的病原菌、发病率及患者病死率见表1。
表1 常见IFD的病原菌、发病率及患者病死率[7,9,15-27]
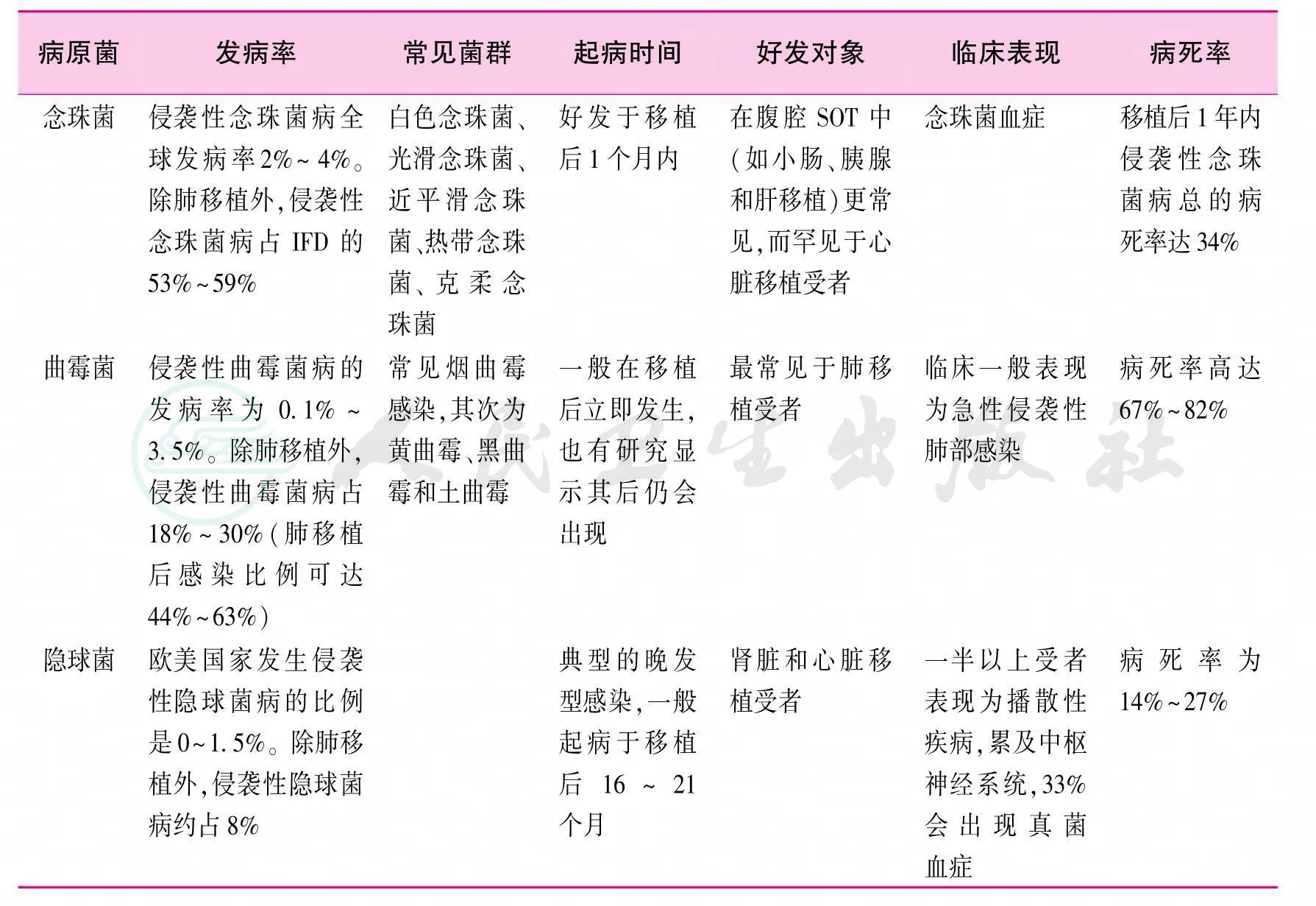
3.2 SOT患者发生IFD的危险因素
SOT受者移植术后长期大剂量免疫抑制剂的应用是发生IFD的高危因素。除此之外,尚包括移植相关的医疗技术、环境和不同移植器官受者群的特殊危险因素(表2)。这些因素构成了SOT受者不同于其他学科患者群体IFD易感性的特点。
表2 不同SOT受者人群发生IFD的危险因素[2,28-32]
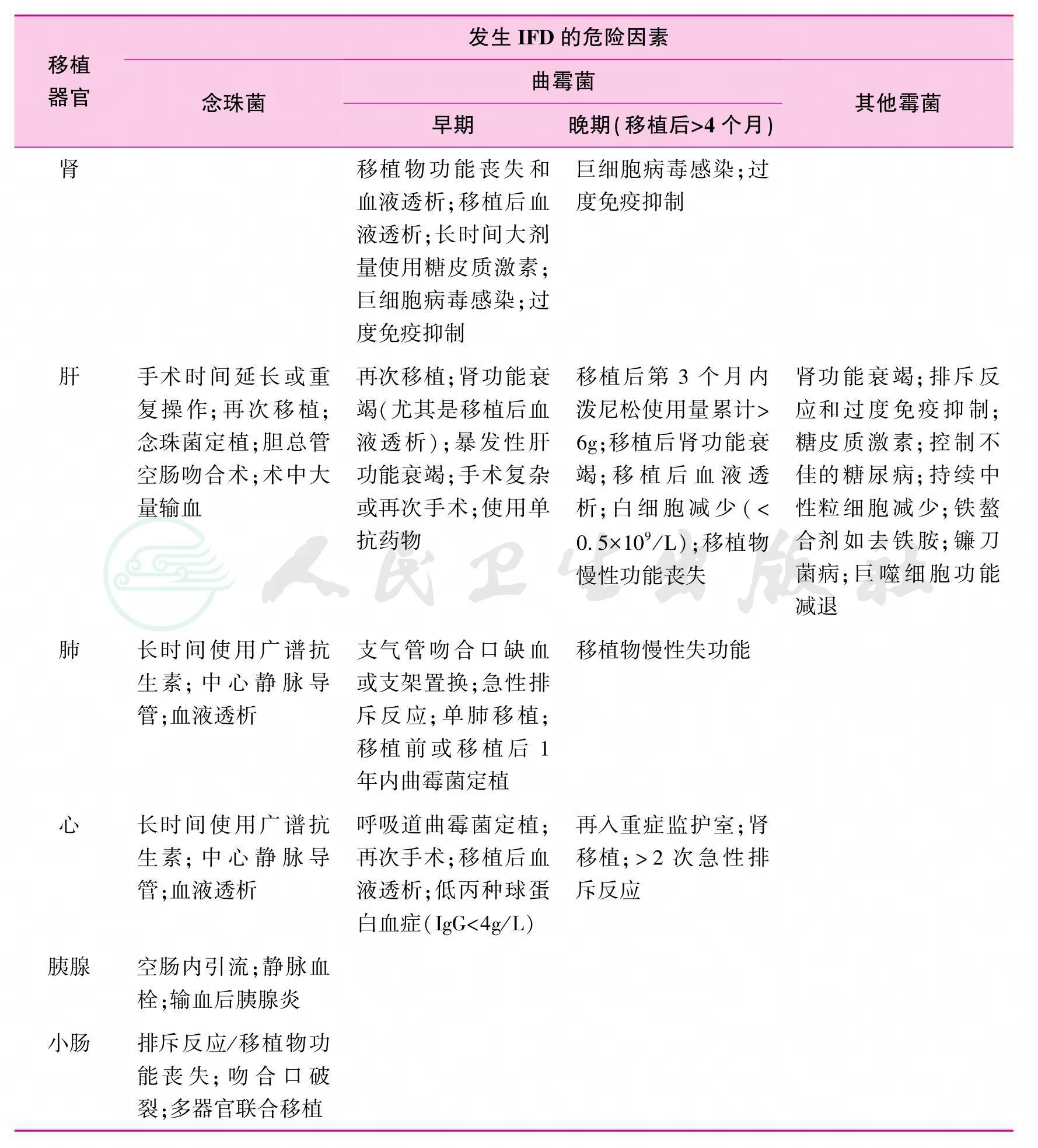
4 SOT受者IFD的诊断
4.1 诊断标准:
鉴于我国目前没有器官移植相关IFD大规模循证医学资料,诊断标准参照欧洲癌症研究和治疗组织/侵袭性真菌感染协作组和美国国立变态反应和感染病研究院真菌病研究组(European organization for research and treatment of cancer/invasive fungal infections cooperative group and the national institute of allergy and infectious diseases mycoses study group,EORTC/MSG)联合发布的IFD修订定义[10],并参考我国《血液病/恶性肿瘤患者侵袭性真菌病的诊断标准与治疗原则(第四次修订版)》[1]、《侵袭性肺部真菌感染的诊断标准与治疗原则》[33]和《重症患者侵袭性真菌感染诊断与治疗指南》[34]中所推荐的诊断标准和方法,沿用分层诊断体系,以宿主因素、临床特征和微生物学或组织感染真菌病理学依据三项指标为诊断要素,保留确诊(proven)、临床诊断(probable)和拟诊(possible),增加了未确定(undefined)的诊断。
4.2 诊断方法:
结合SOT受者的特殊性,SOT受者IFD具体诊断依据见表3。
表3 临床诊断侵袭性真菌病的诊断依据

1.确诊:
(1)深部组织真菌感染。①霉菌:相关组织存在损害时(镜下可见或影像学证据确凿),在针吸或活检取得的组织中,采用组织化学或细胞化学方法检获菌丝或球形体(非酵母菌的丝状真菌);或在通常无菌而临床表现或放射学检查支持存在感染的部位,在无菌术下取得的标本,其培养结果呈阳性。②酵母菌:从非黏膜组织采用针吸或活检取得标本,通过组织化学或细胞化学方法检获酵母菌细胞和(或)假菌丝;或在通常无菌而临床表现或放射学检查支持存在感染的部位(不包括尿道、副鼻窦和黏膜组织),在无菌术下取得的标本,其培养结果呈阳性;或脑脊液经镜检(印度墨汁或黏蛋白卡红染色)发现隐球菌或抗原反应呈阳性。③肺孢子菌:肺组织标本染色、支气管肺泡灌洗液或痰液中发现肺孢子菌包囊、滋养体或囊内小体。
(2)真菌血症。①血液真菌培养出现或获得霉菌(不包括曲霉菌属和除马尔尼菲青霉的其他青霉属)、念珠菌或其他酵母菌阳性。②同时临床症状及体征符合相关致病菌的感染。
2.临床诊断:
至少符合一项宿主因素,一项临床标准和一项微生物学标准。
3.拟诊:
至少符合一项宿主因素,一项临床标准,缺乏微生物学标准。
4.未确定:
至少符合一项宿主因素,临床证据及微生物结果不符合确诊、临床诊断及拟诊IFD标准。
推荐意见:
1.确诊IFD需要得到来自正常无菌部位或感染部位标本培养出的微生物学证据(1-B)。
2.血培养酵母菌或酵母样菌(毛孢子菌属和镰刀菌属)结果阳性,可以考虑诊断IFD(1-B)。
3.鉴别真菌菌株的种类对于选择抗真菌治疗方案,预测受者预后至关重要(1-A)。
4.支气管肺泡灌洗液半乳甘露聚糖抗原检测可用于侵袭性曲霉病的诊断,在条件允许时应尽量检测(1-B)。
5.怀疑侵袭性肺曲霉病时,推荐做高分辨率胸部CT,其敏感度高于胸片(1-B)。
6.血清或脑脊液隐球菌抗原检测和血、尿培养阳性是隐球菌感染的主要确诊手段(1-B)。
7.检测隐球菌感染,磁共振(MRI)的敏感度高于CT(1-B)。
5 SOT受者IFD的预防
鉴于SOT受者的免疫功能低下状态,一旦发生IFD,病情进展迅速,不但影响移植物功能,还可严重威胁受者的生命。由于目前临床上缺少快速、特异的诊断手段,为降低IFD的发病率和病死率,对SOT受者采取合理的预防措施,达到保护移植物良好功能和受者长期存活的目的,同时还可以节省医疗费用。
5.1 一般预防
①优化手术和免疫抑制治疗方案;②减少不必要的侵入性操作,尽早拔除留置导管,缩短静脉通道保留时间等;③严格控制医院内和医院外的环境因素[35]。
5.2 靶向预防
靶向预防是SOT受者出现了某些特定情况时所采取的具有针对性的防范措施,SOT受者预防药物的选择应根据移植器官的特性,选用与免疫抑制剂相互作用小、安全、高效、低毒的药物(表4)。
表4 SOT受者靶向预防用药[32,36-70]

注:MELD为终末期肝病模型评分
推荐意见:
8.作为预防手段,比应用抗真菌药物更有效的是优化手术步骤、制订合适的免疫抑制策略及环境控制等[1-C]。
9.中国公民逝世后器官捐献供肾移植受者常规应用抗真菌药物进行预防治疗,包括采用复方磺胺甲噁唑预防卡氏肺囊虫性肺炎(1-A)。
10.对于存在高危因素的肝移植受者,应使用抗真菌药物进行预防,推荐用药包括米卡芬净(1-B)、卡泊芬净(1-B)、两性霉素B脂质体Ⅳ(1-B)。
11.对于胰腺移植受者,应用氟康唑预防侵袭性真菌感染(1-C)。
12.所有肠移植受者应用氟康唑预防侵袭性真菌感染(1-C),高危患者应用两性霉素B脂质体Ⅳ(1-C)、卡泊芬净(1-C)、米卡芬净(1-C)预防侵袭性真菌感染。
13.肺和心肺联合移植受者应用雾化两性霉素B脂质体预防侵袭性真菌感染(1-B)。
14.心脏移植受者应用伊曲康唑预防侵袭性真菌感染(1-B)。
6 SOT受者并发IFD的治疗[3-4,6-9,71]
SOT受者发生IFD时,多数处于免疫功能低下和危重状态,治疗中应根据移植器官特点选择治疗方案。
6.1 治疗策略
IFD的治疗分为拟诊治疗、临床诊断治疗、确诊治疗三级。IFD病情进展迅速,而SOT受者由于免疫功能低下,其临床特征表现滞后,抗体反应迟缓,故应重视拟诊治疗和临床诊断治疗。
1.拟诊治疗:
又称经验治疗。当诊断证据不足、又高度怀疑IFD时,为避免不必要的致命性并发症,降低病死率,在充分、全面衡量移植受者的整体状况后可以根据以往的经验给予受者适当抗真菌治疗。
2.临床诊断治疗:
又称先发治疗,针对临床有宿主因素、环境因素或临床特点的高危移植受者进行连续监测(影像学和微生物学相关项目),发现阳性结果立即开始抗真菌治疗,以避免因免疫反应低下延误诊断和治疗,同时避免经验治疗带来的用药过度和滥用。
3.确诊治疗:
又称为目标治疗,是针对明确的真菌种类选择抗真菌药物进行特异性抗真菌治疗。
4.加强治疗:
严重肺部真菌病常可危及受者的生命,需加强治疗。如发生低氧血症,应转入监护病房,立即减少或停用霉酚酸(MPA)类和钙调磷酸酶抑制剂(CNI)类药物,尽早采取积极措施,包括面罩吸氧、呼吸机支持、特异性抗真菌治疗等。
6.2 抗真菌治疗药物
目前临床应用的抗真菌药物有多烯类、三唑类、棘白菌素类和氟胞嘧啶,各类药物的适应证、常用剂量和疗程详见附录一。选择抗真菌药物应充分考虑用药的安全性(附录二)、药物之间的相互作用(附录三)及特殊情况下药物剂量的调整(附录四)。
附录一 各类抗真菌药物的抗菌谱[72]、适应证、常用剂量及疗程

续表

续表
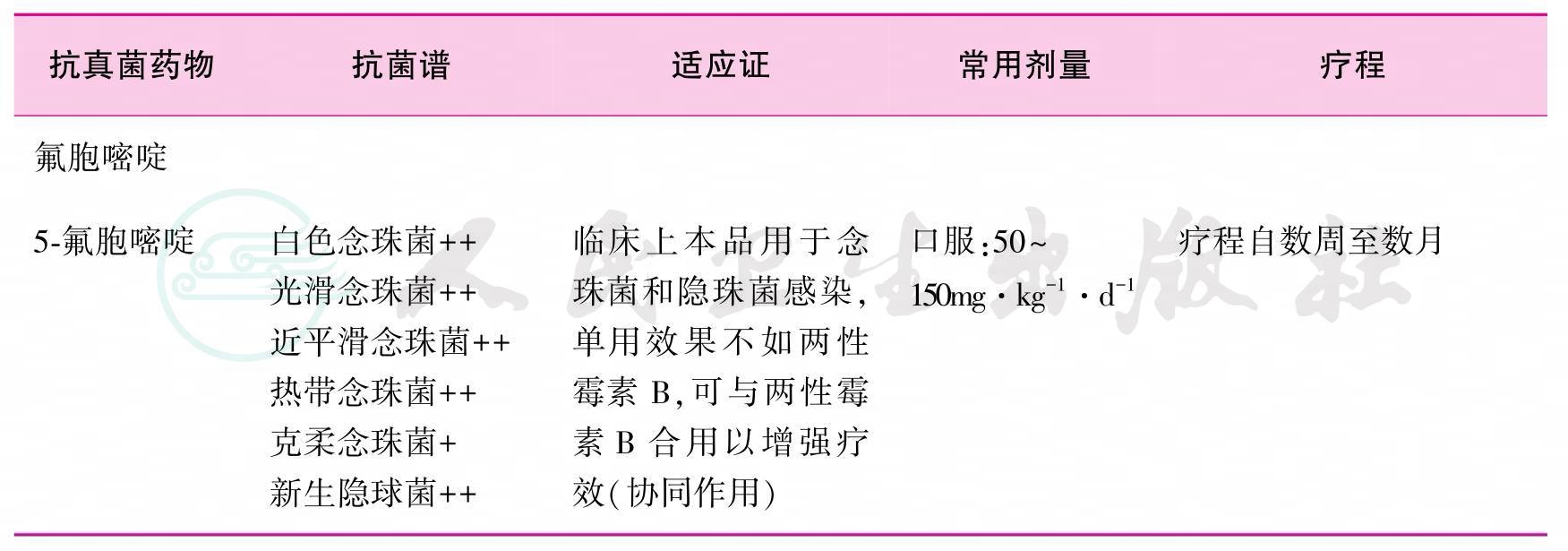
注:表中的“+”表示对药物的敏感程度
附录二 各类抗真菌药物的代谢途径、注意事项和常见毒、不良反应[72]
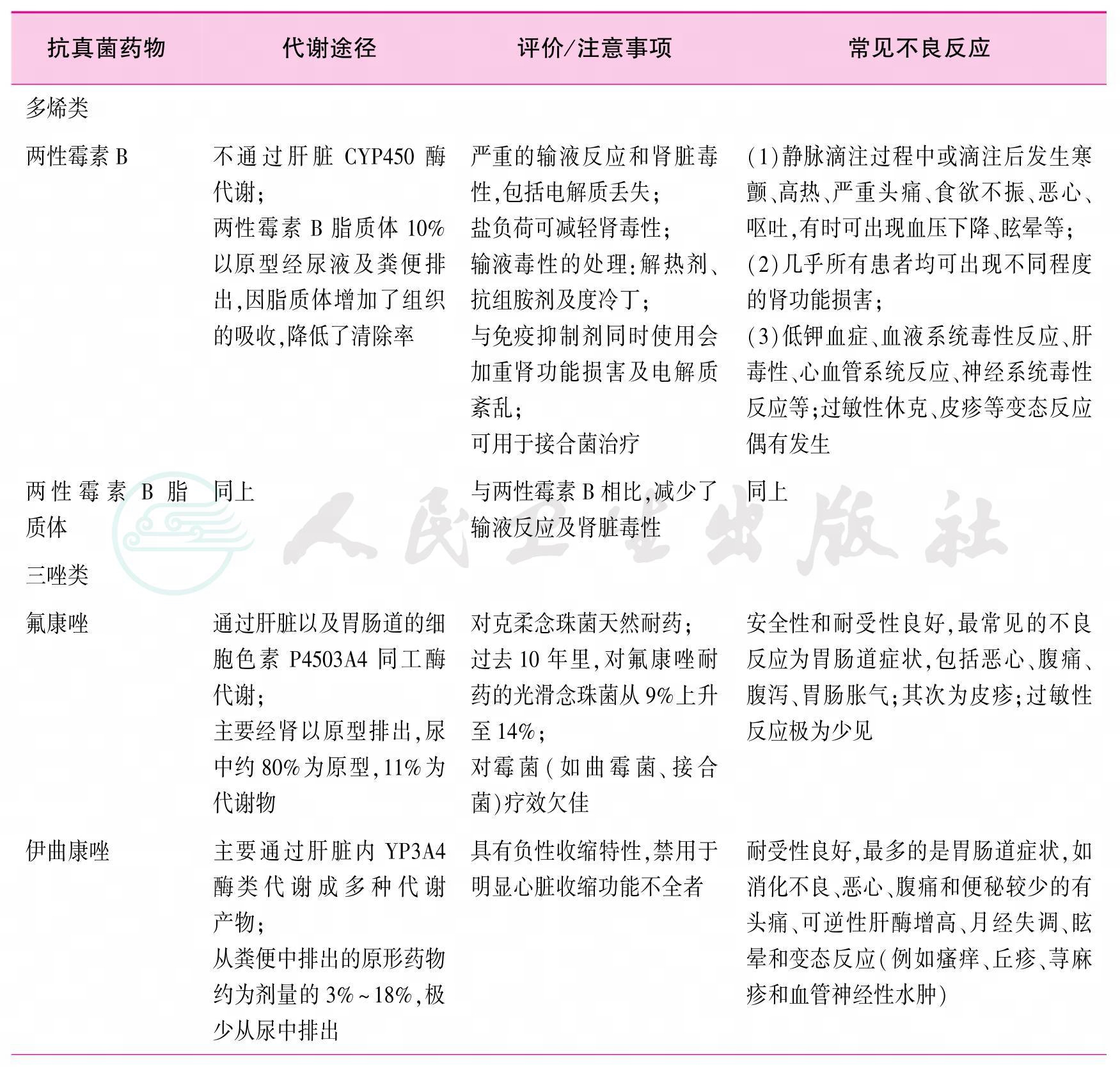
续表

附录三 各类抗真菌药物与免疫抑制剂间的相互作用[73-74]

附录四 各类抗真菌药物在肝、肾功能受损时的剂量调整

推荐意见:
15.侵袭性念珠菌病
(1)念球菌血症:①非中性粒细胞减少患者,强烈推荐使用棘白菌素类药物进行初始治疗(卡泊芬净:负荷剂量70mg,50mg/d;米卡芬净:100mg/d)(1-A),也可以考虑使用两性霉素B脂质体,尤其是肾移植受者,不过要考虑其肾毒性(1-C)。②对于病情不重、没有氟康唑耐药株出现的非中性粒细胞减少患者,可以选择氟康唑(静脉注射或口服,负荷剂量800mg或12mg/kg,400mg/d或6mg·kg-1·d-1)作为棘白菌素类药物的替代治疗(1-A)。③SOT受者不常出现中性粒细胞减少,在这类患者中,一旦出现念珠菌血症,需要强制使用棘白菌素类药物或两性霉素B脂质体进行治疗(1-B)。④必须每天至少进行1次血培养,结果为阴性,才能确认念珠菌血症治愈(1-C)。⑤单纯性念珠菌血症,确认治愈后再治疗14d,对于病情复杂的患者,则需要更长的时间(1-C)。
(2)尿路感染:①出现无症状念珠菌菌尿症,不推荐使用抗真菌药治疗,除非是发展为播散性疾病的高危患者,包括中性粒细胞减少、极低体重儿(<1500g)或患者将接受泌尿系统手术(1-C)。②如菌株对氟康唑敏感,强烈推荐应用氟康唑(200mg/d或3mg·kg-1·d-1)治疗2周(1-B);如氟康唑耐药,则推荐多烯类(或者联合口服5-氟胞嘧啶)作为治疗用药选择(1-C)。③不推荐应用棘白菌素类治疗(1-C)。
(3)肺移植出现吻合口气管支气管念珠菌感染的患者,推荐使用雾化两性霉素B脂质体25mg,每周3次,同时反复使用支气管窥镜清除杂物(1-C)。
(4)念珠菌心内膜炎患者,无论是原发还是人工瓣膜,均推荐1周内(甚至更早)进行手术治疗(1-B)。
(5)眼部念珠菌感染,尚没有菌株药物敏感试验结果时,推荐应用两性霉素B脂质体单药或联合5-氟胞嘧啶治疗,不推荐棘白菌素类(1B);如敏感患者推荐使用氟康唑或伏立康唑(1B);若感染累及玻璃体,则应在全身系统治疗的基础上行玻璃体切除术或玻璃体内注射两性霉素B(1B)。
16.侵袭性曲霉病
(1)对于SOT受者,在高度可疑侵袭性曲霉病时,应早期进行抗真菌治疗(1-C)
(2)根据不同的移植种类、受者的情况、曲霉菌类型及所使用的免疫抑制剂,抗菌治疗应高度个体化(1-C)。
(3)推荐伏立康唑(4mg·kg-1·12h-1,负荷剂量6mg/kg;或200mg/12h口服,负荷剂量400mg/12h口服)或两性霉素B脂质体(3mg·kg-1·d-1)作为初始治疗(1-C)。
(4)对于病情危重的患者,推荐伏立康唑注射给药,以保证生物利用度;对于肾功能受损或病情稳定的患者,可口服给药,并推荐监测血浆浓度保持在2~4mg/L(1-B)。用药过程中注意肝毒性的监测,尤其是肝移植者,并注意其与免疫抑制剂的相互作用(1-C)。
(5)如患者无法用伏立康唑(如肝毒性、严重的药物相互作用、无法耐受及对三唑类过敏等),则推荐使用两性霉素B脂质体(1-C)。
(6)如果病情严重(肺炎或播散性疾病),在保证伏立康唑有效浓度的基础上,可选用伏立康唑加卡泊芬净联合治疗(1-C)。
(7)对于单药初始治疗失败的患者,强烈推荐采用抗真菌药物联合治疗(1-C)。
(8)应根据临床表现和高解析度增强CT定期监测治疗效果(1-C)。
17.侵袭性隐球菌病
(1)对于脑膜炎、播散性疾病或扩散性肺浸润、急性呼吸衰竭患者:①诱导治疗。两性霉素B脂质体3~4mg·kg-1·d-1(1-B);②巩固治疗。氟康唑400~800mg/d,8周(1-B)。③维持治疗。氟康唑200mg/d,6~12个月(1-B)。
(2)对于局灶性肺部感染或无症状患者偶然发现的肺部感染:推荐应用氟康唑400mg/ d(6mg·kg-1·d-1)治疗,疗程为6~12个月(1-B)。
7 利益声明
本指南的发布不存在与任何公司、机构或个人之间的利益冲突。
[1]中国侵袭性真菌感染工作组.血液病/恶性肿瘤患者侵袭性真菌病的诊断标准与治疗原则(第四次修订版)[J].中华内科杂志,2013,52(8):704-709.DOI:10.3760/cma.j.issn.0578-1426.2013.08.030.
[2]Grossi PA,Gasperina DD,Barchiesi F,et al.Italian guidelines for diagnosis,prevention,and treatment of invasive fungal infections in solid organ transplant recipients[J].Transplant Proc,2011,43(6):2463-2471.DOI:10.1016/j.transproceed.2011.06.020.
[3]中华医学会器官移植学分会.实体器官移植患者侵袭性真菌感染的诊断和治疗指南[J].中华器官移植杂志,2009,30(7):440-441.DOI:10.3760/cma.j.issn.0254-1785.2009.07.016.
[4]中华医学会器官移植学分会.实体器官移植患者侵袭性真菌感染的诊断和治疗指南(续)[J].中华器官移植杂志,2009,30(8):503-506.DOI:10.3760/cma.j.issn.0254-1785.2009.08.017.
[5]Castanheira M,Messer SA,Dietrich RR,et al.Antifungal susceptibility patterns of a global collection of fungal isolates and polysorbate-80 effect on the susceptibility of the antifungal classes[R].Philadelphia:Week Meeting of the Infectious Diseases Society of America,2014:1454.
[6]Pappas PG,Kauffman CA,Andes DR,et al.Clinical Practice Guideline for the Management of Candidiasis:2016 Update by the Infectious Diseases Society of America[J].Clin Infect Dis,2016,62(4):e1-50.DOI:10.1093/cid/civ933.
[7]Perfect JR,Dismukes WE,Dromer F,et al.Clinical practice guidelines for the management of cryptococcal disease:2010 update by the infectious diseases society of america[J].Clin Infect Dis,2010,50(3):291-322.DOI:10.1086/649858.
[8]Walsh TJ,Anaissie EJ,Denning DW,et al.Treatment of aspergillosis:clinical practice guidelines of the Infectious Diseases Society of America[J].Clin Infect Dis,2008,46(3):327-360.DOI:10.1086/525258.
[9]Gavaldà J,Meije Y,Fortún J,et al.Invasive fungal infections in solid organ transplant recipients[J].Clin Microbiol Infect,2014,20 Suppl 7:27-48.DOI:10.1111/1469-0691.12660.
[10]De Pauw B,Walsh TJ,Donnelly JP,et al.Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group(EORTC/MSG)Consensus Group [J].Clin Infect Dis,2008,46(12):1813-1821.DOI:10.1086/588660.
[11]Guyatt GH,Oxman AD,Vist GE,et al.GRADE:an emerging consensus on rating quality of evidence and strength of recommendations[J].BMJ 2008,336(7650):924-926.DOI:10.1136/bmj.39489.470347.AD.
[12]Pappas PG,Alexander BD,Andes DR,et al.Invasive fungal infections among organ transplant recipients:results of the Transplant-Associated Infection Surveillance Network(TRANSNET)[J].Clin Infect Dis,2010,50(8):1101-1111.DOI:10.1086/651262.
[13]Neofytos D,Fishman JA,Horn D,et al.Epidemiology and outcome of invasive fungal infections in solid organ transplant recipients[J].Transpl Infect Dis,2010,12(3):220-229.
[14]蒋进发,魏思东,张宇,等.肝脏移植术后侵袭性真菌感染的临床特点分析[J].中华医院感染学杂志,2014,24(8):1998-2000.DOI:10.11816/cn.ni.2014-135058.
[15]Rodríguez C,Muñoz P,Rodríguez-Créixems M,et al.Bloodstream infections among heart transplant recipients [J].Transplantation,2006,81(3):384-391.
[16]Moreno A,Cervera C,Gavald J,et al.Bloodstream infections among transplant recipients:results of a nationwide surveillance in Spain[J].Am J Transplant,2007,7(11):2579-2586.
[17]Zicker M,Colombo AL,Ferraz-Neto BH,et al.Epidemiology of fungal infections in liver transplant recipients:a six-year study of a large Brazilian liver transplantation centre[J].Mem Inst Oswaldo Cruz,2011,106(3):339-345.
[18]Morgan J,Wannemuehler KA,Marr KA,et al.Incidence of invasive aspergillosis following hematopoietic stem cell and solid organ transplantation:interim results of a prospective multicenter surveillance program[J].Med Mycol,2005,43 Suppl 1:S49-58.
[19]Singh N,Avery RK,Munoz P,et al.Trends in risk profiles for and mortality associated with invasive aspergillosis among liver transplant recipients[J].Clin Infect Dis,2003,36(1):46-52.
[20]Gavalda J,Len O,San Juan R,et al.Risk factors for invasive aspergillosis in solid-organ transplant recipients:a case-control study[J].Clin Infect Dis,2005,41(1):52-59.
[21]Lortholary O,Gangneux JP,Sitbon K,et al.Epidemiological trends in invasive aspergillosis in France:the SAIF network(2005-2007)[J].Clin Microbiol Infect,2011,17(12):1882-1889.
[22]Muñoz P,Cerón I,Valerio M,et al.Invasive aspergillosis among heart transplant recipients:a 24-year perspective[J].J Heart Lung Transplant,2014,33(3):278-288.
[23]Grossi P,Farina C,Fiocchi R,et al.Prevalence and outcome of invasive fungal infections in 1963 thoracic organ transplant recipients:a multicenter retrospective study.Italian Study Group of Fungal Infections in Thoracic Organ Transplant Recipients[J].Transplantation,2000,70(1):112-116.
[24]Sun HY,Wagener MM,Singh N.Cryptococcosis in solid-organ,hematopoietic stem cell,and tissue transplant recipients:evidence-based evolving trends[J].Clin Infect Dis,2009,48(11):1566-1576.
[25]Bodro M,Sabé N,Gomila A,et al.Risk factors,clinical characteristics,and outcomes of invasive fungal infections in solid organ transplant recipients[J].Transplant Proc,2012,44(9):2682-2685.DOI:10.1016/j. transproceed.2012.09.059.
[26]Singh N,Alexander BD,Lortholary O,et al.Cryptococcus neoformans in organ transplant recipients:impact of calcineurin-inhibitor agents on mortality[J].J Infect Dis,2007,195(5):756-764.
[27]Husain S,Wagener MM,Singh N.Cryptococcus neoformans infection in organ transplant recipients:variables influencing clinical characteristics and outcome[J].Emerg Infect Dis,2001,7(3):375-381.
[28]Fortún J,Martín-Dávila P,Moreno S,et al.Risk factors for invasive aspergillosis in liver transplant recipients [J].Liver Transpl,2002,8(11):1065-1070.
[29]Fishman JA,Issa NC.Infection in organ transplantation:risk factors and evolving patterns of infection[J].Infect Dis Clin North Am,2010,24(2):273-283.
[30]Fortún J,Meije Y,Fresco G,et al.Aspergillosis.Clinical forms and treatment[J].Enferm Infecc Microbiol Clin,2012,30(4):201-208.
[31]Monforte V,Roman A,Gavalda J,et al.Nebulized amphotericin B prophylaxis for Aspergillus infection in lung transplantation:study of risk factors[J].J Heart Lung Transplant,2001,20(12):1274-1281.
[32]Muñoz P,Rodríguez C,Bouza E,et al.Risk factors of invasive aspergillosis after heart transplantation:protective role of oral itraconazole prophylaxis[J].Am J Transplant,2004,4(4):636-643.
[33]中国侵袭性肺部真菌感染工作组.侵袭性肺部真菌感染的诊断标准与治疗原则(草案)[J].中国实用内科杂志,2006,26(21):1748-1751.DOI:10.3969/j.issn.1005-2194.2006.21.035.
[34]中华医学会重症医学分会.重症患者侵袭性真菌感染诊断与治疗指南(2007)[J].中华内科杂志,2007,46(11):960-966.DOI:10.3760/j.issn:0578-1426.2007.11.031.
[35]Ruiz-Camps I,Aguado JM,Almirante B,et al.Guidelines for the prevention of invasive mould diseases caused by filamentous fungi by the Spanish Society of Infectious Diseases and Clinical Microbiology(SEIMC)[J]. Clin Microbiol Infect,2011,17 Suppl 2:S1-24.DOI:10.1111/j.1469-0691.2011.03477.x.
[36]Gavaldà J,Vidal E,Lumbreras C.Infection prevention in solid organ transplantation[J].Enferm Infecc Microbiol Clin,2012,30 Suppl 2:S27-33.DOI:10.1016/S0213-005X(12)70079-4.
[37]Gavaldà J,Meije Y,Len O’,et al.Invasive fungal infection in solid organ transplant[J].Enferm Infecc Microbiol Clin,2012,30(10):645-653.DOI:10.1016/j.eimc.2012.09.004.
[38]Singh N,Paterson DL,Gayowski T,et al.Preemptive prophylaxis with a lipid preparation of amphotericin B for invasive fungal infections in liver transplant recipients requiring renal replacement therapy[J].Transplantation,2001,71(7):910-913.
[39]Saliba F,Delvart V,Ichaï P,et al.Fungal infections after liver transplantation:outcomes and risk factors revisited in the MELD era[J].Clin Transplant,2013,27(4):E454-461.
[40]Aguado JM,Ruiz-Camps I,Muñoz P,et al.Guidelines for the treatment of Invasive Candidiasis and other yeasts.Spanish Society of Infectious Diseases and Clinical Microbiology(SEIMC)[J].erm Infecc Microbiol Clin,2011,29(5):345-361.DOI:10.1016/j.eimc.2011.01.008.
[41]Singhal S,Ellis RW,Jones SG,et al.Targeted prophylaxis with amphotericin B lipid complex in liver transplantation[J].Liver Transpl,2000,6(5):588-595.
[42]Castroagudín JF,Pontón C,Bustamante M,et al.Prospective interventional study to evaluate the efficacy and safety of liposomal amphotericin B as prophylaxis of fungal infections in high-risk liver transplant recipients [J].Transplant Proc,2005,37(9):3965-3967.
[43]Reed A,Herndon JB,Ersoz N,et al.Effect of prophylaxis on fungal infection and costs for high-risk liver transplant recipients[J].Liver Transpl,2007,13(12):1743-1750.
[44]Hadley S,Huckabee C,Pappas PG,et al.Outcomes of antifungal prophylaxis in high-risk liver transplant recipients[J].Transpl Infect Dis,2009,11(1):40-48.
[45]Fortún J,Martín-Davila P,Moreno S,et al.Prevention of invasive fungal infections in liver transplant recipients:the role of prophylaxis with lipid formulations of amphotericin B in high-risk patients[J].J Antimicrob Chemother,2003,52(5):813-819.
[46]Aguado JM,Varo E,Usetti P,Safety of anidulafungin in solid organ transplant recipients[J].Liver Transpl,2012,18(6):680-685.DOI:10.1002/lt.23410.
[47]Fortún J,Martín-Dávila P,Montejo M,et al.Prophylaxis with caspofungin for invasive fungal infections in high-risk liver transplant recipients[J].Transplantation,2009,87(3):424-435.
[48]Sun HY,Cacciarelli TV,Singh N.Micafungin versus amphotericin B lipid complex for the prevention of invasive fungal infections in high-risk liver transplant recipients[J].Transplantation,2013,96(6):573-578.DOI:10.1097/TP.0b013e31829d674f.
[49]Saliba F,Fischer L,Pascher A,et al.Micafungin as antifungal prophylaxis in high-risk liver transplantation:randomised multicentre trial)[G].Vienna:16th Congress of the European Society for Organ Transplantation, 2013:217.
[50]Saliba F,Fischer L,Pascher A,et al.Efficacy and safety of micafungin as antifungal prophylaxis in high-risk liver transplantation)[G].Denver:53rd International Congress on Antimicrobial Agents and Chemotherapy(ICAAC),2013:810.
[51]Pappas PG,Andes D,Schuster M,et al.Invasive fungal infections in low-risk liver transplant recipients:a multi-center prospective observational study[J].Am J Transplant,2006,6(2):386-391.
[52]San-Juan R,Aguado JM,Lumbreras C,et al.Universal prophylaxis with fluconazole for the prevention of early invasive fungal infection in low-risk liver transplant recipients[J].Transplantation,2011,92(3):346-350.DOI:10.1097/TP.0b013e3182247bb4.
[53]Singh N.Antifungal prophylaxis in solid-organ transplant recipients:considerations for clinical trial design [J].Clin Infect Dis,2004,39 Suppl 4:S200-206.
[54]Cruciani M,Mengoli C,Malena M,et al.Antifungal prophylaxis in liver transplant patients:a systematic review and meta-analysis[J].Liver Transpl,2006,12(5):850-858.
[55]Husain S,Zaldonis D,Kusne S,et al.Variation in antifungal prophylaxis strategies in lung transplantation[J]. Transpl Infect Dis,2006,8(4):213-218.
[56]Palmer SM,Drew RH,Whitehouse JD,et al.Safety of aerosolized amphotericin B lipid complex in lung transplant recipients[J].Transplantation,2001,72(3):545-548.
[57]Drew RH,Dodds Ashley E,Benjamin DK Jr,et al.Comparative safety of amphotericin B lipid complex and amphotericin B deoxycholate as aerosolized antifungal prophylaxis in lung-transplant recipients[J].Transplantation,2004,77(2):232-237.
[58]Monforte V,Ussetti P,Gavald J,et al.Feasibility,tolerability,and outcomes of nebulized liposomal amphotericin B for Aspergillus infection prevention in lung transplantation[J].J Heart Lung Transplant,2010,29(5):523-530.
[59]Gavaldà J,Martín MT,López P,et al.Efficacy of nebulized liposomal amphotericin B in treatment of experimental pulmonary aspergillosis[J].Antimicrob Agents Chemother,2005,49(7):3028-3030.
[60]Monforte V,López-Sánchez A,Zurbano F,et al.Prophylaxis with nebulized liposomal amphotericin B for Aspergillus infection in lung transplant patients does not cause changes in the lipid content of pulmonary surfactant[J].J Heart Lung Transplant,2013,32(3):313-319.DOI:10.1016/j.healun.2012.11.013.
[61]Borro JM,Solé A,de la Torre M,et al.Efficiency and safety of inhaled amphotericin B lipid complex(Abelcet)in the prophylaxis of invasive fungal infections following lung transplantation[J].Transplant Proc,2008,40(9):3090-3093.DOI:10.1016/j.transproceed.2008.09.020.
[62]Monforte V,Ussetti P,López R,et al.Nebulized liposomal amphotericin B prophylaxis for Aspergillus infection in lung transplantation:pharmacokinetics and safety[J].J Heart Lung Transplant,2009,28(2):170-175.DOI:10.1016/j.healun.2008.11.004.
[63]Monforte V,Roman A,Gavaldá J,et al.Nebulized amphotericin B concentration and distribution in the respiratory tract of lung-transplanted patients[J].Transplantation,2003,75(9):1571-1574.
[64]Husain S,Paterson DL,Studer S,et al.Voriconazole prophylaxis in lung transplant recipients[J].Am J Transplant,2006,6(12):3008-3016.
[65]Luong ML,Hosseini-Moghaddam SM,Singer LG,et al.Risk factors for voriconazole hepatotoxicity at 12 weeks in lung transplant recipients[J].Am J Transplant,2012,12(7):1929-1935.DOI:10.1111/j.1600-6143.2012.04042.x.
[66]Cadena J,Levine DJ,Angel LF,et al.Antifungal prophylaxis with voriconazole or itraconazole in lung transplant recipients:hepatotoxicity and effectiveness[J].Am J Transplant,2009,9(9):2085-2091.
[67]Vadnerkar A,Nguyen MH,Mitsani D,et al.Voriconazole exposure and geographic location are independent risk factors for squamous cell carcinoma of the skin among lung transplant recipients[J].J Heart Lung Transplant,2010,29(11):1240-1244.DOI:10.1016/j.healun.2010.05.022.
[68]Singer JP,Boker A,Metchnikoff C,et al.High cumulative dose exposure to voriconazole is associated with cutaneous squamous cell carcinoma in lung transplant recipients[J].J Heart Lung Transplant,2012,31(7):694-699.DOI:10.1016/j.healun.2012.02.033.
[69]Zwald FO,Spratt M,Lemos BD,et al.Duration of voriconazole exposure:an independent risk factor for skin cancer after lung transplantation[J].Dermatol Surg,2012,38(8):1369-1374.DOI:10.1111/j.1524-4725.2012.02418.x.
[70]Epaulard O,Villier C,Ravaud P,et al.A multistep voriconazole-related phototoxic pathway may lead to skin carcinoma:results from a French nationwide study[J].Clin Infect Dis,2013,57(12):e182-188.DOI:10.1093/cid/cit600.
[71]Cornely OA,Bassetti M,Calandra T,et al.ESCMID∗guideline for the diagnosis and management of Candida diseases 2012:non-neutropenic adult patients[J].Clin Microbiol Infect,2012,18 Suppl 7:S19-37.DOI:10.1111/1469-0691.12039.
[72]Nett JE,Andes DR.Antifungal Agents:Spectrum of Activity,Pharmacology,and Clinical Indications[J]. Infect Dis Clin North Am,2016,30(1):51-83.DOI:10.1016/j.idc.2015.10.012.
[73]Shoham S,Marr KA.Invasive fungal infections in solid organ transplant recipients[J].Future Microbiol,2012,7(5):639-655.DOI:10.2217/fmb.12.28.
[74]Chau MM,Kong DC,van Hal SJ,et al.Consensus guidelines for optimising antifungal drug delivery and monitoring to avoid toxicity and improve outcomes in patients with haematological malignancy,2014[J].Intern Med J,2014,44(12b):1364-1388.DOI:10.1111/imj.12600.