 去看看
去看看


1 治疗前评估


【注释】
结外NK/T 细胞淋巴瘤最常见的发病部位是鼻腔。主要表现为鼻或面中线进行性的破坏性病变,以鼻咽及腭部为最常见,其次为口咽、喉咽、扁桃体。鼻腔肿块引起的鼻塞、鼻腔分泌物和鼻出血是常见的首发症状。虽然75%的患者在初始表现时有局限性疾病,但在临床过程中,疾病迅速扩散到皮肤、胃肠道、睾丸等各个部位,但很少累及淋巴结,晚期病变常出现肝脏、脾脏肿大。对于初诊患者,应对于上述部位进行仔细的体格检查。血浆EBV-DNA 检测。全血并不是最佳的检测介质,全血中白细胞计数、记忆B 细胞数量和白细胞DNA 都有可能导致定量聚合酶链反应(PCR) 检测误差。在最近的一项研究中,血浆已被证实优于全血。血浆EBV-DNA 定量在诊断时可间接测定淋巴瘤负荷。治疗过程中,还能提示淋巴瘤对治疗反应的动态变化。在治疗结束时,EBV-DNA 对微小残残留病灶做出估计,对预后有重要意义[1]。
2 病理诊断

【注释】
随着近年来二代测序技术的应用,有研究发现部分基因与预后相关。调控RNA 的一个重要基因——RNA 解旋酶DDX3X 基因在NKTCL 中存在高频突变,是患者预后不良的分子标志。最新研究[8]发现晚期NKT 淋巴瘤患者中,ECSIT(evolutionarily conserved signaling intermediate in tollpathways) 基因V140A[第140 位缬氨酸(Val) 突变为丙氨酸(Ala)]的突变,容易诱发临床噬血细胞综合征[9]。
3 分期
目前尚无标准的ENKTL 分期系统。临床仍参照传统的Lugano 分期(见附录A),但Lugano分期应用在ENKTL 中并不理想。ENKTCL 根据原发病灶不同的解剖部位,分为上呼吸消化道原发NKTCL(Upper aerodigestive tract,UAT-NKTCL) 和非上呼吸消化道原发NKTCL(Non-upperaerodigestive tract,NUAT-NKTCL) 两种亚型。前者临床常见,占NKTCL 的80%以上,好发于面部中线部位,如鼻腔及鼻咽、口腔及口咽等;NUAT-NKTCL 仅占NKTCL 的10% ~20%,常侵犯皮肤、胃肠道、睾丸、肺脏和肝脏等,恶性程度更高,晚期患者比例高,预后差。
附录A 2014 版Lugano 分期标准(CT、MRI 或PETCT作为分期检查方法)

【注释】
1.*.根据2014年Lugano改良分期标准,不再对淋巴瘤的大包块(bulky)病灶进行具体的数据限定,只需在病例中明确记载最大病灶之最大径即可;Ⅱ期伴有大肿块的患者,应根据病理类型及疾病不良预后因素而酌情选择治疗原则,如伴有大包块的惰性淋巴瘤患者可选择局限期治疗模式,但是伴有大包块的侵袭性淋巴瘤患者,则应选择进展期治疗模式。
2.AnnArbor分期对于淋巴结分布区域的定义(仍然适用于Lugano分期):膈上(共12个区域,由于不能被一个放射野涵盖,因此左右各为一个区域):韦氏环(Waldeyer环)(鼻咽及口咽部的淋巴组织环,包括腭扁桃体、咽后壁腺样体、舌扁桃体及其他该部位淋巴组织为一个区域)、左/右颈部(单侧耳前、枕部、颌下、颏下、颈内、锁骨上为一个区域)、左/右锁骨下、左/右腋窝(含胸部及内乳)、左/右滑车上(含肘窝)、纵隔(含气管旁、胸腺区域)、左/右肺门;膈下(共9个区域):脾脏、上腹部(脾门、肝门、腹腔)、下腹部(腹主动脉旁、腹膜后、肠系膜周围、腹部其他非特指淋巴结为一个区域)、左/右髂血管旁、左/右腹股沟(含股部)、左/右腘窝。
3.3.B症状主要在HL中有预后意义并需要记录;最新文献中B症状在NHL的价值较低,但是仍然建议在病例中记录。所谓B症状:不明原因体重下降10%(诊断前6个月内),发热>38℃并排除其他原因发热,盗汗(夜间大量出汗,需要更换衣服被褥)。
4.扁桃体、韦氏环、脾脏视为淋巴器官。
5.备注:淋巴瘤的分期尽管不断改良,但是争议持续存在,主要是对于分期的定义存在解读分歧,或者对特殊部位未能做出全面而明确的定义。正因如此,后续才建立了多种预后指数用于补充临床分期之不足,以指导临床治疗和判断预后。而且,不同于实体瘤的是,淋巴瘤的临床分期不是决定治疗和预后的最关键因素。
4 治疗
4.1 初治Ⅰ / Ⅱ期UAT-NKTCL 治疗策略
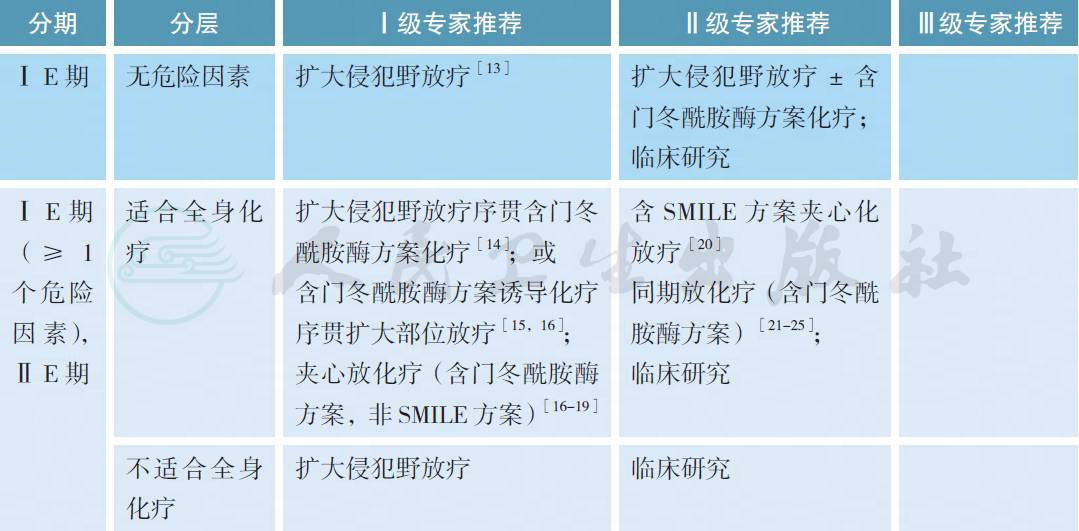
【注释】
(1)COEP-L 方案
CTX 750mg/m2,d1
VCR 1.4mg/m2,d1(最大2mg)
VP-16 60mg/m2,d1-3
PDN 100mg,d1-5
培门冬酶2500IUmg/m2,d2
每21d 重复。
(2)LOP 方案
培门冬酶2500IUmg/m2,d1
VCR 1.4mg/m2,d1(最大2mg)
PDN 100mg,d1-5
每14~21d 重复。
(3)SMILE 方案
甲氨蝶呤2g/m2,连续输注6h,d1
亚叶酸钙15mg×4 次,d2-4
异环磷酰胺1500mg/m2,d2-4
美司钠300mg/m2×3 次,d2-4
地塞米松40mg/d,d2-4
依托泊苷100mg/m2,d2-4
左旋门冬酰胺酶6000U/m2,d8,d10,d12,d14,d16,d18,d20
每28d 重复。
第6天开始给予粒细胞集落刺激因子直至白细胞>5×109/L。
(4)P-Gemox 方案:详见初始Ⅲ / Ⅳ期及难治复发ENKTL 治疗策略。
4.2 初治Ⅰ / Ⅱ期NUAT-NKTCL 治疗策略

【注释】
结外鼻型NK/T 细胞淋巴瘤放疗照射野和照射剂量是治疗成败的关键,与肿瘤局部区域控制率和预后密切相关,早期病人推荐扩大受累野照射50Gy 根治剂量。鼻腔原发NK/T 细胞淋巴瘤局限于一侧鼻腔,未侵犯邻近器官或组织结构(局限Ⅰ期),临床靶区(CTV) 包括双侧鼻腔、双侧前组筛窦、硬腭和同侧上颌窦内壁;若双鼻腔受侵则包括双侧上颌窦内壁。肿瘤超出鼻腔时(广泛Ⅰ期),靶区应扩大至受累的邻近器官和结构。合并上颌窦内壁受侵时,照射受侵侧整个上颌窦、前组筛窦受侵时,应包括同侧后组筛窦。如果肿瘤邻近后鼻孔或侵犯鼻咽,CTV 应扩展至鼻咽。Ⅰ期不做颈预防照射,Ⅱ期需同时做双颈照射或照射中上颈淋巴结。韦氏环包括鼻咽、口咽、扁桃体和舌根,任何原发部位韦氏环NK/T 细胞淋巴瘤CTV 应包括整个韦氏环和后鼻孔。Ⅰ期可以考虑做颈淋巴结预防照射,Ⅱ期做治疗性照射。
早期ENKTCL 需要进行风险分层治疗,Ⅰ期无危险因素(年龄<60 岁,ECOG 0~1 分,LDH 正常,Ⅰ期无原发肿瘤局部广泛侵犯),单纯放疗即可取得较好的效果,与综合治疗结果相似;单纯放疗、放疗后化疗和化疗后放疗的5 年生存率分别为88.8%、86.9%和86.3%(P=0.972)[13]。Ⅰ期伴有危险因素及初治Ⅱ期接受单纯放疗仍存在较高复发风险。因此,需要考虑增加化疗降低复发概率。含左旋门冬酰胺的化疗方案成为治疗NK/T 淋巴瘤最有效的全身化疗方案。同期放化疗在日本和韩国以外的地区很少临床应用[21-24]。有研究认为同期放化疗与序贯化放疗疗效相当[25],接受同期放化疗可带来较高的口腔黏膜毒性。诱导化疗序贯放疗和夹心放化疗已成为目前常用的治疗策略。NCCN 指南推荐的SMILE 和AspaMetDex 方案有效率高[20],但毒性亦非常明显,并出现治疗相关死亡,需慎重选择,并做个体化处理。P-Gemox 方案疗效高,不良反应较轻,可以门诊执行,是现阶段治疗初治ENKTL 患者的一种高效、低毒、应用简便和性价比高的治疗选择[15]。
4.3 初治Ⅲ / Ⅳ期及难治复发ENKTL 治疗策略

【注释】
(1)AspaMetDex 方案
门冬酰胺酶6000U/m2,d2,d4,d6,d8
甲氨蝶呤3g/m2,d1
地塞米松40mg/d,d1-4
每21d 重复。
如果年龄>70 岁,甲氨蝶呤减量至2g/m2,地塞米松减量至20mg。
(2)P-Gemox 方案
培门冬酶2500IU/m2,d1
吉西他滨1250mg/m2,d1
奥沙利铂80mg/m2,d1
每21d 重复。
(3)DDGP 方案
地塞米松15mg/m2,d1-5
顺铂20mg/m2,d1-4
吉西他滨800mg/m2,d1,d8
培门冬酶2500IU/m2,d1
每21d 重复。
SMILE 方案初治Ⅲ / Ⅳ期及难治复发ENKTL 中的疗效显著。ORR 达到67% ~77 %,CR 率达50% ~66%[20,26]。预计5 年OS 为52.3%,4 年无病生存率为68.2%。但该方案骨髓抑制明显,92%患者出现4级中性粒细胞减少,60%出现3 度及以上感染,治疗相关死亡率可达10%。另外一个明显的非血液学毒性是肾功能损害。因此,临床应用该方案时应有足够的支持措施。调整剂量的SMILE 方案安全性较高。AspaMetDex 方案[27]治疗复发患者,疗效与SMILE 相当,安全性略胜一筹。对于复发和难治性NK/T 细胞淋巴瘤,单纯常规化疗预后差,尽管自体造血干细胞移植的确切价值仍存争议,但多个回顾性研究表明,晚期或敏感复发患者,获高质量缓解后,可以从自体移植获益[28]。异基因移植目前处于探索的阶段,因其治疗相关风险较大,可尝试治疗自体移植后复发的难治患者[29,30]。
5 预后评估
PINK-E(prognostic index of natural killer lymphoma) 预后评分系统

【注释】
国际淋巴瘤预后指数(international prognostic index,IPI) 预测ENKTCL 的预后尚不够理想[10]。在含左旋门冬酰胺酶化疗时代,PINK 预后模型,分别从年龄是否>60 岁、分期、是否鼻型、是否累及远端淋巴结4 个方面评分,同时包含血浆EBV-DNA 水平形成PINK-E 模型[11],使ENKTL 的预后预测更加合理准确。基于中国大样本数据的ENKTCL 列线图(nomogram)模型[12]。危险因素包括:年龄>60 岁、Ann Arbor Ⅱ期和Ⅲ ~ Ⅳ期、原发肿瘤侵犯(primary tumor invasion,PTI)、ECOG 评分>2 和LDH 升高。该模型预测能力强,特别是可以对早期NKTCL 进行风险分层,并指导治疗。
[1]Kim SJ,Choi JY,Hyun SH,et al. Asia Lymphoma Study Group. Risk stratification on the basis of Deauville score on PET-CT and the presence of Epstein-Barr virus DNA after completion of primarytreatment for extranodal natural killer/T-cell lymphoma,nasal type:a multicentre,retrospectiveanalysis. Lancet Haematol,2015,2(2):e66-74.
[2]Pongpruttipan T,Sukpanichnant S,Assanasen T,et al. Extranodal NK/T-cell lymphoma,nasal type,includes cases of natural killer cells and αβ,γδ,and αβ/γδ T-cell origin:a comprehensiveclinicopathologic and phenotypic study. Am J Surg Pathol,2012,36(4):481-499.
[3]Asano N,Kato S,Nakamura S. Epstein-Barr virus-associated natural killer/T-cell lymphomas. BestPract Res Clin Haematol,2013,26(1):15-21.
[4]Jiang Q,Liu S,Peng J,et al. An extraordinary T/NK lymphoma,nasal type,occurring primarily in the prostate gland with unusual CD30 positivity:case report and review of the literature. Diagn Pathol,2013,8:94-97
[5]Weiben Yong,Wen Zheng,Jun Zhu,et al. L-Asparaginase–based regimen in the treatment ofrefractory midline nasal/nasal-type T/NK-cell lymphoma. International Journal of Hematology,2003,78:163-167.
[6]Tse E,Kwong YL. How I treat NK/T-cell lymphomas. Blood,2013,121(25):4997-5005.
[7]Takahara M,Kishibe K,Bandoh N,et al. P53,N- and K-Ras,and betacatenin gene mutations and prognostic factors in nasal NK/T cell lymphoma from Hokkaido,Japan. Hum Pathol,2004,35(1):86-95.
[8]Jiang L,Gu ZH,Yan ZX,et al. Exome sequencing identifies somatic mutations of DDX3X in naturalkiller/T-cell lymphoma.Nat Genet,2015 Sep,47(9):1061-1066.
[9]Wen H,Ma H,Cai Q,et al. Recurrent ECSIT mutation encoding V140A triggers hyperinflammationand promotes hemophagocytic syndrome in extranodal NK/T cell lymphoma.Nat Med,2018 Jan 1. doi:10.1038/nm.4456
[10]Lee J,Suh C,Park YH,et al. Extranodal natural killer Tcell lymphoma,nasal-type:a prognosticmodel from a retrospective multicenter study. J Clin Oncol,2006,24(4):612-618.
[11]Kim SJ,Yoon DH,Jaccard A,et al. A prognostic index for natural killer cell lymphoma after non-anthracycline based treatment:a multicentre,retrospective analysis. Lancet Oncol,2016 Mar,17(3):389-400.
[12]Yang Y,Zhang Y J,Zhu Y,et al . Prognostic nomogram for overall survival in previously untreatedpatients with extranodal NK/T-cell lymphoma,nasal-type:a multicenter study. Leukemia,2015,29(7):1571-1577.
[13]Yang Y,Cao JZ,Lan SM,et al. Association of improved locoregional control with prolonged survival in earlystage extranodal nasal-type natural killer/T-cell lymphoma. JAMA Oncol,2017 Jan 1,3(1):83-91.
[14]Yang Y,Zhu Y,Cao JZ,et al. Risk-adapted therapy for early-stage extranodal nasal-type NK/T-celllymphoma:analysis from a multicenter study. Blood,2015,126(12):1424-1432.
[15]Yan Gao,Hui-qiang Huang,Cai QiChun,et al. Efficacy and safety of pegaspargase with gemcitabineand oxaliplatin in patients with treatment-naïve,refractory extranodal natural killer/T-cell lymphoma:a single-centre experience.Blood,2013,122:642.
[16]Ningjing Lin,Yuqin Song,Jun Zhu,et al. A prospective phase Ⅱ study of L-asparaginase- CHOPplus radiation in newly diagnosed extranodal NK/T-cell lymphoma,nasal type. Journal of Hematology& Oncology,2013,6:44-54.
[17]Jiang M,Zhang H,Jiang Y,et al. Phase 2 trial of “sandwich” L-asparaginase,vincristine,and prednisone chemotherapy with radiotherapy in newly diagnosed,stage Ⅰ E to Ⅱ E,nasal type,extranodal natural killer/T-cell lymphoma. Cancer,2012,118(13):3294-3301.
[18]Zhang L,Jiang M,Xie L,et al. Five-year analysis from phase 2 trial of “sandwich” chemoradiotherapy in newly diagnosed,stage Ⅰ E to Ⅱ E,nasal type,extranodal natural killer/T-celllymphoma. Cancer Med,2016,5(1):33-40.
[19]Wang L,Wang ZH,Chen XQ,Li YJ,Wang KF,Xia YF,Xia ZJ. First-line combination ofgemcitabine,oxaliplatin,and L-asparaginase(GELOX) followed by involved-field radiationtherapy for patients with stage Ⅰ E/ Ⅱ E extranodal natural killer/T-cell lymphoma. Cancer,2013,119(2):348-355.
[20]Kwong YL,Kim WS,Lim ST,et al. SMILE for natural killer/T-cell lymphoma:analysis of safetyand efficacy from the Asia Lymphoma Study Group. Blood,2012,120(15):2973-2980.
[21]Yamaguchi M,Tobinai K,Oguchi M,et al. Phase Ⅰ / Ⅱ study of concurrent chemoradiotherapy for localized nasal natural killer/T-cell lymphoma:Japan Clinical Oncology Group Study JCOG0211.J ClinOncol,2009,27(33):5594-5600.
[22]Kim SJ,Kim K,Kim BS,et al. Phase Ⅱ trial of concurrent radiation and weekly cisplatin followed by VIPD chemotherapy in newly diagnosed,stage Ⅰ E to Ⅱ E,nasal,extranodal NK/T-Cell Lymphoma:Consortium for Improving Survival of Lymphoma study. J Clin Oncol,2009,27(35):6027-6032.
[23]Yamaguchi M,Tobinai K,Oguchi M,et al.Concurrent chemoradiotherapy for localized nasal naturalkiller/T-cell lymphoma:an updated analysis of the Japan clinical oncology group study JCOG0211. JClin Oncol,2012,30(32):4044-4046.
[24] Kim SJ,Yang DH,Kim JS,et al. Concurrent chemoradiotherapy followed by L-asparaginase-containing chemotherapy,VIDL,for localized nasal extranodal NK/T cell lymphoma:CISL08-01 phase Ⅱstudy. Ann Hematol,2014,93(11):1895-1901.
[25] Kwong YL,Kim SJ,Tse E,et al. Sequential chemotherapy/radiotherapy was comparable withconcurrent chemoradiotherapy for stage Ⅰ / Ⅱ NK/T-cell lymphoma. Ann Oncol,2018 Jan 1,29(1):256-263.
[26]Yamaguchi M,Kwong YL,Kim WS,et al. Phase Ⅱ study of SMILE chemotherapy for newlydiagnosed stage Ⅳ,relapsed,or refractory extranodal natural killer (NK)/T-cell lymphoma,nasaltype:the NK-Cell Tumor Study Group study.J Clin Oncol,2011,29(33):4410-4416.
[27] Jaccard A,Gachard N,Marin B,et al. GELA and GOELAMS Intergroup. Efficacy of L-asparaginasewith methotrexate and dexamethasone(AspaMetDex regimen) in patients with refractory or relapsingextranodal NK/T-cell lymphoma,a phase 2 study. Blood,2011,117(6):1834-1839.
[28]Lee J,Au WY,Park MJ,et al. Autologous hematopoietic stem cell transplantation in extranodalnatural killer/T cell lymphoma:a multinational,multicenter,matched controlled study.Biol BloodMarrow Transplant,2008 Dec,14(12):1356-1364.
[29]Kwong YL. High-dose chemotherapy and hematopoietic SCT in the management of natural killer-cellmalignancies. Bone Marrow Transplant,2009,44(11):709-714.
[30]Weiben Yong,Wen Zheng,Jun Zhu,et al. L-Asparaginase in the treatment of refractory and relapsedextranodal NK/T-cell lymphoma,nasal type. Ann Hematol,2009,88:647-652.