 去看看
去看看


干扰素α(IFN-α)广泛应用于慢性乙型肝炎(CHB)和慢性丙型肝炎(CHC)的抗病毒治疗,但存在较多不良反应,常见的不良反应有流感样症状、外周血细胞和血小板计数下降、内分泌和代谢性疾病、消化道症状和神经精神异常等,发生率见表1。少数患者可引起严重不良反应,如间质性肺炎、自身免疫性溶血或严重精神性疾病等。正确处理IFN-α治疗中的不良反应可提高患者依从性,从而有效提高IFN-α疗效。发生严重不良反应者常需停止治疗,以保证患者的安全。为进一步规范并优化慢性病毒性肝炎患者IFN-α不良反应的管理和治疗,《中华实验和临床感染病杂志(电子版)》、《中国肝脏病杂志(电子版)》及Infection International(Electronic Edition)编辑部组织国内部分专家对相关资料进行整理与分析,形成《慢性病毒性肝炎患者干扰素α治疗不良反应临床处理专家共识》(以下简称共识)。本《共识》是基于目前该领域的最新成果,遵照循证医学原则编写,可作为慢性病毒性肝炎患者干扰素α不良反应临床处理的指导。随着相关临床证据的不断积累,专家委员会将对《共识》内容进行持续更新。相应证据及推荐等级见表2。
表1 聚乙二醇化干扰素(PegIFN)-α-2a/2b不良反应发生率

续表
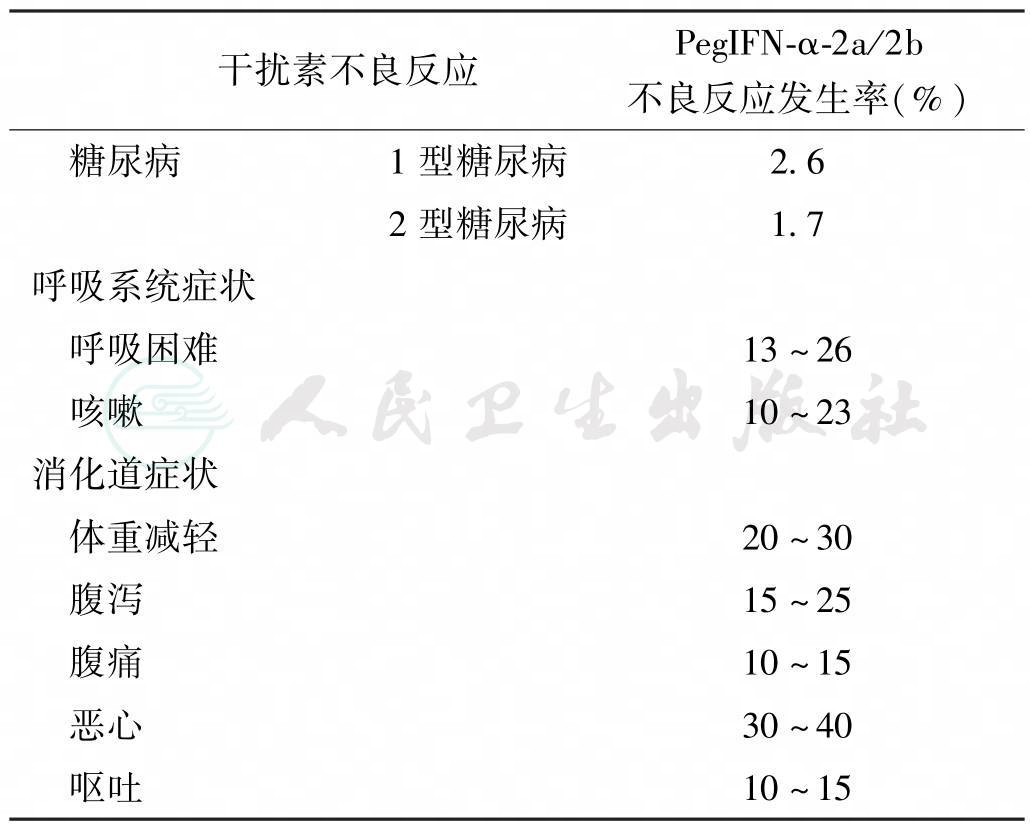
表2 循证医学证据与推荐等级(参照GRADE系统)
1 流感样症状
1.1 概述与机制
IFN-α可引起包括白细胞介素-1 (IL-1)、白细胞介素-6(IL-6)和肿瘤坏死因子α(TNF-α)在内的一系列细胞因子的释放,从而引起流感样症状。
1.2 临床表现
流感样症状包括发热、肌肉关节酸痛和乏力等,绝大多数患者可发生,但严重程度存在个体差异,部分患者可仅表现为轻度乏力。流感样症状常发生于初次注射IFN-α者,发热多出现在初次IFN-α注射后2~4小时,持续2~4小时后常可自行消退,在随后治疗中发热和肌肉关节酸痛等症状逐渐减轻,但患者仍可感觉乏力,尤其在CHC患者的IFN-α联合利巴韦林治疗中,常因利巴韦林所致的贫血,患者乏力症状更加明显。
1.3 临床处理
症状不明显者可不予处理。症状明显者建议休息,多饮水;高体温和肌肉关节酸痛明显而难以耐受者可口服如对乙酰氨基酚等解热镇痛药物治疗(A1)。在长期使用IFN-α过程中出现较长时间发热,且与IFN-α注射有一定规律性的发热、肌肉酸痛等,应检查患者血沉及自身抗体以除外自身免疫相关性发热(B1)。
2 外周血细胞下降
2.1 概述与机制
在IFN-α治疗所致的外周血细胞下降中,以中性粒细胞和血小板(PLT)下降最为明显,其发生机制尚未完全明确,可能与IFN-α直接对骨髓祖细胞(progenitor cells)增殖的直接抑制有关。也可能与粒细胞集落刺激因子(G-CSF)或巨噬细胞粒细胞集落刺激因子(GM-CSF)分泌下降有关。此外,IFN-α所致中性粒细胞计数下降可能与患者基因多态性即IFN-α信号通路基因的单核苷酸多态性(SNPs)有关,故表现为个体差异。
2.2 临床表现
中性粒细胞显著下降常发生在治疗2~314天(平均47天),且低体重患者可能下降程度更加明显。如患者中性粒细胞下降幅度为100%,其中第1周下降约20%,治疗2周下降40%~60%,治疗12周达最低水平。中性粒细胞下降呈IFN-α剂量依赖,常为IFN-α剂量调整的最主要原因,约22%患者因中性粒细胞下降而需调整IFN-α剂量。但目前尚无证据表明IFN-α所致中性粒细胞下降可增加细菌感染率。血小板计数下降更多见于IFN-α联合利巴韦林治疗的CHC患者,血小板计数与基线相比可下降42%,与中性粒细胞下降相似,在治疗12周降至最低水平,9.3%患者下降至<50 000/μl,2.8%患者下降至<25 000/μl;9.3%血小板计数为25 000~50 000/μl 和33.3%血小板计数<25 000/μl患者发生出血,但严重出血很少见。
2.3 临床处理
①PegIFN-α-2a产品说明书指出:外周血中性粒细胞计数<0.75×109/L者需调整IFN-α剂量,而<0.5× 109/L者需停止IFN-α治疗。Soza等研究表明,虽然18%IFN-α长期治疗者发生细菌感染,但与中性粒细胞计数下降无显著相关性,故认为中性粒细胞下降者可使用升白细胞药物而无需停药。但Puoti等队列研究发现中性粒细胞下降与呼吸道感染相关,中性粒细胞下降的CHC患者使用升白细胞药物较降低干扰素剂量疗效更佳。因此,推荐中性粒细胞显著下降者可注射rhG-CSF,也可口服升白细胞药物,尤其对于免疫功能低下或抑制者,粒细胞刺激因子的应用可能更加重要。②PegIFN-α产品说明书指出:PegIFN-α治疗期间血小板计数为25 000~50 000/μl者需减少 PegIFN-α剂量,而 <25 000/μl者需停止PegIFN-α治疗。而在急性粒细胞白血病的诱导化疗中,仅血小板计数低于10 000/μl且有显著出血者需输注血小板进行治疗。IFN-α治疗CHC,即使患者血小板计数<50 000/μl,甚至<25 000/μl者,严重出血发生率极低。因此,在无其他抗病毒方案可选择的情况下,在患者充分知情同意情况下,即使患者血小板计数<25 000/μl,应该权衡利弊也可在严密监测并降低IFN-α剂量进行治疗,而非盲目停药。如血小板计数<20 000/μl,即使仅伴皮肤黏膜出血,建议持谨慎态度,必要时可考虑停用IFN-α。
需特别指出,IFN-α本身所致的中性粒细胞和血小板计数下降常为渐进性,临床实践中出现快速或急剧中性粒细胞、血小板计数下降,包括血红蛋白下降,应考虑为IFN-α所致的自身免疫性溶血或血小板下降,三系急速下降者还应考虑再生障碍性贫血。IFN-α治疗期间一旦出现急剧的白细胞、血小板计数和血红蛋白下降,应立即停止IFN-α治疗并请血液科医师进行诊治。
3 神经精神系统
3.1 概述与机制
IFN-α可通过改变中枢肾上腺素、5-羟色胺、阿片样物质和神经内分泌因子分泌,诱导患者发生或加重抑郁和其他精神神经系统的不良反应。CHC患者精神异常发生更为常见,与丙型肝炎病毒(HCV)诱导白细胞介素 1β (IL-1β)和TNF-α表达有关。
3.2 临床表现
IFN-α治疗所致的精神神经系统不良反应包括急性精神紊乱、抑郁、精神恍惚、焦虑、烦躁等,偶尔也有欣快感。神经系统并发症包括癫痫样发作、脑白质病、动眼神经麻痹、三叉感觉神经病变等。急性精神紊乱常见于大剂量IFN-α治疗中,抑郁多见于CHC患者,发生率约为21%~58%,常发生于IFN-α治疗2个月后,3个月后达高峰,而焦虑在第3~4个月达高峰。
3.3 临床处理
①精神疾病发生率与治疗前危险因素、IFN-α剂量和治疗时间相关。IFN-α治疗前应仔细询问患者的精神疾病史及家族史,对有此类病史的患者进行蒙哥马利-艾森贝格抑郁量表评分。②IFN-α治疗过程中出现情绪低落、焦虑和易怒的患者,应及时请心理专科医师进行评估和诊治,症状严重者或伴自杀或伤害他人倾向时应及时停用IFN-α(A1)。③药物治疗不能控制的抑郁或躁狂患者应及时停用IFN-α。④治疗前应由心理专科医师对高危患者进行评估,在充分知情同意的前提下谨慎使用IFN-α,并由心理和精神科专科医师及家人进行严密监测,目前尚无证据表明高危险人群预防用药可获益(B1)。
IFN-α相关神经精神症状预后良好,多数患者经抗抑郁药物治疗可较快得到缓解。停用IFN-α后,其相应精神症状可于数周至3个月缓解。因再次应用IFN-α还会出现IFN-α相关神经精神症状,故因严重精神神经不良反应而停药者,不建议再次使用IFN-α。
4 皮肤黏膜病变
4.1 概述与机制
IFN-α治疗中出现皮肤黏膜病变可能与IFN-α所致皮肤变态反应和自身免疫反应有关,尤其在慢性HCV感染者和变态反应疾病患者。
4.2 临床表现
IFN-α所致的皮肤黏膜病变以皮疹最为常见,常表现为非特异伴瘙痒的皮疹;其他表现有注射部位红斑、皮肤溃烂、口腔黏膜溃烂和口唇炎等。
4.3 处理
①皮疹伴瘙痒:避免食用海鲜或辛辣等易过敏或加重病情的食物,避免使用强有力的皮肤去污剂,可予炉甘石洗剂、含糖皮质激素成分的乳膏涂抹,亦可口服抗组胺类药物(B1)。②对常规药物不能控制的皮肤黏膜病变,在无激素治疗禁忌证下,可口服低剂量激素治疗。③药物不能控制和严重影响患者生活质量的皮肤黏膜病变,也应停止IFN-α治疗并请皮肤病专科医师协助诊治。一般皮疹可在停用IFN-α后4~7周逐渐消失。
5 内分泌与代谢性疾病
5.1 甲状腺功能异常
5.1.1 概述与机制:
IFN-α治疗可通过自身免疫和非自身免疫机制导致甲状腺功能异常。在自身免疫机制中,IFN-α可增加细胞表面主要组织相容性复合物-1(MHC-I)表达并诱发自身抗体形成,患者常伴甲状腺过氧化物酶抗体(TPoAb)和甲状腺球蛋白抗体(TGAb)阳性;非自身免疫机制可能与IFN-α对甲状腺直接作用相关,表现为破坏性甲状腺炎和非自身免疫性甲状腺功能减退,TPoAb和TGAb均为阴性。
甲状腺功能异常以甲状腺功能低下最为常见。接受IFN-α治疗的CHC患者中约40%产生甲状腺抗体,15%发展为临床型甲状腺疾病。TPoAb或TGAb阳性患者在IFN-α治疗中有60%发生甲状腺疾病,而甲状腺抗体阴性患者中发生率则低于15%,治疗前TPoAb或TGAb阳性者更易发生持续性甲状腺疾病。
5.1.2 临床表现:
根据患者甲状腺功能指标(TT3、TT4、FT3、FT4和TSH)异常,且出现相应甲状腺功能亢进或低下的临床表现可诊断为相应的甲状腺功能异常。患者可出现以下甲状腺疾病:①Graves病:全身高代谢表现,弥漫性、对称性、无痛性甲状腺肿,单纯性或浸润性突眼;②桥本甲状腺炎:甲状腺自身抗体和甲状腺功能减退,伴或不伴甲状腺肿大;③部分患者可出现TPoAb或TGAb阳性和甲状腺功能指标异常,但并未出现临床症状;④非自身免疫型甲状腺疾病,表现为破坏性甲状腺炎和甲状腺功能减退。尤需注意破坏性甲状腺炎患者可由甲状腺功能亢进转为甲状腺功能低下。
5.1.3 临床处理:
①对所有IFN-α治疗者,尤其是CHC患者,在IFN-α治疗前均需进行甲状腺功能、TPoAb和TGAb检测,并结合甲状腺B超进行甲状腺疾病的诊断;②在IFN-α治疗前有甲状腺功能异常者应在内分泌专科医师指导下,在IFN-α治疗前进行相应治疗,在甲状腺功能异常得到有效控制后再开始IFN-α治疗;③IFN-α治疗期间应密切监测甲状腺功能,同时监测TPoAb和TGAb,若发现TPoAb和(或)TGAb阳性者,建议继续监测甲状腺功能及临床症状;④甲状腺功能亢进者可在专科医师指导下口服甲巯咪唑或丙硫氧嘧啶进行治疗,甲状腺功能低下者可口服甲状腺素进行替代治疗;⑤可控制的甲状腺功能异常者可继续IFN-α治疗,不能控制的甲状腺功能亢进者如伴甲状腺毒症的Graves病患者,尤其发生甲状腺危象时需立即终止IFN-α治疗;⑥甲状腺功能减退患者一般口服左甲状腺素钠片并调整剂量后,大多甲状腺功能可正常,很少因此终止IFN-α治疗;⑦仅TSH异常而不伴FT3、FT4、TT3、TT4异常的亚临床甲状腺功能减退或亢进者,可暂不处理并继续观察(B1);⑧停止IFN-α治疗后,如TPOAb、TGAb持续阳性则预示可能发展为甲状腺功能不全(B1)。
5.2 糖尿病
5.2.1 概述与机制:
IFN-α可诱导对胰岛β细胞的自身免疫性损伤而诱发糖尿病。约50%IFN-α诱发的糖尿病患者在治疗前可检测到胰腺自身抗体。PegIFN-α治疗可诱使0.1%~0.7%CHC患者发生糖尿病。需注意,因肝脏为重要的糖代谢器官,部分患者尤其是CHC患者在IFN-α治疗前即已存在糖尿病,IFN-α治疗可使糖尿病加重,亦可因抗病毒治疗过程中肝功能得到改善而有助于糖尿病的控制。
5.2.2 临床表现:
IFN-α治疗过程中糖尿病的诊断参照普通人群诊断标准,但患者往往缺乏糖尿病典型症状,必要时可请内分泌专业医师协助诊断。
5.2.3 处理:
①IFN-α治疗前应对患者进行空腹和餐后血糖检测;②IFN-α治疗期间定期监测,对有糖尿病家族史及肥胖者,即使空腹血糖正常,也应于IFN-α治疗中每2个月复查空腹血糖和糖化血红蛋白水平;③IFN-α治疗前即发生糖尿病的患者,应在IFN-α治疗前治疗糖尿病,待有效控制后再开始IFN-α治疗;④已诊断为糖尿病者应在饮食控制和适量运动基础上,血糖轻度升高者可选择对肝脏损害较轻的口服降糖药物,口服药物不能有效控制者应使用胰岛素,而血糖严重升高者则首选胰岛素注射治疗;⑤药物治疗不能控制的血糖升高或出现急性并发症如糖尿病酮症酸中毒或高渗性非酮症糖尿病昏迷者须停用IFN-α(B1)。
6 其他少见不良反应
6.1 间质性肺病
6.1.1 概述与机制:
IFN-α诱发间质性肺病的发病机制尚不明确,可能与自身免疫和变态反应相关。IFN-α治疗相关的肺部并发症较少见,但为严重不良反应之一,应引起高度重视。
6.1.2 临床表现:
IFN-α治疗中常出现干咳和气促等呼吸系统症状,发生率分别为24%和26%。少数患者结合相应影像学和肺功能检查可诊断为间质性肺炎、结节病等弥漫性肺病。IFN-α治疗CHC而诱发间质性肺炎常见于IFN-α治疗初始12周内,多见于老年患者。
6.1.3 临床处理:
①IFN-α治疗前行双肺影像学检查,以排除潜在或已存在的肺部病变;②IFN-α治疗中出现持续性咳嗽、发热和呼吸困难者,应进一步行胸部X线或CT检查;③患者出现持续并进行性加重的咳嗽、咳痰,甚至呼吸困难,应经影像学检查,一旦诊断为间质性肺炎则必须停止IFN-α治疗,并请呼吸科专业医师协助诊治;④对干咳明显而无胸肺影像学改变者,可使用抗组胺药物治疗,对不能控制症状者可在无激素使用禁忌证情况下使用低剂量激素。
6.2 视网膜病变
6.2.1 概述与机制:
IFN-α所致视网膜病变较为少见。大多视网膜病变并不代表视力丧失。IFN-α所致视网膜出血可能与IFN-α所致血管痉挛、免疫复合物在视网膜脉管系统沉积等有关,常继发于视网膜缺血、糖尿病、高血压等全身疾病。
6.2.2 临床表现:
可表现为视网膜出血、棉绒斑、色觉丧失,偶见失明。更少见的为视网膜动脉或静脉阻塞。典型的视网膜病变包括后极视乳头周围大量棉绒斑和火焰状出血,浅层呈线状或盘状出血,对视力无显著影响,呈现症状与体征分离状态,但若病变波及黄斑及视神经,则可导致视力明显下降。患者可为单侧或双侧视网膜病变。IFN-α也可对视神经有直接毒性,导致类似视神经炎的视力模糊。尚无证据表明IFN-α可导致青光眼。IFN-α所致眼部并发症常发生于视网膜后极部,多于IFN-α治疗1~3个月时发生。
6.2.3 临床处理:
对患有糖尿病和高血压的患者,应于IFN-α治疗前行眼底检查,眼底病变严重者需慎用IFN-α。建议患者视物不适尤其视力下降时,应警惕视觉障碍并及时进行眼科检查和治疗,必要时停用IFN-α。棉绒斑和视网膜出血常可在IFN-α治疗中或治疗后自发缓解(B1)。
6.3 体重减轻
6.3.1 概率与机制:
IFN-α治疗过程中,19.7%患者可出现体重下降(可下降5% ~10%)。可能与食欲下降、恶心、腹泻、甲状腺功能异常、糖尿病等多种不良反应相关。
6.3.2 临床表现:
体重下降较快者在IFN-α治疗第1周常出现食欲下降。多数患者在治疗第24周后出现体重逐渐下降。
6.3.3 临床处理:
患者可少食多餐,饮食宜少而精,应保证必需的蛋白质、脂肪、碳水化合物以及维生素摄入。规律作息,养成良好的作息习惯。患者体重下降一般并不影响正常的学习、生活、工作,因而可继续IFN-α治疗(B1)。对体重下降过于明显且短期内显著下降者,应排除甲状腺功能亢进、恶性肿瘤和其他特殊疾病。
6.4 腹泻
少数患者在IFN-α治疗过程中出现腹泻,具体机制尚未明确,推测可能与肠道功能紊乱有关。如患者在IFN-α治疗期间发生腹泻,首先应进行粪便常规、潜血、甚至细菌学检查,伴体重明显下降者须进行肠镜检查以排除结肠器质性病变、炎症性肠病和感染性腹泻后,继续IFN-α治疗。IFN-α治疗期间宜进食易消化食物,口服微生态制剂,腹泻明显者可应用止泻药物。
6.5 脱发
IFN-α可使约30%患者出现可逆性脱发,多数表现为头发稀疏,不可逆性光秃和自身免疫性斑秃虽可发生,但较为少见。脱发主要发生在应用IFN-α3个月后,且与药物剂量相关。脱发为一过性且在脱发过程中即可伴毛发再生。目前尚无有效预防脱发的措施。可减少洗头频率及对头发的摩擦,避免使用化学性洗发液和烫发。脱发不影响IFN-α治疗,脱发明显而影响美观者可配戴假发。停用IFN-α后3~6个月可恢复生发(B1)。
6.6 其他
其他少见IFN-α不良反应如听力丧失和耳鸣,在普通IFN-α和PegIFN-α联合利巴韦林治疗中也可见到,具体机制尚未明确,可能与IFN-α直接耳毒性、自身免疫性或血液系统改变相关。若中断IFN-α治疗,听力丧失并不能完全恢复;继续IFN-α治疗则可使症状恶化(B1)。IFN-α应用期间也可发生口腔溃疡,可能与自身免疫反应相关,如患者无法耐受,CHB患者建议停用IFN-α,CHC患者如无激素使用禁忌证,则在知情同意后可口服泼尼松5mg,每日1次。如出现急性胰腺炎,考虑与自身免疫反应有关,建议停用IFN-α(B1)。
临床常见的仅自身抗体阳性而无自身免疫性疾病临床表现的患者,尤其是CHC患者并非IFN治疗禁忌证,需在IFN-α治疗过程中严密监测是否发生自身免疫性疾病,一旦出现不可控制的自身免疫性疾病应立即停用IFN-α。
附:中英文缩略词表

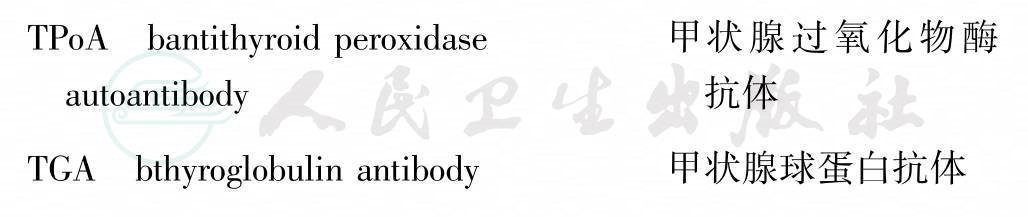
[1]Gupta S,Jen J,Kolz K,et al.Dose selection and population pharmacokinetics of Peg-intron in patients with chronic myelogenous leukaemia[J].Br JClin Pharmacol,2007,63(3):292-299.
[2]Sulkowski MS,Cooper C,Hunyady B,et al.Management of adverse effects of Peg-IFN and ribavirin therapy for hepatitis C [J].Nat Rev Gastroenterol Hepatol,2011,8(4):212-223.
[3]McHutchison JG,Lawitz EJ,Shiffman ML,et al.Peginterferon alfa-2b or alfa-2awith ribavirin for treatmentof hepatitis C infection[J].N Engl JMed,2009,361(6):580-593.
[4]Roomer R,Hansen BE,Janssen HL,et al.Thrombocytopenia and the risk of bleeding during treatmentwith peginterferon alfa and ribavirin for chronic hepatitis C[J].JHepatol,2010,53 (3):455-459.
[5]Lau GK,Piratvisuth T,Luo KX,et al.Peginterferon Alfa-2a,Lamivudine,and the Combination for HBeAg-Positive Chronic Hepatitis B.N Engl JMed.,2005,352(26):2682-2695.
[6]Guyatt G H,Oxman AD,Vist GE,et al.Rating quality of evidence and strength of recommendations:GRADE:an emerging consensus on rating quality of evidence and strength of recommendations[J].BMJ,2008,336(7650):924.
[7]Kirkwood JM,Bender C,Agarwala S,et al.Mechanisms and management of toxicities associated with high-dose interferon alfa-2b therapy[J].JClin Oncol,2002,20(17):3703-3718.
[8]Hauschild A,Gogas H,Tarhini A,et al.Practical guidelines for themanagement of interferon-alpha-2b side effects in patients receiving adjuvant treatment formelanoma:expert opinion[J]. Cancer,2008,112(5):982-994.
[9]Nissen C,Speck B,EmödiG,et al.Toxicity of human leucocyte interferon preparations in human bone-marrow cultures[J]. Lancet,1977,1(8004):203-204.
[10]Ganser A,Carlo-Stella C,Greher J,et al.Effect of recombinant interferons alpha and gamma on human bone marrow-derived megakaryocytic progenitor cells[J].Blood,1987,70(4):1173-1179.
[11]Liu YL,Du XF,Chen XY,et al.Bone marrow suppression or active proliferation?An analysis of neutropenia after pegylated interferon treatment of patients with chronic hepatitis C[J]. Scand J Infect Dis,2013,45(12):939-943.
[12]Wada M,Marusawa H,Yamada R,etal.Association of genetic polymorphisms with interferon-induced haematologic adverse effects in chronic hepatitis C patients[J].J Viral Hepat,2009,16(6):388-396.
[13]Rotman Y,Katz L,Cohen M,etal.Low weightpredicts neutropenia and peginterferon alfa-2a dose reductions during treatment for chronic hepatitis C[J].JViral Hepat,2009,16(5):340-345.
[14]Fried MW.Side effects of therapy for hepatitis C and theirmanagement[J].Hepatology,2002,36(5 Suppl 1):S237-244.
[15]Manns MP,McHutchison JG,Gordon SC,et al.Peginterferon alfa-2b plus ribavirin compared with interferon alfa-2b plus ribavirin for initial treatment of chronic hepatitis C:a randomisedtrial[J].Lancet,2001,358(9286):958-965.
[16]Glue P,Rouzier-Panis R,Raffanel C,et al.A dose-ranging study of pegylated interferon alfa-2b and ribavirin in chronic hepatitis C.The Hepatitis C Intervention Therapy Group[J]. Hepatology,2000,32(3):647-653.
[17]Soza A,Everhart JE,Ghany MG,et al.Neutropenia during combination therapy of interferon alfa and ribavirin for chronic hepatitis C[J].Hepatology,2002,36(5):1273-1279.
[18]Fried MW,Shiffman ML,Reddy KR,et al.Peginterferon alfa-2a plus ribavirin for chronic hepatitis C virus infection[J].N Engl JMed,2002,347(13):975-982.
[19]Cooper CL,Al-Bedwawi S,Lee C,et al.Rate of infectious complications during interferon-based therapy for hepatitis C is not related to neutropenia[J].Clin Infect Dis,2006,42(12):1674-1678.
[20]Juarez-Navarro A,Vera-de-Leon L,Navarro JM,et al.Incidence and severity of infections according to the development of neutropenia during combined therapy with pegylated interferon-alpha2a plus ribavirin in chronic hepatitis C infection [J].Methods Find Exp Clin Pharmacol,2005,27(5):317-322.
[21]Curry MP,Afdhal NH.Use of growth factors with antiviral therapy for chronic hepatitis C[J].Clin Liver Dis,2005,9 (3):439-451.
[22]PuotiM,Babudieri S,Rezza G,etal.Use of pegylated interferons is associated with an increased incidence of infections during combination treatment of chronic hepatitis C:a side effect of pegylation[J]?Antivir Ther,2004,9(4):627-630.
[23]Koirala J,Gandotra SD,Rao S,et al.Granulocyte colony-stimulating factor dosing in pegylated interferon alpha-induced neutropenia and its impact on outcome of anti-HCV therapy [J].JViral Hepat,2007,14(11):782-787.
[24]Gonzalez SA,Jacobson IM.The role of hematopoietic growth factors in special populationswith chronic hepatitis C:patients with HIV coinfection,end-stage renal disease,or liver transplantation[J].Cleve Clin J Med,2004,71(Suppl 3):S22-S26.
[25]Golia P,Talal AH,Jacobson IM,et al.A preliminary study of growth factors versus dose reduction for peginterferon alfa-2b and ribavirin associated neutropenia and anemia in HIV/HCV co-infected patients[J].Gastroenterology,2003,124(suppl 1):A766.
[26]Gmur J,Burger J,Schanz U,et al.Safety of stringent prophylactic platelet transfusion policy for patientswith acute leukaemia[J].Lancet,1991,338(8777):1223-1226.
[27]Zdilar D,Franco-Bronson K,Buchler N,et al.Hepatitis C,interferon alfa,and depression[J].Hepatology,2000,31(6):1207-1211.
[28]Fontana RJ.Neuropsychiatric toxicity of antiviral treatment in chronic hepatitis C[J].Dig Dis,2000,18(3):107-116.
[29]Bonaccorso S,Marino V,Puzella A,et al.Increased depressive ratings in patients with hepatitis C receiving interferon-alphabased immunotherapy are related to interferon-alpha-induced changes in the serotonergic system[J].JClin Psychopharmacol,2002,22(1):86-90.
[30]Loftis JM,Huckans M,Ruimy S,etal.Depressive symptoms in patientswith chronic hepatitis C are correlated with elevated plasma levels of interleukin-1beta and tumor necrosis factoralpha[J].Neurosci Lett,2008,430(3):264-268.
[31]Raison CL,Demetrashvili M,Capuron L,et al.Neuropsychiatric adverse effects of interferon-α:recognition andmanagement [J].CNSDrugs,2005,19(2):105-123.
[32]Conrad B.Potential mechanisms of interferon-alpha induced autoimmunity[J].Autoimmunity,2003,36(8):519-523.
[33]Mandac JC,Chaudhry S,Sherman KE,et al.The clinical and physiological spectrum of interferon-alpha induced thyroiditis:toward a new classification[J].Hepatology,2006,43(4):661-672.
[34]Watanabe U,Hashimoto E,Hisamitsu T,et al.The risk factor for development of thyroid disease during interferon-alpha therapy for chronic hepatitis C[J].Am JGastroenterol,1994,89(3):399-403.
[35]MazziottiG,Sorvillo F,Stornaiuolo G,et al.Temporal relationship between the appearance of thyroid autoantibodies and development of destructive thyroiditis in patients undergoing treatmentwith two different type-1 interferons for HCV-related chronic hepatitis:a prospective study[J].JEndocrinol Invest,2002,25(7):624-630.
[36]Oppenheim Y,Ban Y,Tomer Y.Interferon induced autoimmune thyroid Disease(AITD):a model for human autoimmunity[J].Autoimmun Rev,2004,3(5):388-393.
[37]Wong V,Fu AX,George J,et al.Thyrotoxicosis induced by alpha-interferon therapy in chronic viral hepatitis[J].Clin Endocrinol(Oxf),2002,56(6):793-798.
[38]Carella C,MazziottiG,Morisco F,et al.Long-term outcome of interferon-alpha-induced thyroid autoimmunity and prognostic influence of thyroid autoantibody pattern at the end of treatment[J].JClin Endocrinol Metab,2001,86(5):1925-1929.
[39]陈灏珠.实用内科学[M].11版.北京:人民卫生出版社,2001:1143-1159.
[40]Fabris P,Floreani A,Tositti G,et al.Type 1 diabetesmellitus in patients with chronic hepatitis C before and after interferon therapy[J].Aliment Pharmacol Ther,2003,18(6):549-558.
[41]Schreuder TC,Gelderblom HC,Weegink CJ,et al.High incidence of type 1 diabetes mellitus during or shortlyafter treatmentwith pegylated interferon alpha for chronic hepatitis C virus infection[J].Liver Int,2008,28(1):39-46.
[42]Karim A,Ahmed S,Khan A,etal.Interstitial pneumonitis in a patient treated with alpha-interferon and ribavirin for hepatitis C infection[J].Am JMed Sci,2001,322(4):233-235.
[43]Sene D,Touitou V,Bodaghi B,et al.Intraocular complications of IFN-alpha and ribavirin therapy in patients with chronic viral hepatitis C[J].World J Gastroenterol,2007,13(22):3137-3140.
[44]Wirth S,Pieper-Boustani H,Lang T,et al.Peginterferon alfa-2b plus ribavirin treatment in children and adolescents with chronic hepatitis C[J].Hepatology,2005,41(5):1013-1018.
[45]Tosti A,Mistiali C,Bardazzi F,et al.Telogen effluvium due to recombinant interferon alfa-2b[J].Dermatology,1992,184 (2):124-125.