 去看看
去看看


结核病是实体器官移植(solid organ transplantation,SOT)术后一种较为少见但后果严重的感染性疾病,SOT受者结核病患病率明显高于正常人群。由于免疫抑制剂的长期使用,抗结核药物肝肾毒性及其与免疫抑制剂相互的代谢干扰,使得SOT受者临床抗结核治疗复杂性明显增加,致死率明显高于非移植结核病患者。随着器官移植受者以及结核病患病人数的增加,需要建立规范的诊疗程序和治疗指导原则,以便合理制定化学治疗和免疫抑制方案,提高SOT术后结核病的诊疗水平,利于受者和移植器官的长期存活。为此,中华医学会器官移植学分会和中国医师协会器官移植医师分会组织器官移植专家和结核病专家,共同制定《中国器官移植术后结核病临床诊疗指南(2016版)》(以下简称“指南”)。本指南按照“推荐分级的评估、制定与评价(GRADE)”系统[1]对证据质量等级和推荐强度进行分级。
1 流行病学特点
免疫抑制剂的长期使用,使SOT受者结核病患病率高于正常人群20~74倍[2-3],且病死率高达31%[4-6]。移植术后结核病发病具有一定地域性,高发地区移植受者结核发病率为15.2%,而非高发地区仅为0.5%~6.4%[2,6]。SOT术后结核病发病率与移植器官种类密切相关,肺移植后结核病发病风险是其他器官移植的5.6倍[7],肾移植后结核病发病率为0.56%~2.61%[8],肝移植为0.47%~2.30%[9]。此外,SOT术后发生结核病的高危因素包括:使用淋巴细胞清除抗体、强化的免疫抑制治疗、慢性肾功能不全、贫血、糖尿病、丙型肝炎、慢性肝病、高龄受者等[10-13]。约2/3结核病发生在移植后1年内,中位时间为6~11个月[2,10,14]。既往结核菌素皮肤试验(tuberculin skin tests,TST)阳性或影像资料明确有陈旧性肺结核表现的患者移植后结核病发生时间较早。SOT术后结核病患者中,继发性肺结核占51%,肺外结核占16%,血行播散型肺结核占33%[2,11]。移植后结核病致死率达19%~40%,是普通结核病患者总体致死率的10倍。而且,由于抗结核药物和免疫抑制剂复杂的药物相互作用,使移植物丢失率高达33.3%[2,11,15-16]。
2 结核病的诊断
SOT术后结核病的临床诊断依赖于临床症状和实验室检测。但由于免疫抑制剂的使用,结核分枝杆菌相关的细胞免疫应答反应减弱,甚至缺如,从而导致临床症状不典型和实验室检查敏感性降低。临床典型症状为发热、盗汗和体力下降,对于未明确病原体的发热,要高度怀疑结核病的可能。SOT术后结核病的临床表现中,发热较为常见,但并不具有特异性。SOT受者中,64%局灶性结核病患者以发热为首发表现,91%播散型结核病患者具有发热症状[2,11]。发生播散型结核病的SOT受者多见于供者来源的感染,且伴有典型的临床症状[17]。
在临床诊断中病原学检测是最为直接的证据,但仍推荐采用细胞免疫学检测对SOT供、受者进行结核病筛查。需注意,由于免疫抑制剂的应用,细胞免疫应答反应的降低、甚至缺失,可使实验室检测敏感性明显降低,导致结核病诊断延迟。TST可衡量结核分枝杆菌感染时细胞介导的免疫应答反应,但对接种过卡介苗的患者特异性较差;γ干扰素释放试验(interferon gamma release assay,IGRA)是基于血标本的体外试验,其原理是快速诱导T淋巴细胞产生针对抗原的IFN-γ,对于发现潜在结核病的特异性优于结核菌素纯蛋白衍生物试验[18]。TST和IGRA联合检测阳性率高,行IGRA和TST筛查后,患者进展为SOT术后结核病的风险仍需要更多的纵向研究来评价。
推荐意见:
1.痰液、支气管冲洗液或支气管肺泡灌洗液、经支气管肺活检、尿液、肺结核和肺外结核病变处组织活检标本等抗酸杆菌检测是诊断实体器官移植(SOT)术后结核病较为直接的证据,标本应送抗酸杆菌涂片、培养以及组织病理检测,但阳性率和培养分离率相对较低,且受标本质量的影响(2-C)。
2.结核菌素皮肤试验(TST)和γ干扰素释放试验(IGRA)联合检测阳性率高,诊断价值大(1-B)。
3.TST检测可以应用于移植前后各个阶段,48~72h硬结直径>5mm考虑阳性结果。(1-C)。
影像学检查具有重要的参考和补充价值。肺结核X线常见表现:多发生在肺上叶尖后段、肺下叶背段;呈多形性表现(即同时呈现渗出、增殖、纤维和干酪性病变);易合并空洞;可伴有胸腔积液、胸膜增厚与粘连;病灶吸收慢。CT扫描具有重要的补充性诊断价值:发现胸内隐匿部位病变包括气管、支气管内病变;早期发现肺内粟粒阴影;诊断有困难的肿块、空洞、孤立结节和浸润阴影的鉴别;了解肺门、纵隔淋巴结肿大情况,鉴别纵隔淋巴结结核和肿瘤;少量胸腔积液、包裹性积液、叶间积液和其他胸膜病变的检出;囊性与实体肿块的鉴别。
推荐意见:
4.影像学检查是SOT术后结核病的重要诊断手段,特别是肺结核的诊断(1-C)。
5.与非移植结核病患者相比,肺外结核较多见。各器官结核表现不同,特色鲜明,需针对具体临床病例进行分析(2-C)。
3 结核病的预防和治疗
理论上移植相关结核病有4种来源[2,11]:①结核分枝杆菌潜伏感染(latent tuberculosis infection,LTBI)受者;②供者有结核病;③移植后结核分枝杆菌的初次暴露;④急需移植的受者具有活动性结核病。对LTBI供、受者的及时发现、治疗以及预防移植后结核暴露的意识,是预防SOT术后结核病和降低发病率、病死率的重要措施。
推荐意见
6.活动性结核是器官移植和捐献的禁忌证(1-A)。
7.受者有肺结核病史并接受过足量、正规治疗,可以行器官移植(1-B)。足量正规治疗指2HRZE/4HR的标准治疗方案:即4联强化用药(异烟肼、利福平、吡嗪酰胺和乙胺丁醇)2个月,然后持续用药(异烟肼和利福平)4个月。
8.所有等待移植的受者均应详细询问结核相关病史,包括TST或IGRA结果、疫区或家人结核病接触史、卡介苗接种史(1-C);在移植前对受者进行常规TST或IGRA筛查(1-C)。
对于LTBI供、受者进行预防性抗结核治疗,是防止其发展为活动性结核病的有效措施。对等待移植者,LTBI预防治疗前,应详细询问病史、行体格检查及辅助检查排除急性结核分枝杆菌感染可能。预防性治疗药物不良反应主要是肝功能损害,因此治疗过程中应做好监测工作:(1)依据详细体格检查做出及时的评估(评估内容包括AST、ALT及胆红素);(2)停药指征:出现消化道症状且AST和ALT水平超过正常上限3次以上,或虽无临床症状,但AST和ALT水平超过正常上限5次。
推荐意见:
9.对结核分枝杆菌潜伏感染(LTBI)活体供、受者进行预防性抗结核治疗时,均应仔细评估,以排除活动性结核(未分级)。
10.LTBI受者预防性治疗方案建议与当地普通人群相同(未分级)。
11.预防性抗结核治疗不一定非要在移植前完成,因移植而中断的治疗应在移植术后受者病情稳定后尽快重启;且中断治疗后,需对患者进行重新评估,以判断是否已转变为活动性结核及确定LTBI治疗需要的延长时间(1-C)。
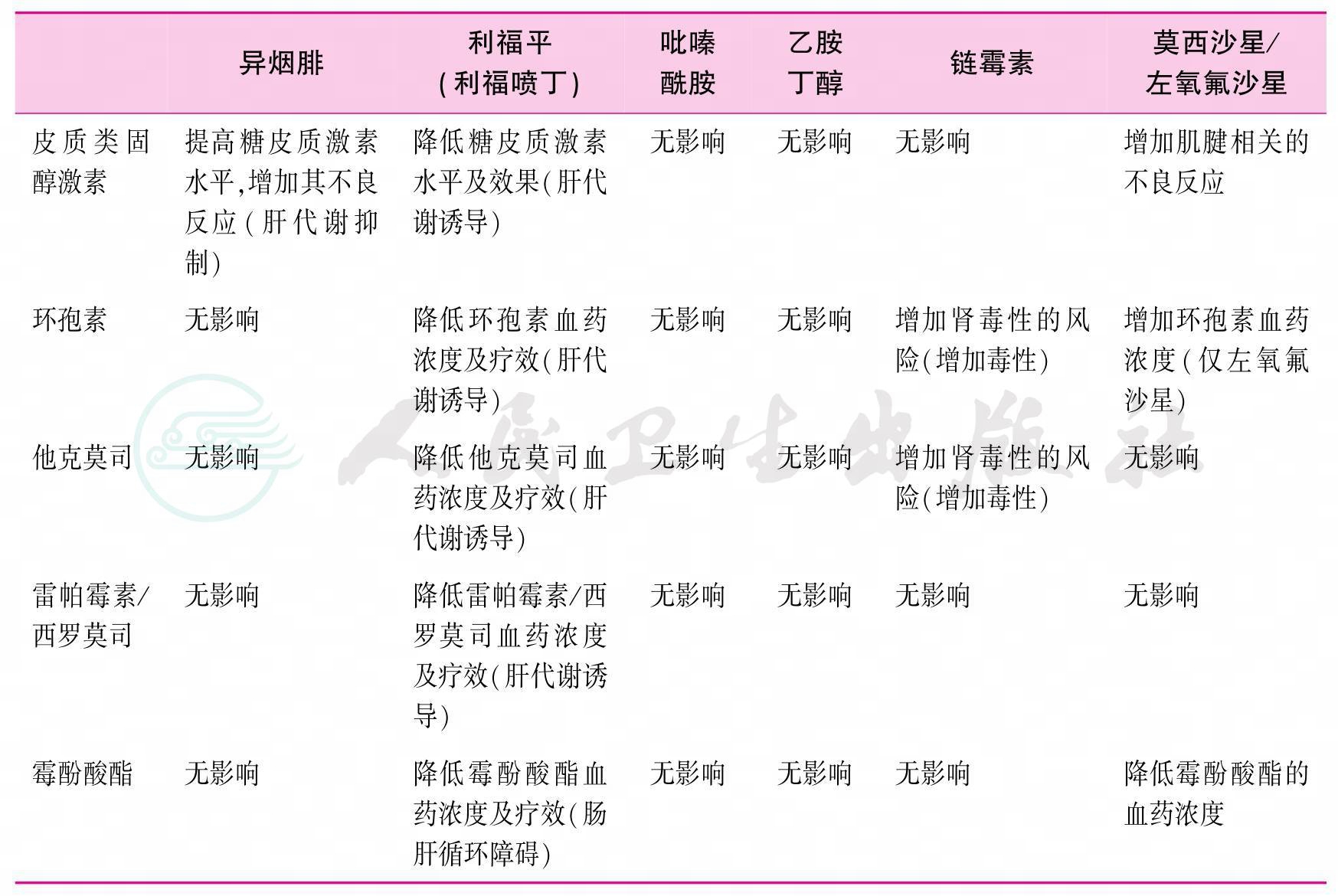
由于抗结核药物与抗排斥反应药物间相互作用以及抗结核药物自身的不良反应都会增加SOT术后结核病治疗的复杂性,临床上需要全面、综合的考虑,降低移植物丢失,避免移植受者死于结核病。由于移植后活动性结核病的治疗比较困难,应尽可能在移植前诊断和治疗活动性结核病。抗结核药物与免疫抑制剂间代谢干扰如表1所示。
表1 部分抗结核药物对抗排斥反应药物的影响作用
推荐意见:
12.建议对移植受者使用与当地普通人群相同的结核病治疗方案(2-D);短程化疗推荐2HRZE/4HR(1-A)。
13.利福霉素类抗结核药物与免疫抑制剂之间代谢干扰明显增加抗结核治疗的复杂性,且明显增加了抗结核药物自身不良反应的发生频率(1-C)。
14.对于不严重的病例,可选用不联合利福霉素类的抗结核方案,从而降低移植排斥反应发生的风险(1-C);可使用利福喷丁代替利福平,以减少利福平与钙调磷酸酶抑制剂(CNI)和哺乳动物雷帕霉素靶蛋白抑制剂(mTORi)的相互作用(1-A)。
15.对于接受利福平治疗的受者,推荐监测CNI和mTORi血药浓度(1-C)。
16.骨、关节结核治疗疗程推荐6~9个月(1-A);中枢神经系统结核治疗疗程推荐9~12个月(2-B);严重播散的结核治疗疗程推荐6~9个月(1-B);治疗周期的长短取决于对抗结核治疗的反应性和继续治疗阶段中的用药方案(2-C);继续治疗除标准方案外,多数推荐针对尚有免疫活性患者的个体化或经验性用药治疗(未分级)。
移植术后发生结核病提示患者免疫功能低下,在临床观察没有排斥反应和抗结核药物自身不良反应的前提下,抗结核药物应尽可能足量、足疗程,保证抗结核治疗的有效性;不要单纯考虑抗结核药物会导致CNI类药物浓度下降这一现象,而将抗结核药物减量;同时不需要刻意提高CNI类药物浓度,只要规律监测移植器官功能、T淋巴细胞亚群及尿常规等变化,及时发现和调整即可。
关于儿童受者结核病的研究及样本量都较少,但目前已有数据显示其临床特点与成人受者的一致性。在移植后免疫抑制状态下,一些儿童结核病的特异性症状可能会进一步放大。换言之,即增加了诸如播散型肺结核和一些肺外结核以及因结核病直接或间接死亡的风险。
推荐意见:
17.加强对儿童移植候选者及其亲属活动性结核病的筛查,对LTBI儿童患者应考虑使用异烟肼预防治疗,以降低其移植后结核病发病风险(1-C)。
4 总结与展望
SOT术后结核病的诊断和治疗面临许多挑战,本指南的发布对提高SOT术后潜在性和活动性结核病的诊疗水平有着重要意义。希望今后能开发不良反应少且与免疫抑制剂无相互作用的抗结核药物,缩短和简化抗结核治疗,简化SOT术后结核病预防和治疗的复杂性,利于提高SOT受者与移植物的长期存活。
5 利益声明
本指南的发布不存在与任何公司、机构或个人之间的利益冲突。
[1]GRADE working group[DB/OL].http://www.gradeworkinggroup.org/index.htm.
[2]Subramanian A,Dorman S.Mycobacterium tuberculosis in solid organ transplant recipients[J].Am J Transplant,2009,9(Suppl 4):S57-S62.
[3]Singh N,Paterson DL.Mycobacterium tuberculosis infection in solid-organ transplant recipients:impact and implications for management[J].Clin Infect Dis,1998,27(5):1266-1277.
[4]Aguado JM,Herrero JA,Gavaldá J,et al.Clinical presentation and outcome of tuberculosis in kidney,liver,and heart transplant recipients in Spain.Spanish Transplantation Infection Study Group,GESITRA[J].Transplantion,1997,63(9):1278-1286.
[5]Horne DJ,Narita M,Spitters CL,et al.Challenging issues in tuberculosis in solid organ transplantation[J].Clin Infect Dis,2013,57(10):1473-1482.
[6]Currie AC,Knight SR,Morris PJ.Tuberculosis in renal transplant recipients:the evidence for prophylaxis.Challenging issues in tuberculosis in solid organ transplantation[J].Transplantion,2010,90(7):695-704.
[7]Torre-Cisneros J,Doblas A,Aguado JM,et al.Tuberculosis after solid-organ transplant:incidence,risk factors,and clinical characteristics in the RESITRA(Spanish Network of Infection in Transplantation)cohort[J].Clin Infect Dis,2009,48(12):1657-1665.
[8]Reis-Santos B,Gomes T,Horta BL,et al.Tuberculosis prevalence in renal transplant recipients:systematic review and meta-analysis[J].J Bras Nefrol,2013,35(3):206-213.
[9]Yehia BR,Blumberg EA.Mycobacterium tuberculosis infection in liver transplantation[J].Liver Transpl,2010,16(10):1129-1135.
[10]Subramanian AK,Morris MI;AST Infectious Diseases Community of Practice.Mycobacterium tuberculosis infections in solid organ transplantation[J].Am J Transplant.2013,13(Suppl 4):68-76.
[11]Bumbacea D,Arend SM,Eyuboglu F,et al.The risk of tuberculosis in transplant candidates and recipients:a TBNET consensus statement[J].Eur Respir J,2012,40(4):990-1013.
[12]Sun HY.Treating tuberculosis in solid organ transplant recipients[J].Curr Opin Infect Dis,2014,27(6):501-505.
[13]Aguado JM,Torre-Cisneros J,Fortún J,et al.Tuberculosis in solid-organ transplant recipients:consensus statement of the group for the study of infection in transplant recipients(GESITRA)of the Spanish Society of Infectious Diseases and Clinical Microbiology[J].Clin Infect Dis,2009,48(9):1276-1284.
[14]Lopez de Castilla D,Schluger NW.Tuberculosis following solid organ transplantation[J].Transpl Infect Dis,2010,12(2):106-112.
[15]Hall CM,Willcox PA,Swanepoel CR,et al.Mycobacterial infection in renal transplant recipients[J].Chest,1999,106(2):435-439.
[16]Borgdorff MW,Veen J,Kalisvaart NA,et al.Mortality among tuberculosis patients in the Netherlands in the period 1993-1995[J].Eur Respir J,1998,11(4):816-820.
[17]Centers for Disease Control and Prevention(CDC).Transplantation-transmitted tuberculosis-Oklahoma and Texas,2007[J].MMWR Morb Mortal Wkly Rep,2008,57(13):333-336.
[18]中华医学会结核病学分会.肺结核诊断和治疗指南[J].中华结核和呼吸杂志,2001,24(2):70-73.