 去看看
去看看


弥漫性间质性肺病原因众多,其中有一组属于原因不明的疾病,称之为特发性间质性肺炎(IIP)。目前按照病理学分类,IIP共有10个病理类型,其中只有特发性肺纤维化(IPF)有临床诊断标准,其余的诊断均需要依靠病理诊断。国际上第1个《关于IPF的临床诊治专家共识》是2000年美国胸科协会(ATS)和欧洲呼吸病学会(ERS)制定的[1]。我国于2002年及时发布了《特发性肺(间质)纤维化诊断和治疗指南(草案)》(表22-1)[2],该指南对规范和推动我国特发性肺纤维化的诊断和治疗方面起到了巨大的推动作用。
表22-1 2000年IPF临床诊断和治疗指南

虽然2000年的《IPF临床专家共识》在IPF定义、诊断和治疗方面制定比较全面和规范,但是应该说,2000年的《IPF临床专家共识》还是缺乏循证医学证据的。从2000—2010年,10年过去了,有关IPF的临床诊断和治疗方面有了一些新进展,故在2011年由美国胸科学会(ATS)、欧洲呼吸学会(ERS)、日本呼吸学会(JRS)和拉丁美洲胸科学会(ALAT)共同制定了新的IPF诊治指南并正式发表[3]。新的指南包括疾病定义、流行病学特征、危险因素、诊断、自然病程、分期及预后、治疗和疾病进程监测等内容,目的是分析自2000年《ATS/ERS共识》发表以来所积累的相关证据,为IPF疾病管理,尤其是诊断及治疗提供循证医学建议。2011年的诊治指南内容简介如下。
一、IPF的定义
IPF是病因未明的慢性进展性纤维化型间质性肺炎的一种特殊类型,好发于老年人,病变局限于肺部,组织病理学和(或)影像学表现具有寻常型间质性肺炎(UIP)的特征。诊断IPF需要排除其他各种间质性肺炎,包括其他类型的特发性间质性肺炎(IIP)及与环境暴露、药物或系统性疾病相关的间质性肺疾病。
二、UIP的胸部高分辨率CT(HRCT)特征
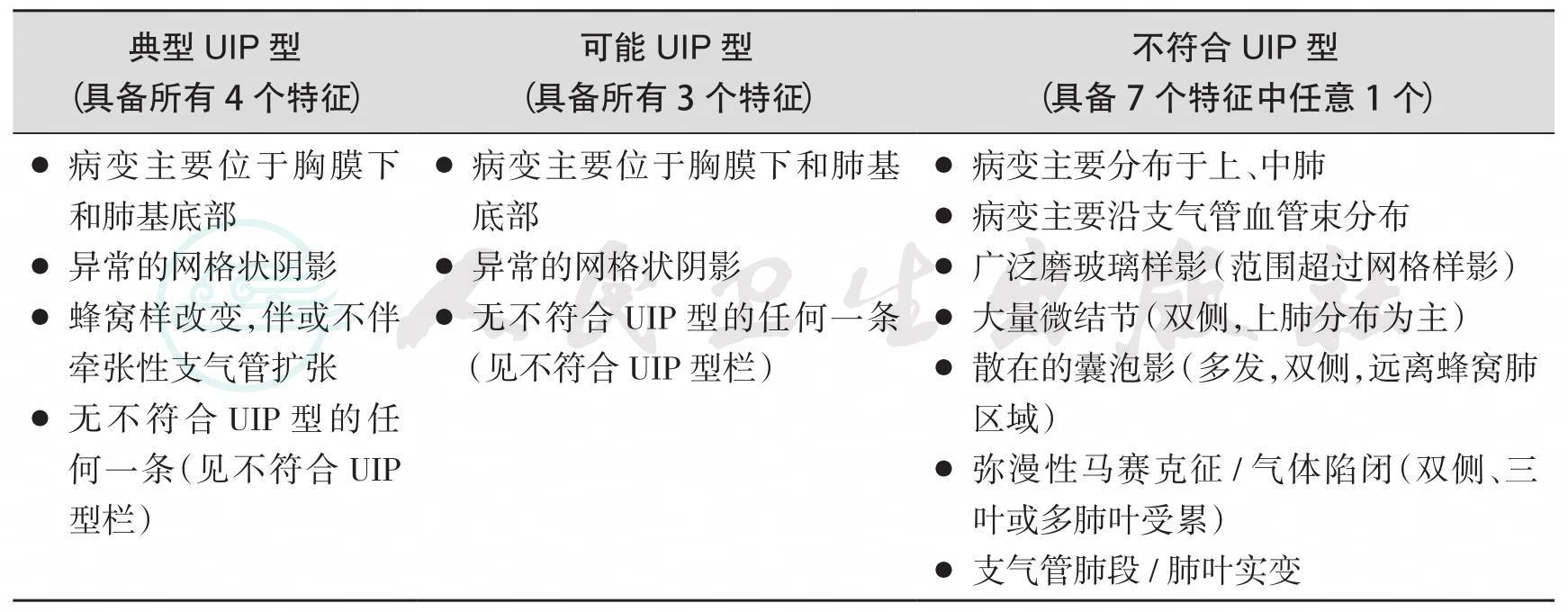
HRCT是IPF诊断过程中的重要组成部分。HRCT上UIP的特征为胸膜下和肺基底部的网格状阴影、蜂窝影,常伴有牵拉性支气管扩张,尤其是蜂窝影对IPF的诊断有很重要的意义(表22-2)。HRCT上的蜂窝影指成簇的囊泡样气腔,蜂窝壁边界清楚。囊泡直径在3~10mm之间,偶尔可大至2.5cm。部分患者可伴纵隔淋巴结轻度增大(短径通常<1.5cm)。如果HRCT上出现大量微结节、气体陷闭、非蜂窝样囊泡、大量磨玻璃样改变、肺实变或者病变以沿支气管血管束分布为主,应该考虑其他诊断(即非UIP)。
HRCT诊断UIP的阳性预测值为90%~100%。如果HRCT上无蜂窝影,但其他影像特征符合UIP标准,定义为可能是UIP,需进行外科肺活检来确诊。HRCT不符合UIP型的患者,外科肺活检的病理表现仍有可能符合UIP型表现。
表22-2 UIP型的HRCT标准
三、UIP的组织病理学特征
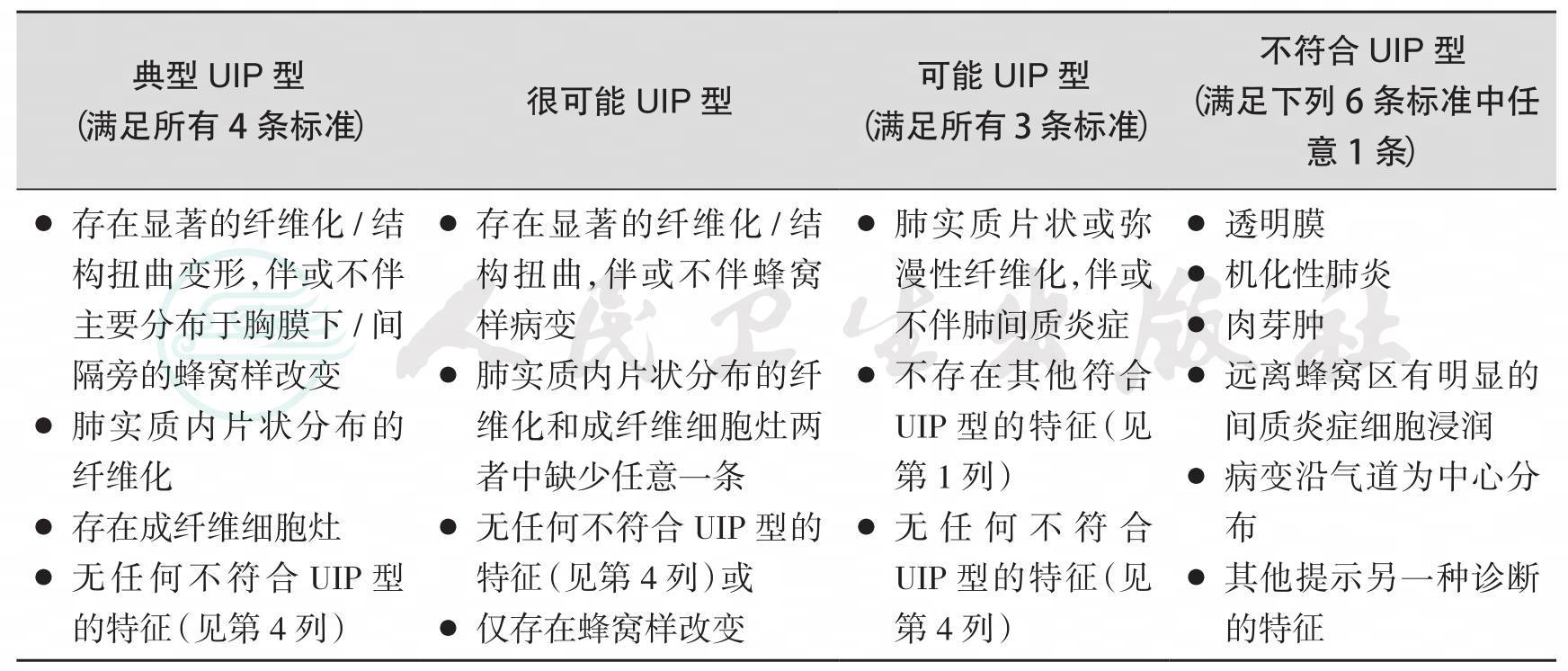
UIP的组织病理学特征和主要诊断标准(表22-3)是在低倍镜下病变的不均一性,即瘢痕形成和蜂窝样改变的纤维化区域与病变轻微或正常的肺实质区域交替出现。病变主要位于胸膜下和间隔旁的肺实质。一般情况下炎症反应轻,表现为淋巴细胞和浆细胞在肺间质中的斑片状浸润,伴Ⅱ型肺泡上皮细胞和细支气管上皮细胞增生。纤维化区域主要由致密胶原组成,伴上皮下散在的成纤维细胞灶。蜂窝样改变区域由囊状纤维化气腔构成,这些气腔内衬细支气管上皮细胞,充满黏液和炎性细胞。纤维化和蜂窝样改变区域的间质内常有平滑肌细胞化生。
表22-3 UIP型的组织病理学标准
四、诊断标准
由于许多研究证实HRCT诊断UIP准确性可达到90%~100%,因此新指南提出具备UIP典型HRCT表现者不必行病理活检,根据UIP的HRCT特点可作为独立的IPF诊断手段,从而废除了2000年《ATS/ERS共识》中提出的主要和次要诊断标准。诊断IPF需要符合以下3条。
1.排除其他已知的ILD病因(例如家庭和职业环境暴露、结缔组织病和药物)。
2.未行外科肺活检的患者,HRCT呈现典型UIP型表现(表22-2)。
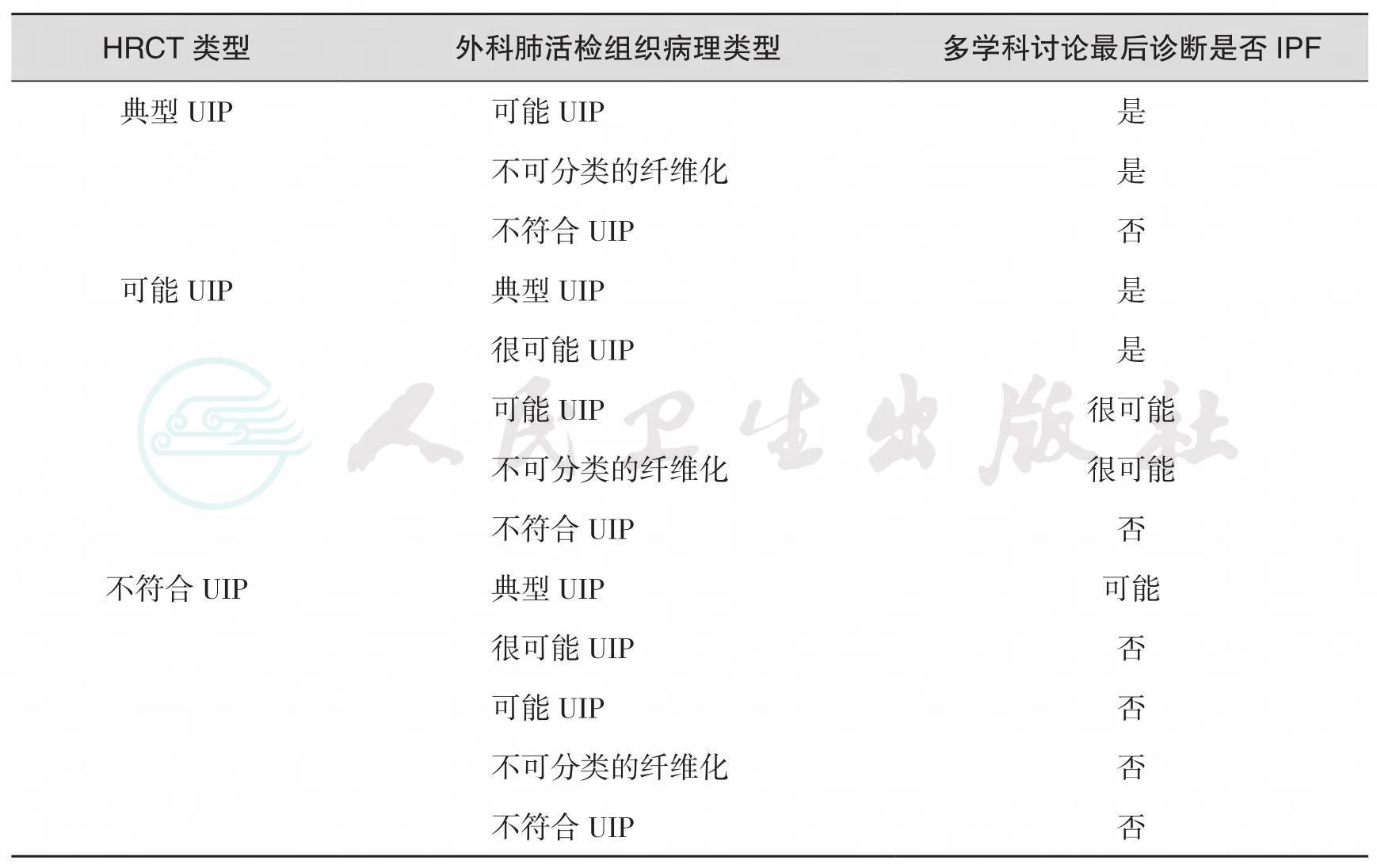
3.接受外科肺活检的患者,HRCT和肺活检组织病理类型符合特定的组合(表22-4)。
表22-4 结合HRCT和组织病理学表现的IPF诊断标准(需要多学科讨论)

续表
五、治疗
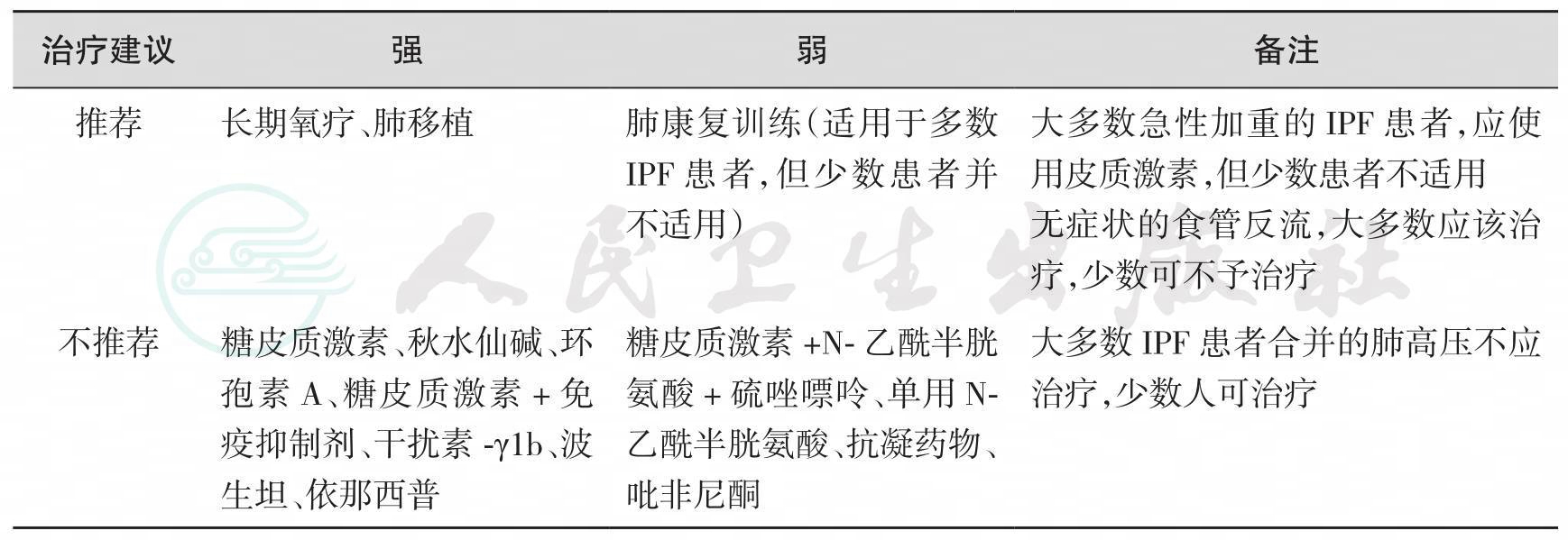
对于IPF,新指南将大多数治疗措施分为不同强度的推荐意见(表22-5)。
表22-5 IPF推荐治疗建议
2011年由ATS/ERS/JRS/ALAT共同制定的IPF指南中[3],将泼尼松+硫唑嘌呤+NAC(三联治疗)、抗凝治疗、NAC和吡非尼酮作为弱不推荐方案供大家选择,其原因就在于这些方案在临床上没有得到确切的验证结果,同时专家组也期待进一步的RCT研究能够对此进行验证。就在2011年全球《关于IPF诊治指南》发表后,又有一些全球多中心随机双盲对照研究陆续公布,其中包括PANTHER-IPF、ACE-IPF、ASCEND和INPULSIS。
PANTHER-IPF研究的目的是探讨三联药物方案(泼尼松、硫唑嘌呤、乙酰半胱氨酸)和单用NAC是否对IPF有治疗作用[4,5],结果显示,三联药物方案的安全性存在问题而被迫终止;而单用NAC与安慰剂相比,FVC改变无显著差异。提示不论是三联药物方案还是单用NAC治疗,IPF患者均无明显获益。ACE-IPF研究的目的是探讨华法林抗凝治疗对IPF死亡率、住院率和FVC下降的影响[6]。结果显示,华法林组患者的死亡人数明显高于安慰剂组(14名与3名,P=0.005),并且IPF获益可能性低。ASCEND研究的目的旨在再次证明吡非尼酮对IPF患者治疗的有效性[7],结果表明,吡非尼酮能够减慢IPF患者的病情进展,主要表现在肺功能、活动耐量、无疾病进展生存期等方面,合并数据分析发现能够减少患者的死亡率,而药物的副作用可被患者接受。INPULSIS研究的目的是探讨尼达尼布(nintedanib,是一种血管内皮生长因子、成纤维细胞生长因子、血小板源性生长因子受体酪氨酸激酶抑制剂)治疗IPF的安全性和有效性[8],结果显示,尼达尼布150mg,2次/日,口服,能够减慢IPF患者FVC的下降,即可以减慢疾病的进展。
鉴于吡非尼酮和尼达尼布已被RCT研究证实可以延缓IPF患者的FVC下降,减慢疾病进展,因此在2014年10月美国国家药品食品管理局已经正式批准这两种药物为IPF的治疗药物。相信不久的将来,由ATS/ERS/JRS/ALAT共同制定的2011年版IPF指南会被更新。
我国的IPF指南现在还停留在2002年版,目前已不适应临床诊治的需要,中华医学会呼吸病分会间质病学组目前正在根据国际最新研究进展和国内自己的临床实际对IPF指南进行更新。
1.American Thoracic Society.Idiopathic pulmonary fibrosis:diagnosis and treatment.International consensus statement.American Thoracic Society and the European Respiratory Society.Am J Respir Crit Care Med,2000,161:646-664.
2.中华医学会呼吸病分会.特发性肺(间质)纤维化诊断和治疗指南(草案).中华结核和呼吸杂志,2002,25:387-389.
3.Rahgu G,Collard HR,Egan JJ,et al.ATS/ERS/JRS/ALAT Committee on Idiopathic Pulmonary Fibrosis.An Official ATS/ERS/JRS/ALAT Statement:Idiopathic Pulmonary Fibrosis:Evidence-based Guidelines for Diagnosis and Management.Am J Respir Crit Care Med,2011,183:788-824.
4.Raghu G,Anstrom KJ,King TE,et al.Prednisone,Azathioprine,and N-Acetylcysteine for Pulmonary Fibrosis.N Engl J Med,2012,366:1968-1977.
5.Martinez FJ,Andrade JA de,Anstrom KJ,et al.Randomized Trial of Acetylcysteine in Idiopathic Pulmonary Fibrosis.N Engl J Med,2014,370:2093-2101.
6.Noth I,Anstrom KJ,Calvert SB,et al.A Placebo-Controlled Randomized Trial of Warfarin in Idiopathic Pulmonary Fibrosis.Am J Respir Crit Care Med,2012,186(1):88-95.
7.King TE,Bradford WZ,Castro-Bernardini S,et al.A Phase 3 Trial of Pirfenidone in Patients with Idiopathic Pulmonary Fibrosis.N Engl J Med,2014,370:2083-2092.
8.Richeldi L,du Bois RM,Raghu G,et al.Efficacy and Safety of Nintedanib in Idiopathic Pulmonary Fibrosis.N Engl J Med,2014,370:2071-2082.