 去看看
去看看


1 治疗前评估
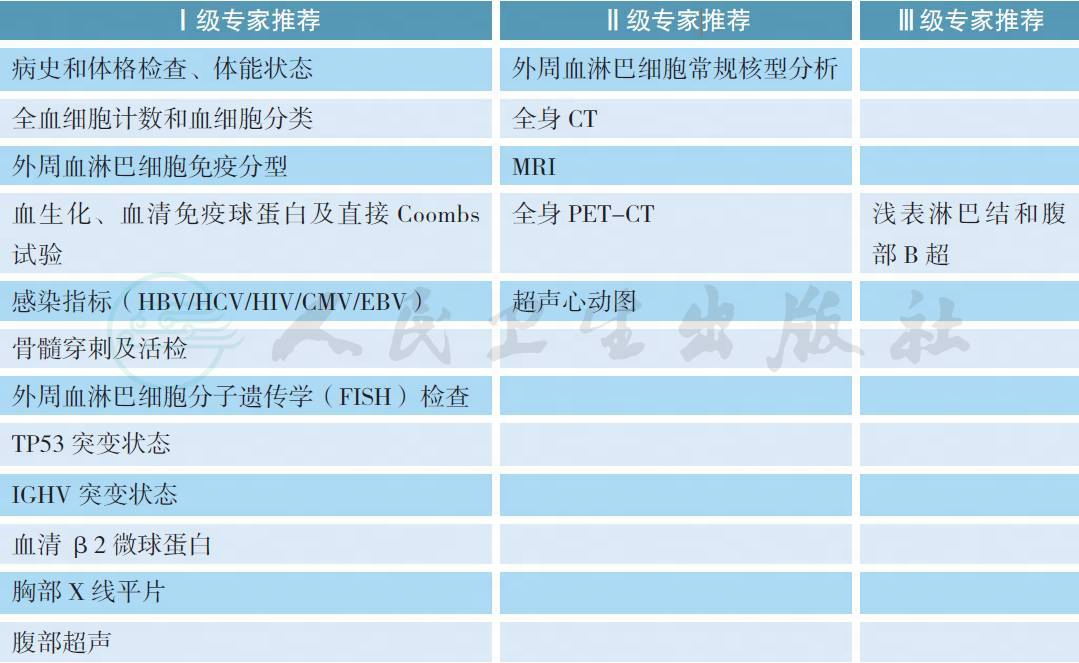
2 病理诊断

【注释】
达到以下3 项标准可以诊断CLL:①外周血B 淋巴细胞(CD19+ 细胞) 计数≥ 5×109/L,且持续至少3 个月。②外周血涂片中特征性的表现为小的、形态成熟的淋巴细胞显著增多,其细胞质少、核致密、核仁不明显、染色质部分聚集,外周血淋巴细胞中不典型淋巴细胞及幼稚淋巴细胞≤ 55%。③典型的免疫表型:CD19+、CD5+、CD23+、CD43+/-、CD10-、cyclin D1-、CD200+;表面免疫球蛋白(sIg)、CD20 及CD79b 弱表达(dim)。流式细胞学确认B 细胞的克隆性,即B细胞表面限制性表达κ 或λ 轻链(κ ∶ λ>3 ∶ 1 或<0.3 ∶ 1) 或>25%的B 细胞sIg 不表达。
单克隆B 淋巴细胞增多症(MBL):MBL 是指健康个体外周血存在低水平的单克隆B 淋巴细胞。
诊断标准:① B 细胞克隆性异常;②外周血B 淋巴细胞<5×109/L;③无肝、脾、淋巴结肿大(所有淋巴结长径均<1.5cm);④无贫血及血小板减少;⑤无慢性淋巴增殖性疾病(CLPD) 的其他临床症状。每年1% ~2%的MBL 进展为需要治疗的CLL[3-4]。
分子生物学标志物的检测可提供患者预后相关的信息:如IGHV 野生型、TP53 基因缺失或突变均提示预后不良[5]。CLL 患者需进行FISH 检测del(13q)、+12、del(11q)、del(17p) 以及TP53、IGHV、NOTCH1、SF3B1、BIRC3、MYD88 等基因突变,以帮助判断预后和指导治疗。
3 分期
临床上对于CLL 广泛应用Rai 和Binet 两种临床分期系统[6,7]。这两种分期均仅依赖体检和简单实验室检查,不需要进行超声、CT 或MRI 扫描等影像学检查。

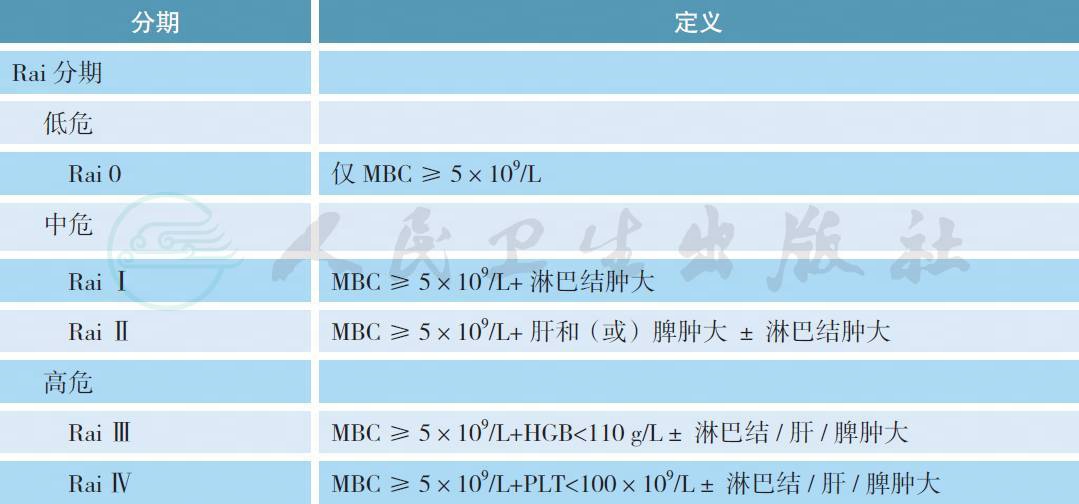
【注释】
淋巴区域:包括颈、腋下、腹股沟(单侧或双侧均计为1 个区域)、肝和脾。MBC:单克隆B 淋巴细胞计数。免疫性血细胞减少不作为分期的标准。
4 治疗
4.1 初治患者
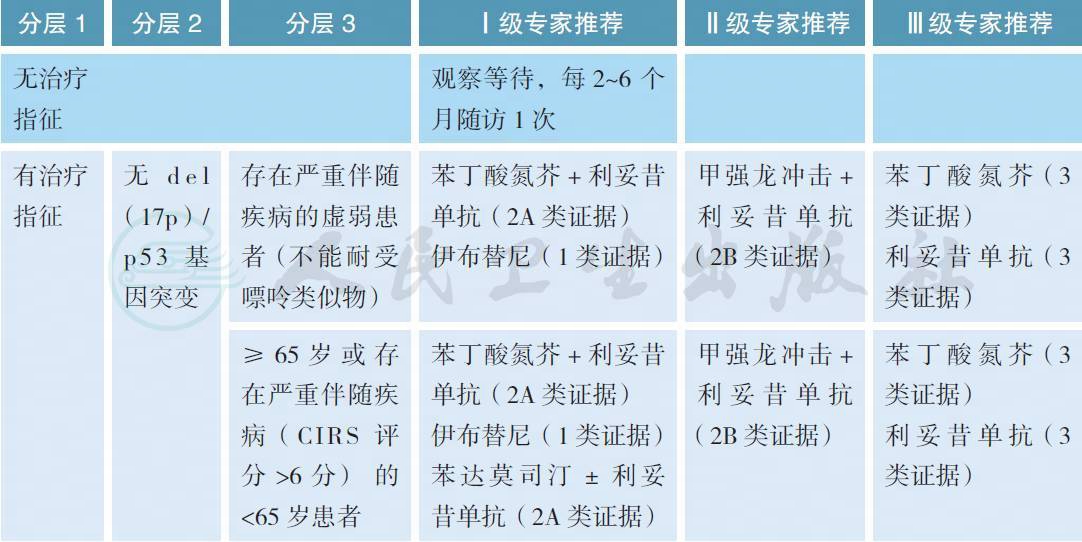
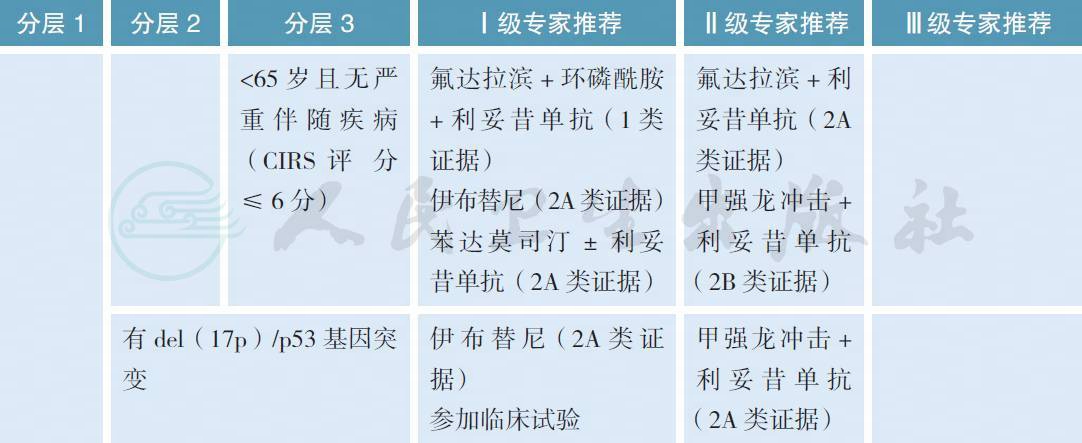
【注释】
(1) 苯丁酸氮芥+ 利妥昔单抗方案
苯丁酸氮芥10mg/m2,d1-7
利妥昔单抗375mg/m2,第1 周期;此后500mg/m2
每28d 重复。
(2) 伊布替尼方案
伊布替尼420mg,口服,每日1 次。
(3) 苯达莫司汀± 利妥昔单抗方案
苯达莫司汀90mg/m2,d1-2
利妥昔单抗375mg/m2,d0,第1 周期;此后500mg/m2
每28d 重复。
(4) 甲强龙冲击+ 利妥昔单抗方案
甲泼尼龙1g/m2,d1-5
利妥昔单抗375mg/m2,每周1 次,连用4 周
每28d 重复。
(5) 氟达拉滨+ 环磷酰胺+ 利妥昔单抗方案
氟达拉滨25mg/m2,d1-3
环磷酰胺250mg/m2,d1-3
利妥昔单抗375mg/m2,d0,第1 周期;此后500mg/m2
每28d 重复。
(6) 氟达拉滨+ 利妥昔单抗方案
氟达拉滨25mg/m2,d1-5
利妥昔单抗375mg/m2,每周1 次,连用4 周每28d 重复。
4.2 复发难治患者
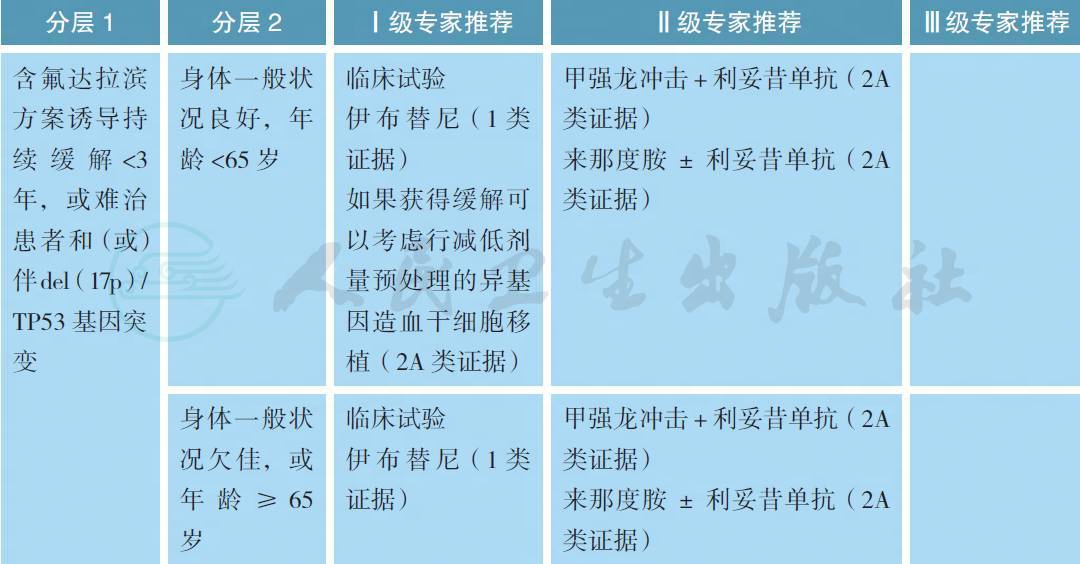

【注释】
来那度胺+ 利妥昔单抗方案
来那度胺10mg/m2,d9 开始口服
利妥昔单抗375mg/m2,每周1 次,连用4 周,第1 周期;第3~12 周期第1 天给药
每28d 重复。
CLL 的治疗指征包括以下几项,只有具备以下至少1项时方可开始治疗:①进行性骨髓衰竭的证据:表现为血红蛋白和(或) 血小板进行性减少。②巨脾(如左肋缘下>6cm) 或进行性或有症状的脾肿大。③巨块型淋巴结肿大(如最长直径>10cm) 或进行性或有症状的淋巴结肿大。④进行性淋巴细胞增多,如2 个月内淋巴细胞增多>50%,或淋巴细胞倍增时间(LDT)<6 个月。当初始淋巴细胞<30×109/L,不能单凭LDT 作为治疗指征。⑤淋巴细胞计数>200×109/L,或存在白细胞淤滞症状。⑥自身免疫性溶血性贫血(AIHA) 和(或) 免疫性血小板减少症(ITP) 对皮质类固醇或其他标准治疗反应不佳。⑦至少存在下列一种疾病相关症状:a. 在以前6 个月内无明显原因的体重下降≥ 10%;b. 严重疲乏(如ECOG 体能状态≥ 2;不能进行常规活动);c. 无感染证据,体温>38.0℃,≥ 2 周;d. 无感染证据,夜间盗汗>1 个月。⑧临床试验:符合所参加临床试验的入组条件。不符合上述治疗指征的患者,每2~6 个月随访1 次,随访内容包括临床症状及体征、肝/ 脾/ 淋巴结肿大情况和血常规等。
CLL 的一线治疗根据FISH 结果[del(17p) 和del(11q)]、年龄及身体状态进行分层治疗。患者的体能状态和实际年龄均为重要的参考因素;治疗前评估患者的伴发疾病和身体适应性极其重要。体能状态良好的患者建议选择一线标准治疗,其他患者则使用减低剂量化疗或支持治疗。对于del(17p) 或P53 基因突变的患者,常规化疗方案疗效不佳,建议参加新药临床试验。若无临床试验,建议首选伊布替尼治疗。在一项包括35 例初治的伴有P53 基因缺失或突变的CLL 患者的Ⅱ期临床试验中,伊布替尼单药的客观有效率达97%,2 年生存率84%,2 年时的疾病累积进展率仅9%,显示出较好的疗效
5 预后评估
目前推荐使用CLL 国际预后指数(CLL-IPI)进行综合预后评估[8]。
慢性淋巴细胞白血病国际预后指数(CLL-IPI)
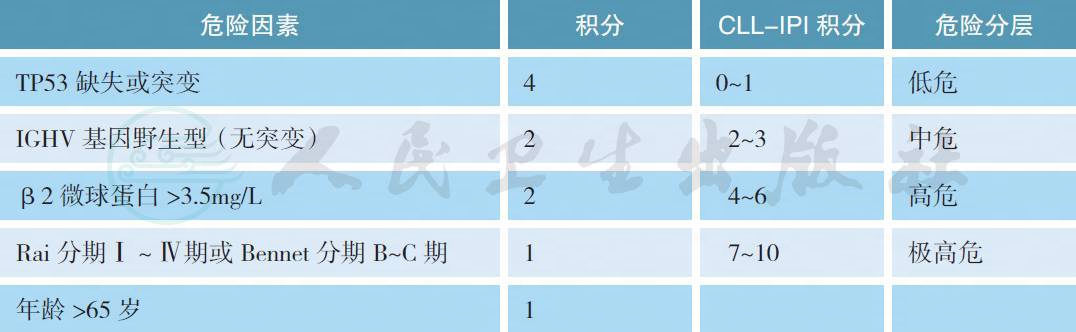
IGHV. 免疫球蛋白重链可变区
[1]Catovsky D,Müller-Hermelink HK,Montserrat E,et al. B-cell prolymphocytic leukaemia. In:JaffeES,Harris NL,Stein H,Vardiman JW,eds. World Health Organization Classification of TumoursPathology and Genetics of Tumours of Haematopoietic and Lymphoid Tissues. Lyon:IARC Press,2001:131-132.
[2]Catovsky D,Ralfkiaer E,Müller-Hermelink HK. T-cell prolymphocytic leukaemia. In:JaffeES,Harris NL,Stein H,Vardiman JW,eds. World Health Organization Classification of Tumours Pathology andGenetics of Tumours of Haematopoietic and Lymphoid Tissues. Lyon:IARC Press,2001:195-196.
[3]Rawstron AC,Bennett FL,O′Connor SJ,et al. Monoclonal B-cell lymphocytosis and chroniclymphocytic leukemia. N Engl J Med,2008,359(6):575-583.
[4]Strati P,Shanafelt TD. Monoclonal B-cell lymphocytosis and early-stage chronic lymphocytic leukemia:diagnosis,natural history,and risk stratification. Blood ,2015,126(4):454-462.
[5]Parikh SA,Shanafelt TD. Prognostic factors and risk stratification in chronic lymphocytic leukemia.Semin Oncol ,2016,43:233-240.
[6]Rai KR,Sawitsky A,Cronkite EP,et al. Clinical staging of chronic lymphocytic leukemia. Blood ,1975,46(2):219-234.
[7]Binet JL,Auquier A,Dighiero G,et al. A new prognostic classification of chronic lymphocyticleukemia derived from a multivariate survival analysis. Cancer,1981,48:198-204.
[8]International CLL-IPI working group. An international prognostic index for patients with chroniclymphocytic leukaemia (CLL-IPI):a meta-analysis of individual patient data. Lancet Oncol ,2016,17(6):779-790.
[9]Farooqui MZ,Valdez J,Martyr S,et al. Ibrutinib for previously untreated and relapsed or refractorychronic lymphocytic leukaemia with TP53 aberrations:a phase 2,single-arm trial. Lancet Oncol,2015,16:169-176.
[10]Byrd JC,Brown JR,O’Brien S,et al. Ibrutinib versus Ofatumumab in Previously Treated ChronicLymphoid Leukemia. N Engl J Med,2014,371:213-223.
[11]Reljic T,Kumar A,Djulbegovic B,et al. High-dose therapy and autologous hematopoietic celltransplantation as front-line consolidation in chronic lymphocytic leukemia:a systematic review. BoneMarrow Transplant,2015,50:1069-1074.
[12]Hillmen P,Gribben JG,Follows GA,et al. Rituximab plus chlorambucil as first-line treatment forchronic lymphocytic leukemia:Final analysis of an open-label phase Ⅱ study. J Clin Oncol,2014Apr 20,32(12):1236-1241. doi:10.1200/JCO.2013.49.6547.
[13]Burger JA,Tedeschi A,Barr PM,et al. Ibrutinib as initial therapy for patients with chroniclymphocytic leukemia. N Engl J Med,2015 Dec 17,373(25):2425-2437. doi:10.1056/NEJMoa1509388.
[14]Eichhorst B,Fink AM,Bahlo J,et al. First-line chemoimmunotherapy with bendamustine andrituximab versus fludarabine,cyclophosphamide,and rituximab in patients with advanced chroniclymphocytic leukaemia (CLL10):an international,open-label,randomised,phase 3,noninferioritytrial. Lancet Oncol,2016 Jul,17(7):928-942. doi:10.1016/S1470-2045(16)30051-1.
[15]Castro JE,Sandoval-Sus JD,Bole J,et al. Rituximab in combination with high-dosemethylprednisolone for the treatment of fludarabine refractory high-risk chronic lymphocytic leukemia.Leukemia,2008 Nov,22(11):2048-2053. doi:10.1038/leu.2008.214.
[16]Byrd JC,Peterson BL,Morrison VA,et al. Randomized phase 2 study of fludarabine with concurrentversus sequential treatment with rituximab in symptomatic,untreated patients with B-cell chroniclymphocytic leukemia:results from Cancer and Leukemia Group B 9712 (CALGB 9712). Blood,2003 Jan 1,101(1):6-14.
[17]Badoux XC,Keating MJ,Wen S,et al. Phase Ⅱ study of lenalidomide and rituximab as salvagetherapy for patients with relapsed or refractory chronic lymphocytic leukemia. J Clin Oncol,2013 Feb10,31(5):584-591. doi:10.1200/JCO.2012.42.8623.