 去看看
去看看


1 治疗前评估
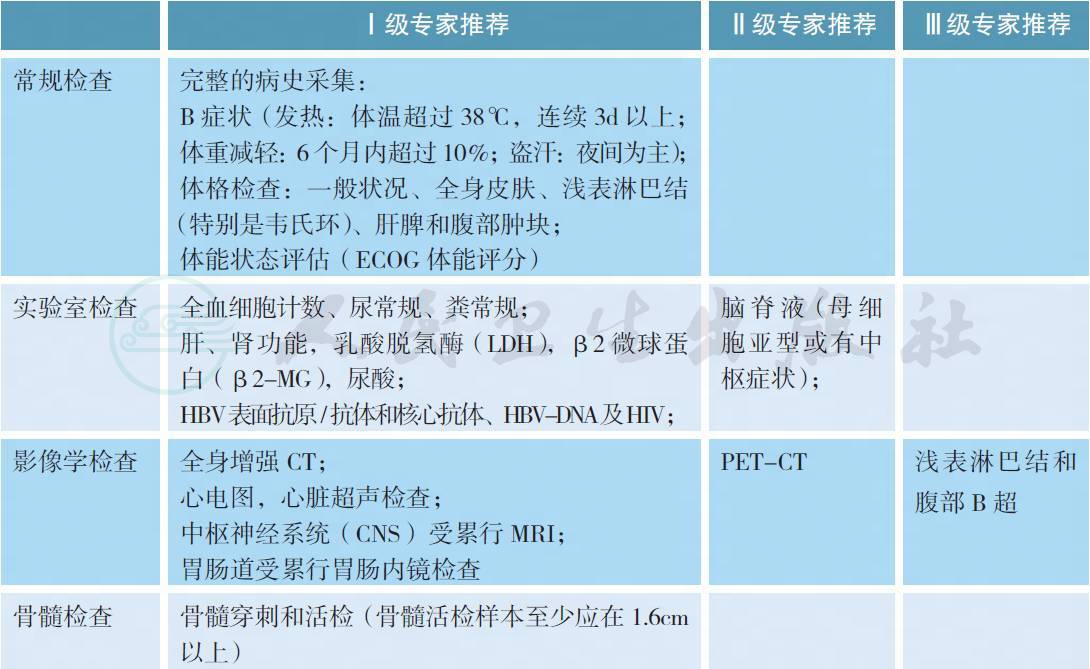
2 病理诊断
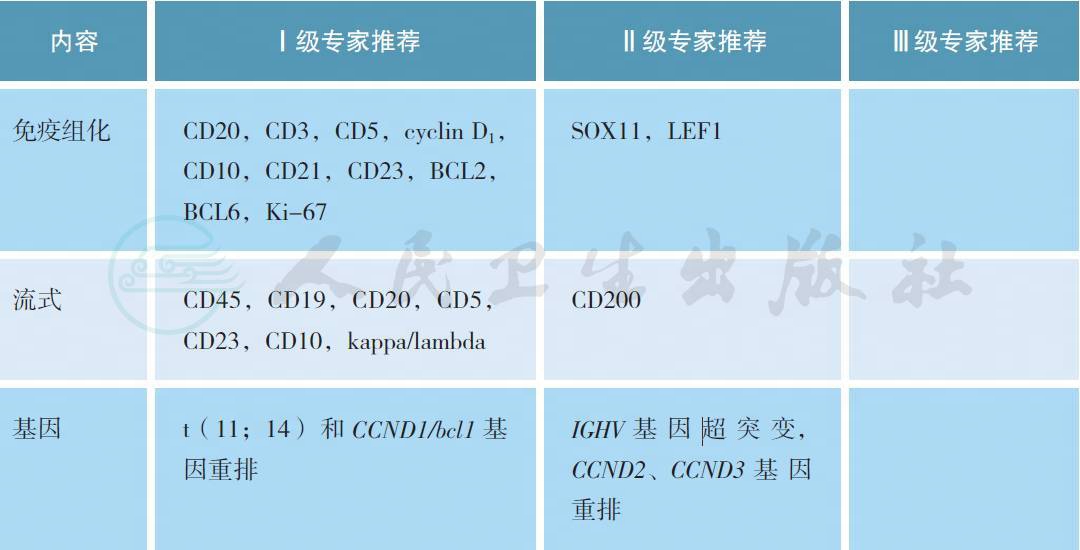
【注释】
套细胞淋巴瘤(mantle cell lymphoma,MCL)主要依据典型的组织形态学特征、免疫表型和(或)t(1l:14)/CCND1 异常来诊断[1]。典型的免疫表型为:CD5+,CD20+,CD23-/+,Cyclin D1+,CD10-/+。目前MCL 主要分为以下几型:①经典型套细胞淋巴瘤,对应于生发中心前阶段的B 细胞,通常不伴免疫球蛋白重链可变区(IGHV) 基因超突变,SOX11 阳性。②白血病样非淋巴结性套细胞淋巴瘤[2],肿瘤细胞表现为非复杂核型,伴有IGHV 基因突变,不表达或低表达SOX11,无TP53基因突变或缺失。临床上常侵犯外周血、骨髓和脾,病情发展缓慢,但如果出现TP53 异常则可以进展为侵袭性较高的疾病。③原位套细胞瘤变(ISMCN)[3],指cyclin D1 阳性的B 细胞局限于滤泡套区的内层,并未达到MCL 的诊断标准。ISMCN 常偶然被发现,有时与其他淋巴瘤共存,可呈播散性表现,但很少出现进展。
3 分期
参照2014 年Lugano 分期标准,见附录A。
附录A 2014 版Lugano 分期标准(CT、MRI 或PETCT作为分期检查方法)

【注释】
1.*.根据2014年Lugano改良分期标准,不再对淋巴瘤的大包块(bulky)病灶进行具体的数据限定,只需在病例中明确记载最大病灶之最大径即可;Ⅱ期伴有大肿块的患者,应根据病理类型及疾病不良预后因素而酌情选择治疗原则,如伴有大包块的惰性淋巴瘤患者可选择局限期治疗模式,但是伴有大包块的侵袭性淋巴瘤患者,则应选择进展期治疗模式。
2.AnnArbor分期对于淋巴结分布区域的定义(仍然适用于Lugano分期):膈上(共12个区域,由于不能被一个放射野涵盖,因此左右各为一个区域):韦氏环(Waldeyer环)(鼻咽及口咽部的淋巴组织环,包括腭扁桃体、咽后壁腺样体、舌扁桃体及其他该部位淋巴组织为一个区域)、左/右颈部(单侧耳前、枕部、颌下、颏下、颈内、锁骨上为一个区域)、左/右锁骨下、左/右腋窝(含胸部及内乳)、左/右滑车上(含肘窝)、纵隔(含气管旁、胸腺区域)、左/右肺门;膈下(共9个区域):脾脏、上腹部(脾门、肝门、腹腔)、下腹部(腹主动脉旁、腹膜后、肠系膜周围、腹部其他非特指淋巴结为一个区域)、左/右髂血管旁、左/右腹股沟(含股部)、左/右腘窝。
3.3.B症状主要在HL中有预后意义并需要记录;最新文献中B症状在NHL的价值较低,但是仍然建议在病例中记录。所谓B症状:不明原因体重下降10%(诊断前6个月内),发热>38℃并排除其他原因发热,盗汗(夜间大量出汗,需要更换衣服被褥)。
4.扁桃体、韦氏环、脾脏视为淋巴器官。
5.备注:淋巴瘤的分期尽管不断改良,但是争议持续存在,主要是对于分期的定义存在解读分歧,或者对特殊部位未能做出全面而明确的定义。正因如此,后续才建立了多种预后指数用于补充临床分期之不足,以指导临床治疗和判断预后。而且,不同于实体瘤的是,淋巴瘤的临床分期不是决定治疗和预后的最关键因素。
4 治疗
4.1 初治MCL 的治疗

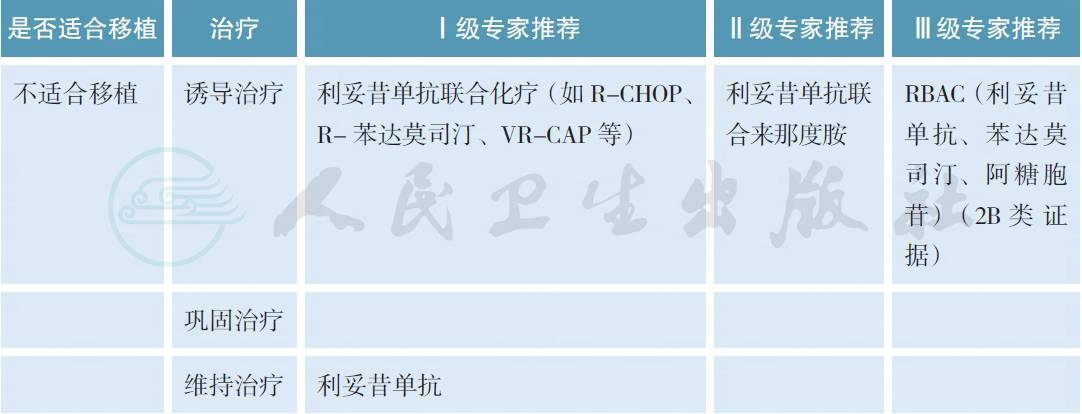
【注释】
(1)R-CHOP/R-DHAP 方案
R-CHOP 方案
利妥昔单抗375mg/m2,d0
环磷酰胺750mg/m2,d1
多柔比星50mg/m2,d1
长春新碱1.4mg/m2,d1(最大剂量2mg)
泼尼松40mg/m2,d1-5
每21d 重复。
R-DHAP 方案
利妥昔单抗375mg/m2,d0
地塞米松40mg/d,d1-4(原方案为该剂量,各中心可酌情调整)
顺铂100mg/m2,24h 连续输注,d1
阿糖胞苷2g/m2,q12h,d2
每21d 重复。
(2)R- 大剂量CHOP/R- 大剂量阿糖胞苷方案
R- 大剂量CHOP 方案
利妥昔单抗375mg/m2,d0
环磷酰胺1200mg/m2,d1
多柔比星75mg/m2,d1
长春新碱2mg,d1
泼尼松100mg,d1-5
每21d 重复。
R- 大剂量阿糖胞苷方案
利妥昔单抗375mg/m2,d0
阿糖胞苷3g/m2,q12h,d1-2(备注:年龄大于60 岁时,剂量调整为2g/m2)
(3)R-HyperCAVD 方案
A 方案
利妥昔单抗375mg/m2,d1
环磷酰胺300mg/m2,q12h,IV(持续2h 以上),d2-4
美司钠600mg/(m2·d),CTX 用药前1h 至最后1 次CTX 后12h
多柔比星16.7mg/ (m2·d),连续输注72h,d5-7
地塞米松40mg/d,d2-5,d12-15
长春新碱1.4mg/m2,最大2mg,d5,d12
B 方案
利妥昔单抗375mg/m2,d1
甲氨蝶呤1g/m2,d2(亚叶酸钙解救)
阿糖胞苷3g/m2,q12h,d3-4(备注:鉴于阿糖胞苷骨髓抑制毒性较重,尤其是对血小板的抑制较重,可导致化疗延迟甚至中止,因此各中心可根据患者年龄、体力情况、淋巴瘤病情等综合判断,酌情调整剂量)
(4)R- 苯达莫司汀方案
利妥昔单抗375mg/m2,d0
苯达莫司汀90mg/m2,d1-2
每28d 重复。
(5)VR-CAP 方案
硼替佐米1.3mg/m2,d1,d4,d8,d11
利妥昔单抗375mg/m2,d1
环磷酰胺750mg/m2,d1
多柔比星50mg/m2,d1
泼尼松100mg,d1-5
每21d 重复。
(6) 利妥昔单抗联合来那度胺方案
利妥昔单抗375mg/m2,d0
来那度胺15~25mg,d1-21
每28d 重复。
4.2 复发难治MCL 的治疗

【注释】
(1) 伊布替尼+ 利妥昔单抗方案
伊布替尼560mg 口服,每日1 次
利妥昔单抗375mg/m2,每周1 次,连用4 周,此后第3~8 周期第1 天用药,随后每2 周期用药
1 次,最长2 年。
每28d 重复。
(2) 硼替佐米± 利妥昔单抗方案
硼替佐米1.3~1.5mg/m2,d1,d4,d8,d11
利妥昔单抗375mg/m2,d1,d8
(3) 伊布替尼+ 来那度胺+ 利妥昔单抗方案
伊布替尼560mg 口服,每日1 次
来那度胺15mg 口服,每日1 次,d1-21
利妥昔单抗375mg/m2,每周1 次,连用4 周,此后每8 周1 次
每28d 重复。
白血病样非淋巴结性套细胞淋巴瘤和原位套细胞淋巴瘤由于病情进展缓慢且不可治愈,参照惰性淋巴瘤的治疗原则可能不需要马上开始治疗,而只有在有治疗指征如患者有症状或病情快速进展或肿瘤负荷非常大等时才需要治疗。
对于需要治疗的初治患者,Ⅰ / Ⅱ期的患者(极罕见) 可以考虑局部放疗或免疫化疗联合局部放疗。而对于Ⅱ期伴有大包块或Ⅲ / Ⅳ期患者,我们根据患者的年龄(通常为65 岁) 及体力状况等将患者分为可以移植组和不可移植组,再给予相应的诱导治疗。对于不可移植组患者,常规推荐的方案为利妥昔单抗联合化疗,如R-CHOP、R- 苯达莫司汀和硼替佐米联合R-CAP 等方案[7-9]。在Rummel 教授的研究里,R- 苯达莫司汀组较R-CHOP 组的病情进展率要低,且血液学毒性及脱发更少[8]。在另一项随机对照研究中,硼替佐米联合R-CAP 组较R-CHOP 组中位PFS 明显延长,但需注意其血液学毒性和神经毒性[9]。对于可以移植的患者,均推荐在诱导治疗达到缓解后行自体造血干细胞移植巩固[10]。而移植前选择什么的诱导化疗方案到目前为止仍然未达到统一。但数个临床研究都提示诱导方案使用含有大剂量阿糖胞苷的方案可能更好,如R-CHOP 与R-DHAP 交替、R- 大剂量CHOP 与大剂量阿糖胞苷交替或R-HyperCAVD 方案[11-13]。对于一线治疗达到缓解的患者,无论能否行自体造血干细胞移植,均可以考虑利妥昔单抗维持[14,15]。
由于传统的挽救化疗在复发难治的MCL 患者中疗效有限,大家自然会更多地关注一些新的靶向治疗药物。如硼替佐米,单药总有效率为33%[16],如来那度胺,单药总有效率为28%[17],目前认为有效率最高的为伊布替尼,总有效率为68%,完全缓解率为21%[18],或这些药物的联合应用[19]。但这些药物目前价格都比较昂贵,有条件的患者可以尝试。还可以选择之前未使用过的无交叉耐药的化疗方案,如苯达莫司汀[20]。如果是年轻患者,也可以考虑减低预处理剂量的异基因造血干细胞移植[21]等。
5 预后评估
简易套细胞淋巴瘤国际预后评分系统(MIPI):低危组:0~3 分;中危组:4~5 分;高危组:6~11 分。
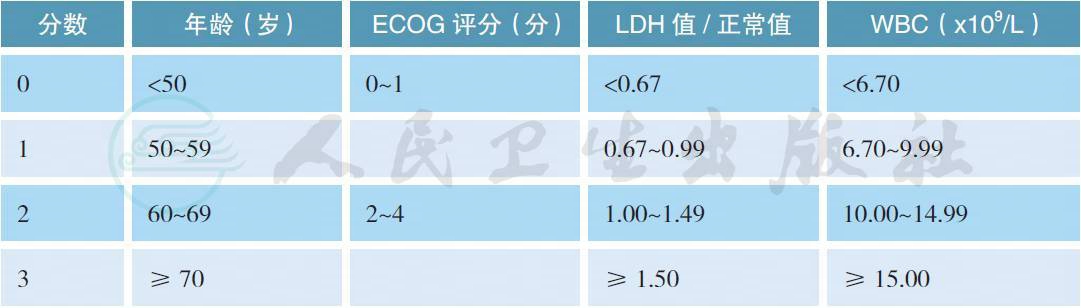
【注释】
在应用IPI 来评价MCL 患者的预后时,并不能很好地区分这部分患者的预后。因此,欧洲MCL工作组提出了MIPI[4],主要包括年龄、ECOG 评分、LDH 及白细胞这几项指标,根据评分可以将所有患者分为3 个组,但这个评分系统较复杂,后来又提出了简化的MIPI[5],便于临床操作。还有研究将Ki-67(阳性标准为>30%) 联合MIPI 将患者进行危险分层,能更好地预测患者预后,也值得推荐[6]。
[1]Swerdlow SH,Campo E,Pileri SA,et al. The 2016 revision of the World Health Organizationclassification of lymphoid neoplasms. Blood,2016,127(20):2375-2390.
[2]Jares P,Colomer D,Campo E. Molecular pathogenesis of mantle cell lymphoma. J Clin Invest,2012,122(10):3416-3423.
[3]Carvajal-Cuenca A,Sua LF,Silva NM,et al. In situ mantle cell lymphoma:clinical implications ofan incidental finding with indolent clinical behavior. Haematologica,2012,97(2):270-278.
[4]Hoster E,Dreyling,M,Klapper W,et al. A new prognostic index (MIPI) for patients withadvanced mantle cell lymphoma. Blood,2008,111:558-565.
[5]Geisler CH,Kolstad,A,Laurell A,et al. The mantle cell lymphoma International PrognosticIndex (MIPI) is superior to the International Prognostic Index (IPI) in predicting survival followingintensive first line immunochemotherapy and autologous stem cell transplantation (ASCT). Blood,2010,115:1530-1533.
[6]Hoster E,Rosenwald A,Berger F,et a1.Prognostic value of Ki-67index.cytology,and growthpattern in mantle-cell lymphoma:results from randomized trials of the European Mantle Cell LymphomaNetwork.J Clin Oncol,2016,34 (12):1386-1394.
[7]Lenz G,Dreyling,M,Hoster E,et al. Immuno-chemotherapy with rituximab and cyclophosphamide,doxorubicin,vincristine,and prednisone significantly improves response and time totreatment failure,but not long term outcome in patients with previously untreated mantle cell lymphoma:Results of a prospective randomized trial of the German Low Grade Lymphoma Study Group (GLSG). JClin Oncol,2005,23:1984-1992.
[8]Rummel M,Niederle,N,Maschmeyer G,et al. Bendamustine plus rituximab versus CHOP plusrituximab as first-line treatment for patients with indolent and mantle-cell lymphomas:An open-label,muticentre,randomised,phase 3 non-inferiority trial. Lancet,2013,381:1203-1210.
[9]Robak T,Huang H,Jin J,et al. Bortezomib-based therapy for newly diagnosed mantle-cell lymphoma.N Engl J Med,2015,372:944-953.
[10]Dreyling M. Lenz G. Hoster E,et al. Early consolidation by myeloablative radiochemotherapy followedby autologous stem cell transplantation in first remission significantly prolongs progression-free survivalin mantle-cell lymphoma:results of a prospective randomized trial of the European MCL Network.Blood,2005,105:2677-2684.
[11]Hermine O,Hoster E,Walewski J,et al. Addition of high-dose cytarabine to immunochemotherapybefore autologous stem-cell transplantation in patients aged 65 years or younger with mantle celllymphoma (MCL Younger):a randomised,open-label,phase 3 trial of the European Mantle CellLymphoma Network. Lancet,2016 Aug 6,388:565-575.
[12]Eskelund CW,Kolstad A,Jerkeman M, et al. 15-year follow-up of the Second Nordic Mantle CellLymphoma trial (MCL2):prolonged remissions without survival plateau. Br J Haematol,2016 Nov,175(3):410-418.
[13]Romaguera JE,Fayad L,Rodrignez MA,et a1.High rate of durable remissions after treatment ofnewly diagnosed aggressive mantle cell lymphoma with rituximab plus hyperCVAD alternating withrituximab plus high—dose methotrexate andcytarabine.J clin Oncol,2005,23(28):7013-7023.
[14]Vidal L,Gafter-Gvili A,Dreyling M,et al. Rituximab maintenance (MR) for patients with mantelcell lymphoma( MCL)—A systemic review and meta-analysis of the randomized controlled trials( RCTs).Blood,2016,128:1802.
[15]Le Gouill S,Thieblemont C,Oberic L,et al. Rituximab after Autologous Stem-Cell Transplantationin Mantle-Cell Lymphoma. N Engl J Med,2017,377(13):1250-1260.
[16]Fisher RI,Bernstein SH,Kahl BS,et al. Multicenter phase Ⅱ study of bortezomib in patients withrelapsed or refractory mantle cell lymphoma. J Clin Oncol,2006,24:4867-4874.
[17]Goy A,Sinha R,Williams ME,et al. Single agent lenalidomide in patients with mangle-celllymphoma who relapsed or progressed after or were refractory to bortezomib:Phase Ⅱ MCL-001(EMERGE) Study. J Clin Oncol,2013,49:2835.
[18]Wang L,Rule,S,Martin P,et al. Targeting BTK with Ibruitinib in relapsed or refractory mantle cell lymphoma. N Engl J Med,2014,369:507-516.
[19]Jerkeman M,Eskelund CW,Hutchings M,et al. Ibrutinib,lenalidomide,and rituximab in relapsedor refractory mantle cell lymphoma (PHILEMON):a multicentre,open-label,single-arm,phase2 trial. Lancet Haematol,2018,5(3):e109-116.
[20]Robinson KS,Williams ME,van der Jagt RH,et al. Phase Ⅱ multicenter study of bendamustine plusrituximab in patients with relapsed indolent B-cell and mantle cell non-Hodgkin′s lymphoma. J ClinOncol,2008,26:4473-4479.
[21]Tessoulin B,Ceballos P,Chevallier P,et al. Allogeneic stem cell transplantation for patients withmantle cell lymphoma who failed autologous stem cell transplantation:a national survey of the SFGMTC.Bone Marrow Transplant,2016,51(9):1184-1190.
[22]Delarue R,Haioun C,Ribrag V,et al. CHOP and DHAP plus rituximab followed byautologous stem cell transplantation in mantle cell lymphoma:a phase 2 study from the Grouped′Etude des Lymphomes de l′Adulte. Blood,2013 Jan 3,121(1):48-53. doi:10.1182/blood-2011-09-370320.
[23]Geisler CH,Kolstad A,Laurell A,et al. Long-term progression-free survival of mantle celllymphoma after intensive front-line immunochemotherapy with in vivo-purged stem cell rescue:anonrandomized phase 2 multicenter study by the Nordic Lymphoma Group. Blood,2008 Oct 1,112(7):2687-2693. doi:10.1182/blood-2008-03-147025.
[24]Romaguera JE,Fayad L,Rodriguez MA,et al. High rate of durable remissions after treatment ofnewly diagnosed aggressive mantle-cell lymphoma with rituximab plus hyper-CVAD alternating withrituximab plus high-dose methotrexate and cytarabine. J Clin Oncol,2005 Oct 1,23(28):7013-7023.
[25]Wang ML,Lee H,Chuang H,et al. Ibrutinib in combination with rituximab in relapsed or refractorymantle cell lymphoma:a single-centre,open-label,phase 2 trial. Lancet Oncol,2016 Jan,17(1):48-56. doi:10.1016/S1470-2045(15)00438-6.
[26]Baiocchi RA,Alinari L,Lustberg ME,et al. Phase 2 trial of rituximab and bortezomib in patientswith relapsed or refractory mantle cell and follicular lymphoma. Cancer,2011,117(11):2442-2451.