 去看看
去看看


一、简介
子宫内膜癌为女性生殖道常见恶性肿瘤之一,发达国家中发病率居女性生殖道恶性肿瘤首位,死亡率居第二位。多见于老年妇女,高发年龄50~60岁,年轻患者有增多趋势。由于人类寿命延长和肥胖人群增多,近二十年间子宫内膜癌发病率仍居高不下,而死亡率也明显上升。死亡率的上升除与老年、肥胖、内科并发症多等相关外,与晚期病例、高危组织类型增多及一些患者未能受到适宜诊治相关。目前对两种类型内膜癌的病理及基础研究已取得较大进展;临床手术、化疗、激素治疗亦积累了更多资料,临床研究更加深入;对年轻早期患者的保守治疗亦作了一定探索。但在治疗中对术前影像学评估价值,术中肉眼及病理冷冻切片检查对肌层受累程度的判断准确性,淋巴结切除范围等均尚存争议。为进一步改善预后,妇科肿瘤医师应进一步识别、区分高危子宫内膜癌患者,进行适宜治疗,以期降低死亡率,达到最佳疗效。
二、诊断
1.病史
子宫内膜癌多见于绝经后妇女(70%),围绝经期20%~25%,< 40岁约5%,发病与肥胖、雌激素持续增高、遗传等因素相关,询问病史时应重视以下高危因素:
(1) 肥胖、无排卵性不孕、不育、延迟绝经(52岁以后绝经)。
(2) 代谢紊乱性疾病:糖尿病、高血压。
(3) 与雌激素增高有关的妇科疾病:多囊卵巢综合征、卵巢颗粒细胞瘤、子宫内膜增生或不典型增生史和子宫肌瘤有不规则出血者。
(4) 有使用外源性雌激素史者,特别是无孕激素对抗雌激素替代治疗(ERT),或长期应用他莫昔芬(tamoxifen)患者。
(5) 有癌家族史、多发癌及重复癌倾向者(乳腺癌、卵巢癌等),Lynch Ⅱ综合征。遗传性非息肉样结肠直肠癌(HNPCC)患者其内膜癌发病危险为40%~60%等。
有高危因素的患者应密切随访,若有月经过多、阴道不规则出血等症状出现应行分段诊刮,明确诊断。Ⅱ型Lynch综合征患者亦可在完成生育任务后行预防性子宫切除术。
2.症状
(1) 阴道出血:
①绝经后阴道出血:绝经后阴道流血,为子宫内膜癌患者的主要症状,子宫内膜癌患者多为绝经后妇女,90%以上有阴道流血症状,绝经时间愈长,发生内膜癌的概率愈高。②围绝经期妇女月经紊乱:约20%的内膜癌患者为围绝经期妇女,以围绝经期月经紊乱及血量增多为主要表现。③40岁以下妇女月经紊乱或经量增多者,近年来年轻患者已有增多趋势(5%~10%),多为肥胖、不孕或多囊卵巢综合征患者。
(2) 阴道异常排液:
可为浆液性或血性分泌物。
(3) 下腹疼痛及其他症状:
下腹疼痛可由宫腔积脓或积液引起,晚期则因癌肿扩散导致消瘦、下肢疼痛及贫血等。
应重视阴道流血、排液等症状。有以上症状妇女均应考虑有无内膜癌可能性,并应及时进行妇科及其他相关检查。
3.检查
(1) 全面查体:
注意有无糖尿病、高血压、心血管及肺部疾病。
(2) 妇科检查:
排除阴道、宫颈病变出血及炎性感染引起的排液。早期盆腔检查多正常,晚期可有子宫增大、附件肿物、贫血及远处转移的相应体征。
4.辅助检查
(1) 细胞学涂片检查:
宫颈和阴道脱落细胞学涂片检查阳性率低,宫腔刷片或宫腔冲洗液细胞学涂片检查阳性率增高,但均不能作为确诊依据。
(2) 经阴道B型超声检查:
可了解子宫大小、宫腔内有无异常回声、内膜厚度、肌层有无浸润、附件肿物大小及性质等,为首选无创辅助检查方法。绝经后妇女内膜厚度< 5mm时,其阴性预测值可达96%。
(3) 诊刮或内膜活检:
是确诊或排除子宫内膜癌的重要方法。对绝经后内膜增厚> 5mm或有宫腔赘生物者;年龄大于40岁阴道不规则流血怀疑内膜癌者行诊刮术。40岁以下有内膜癌高危因素,高度怀疑内膜癌者也应行诊刮术。
(4) 宫腔镜检查:
近年来,宫腔镜检已广泛应用于宫内膜病变的早期诊断。可直接对可疑部位进行活检,提高诊断准确性,避免常规活检或诊刮的漏诊。多用于经阴道B超检查子宫内膜无明显增厚和病变或呈内膜息肉样变者;或经诊刮活检阴性,仍有反复出血的患者。
(5) MRI、CT、CA125等检查:
病情需要者可选用MRI、CT检查及CA125检测。MRI、CT对淋巴结转移诊断价值相同,MRI对宫颈受累及肌层浸润深度的预测准确度优于CT。CA125值明显升高者,应考虑可能有子宫外病灶存在,术后亦可用作监测指标。对疑有宫外病灶的高危患者亦可选用PET-CT检查,明确病变范围。
5.诊断
应根据诊刮或直接宫腔活检,或宫腔镜下活检及病理组织学检查结果等作出诊断。
三、分期
子宫内膜癌采用FIGO手术病理分期,目前使用的是FIGO 2009年子宫内膜癌的手术病理分期。对于未行手术治疗的患者或者是先行放疗的患者,采用1971年制定的临床分期。
1.手术-病理分期(表1)
表1 子宫内膜癌手术-病理分期(FIGO,2009年)

续表

注意:1.宫颈腺体受累为Ⅰ期,不再按照以前的分期作为Ⅱ期
2.腹水细胞学阳性应当单独报告,不改变分期
2.临床分期(表2)
表2 FIGO子宫内膜癌临床分期(1971年)

四、病理类型
子宫内膜癌病理类型:腺癌为最主要的病理类型,其中以子宫内膜样腺癌最为常见(60%~65%),其他较少见亚型见表3。2003年WHO分类将子宫恶性中胚叶混合瘤中癌肉瘤归为子宫内膜癌肉瘤。NCCN 2010年分类中亦将子宫癌肉瘤归于Ⅱ型子宫内膜癌,即特殊类型。
子宫内膜样腺癌分为高、中、低分化(Grad:1,2,3),为预后重要因素。G1、G2病变多为来源于增生过长子宫内膜,与雌激素作用相关;G3则可能来源于萎缩的内膜,或为内膜样癌晚期事件,因基因突变而恶变与雌激素无关。
伴鳞状分化成分的子宫内膜样癌,其腺癌的分化程度(G1~G3)为预后的重要因素。
子宫浆液性(乳头状)腺癌(uterine papillary serous carcinoma,UPSC)现多称子宫浆液性癌(uterine serous carcinoma,USC 或endometrial serous carcinoma,ESC),恶性程度极高,占1%左右(详见后)。透明细胞癌常见于老年患者,预后差,Ⅰ期5年生存率仅44%。其他特殊类型均属Ⅱ型子宫内膜癌。
表3 子宫内膜癌病理类型
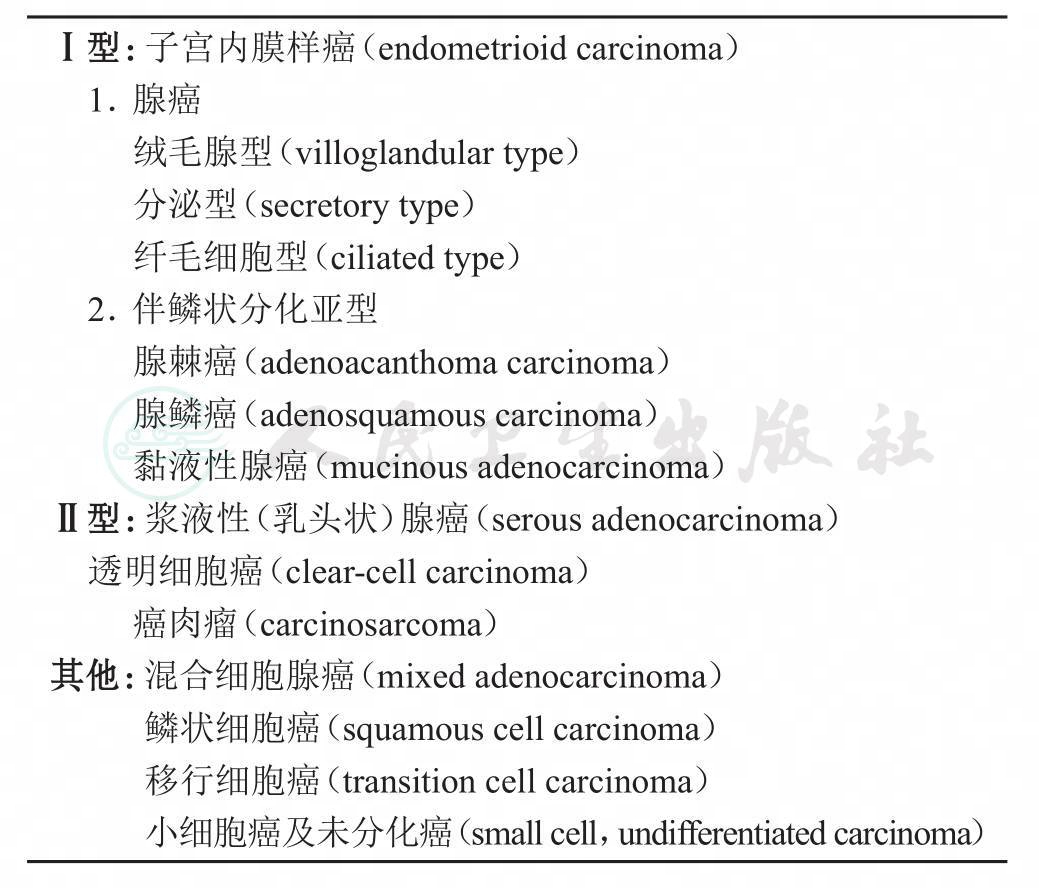
2010年NCCN病理分类中,将癌肉瘤(carcinosarcoma)列入子宫内膜癌特殊类型,病理学家认为癌肉瘤属化生癌(metaplastic carcinoma),其恶性程度高,早期易发生淋巴、血行、腹腔播散,应按高级别的内膜癌治疗。
五、术前评估及手术方式的选择
1.术前评估
术前根据患者年龄、有无内科合并症、肥胖程度、病理、MRI等检查结果对患者进行评估,初步判断肿瘤累及范围,指导初次治疗方案的选择。术前评估时年龄大、手术风险高、内科合并症多的患者应送至条件好,有较强医疗技术医院治疗。
2.术式选择及建议
子宫内膜癌标准的手术方式是筋膜外全子宫切除术加双附件切除术。尽管分期标准要求进行盆腔和腹主动脉旁淋巴结切除,但是否进行切除仍存在争议。对于有深肌层浸润或者是影像学检查怀疑淋巴结转移的患者,应当行腹膜后淋巴结切除。可疑腹主动脉旁淋巴结或者髂总淋巴结转移,明显的附件受累,明显的盆腔淋巴结转移,全肌层浸润的高级别肿瘤,透明细胞癌,浆液性乳头状癌或癌肉瘤应行腹主动脉旁淋巴结取样或切除。
3.治疗选择
(1) 子宫内膜非典型增生:
治疗中应重视患者年龄和内膜非典型增生的程度(轻、中、重度);年轻、未生育或要求保留子宫者,可采用激素治疗,密切随访;由于内膜复杂性增生伴非典型增生中约40%伴子宫内膜癌,对40岁以上无生育要求者,若为中或重度非典型增生,建议行筋膜外子宫切除术。
轻度非典型增生可选用醋酸甲羟孕酮(10~30mg/d),于经前10天周期性用药。中度以上非典型增生则应用大剂量孕激素持续治疗(甲羟孕酮250~500mg/d或甲地孕酮80~160mg/d,3个月;或18-甲基炔诺酮3~4mg/d,3个月),定期诊刮或宫腔镜送组织学检查,根据内膜对治疗的反应,决定是否继续激素治疗或改用手术治疗。要求生育者,待内膜正常后可加促排卵药物治疗,如氯米芬50~100mg每日1次,周期5~9天用药。亦可用己酸孕酮500mg肌注,每周2~3次,3个月后减量再用3个月,或用丹那唑、GnRH-α或局部用药(曼月乐节育环)等治疗。因其恶变率较高,治疗后2~13年内可有复发,故应密切随访。个别病例亦可试用芳香化酶抑制剂和选择性雌激素受体拮抗剂治疗。
(2) 子宫内膜癌:
子宫内膜癌的治疗以手术治疗为主,辅以放疗、化疗和激素等综合治疗。应结合患者的年龄、全身状况和有无内科并发症及临床判断肿瘤累及的范围综合评估,选择和制订治疗方案。
1) 肿瘤局限于子宫体(Ⅰ期):应施行手术分期(surgical staging),若因内科情况无法手术者应选用放疗。
开腹后应冲洗盆腹腔,冲洗液作细胞学检查。术式为筋膜外子宫切除术及双附件切除术、盆腔及腹主动脉旁淋巴结切除。盆腔及腹主动脉旁淋巴结切除为分期手术中重要组成部分,目前多行系统切除(完全切除术,complete lymphadenectomy);应重视腹主动脉旁淋巴结切除,因此区域淋巴结若有转移属ⅢC2期,预后差于盆腔淋巴结阳性者。手术步骤见图1。
有关手术范围及需要注意的几个问题:①筋膜外子宫全切除术应完整切除子宫及宫颈,不强调宫旁及阴道切除范围。②术中剖视子宫,检查癌肿大小、部位、肌层受浸深度,根据肿瘤分化程度,肌层浸润深度(冷冻病理检查确定)决定是否行盆腔及腹主动脉旁淋巴结切除。③很多子宫内膜癌患者伴肥胖或者是老年患者,有其他内科合并症,对手术耐受性差,对这样的患者需要临床综合判断是否需要进行淋巴结切除。④子宫内膜样腺癌G1无肌层或浅肌层浸润,因淋巴转移< 1%,可不行淋巴结切除或取样。⑤以下情况者应作腹主动脉旁淋巴结切除:可疑腹主动脉旁淋巴结或者髂总淋巴结转移,明显的附件受累,明显的盆腔淋巴结转移,全肌层浸润的高级别肿瘤,透明细胞癌,浆液性乳头状癌或者癌肉瘤。
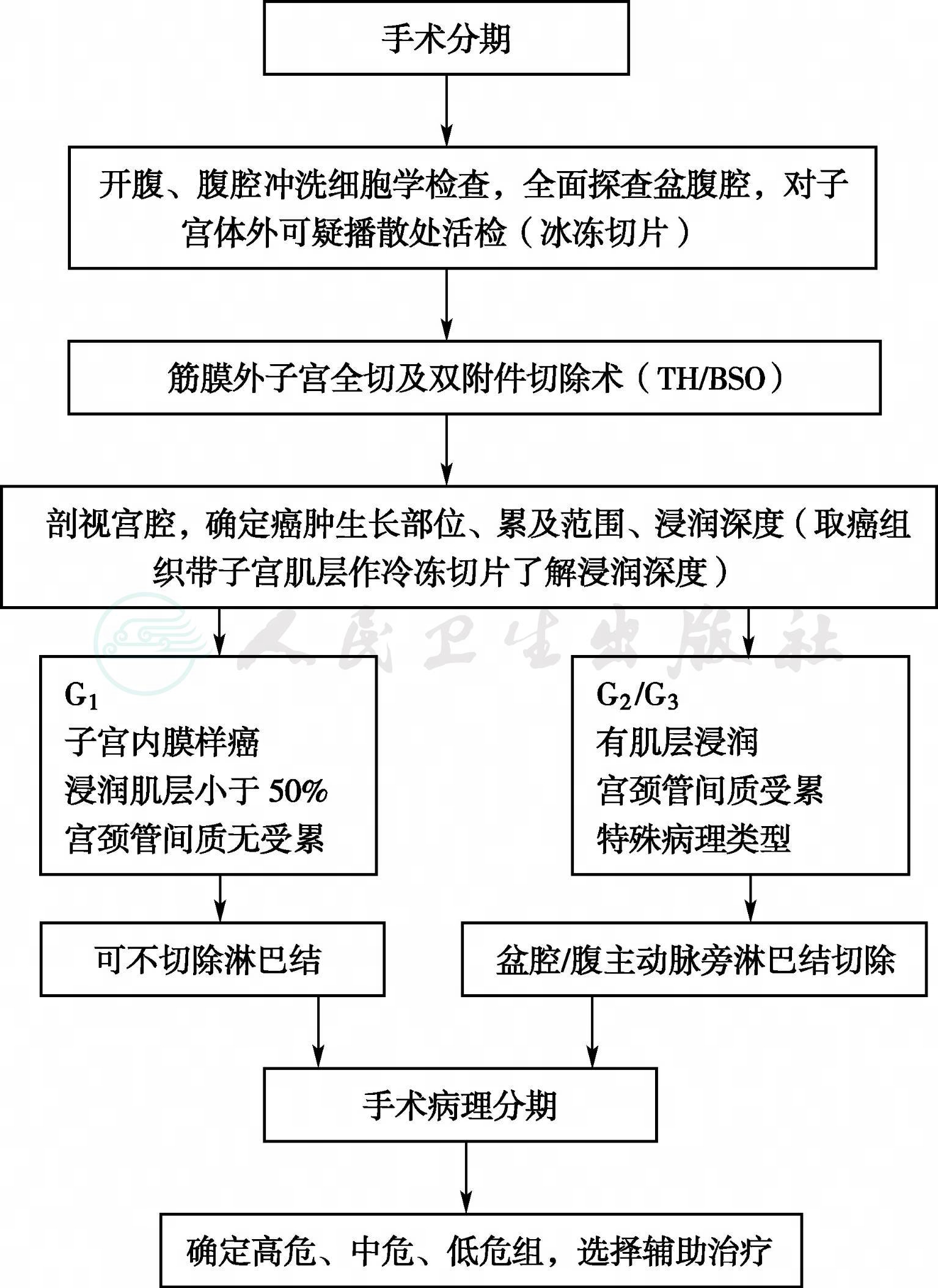
图1 子宫内膜癌手术分期步骤
术后辅助治疗的选择:术后根据预后高危因素对患者进行分类,分为低、中、高危组,以指导术后的放疗、化疗等辅助治疗。影响预后的高危因素包括:年龄大于60岁,深肌层浸润,低分化,浆液性或者透明细胞癌,脉管浸润。①低危组:高中分化,肌层浸润小于50%的子宫内膜癌,或者是仅有一个高危因素的子宫内膜癌患者。低危组多不需作任何辅助治疗。②中危组:有2个及2个以上高危因素的子宫内膜癌患者。中危组单纯进行阴道后装放疗优于盆腔外照射,因其不仅能很好地控制阴道局部的复发,而且对患者的生活质量没有明显影响。阴道后装放疗已经代替盆腔外照射成为中危组患者标准的辅助治疗模式。③高危组:有3个及3个以上高危因素,Ⅱ期或者Ⅲ期肿瘤的患者。对高危组患者给予盆腔外照射和(或)化疗的治疗效果目前正在研究,盆腔外照射加化疗是可选择的治疗手段。④术后有宫颈受累、淋巴转移、宫外病变及特殊类型的子宫内膜癌患者可根据转移部位及病灶状况给以放疗及化疗为宜。若仅为宫颈受累(无淋巴及其他部位转移)也可仅给腔内照射。
2) 肿瘤累及宫颈(Ⅱ期):根据患者具体情况选用以下一种术式:①广泛性子宫切除,双附件切除,盆腔、腹主动脉旁淋巴结切除。②若手术切除困难可做术前放疗后再行筋膜外子宫全切、双附件切除、盆腔及腹主动脉旁淋巴结切除,有缩小手术范围,减少术中、术后风险的优点,分期应按1971年临床分期。③先行改良广泛子宫切除(modified radical hysterectomy)、双附件切除、盆腔及腹主动脉旁淋巴结切除,再根据手术分期病理结果,选用必要术后辅助治疗。因子宫内膜癌术前疑为Ⅱ期者与术后病理分期符合率仅为30%~40%(Creasm等,2003)。④若因高龄、内科并发症无法行手术治疗,可像宫颈癌一样行全盆腔放疗和腔内后装放疗。
3) 肿瘤超出子宫(Ⅲ期):①术中应全面探查,多处活检,若为腹腔内病变,如附件包块,应先行探查及缩瘤术,术中病理冷冻切片检查以明确诊断,尽可能切除肿瘤,为术后放疗及化疗创造条件。②若为宫旁、阴道及阴道旁转移,可先行放疗,完成放疗后,若病灶可能切除,应行探查并切除病灶。③若为腹膜后淋巴转移,可行淋巴结切除或局部放疗或化疗。
有子宫外病变者为复发高危人群,术后应行辅助放疗及化疗。如:ⅢC1期盆腔淋巴结转移(腹主动脉旁无转移者),术后行盆腔外照射,其无疾病生存率,可达57%~72%(Nelson等,1997)(Level Ⅱ)。腹主动脉旁淋巴结转移(ⅢC2)完全切除后,应行影像学全面检查(如胸部CT或positron emission tomography scans,PET-CT)明确有无腹腔外隐匿性病变。若无腹腔外转移灶,行腹主动脉旁照射可提高生存率(中位生存期27~34个月),对镜下转移者疗效更佳(Level Ⅱ)。对术后腹腔内病变在满意的缩瘤术后再行全身化疗,5年生存率优于全腹放疗(WAI)(58% vs 42%)。卡铂、紫杉醇联合用药有疗效好、毒性轻的优点。
4) 肿瘤累及腹腔或有远处转移(Ⅳ期):根据患者有无腹腔外病灶选择不同的治疗方案。
(1) 无腹腔外转移的患者建议行肿瘤细胞减灭术,腹腔内转移的Ⅳ期患者能够从没有癌灶残留的肿瘤细胞减灭术中获益。新辅助化疗对于有腹水的患者是一种可选择的治疗方案,但是术后的死亡率是相似的。术后应给予以铂类为基础的化疗。
(2) 对于有腹腔外转移证据的患者通常要给予以铂类为基础的全身化疗,如果为高分化癌和(或)孕激素受体阳性时可给予激素治疗。晚期病例和复发病例一样可选择联合化疗。盆腔放疗主要用于控制局部肿瘤生长和(或)治疗局部肿瘤包块引起的阴道出血或者疼痛,或者由淋巴结受累引起的下肢水肿。短程放疗(1~5组放疗)可有效减轻脑和骨转移引起的疼痛。
4.放疗
分为单纯放疗、术前放疗及术后放疗。单纯放疗主要用于晚期或有严重内科疾患、高龄和无法手术的其他期患者,可按临床分期进行放疗。术前放疗,主要是为控制、缩小癌灶创造手术机会或缩小手术范围。术后放疗是对手术-病理分期后具有复发高危因素患者重要的辅助治疗,或作为手术范围不足的补充治疗。
1) 单纯放疗:①腔内照射(后装)高剂量率:A点及F点总剂量为45~50Gy,每周1次,分6~7次完成。②体外照射:40~45Gy,6周内完成。
2) 术前放疗:①全剂量照射:腔内加体外照射同单纯放疗,于完成放疗后8~10周行单纯全子宫及附件切除术。②腔内照射:腔内照射45~50Gy,完成照射后8~10周手术;部分性腔内术前放疗:A点及F点总剂量不低于20Gy,分2~3次治疗完成,每周1次,放疗后10~14天手术(切除子宫及双侧附件)。③术前体外照射:用于不利于腔内照射者(如子宫> 10~12周,或有宫腔以外播散者)。盆腔外照射剂量为20Gy,2~3周完成;或A点及F点20Gy,每周1次,分3次完成。
3) 术后放疗:①术后全盆腔照射:总剂量40~50Gy,4~6周完成。②腹主动脉旁扩大照射区:总剂量30~40Gy,3~4周完成。照射前行肾扫描,放疗时应加以屏障(若术前已行体外放疗,应减少术后照射剂量)。若采用适形及调强技术,保护好正常组织,对主动脉淋巴结转移照射量可达50~60Gy。③术后腔内放疗:手术范围不够;有癌瘤残存,或疑有癌瘤残存者,或有局部复发高危因素者可于手术后2周行腔内放疗,总剂量10~20Gy,2~3周完成。
大量临床研究已证实,对Ⅰ期患者来说,术后辅助放疗仅有ⅠC G3患者可获益,并多采用腔内照射。对ⅠB G2、G3,ⅠC G2、G3期若无淋巴转移及宫外病变,术后多不主张采用辅助放疗。
5.激素治疗
仅用于晚期或复发的子宫内膜样癌患者。以高效药物、大剂量、长疗程为宜,4~6周可显效。对癌瘤分化良好,孕激素受体(PR)阳性者疗效好,对远处复发者疗效优于盆腔复发。治疗时间尚无统一看法,但至少应用药1~2年以上。总有效率25%~30%,可延长患者的疾病无进展生存期,对生存率无影响。目前Ⅰ期患者术后多不采用孕激素作辅助治疗。
1) 孕激素治疗:①甲羟孕酮(MPA):口服,250~500mg/d。②甲地孕酮(MA):口服,每日80~160mg。③氯地孕酮:口服,每日20~40mg。孕激素治疗总有效率25%,病变无进展期间(PFI)为4个月左右,但总生存率不变(10~12个月)。研究证明,MPA剂量> 200mg/d,不增加有效率,有水钠潴留、体重增加及增加栓塞危险。
2) 抗雌激素药物治疗:他莫昔芬(三苯氧胺)为雌激素受体拮抗剂,有抗雌激素作用,可使PR水平上升,有利于孕激素治疗。口服每日20mg,数周后可增加剂量,或先用2~3周后再用孕激素,可提高孕激素治疗效果。在孕激素治疗无效患者中,约20%他莫昔芬治疗有效。
3) 近年来亦有采用芳香化酶抑制剂(aromatase inhibitors)或选择性雌激素受体调节剂(SERM)行激素治疗报道,如:雷洛昔芬(raloxifen)有效率为28%。
6.化疗
1) 多用于特殊病理类型:癌瘤分化差,孕激素受体(PR)、雌激素受体(ER)阴性患者;或为晚期复发癌的辅助治疗。常用药物有DDP、ADM、Taxol(紫杉醇)、CDDP(卡铂)、5-FU 和CTX等。单一药物的有效率为25%~37%。目前单一用药已被联合用药取代。
2) 常用的联合化疗方案:经临床观察,疗效可达40%~60%。疗程根据患者病情、全身状况和术后是否放疗等确定,一般可应用3~6个疗程。
对化疗的建议:
(1) 对于放疗后的高危患者给予辅助化疗能提高肿瘤无进展生存时间,但是对于总体生存率的好处还没有得到证实。
(2) 对于早期的高风险患者的化疗只应该在临床试验内进行。
(3) 对于腹腔残留病灶小于2cm的患者和Ⅲ期内膜癌患者,化疗优于全腹照射。
(4) 子宫内膜癌患者大多年老虚弱,在给予辅助治疗时要考虑到这一点。
建议方案:AP:多柔比星(ADM)50mg/m2、顺铂(DDP)50mg/m2静脉用药,间隔3~4周。
TP:紫杉醇(Taxol)135mg/m2、卡铂(CBP)AUC(曲线下面积)4~5静脉用药,间隔3~4周。
CBP + Taxol有效率40%,目前亦有用两者低剂量周疗(TAP因毒性高且临床疗效与AP相近故少用)。
六、子宫浆液性腺癌
子宫浆液性乳头状腺癌(UPSC)现多称子宫浆液性腺癌(USC),较少见,为子宫内膜癌的特殊亚型(Ⅱ型)。其病理形态上与卵巢浆液性乳头状癌相同,以含砂粒体的浆液性癌,有或无乳头状结构为其诊断特征。恶性程度高,分化低,早期可发生脉管浸润、深肌层受累、盆腹腔淋巴结转移。预后差,Ⅰ期复发转移率达31%~50%;早期5年存活率40%~50%,晚期则低于15%。其癌前病变为子宫内膜腺体异型增生(EmGD)。子宫内膜浆液性上皮内癌(EIC)为子宫浆液性癌早期病变(或一种可转移特殊形式),33%~67%伴宫外转移,14%~25%伴宫颈转移,临床处理同浆液性癌。
诊治中应注意以下几点:
1.严格进行手术-病理分期
诊刮病理检查一旦诊断为子宫浆液性癌,无论临床诊断期别早晚,均应进行全面手术分期(包括盆腹腔冲洗液细胞学检查、盆腹腔腹膜多处活检、腹膜后淋巴结切除等)。
2.手术治疗
同卵巢癌细胞减灭缩瘤术,包括大网膜切除等。
3.重视术后辅助放化疗
因该类肿瘤多数分化不良,盆腹腔早期播散。术后化疗中以铂类为主,常选用与卵巢浆液性乳头状瘤相同方案,如:TP、CP或CAP等。放疗则多选用阴道腔内照射控制局部复发。
4.与卵巢浆液性乳头状癌鉴别
要点:①卵巢与子宫均受累,但主要病灶在子宫;②卵巢内病变仅为卵巢门淋巴管瘤栓;③若盆腹腔内有病变,卵巢皮质仅有镜下受累,则可诊断为本病。
七、子宫癌肉瘤
病理学家认为子宫癌肉瘤(carcinosarcoma)属化生癌(metaplastic carcinoma),应属上皮癌,故WHO 2003年提出归于子宫内膜癌的范畴,NCCN将其划入特殊类型的子宫内膜癌。可为同源性或异源性,以前归属恶性中胚叶混合性瘤(MMMT),其恶性程度高,早期腹腔、淋巴、血液循环转移。手术治疗上应按高级别特殊类型内膜癌处理。对化疗敏感,异环磷酰胺(ifosfamide)为其单一最有效药物。联合治疗方案以异环磷酰胺联合顺铂方案最有效,已广泛应用。术后盆腔照射可有效控制复发提高生存率。
八、特殊情况处理
1.子宫切除术后诊断为子宫内膜癌
应根据术后对与子宫外播散相关的高危因素,如组织分级、肌层浸润深度、病理类型等制订进一步治疗方案。G1或G2、浅肌层浸润无脉管受累,不需要进一步治疗。G3、深肌层浸润、脉管受累、特殊病理类型等,均应再次手术完成分期及切除附件,亦可根据情况采用盆腔外照射代替手术。
2.年轻妇女内膜癌的诊治问题
子宫内膜癌在35岁以下妇女少见,诊断中注意与内膜重度不典型增生鉴别、有无与雌激素相关疾病存在。孕激素可治愈内膜不典型增生且保留生育能力。若确诊为癌,已有生育者可选用全子宫及附件切除术。若癌的病理诊断不能肯定,应由患者自己决定是否进行保守治疗,在患者充分咨询,了解风险,签署必要的医疗文件后,采用大剂量孕激素治疗,严密随访治疗3个月后行全面诊刮评估疗效。
3.保留生育功能问题
对年轻早期患者保留生育功能及生理功能治疗是极富挑战性的治疗。
(1) 风险:
①子宫是孕卵种植、胚胎和胎儿发育场所,是内膜癌发生、发展器官。在治疗过程中,内膜癌变可能进展、恶化甚至能影响患者生命安全。②内膜癌患者可同时伴有卵巢癌的风险:转移至卵巢,属病变本身累及卵巢(Ⅲ期);合并原发性卵巢癌。③内膜癌病理类型诊断困难,重复性差〔子宫内膜不典型增生(或瘤样病变)与高分化腺癌鉴别困难〕,影响病例选择。④即使保留生育功能治疗成功后,生育问题及促排卵药物与内膜癌的关系尚不明确。
(2) 可行性:
①年轻(≤40岁)内膜癌:多为早期,多数预后良好;②孕激素对高分化内膜癌疗效好(成功病例报道较多);③内膜癌癌变进展相对缓慢,有长期监测观察的可能性,若无缓解或有复发,及时治疗预后影响小。若治疗成功,妊娠对子宫内膜有保护作用。
(3) 适应证:
病例选择尚无统一标准,但多按以下标准进行:年龄< 40岁;分期ⅠA G1:子宫内膜样癌。检查:癌组织PR(+)、血清CA125 < 35kU/L及肝、肾功能正常;渴望保留生育功能要求,同意承担治疗风险。术前评估:全面评估,严格选择,充分准备。
总之,对年轻、早期子宫内膜癌患者,保留生育功能治疗是特殊的保守治疗,风险大,处于探索阶段,治疗方案尚不成熟,但也有成功案例的研究报道。尚待妇科肿瘤和生殖内分泌的同道共同努力,进行设计完善、样本量大些的临床研究。
九、随访
临床Ⅰ、Ⅱ期复发率为15%,多数为有症状复发(58%),复发时间多在治疗后3年内。完成治疗后应定期随访,及时确定有无复发。对于未放疗的患者,规律随访可以尽早发现阴道复发,可以再行放疗得到补救治疗。
随访时间:术后2年内,每3~4个月1次;术后3~5年,每6个月至1年1次。
随访检查内容:由于只有在有症状的复发患者中才会发现阴道细胞学检查阳性,因此阴道细胞学检查可以不作为常规检查内容,视诊检查就足够了。包括:①阴道视诊、盆腔检查(三合诊);②期别晚者,可进行血清CA125检查,根据不同情况,可选用CT、MRI等检查;③有家族史者宜行相关基因检测。应对患者进行口头或书面交代相关复发症状,如:阴道流血、食欲下降、体重减轻、疼痛(盆腔、背、腰部)、咳嗽、气促,腹水或下肢水肿等,一旦出现异常应及时就诊。
附:复发癌或转移癌治疗
多在治疗后3年内复发:①局部复发可选择手术、放射治疗,或手术与放射联合治疗。术后1~2年单个盆腔复发灶,若能切除多可治愈。若患者为已接受放射治疗后复发,治疗则与宫颈癌复发相同;对中心性复发符合条件者选用盆腔脏器清扫术。②若非局部复发,可选用孕激素治疗,MPA 250mg每日一次或MA 80mg每日3次,可长期服用,一般治疗3个月后方显效。化疗药物DDP、Taxol及ADM等可用于手术及放疗无法治愈的复发患者。
1.手术治疗
手术后局部或区域复发可进行手术探查,切除病灶;或行RT放射治疗。若为盆腔RT后复发(原照射部位复发),处理上仍存争议。
(1) 复发性内膜癌行广泛手术如盆腔脏器切除术等的存活率仅为20%,故可采用局部阴道切除,加或不加术中放射治疗(IORT)。对以前未接受过RT复发癌部位,或以前仅为近距离放疗复发,以手术探查盆、腹腔,再切除复发灶,加或不加用IORT;RT加近距离照射对这些患者亦为可选用治疗之一。
对于局限于阴道的复发或有盆腔淋巴结复发,推荐瘤区RT,加或不加腔内近距离照射或化疗。阴道复发用RT治疗其生存率为40%~50%,若有阴道外扩散或盆腔淋巴结受累,其预后更差(Poulsen等,1988)。
腹主动脉旁或髂总淋巴结复发可作瘤区RT,加用或不加用阴道照射、化疗。
对上腹部及盆腔转移或复发的镜下残留癌灶,行化疗加用或不加用瘤区直接RT。对残留单个大癌灶可切除者应行手术切除,术后加或不加RT;对不能切除的单个大癌灶按已扩散病灶处理。处理全身的病变可行保守性治疗。
(2) 对以前已行过外照射的复发部位推荐治疗如下:手术探查盆腔,切除复发灶,加或不加IORT,激素治疗,化疗。
2.复发和晚期内膜癌的激素治疗和化疗
用于子宫内膜样癌激素治疗的药物主要是孕激素类药物(progestational agents)、他莫昔芬(tamoxifen)、芳香化酶抑制剂(aromatase inhibitors)也可应用。目前尚无特别有效的孕激素药物和方案。高分化转移癌瘤激素治疗反应好,可有一定的缓解期,特别是对盆腔外的局部的转移和复发病灶,如对肺转移疗效较好。对无症状或低级别(高分化)弥散的转移灶,激素治疗(应用激素类药物)有效,特别是雌、孕激素受体阳性患者。对孕激素标准治疗无效的病例,约20%对他莫昔芬治疗有效。有研究报道选择性雌激素受体调节剂在转移性内膜癌治疗有效率为28%(Burke等,2003)。在激素治疗中若病变进展,可应用细胞毒性类药物进行化疗。对激素和化疗无效者,全身转移患者可行保守性治疗。
3.复发和转移癌的化疗(chemotherapy for metastatic recurrent disease)
内膜癌化疗方面研究很多,单药物多用:顺铂、卡铂、紫杉醇、多柔比星等,治疗有效率为21%~36%。
多药联合治疗有效率31%~81%,但存活期相对较短,中位生存期近1年。在对卵巢癌治疗研究应用基础上卡铂和紫杉醇已逐渐应用于内膜癌的复发和晚期癌的治疗。有效率为40%,总生存期为13个月。低剂量紫杉醇和卡铂周疗仍有一定疗效(Secord等,2007)。化疗和(或)保守性放疗是对有症状G2、G3、有大转移癌灶复发和晚期癌可缓解症状的治疗方法(若2个疗程化疗均无效则可纳入临床研究)。
[1] Amant F,Mirza MR,Creutzberg CL. Cancer of the corpus uteri. Int J Gynaecol Obstet,2012,119(Suppl 2):S110-117
[2] National Comprehensive Cancer Networks. NCCN practice guidelines in Oncology:Uterine Neoplasms.V.1.2013. Available at:http://www.nccn.org/professionals/physician_gls/ pdf/uterine.pdf
[3] May K,Bryant A,Dickinson HO. Lymphadenectomy for the management of endometrial cancer. Cochrane Database Syst Rev,2010,20(1):CD007585
[4] Nout RA,Smit VT,Putter H,et al. Vaginal brachytherapy versus pelvic external beam radiotherapy for patients with endometrial carcinoma of high-intermediate risk(PORTEC-2):an open-label,non-inferiority,randomised trial. Lancet,2010,375(9717):816-823
[5] Kong A,Johnson N,Kitchener HC. Adjuvant radiotherapy for stage I endometrial cancer:an updated Cochrane systematic review and meta-analysis. J Natl Cancer Inst,2012,104(21):1625-1634
[6] Barlin JN,Puri I,Bristow RE. Cytoreductive surgery for advanced or recurrent endometrial cancer:a meta-analysis. Gynecol Oncol,2010,118(1):14-18
[7] ASTEC study group,Kitchener H,Swart AM,et al. Efcacy of systematic pelvic lymphadenectomy in endometrial cancer (MRC ASTEC trial):a randomised study. Lancet,2009,373 (9658):125-136