 去看看
去看看


妇科恶性肿瘤是严重威胁女性健康的重大疾病,以子宫颈癌、子宫内膜癌和卵巢癌最常见,手术治疗、放射治疗(放疗)和化学药物治疗(化疗)是其主要治疗方法,其中化疗因其具有全身治疗的特点而在综合治疗中占有重要地位。聚乙二醇化脂质体多柔比星(pegylated liposomal doxorubicin, PLD)是妇科恶性肿瘤常用化疗药物,尤其对卵巢癌具有显著的疗效。中华医学会妇科肿瘤学分会专家组在循证医学证据基础上,经过多次讨论,形成《妇科恶性肿瘤聚乙二醇化脂质体多柔比星临床应用专家共识》(以下简称本共识)。
本共识采用下列专家共识推荐级别(表1)。

1 聚乙二醇化脂质体多柔比星的药学特性
蒽环类药物是由微生物产生的具有抗肿瘤活性的化学物质,属于抗肿瘤抗生素,包括柔红霉素、多柔比星、表柔比星、吡柔比星、米托蒽醌和卡柔比星等[1]。此类药物是细胞周期非特异性药物,主要作用机制包括:嵌入DNA碱基对之间,干扰 DNA转录和mRNA合成;抑制拓扑异构酶Ⅱ,导致染色体结构异常;螯合铁离子后产生氧自由基,破坏细胞膜功能,这与心脏毒性相关[2]。
20世纪60年代,从链霉菌中分离出多柔比星,随后用于临床研究[3]。多柔比星于1974年在美国获批上市,后被用于治疗急性白血病、乳腺癌、淋巴瘤、卵巢癌等恶性肿瘤[4,5],但因其骨髓抑制和心脏毒性等不良反应较为严重,临床应用受到限制。脂质体制剂具有靶向性、缓释作用、良好的组织相容性等优点,可有效减轻药物不良反应。20世纪80 年代末,脂质体开始用作多柔比星的有效载体,经聚乙二醇化结构修饰后,脂质体的稳定性增加,半衰期明显延长。
1995年,PLD(Doxil®,多喜)在美国上市,并于1999年被美国食品药品监督管理局(Food and Drug Administration,FDA)加速批准用于治疗铂耐药复发卵巢癌;2005年,美国FDA正式批准PLD用于治疗复发性卵巢癌。目前,PLD临床应用日趋广泛,多项研究表明PLD单独或联合应用可有效治疗多种妇科恶性肿瘤。
PLD是将多柔比星包封于聚乙二醇化脂质体中的新型蒽环类药物,在传统蒽环类药物抗肿瘤活性的基础上,因药物剂型的改变,使其药代动力学与多柔比星截然不同。脂质体经聚乙二醇化结构修饰后具有亲水性,保护脂质体不被血浆中的血浆蛋白调理素接近,可逃逸网状内皮系统的吞噬清除,增加药物在体内的稳定性,延长半衰期[6]。
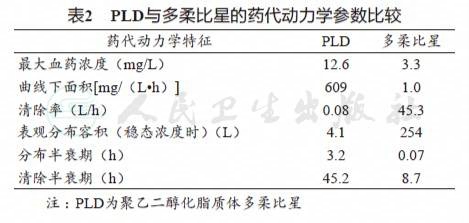
PLD的药代动力学研究显示,在体循环系统中,> 95%的PLD以脂质体形式存在,与游离的多柔比星相比,PLD血浆药物浓度升高,清除率下降,延长了多柔比星在循环系统中的滞留时间。在相同剂量(25 mg/m2)条件下,PLD的最大血药浓度较多柔比星高近4倍,药时曲线下面积(area under the curve,AUC)高609倍,清除率下降至1/566,表观分布容积减少至1/62。此外,PLD在循环系统中的滞留时间较多柔比星明显延长,其分布半衰期延长45倍,清除半衰期延长5倍(表2)[7,8]。国产 PLD(多美素®)与国外PLD的人体药代动力学比较试验提示,在50 mg/m2剂量条件下,二者具有相似的药代动力学特征,其半衰期为41.2 ~ 99.3 h[8]。
PLD在肿瘤组织中分布较多,这是由于肿瘤组织的血管内皮间隙(400 ~ 500 nm)远大于正常组织(2 ~ 8 nm)[9] ;而PLD的粒径约为90 nm,可通过大间隙肿瘤新生血管内皮细胞到达肿瘤组织,而肿瘤组织的淋巴循环系统受损,使药物滞留其中,形成被动靶向富集,这种作用被称为高通透性和滞留效应,即EPR效应[10],此效应使药物在实体肿瘤组织中的浓度得以升高。
一项荷瘤小鼠模型研究证实:小鼠尾静脉注射 PLD 8 mg/kg后,比较不同时间点不同组织的血药浓度,其中,PLD给药24 h后在不同组织中蓄积的浓度依次为:肿瘤(最高,37.8 μg/g)>肺、肝、脾、肾、小肠(相似)>心脏(5.07 μg/g)>骨髓(最低,0.74 μg/g)[8]。此外,因PLD具有亲水性,故其在皮肤中的分布较多,易随汗液运输至汗腺密集部位。临床前实验证实动物爪部位PLD水平较皮肤更高,这是临床上发生手足综合征(hand-foot syndrome,HFS)的原因[11,12]。多柔比星引发的心力衰竭(心衰)风险随着剂量的累积而升高,剂量为400、550、700 mg/m2,心衰发生风险分别为 3% ~ 5%、7% ~ 26%、18% ~ 48%[13,14]。因多柔比星的心脏毒性,临床上将其最大累积剂量限制为 360 ~ 550 mg/m2[14,15],而目前尚无确切数据显示 PLD的最大累积剂量。有研究指出,PLD累积剂量达到900 mg/m2后,心脏毒性风险升高[15]。一项有关复发性卵巢癌患者采用PLD +托泊替康或PLD单药维持治疗的研究显示,PLD的中位累积剂量为1680 mg/m2,最大剂量高达2460 mg/m2,患者未出现明显的心脏毒性[16]。但对此结论尚需更多临床研究数据证实。
PLD的代谢途径和药物间相互作用尚不明确,一般多参照既往多柔比星相关研究数据。
2 临床应用
2.1 卵巢恶性肿瘤
卵巢恶性肿瘤以上皮性卵巢癌最常见,手术和化疗是其最主要的治疗方法。化疗分为初始化疗和挽救化疗。多项研究表明PLD是卵巢癌化疗的有效药物。
2.1.1 初始化疗
初始化疗包括手术前新辅助化疗和手术后一线化疗。卡铂+紫杉醇(CP)方案是卵巢癌初始化疗的标准方案。有研究表明,在初始化疗方案中,PLD可以作为紫杉类药物的替代药物。
MITO-2研究是一项Ⅲ期临床研究,旨在评价卡铂+PLD(CD)方案是否优于CP方案。结果显示: CD组和CP组患者中位无进展生存(progress free survival,PFS)时间(19.0个月∶16.8个月;HR = 0.95, 95%CI:0.81 ~ 1.13,P = 0.58)、中位总生存(overall survival,OS)时间(61.6个月∶53.2个月;HR=0.89, 95%CI :0.72 ~ 1.12,P = 0.32)比较差异均无统计学意义。与CP组相比,CD组患者反应率与之相似但不良反应不同(神经毒性和脱发发生率均较低,但血液系统不良反应发生率较高)[17]。该研究提示, CD方案的疗效与CP标准化疗方案并无差异,可以作为标准一线化疗方案的替代方案。
依据上述证据,推荐CD方案用于卵巢癌的初始化疗(2A类),尤其适用于对紫杉类药物过敏、周围神经病变和顾虑脱发的患者。
2.1.2 挽救化疗
卵巢癌复发后化疗又称挽救化疗。卵巢癌复发分为铂敏感复发和铂耐药复发,前者指完全缓解后6个月以上复发,后者指完全缓解后不足6个月复发。初始治疗后未控制,呈持续性甚至进展性疾病者,也属于铂耐药范畴。
2.1.2.1 铂敏感复发卵巢癌
铂敏感复发卵巢癌患者一般继续选用以铂类药物为基础的联合化疗方案。一些研究显示PLD是铂敏感复发卵巢癌的有效治疗药物[18-22]。
CALYPSO研究是一项Ⅲ期非劣效临床试验,比较了CD方案与CP方案在铂敏感复发卵巢癌患者中的疗效与安全性。结果显示:与CP组相比,CD 组患者中位PFS时间延长1.9个月(11.3个月∶9.4 个月),复发或死亡风险降低18%(HR = 0.82, 95%CI :0.72 ~ 0.94,P = 0.005)[18] ;但两组患者中位OS时间比较差异无统计学意义(30.7个月∶33.0 个月;HR= 0.99,95%CI:0.85 ~ 1.16,P= 0.94)[19]。 CP组患者严重的非血液系统毒性发生率较高,其中脱发、过敏和感觉神经毒性发生率较高,而CD 组患者HFS、恶心和黏膜炎发生率较高。CD组患者健康相关生活质量优于CP组患者[20]。亚组分析显示,在铂部分敏感复发卵巢癌患者(6 ~ 12个月复发)中,CD组的疗效和安全性更具优势(与CP 组相比,CD组患者复发或死亡风险降低27% ;CP 组患者3 ~ 4级中性粒细胞减少、2级脱发、神经毒性和超敏反应发生率均较高;CD组患者HFS发生率较高,但3 ~ 4级HFS发生率较低)[21]。
AGO-OVAR 2.21/ENGOT-ov 18研究是一项头对头研究,比较了CD方案联合贝伐珠单抗(bevacizumab,BEV)与卡铂+吉西他滨(CG)方案联合BEV在铂敏感复发卵巢癌患者中的应用价值。结果显示:与CG-BEV组相比,CD-BEV组患者中位 PFS时间延长1.7个月(13.3个月∶11.6个月),复发或死亡风险降低19%(HR = 0.81,95%CI:0.68 ~ 0.96,P = 0.012);与CG-BEV组相比,CD-BEV 组患者中位OS时间延长4.1个月(31.9个月∶27.8 个月),死亡风险降低19%(HR = 0.81,95%CI :0.67 ~ 0.98,P = 0.032)。两组患者与既往化疗和BEV治疗的不良反应相似,CG-BEV组患者3级及以上不良反应发生率较高。CD-BEV组患者3级及以上高血压发生率较高,CG-BEV组患者3级及以上血小板减少和中性粒细胞减少发生率均较高[22]。该研究支持CD-BEV作为铂敏感复发卵巢癌的标准治疗方案。
依据上述证据,对于铂敏感复发卵巢癌患者,推荐PLD联合铂类化疗加或不加BEV为首选治疗方案之一(1类)。
2.1.2.2 铂耐药复发卵巢癌
铂耐药复发卵巢癌对含铂化疗方案不敏感,临床上一般推荐非铂化疗,但反应率一般不足30%。
一项比较PLD与托泊替康单药治疗复发卵巢癌的Ⅲ期临床研究显示:PLD组和托泊替康组患者 PFS时间和OS时间比较差异均无统计学意义,两组患者总体应答率(overall response rate,ORR)相似(19.7% ∶ 17.0%,P = 0.390);对铂耐药复发亚组的分析显示,PLD组和托泊替康组患者ORR (12.3% ∶ 6.5%,P= 0.118)、PFS时间(9.1周∶13.6 周,P = 0.733)和OS时间(35.6周∶41.3周,P = 0.455)比较差异均无统计学意义。托泊替康组患者严重的血液学毒性发生率更高,易致剂量调整和相关支持治疗[23]。
MITO-3研究是一项比较PLD与吉西他滨单药治疗复发时间< 12个月的卵巢癌的Ⅲ期临床研究。结果显示:PLD组和吉西他滨组患者ORR (16% ∶ 29%,P = 0.056)、疾病进展时间(time to progression,TTP)(16周∶20周,P = 0.411)比较差异均无统计学意义,PLD组患者OS时间有获益趋势(56周∶51周,P = 0.048);但在铂耐药复发(复发时间< 6个月)亚组,两组患者PFS时间和OS时间比较差异均无统计学意义。吉西他滨组患者3 ~ 4级中性粒细胞减少发生率更高(7% ∶ 22%, P = 0.007),PLD组患者3 ~ 4级HFS发生率更高(6% ∶ 0,P = 0.061);PLD组患者整体生活质量评分显著高于吉西他滨组(P < 0.05)[24]。
AURELIA研究是在铂耐药复发卵巢癌患者中开展的一项Ⅲ期临床试验。结果显示:相对于紫杉醇周疗或托泊替康或PLD单药化疗,联合BEV治疗组患者的中位PFS时间延长3.3个月(3.4个月∶6.7 个月),复发或死亡风险降低52%(HR = 0.48, 95%CI :0.38 ~ 0.60,P < 0.001);但因组间交叉等原因,中位OS时间无显著延长[25]。对化疗方案进行分析,与PLD单药化疗组相比,PLD + BEV组患者的ORR提高5.9%(13.7% ∶ 7.8%),PFS时间延长1.9个月(5.4个月∶3.5个月,HR = 0.57,95%CI : 0.39 ~ 0.83),但两组患者OS时间比较差异无统计学意义[26]。
北京协和医院开展了一项单臂、开放、多中心前瞻性临床研究,对铂类药物初始化疗后12个月内进展的复发和难治性卵巢癌患者应用PLD治疗。该研究的中期数据显示,铂耐药和铂难治卵巢癌患者的ORR可达29.9%,且80.7%铂耐药卵巢癌和32.3% 铂难治卵巢癌患者有机会延长无铂间期[27]。
依据上述证据,本共识推荐PLD联合或不联合BEV作为治疗铂耐药复发卵巢癌的首选方案之一(2A类)。
此外,有研究报道PLD治疗有效者在前2个周期中糖类抗原125(carbohydrate antigen 125,CA125)水平可能出现短暂升高[28-31],对PLD治疗过程中 CA125水平下降不理想或升高的患者,建议在第3~4 个周期进行化疗评估,结合既往诊治经过、临床症状和体征以及影像学资料,综合判断患者是否获益。
PLD治疗卵巢癌的推荐方案见表3。

2.2 子宫体恶性肿瘤
主要包括子宫内膜癌和子宫肉瘤。
2.2.1 子宫内膜癌
手术治疗是子宫内膜癌患者的首选初始治疗方案。除低危患者外,早期中、高危或晚期患者术后应行辅助治疗。辅助治疗虽然以放疗为主,但化疗应用日益广泛,其主要用于晚期转移、复发癌、特殊组织类型和部分早期高危患者。
GOG 129H研究是一项针对既往接受过治疗的复发/持续性子宫内膜癌患者的Ⅱ期临床研究。结果显示:接受PLD治疗患者的ORR为9.5%(95%CI:2.7 ~ 22.6),严重不良反应发生率低[32]。
MITO-END1研究是一项评估未经化疗的晚期/ 复发子宫内膜癌患者的Ⅱ期临床研究。结果显示:接受CD方案治疗的患者ORR为59.5%(95%CI : 43.3 ~ 74.3),不良反应主要体现在血液系统,未显著影响化疗周期和疗程数,脱发和神经毒性发生率较低[33]。
AGO-OVAR/AGO-K-Ut研究是一项评估CD方案用于既往接受过≤二线化疗的妇科恶性肿瘤患者的Ⅱ期临床研究。结果显示:CD方案治疗晚期/复发子宫内膜癌的ORR为44%(95%CI :25.5 ~ 64.7),中位PFS时间为9.5个月(95%CI :6.6 ~ 12.6),中位OS时间为21.4个月(95%CI :11.9 ~)[34]。
依据上述证据,推荐PLD联合(2A类)或不联合(2B类)卡铂用于治疗晚期/持续性/复发性子宫内膜癌。
PLD治疗子宫内膜癌的推荐方案见表4。

2.2.2 子宫肉瘤
子宫肉瘤包括低级别子宫内膜间质肉瘤、高级别子宫内膜间质肉瘤、未分化子宫肉瘤和子宫平滑肌肉瘤等;以手术治疗为主,化疗的意义尚未明确。
GOG 87J研究是一项Ⅱ期临床研究,旨在评估 PLD治疗未经化疗的晚期/转移子宫平滑肌肉瘤的安全性和有效性。结果显示患者的ORR为16.1%,与既往接受多柔比星治疗的子宫平滑肌肉瘤患者的
ORR相比未见明显提高[35]。
AGO-GYN 7研究是一项评价CD方案对新诊断或复发的妇科肉瘤与癌肉瘤疗效的Ⅱ期临床研究,入组平滑肌肉瘤患者14例、子宫内膜间质肉瘤患者 6例。肉瘤亚组(平滑肌肉瘤和子宫内膜间质肉瘤)患者的ORR为28.0%,中位PFS时间和OS时间分别为7.7个月和32.3个月[36]。
依据上述证据,推荐PLD联合或不联合卡铂用于治疗晚期/持续性/复发性子宫平滑肌肉瘤(2B类)。
PLD治疗子宫肉瘤的推荐方案见表5。

2.3 子宫颈癌
手术和放疗是子宫颈癌的主要治疗方法。化疗主要用于晚期转移、复发性子宫颈癌患者。
GOG 127R研究是一项针对复发/持续性子宫颈癌二线化疗的Ⅱ期临床研究,该研究结果显示:接受PLD治疗的患者ORR为11.1%(均为部分缓解),不良反应较轻,未观察到4级不良反应[17]。
另外一项评价CD方案治疗复发性子宫颈癌的Ⅱ期临床研究结果显示:患者的ORR为38%,中位 OS时间为37周;主要不良反应为骨髓抑制,3 ~ 4 级中性粒细胞减少、贫血和血小板减少的发生率分
别为66%、40%和46%[18]。
依据上述证据,推荐PLD联合或不联合卡铂用于治疗晚期/持续性/复发性子宫颈癌(2B类)。
PLD治疗子宫颈癌的推荐方案见表6。

2 不良反应及其管理
3.1 输液反应[39]
是输液过程中发生的一种速型的以寒战、高热为特点的变态反应。多发生于用药的第1个周期,发生率约为10%。少于1%的患者因此停止治疗。常见表现为潮红、气短、面部水肿、头痛、寒战、背痛、胸部和喉部收窄感、血压异常、眩晕、恶心等;极少数表现为痉挛。
3.1.1 处理
停止输液或减慢输液速度通常可缓解输液反应,无需后续处理;但应备有对症处理药物( 抗组胺药、皮质类固醇、肾上腺素和抗惊厥药)及相关急救设备。多数患者症状缓解后可重新用药,且不会再次发生输液反应。对出现输液反应的患者,静脉滴注方法应作如下调整:总剂量的5%应在开始的15 min缓慢滴注,如果患者可以耐受且无反应,接下来的15 min内滴注速度可以加倍;如果患者仍可耐受,可在接下来的1 h内完成剩余药物的滴注,总滴注时间控制为90 min。
3.1.2 预防
为降低输液反应的发生风险,起始给药速率不应超过1 mg/min。如果患者无输液反应,后续的滴注可在60 min内完成。
3.2 骨髓抑制[39]
多为轻至中度的可逆性不良反应,最常见为白细胞减少(33.2%),其他不良反应依次为贫血(32.2%)、中性粒细胞减少(31.6%)、血小板减少(10.7%);少有4级不良反应[不良事件通用术语标准(common terminology criteria for adverse events,CTCAE)]发生(上述4级不良反应发生率依次为1.6%、0.4%、2.9%及0.2%)。
3.2.1 处理
对症支持治疗,PLD所致卵巢癌患者血液学毒性(中性粒细胞或血小板减少)的剂量调整方案见表7。

3.2.2 预防
综合判断,对于有指征的患者可考虑使用重组人粒细胞集落刺激因子、聚乙二醇化重组人粒细胞集落刺激因子或粒细胞-巨噬细胞集落刺激因子预防化疗引起的中性粒细胞减少;使用促血小板生长因子(重组人白细胞介素11、重组人血小板生成素)预防化疗引起的血小板减少。
3.3 手足综合征[39]
HFS也称掌跖感觉丧失性红斑,主要表现为手掌和足底感觉异常、红斑、脱皮或水肿,严重者出现发热、溃疡、局部感染等并发症,通常发生于用药后第2 ~ 3个周期,发生率为46.1%,多数患者反应较轻,1 ~ 2周后可恢复,不影响继续用药,3、4级不良反应发生率分别为19.5%、0.6% ;少于5%的患者因此停止治疗。
3.3.1 处理
HFS为剂量和周期相关性不良反应,通过延长用药间隔1 ~ 2周或减量多可缓解。PLD 所致卵巢癌患者HFS的剂量调整方案见表8。

3.3.2 预防
维生素B6常用于预防和治疗HFS[40] ;其他预防措施包括用药后4 ~ 7 d手足部冷水浸泡、避免接触热源引起局部皮温升高[41];穿戴宽松手套、鞋袜,避免局部皮肤受压和摩擦。研究提示,地塞米松、塞来昔布以及局部应用尿素乳膏等可减少 HFS发生[42]。目前尚缺乏高级别循证医学证据支持PLD所致妇科恶性肿瘤患者HFS的预防措施。
3.4 口腔黏膜炎[39]
临床表现为口腔黏膜轻度不适、红斑、疼痛性红斑、水肿和溃疡,发生率为 38.9%,多数患者反应较轻,1 ~ 2周后可恢复,不影响继续用药,3、4级不良反应发生率分别为8.0%、0.8% ;少于1%的患者因此停止治疗。
3.4.1 处理
口腔黏膜炎为剂量和周期相关性不良反应,PLD所致卵巢癌患者口腔黏膜炎的剂量调整方案见表9。

3.4.2 预防
保持良好的卫生习惯,洁净的口腔环境有助于预防口腔黏膜炎[43]。研究提示,治疗前、治疗期间和治疗后给予局部降温,促使口腔黏膜血管收缩,可在一定程度上改善口腔黏膜炎[44]。药物干预,包括别嘌呤醇、L-谷氨酰胺、氨磷汀、巨噬细胞集落刺激因子、角化细胞生长因子、地塞米松、塞来昔布等可有效缓解口腔黏膜炎[45-49]。但上述药物干预研究多为其他肿瘤的其他药物的相关研究,疗效尚存争议,目前尚缺乏高级别循证医学证据支持PLD 所致妇科恶性肿瘤患者口腔黏膜炎的预防措施。
3.5 心脏毒性[39]
蒽环类药物导致的心脏毒性可分为急性、慢性和迟发性。慢性和迟发性心脏毒性与药物累积剂量呈正相关。PLD的心脏毒性显著低于多柔比星,其发生率为1% ~ 10%,最大累积剂量尚待进一步研究确认。
3.5.1 预防和处理
蒽环类药物治疗期间应进行常规心电图监测,必要时检测左室射血分数或行心内膜心肌活检。当检测结果显示心脏损害与PLD有关时,应认真权衡继续治疗的益处与心脏损伤的利害关系。
心电图监测:发生一过性心电图改变,如T波平坦,ST段压低和良性心律失常等情况时,不必立即中止治疗。当出现QRS波异常这一心脏毒性的重要指征时,应考虑采用检测蒽环类药物心脏毒性最可靠的方法进行检查,如心内膜心肌活检。在定期复查心电图无改变的情况下,充血性心衰可能会突然出现,亦可于停药后数周出现。
与心电图相比,评价心脏功能更具特异性的方法是通过超声心动图或多孔动脉造影术测定左室射血分数。当PLD累积剂量超过450 mg/m2时,必须在每次用药前考虑评估心脏功能。
出现心脏可疑病变时,如左室射血分数明显低于治疗前和/或低于预后相应值(< 45%),均应进行心内膜心肌活检,必须对继续治疗的益处与产生不可逆性心脏损害的危险进行认真评估。
3.5.2 注意事项
对于有心血管疾病病史、心功能不全的患者,给予PLD治疗时应谨慎。对已用过其他蒽环类药物治疗患者,应密切观察。PLD限制剂量的确定亦应考虑既往(或同时)使用的心脏毒性药物,如其他蒽环类/蒽醌类药物、氟尿嘧啶等。
3.6 其他不良反应
恶心、呕吐是最常见的胃肠道不良反应,其他胃肠道不良反应包括厌食、便秘、腹泻等,通过预防或治疗性应用胃肠动力药、5-羟色胺受体拮抗剂、地塞米松等可减轻此类不良反应。疲劳也是常见的不良反应,大多为1 ~ 2级。PLD引起的脱发通常较轻,3级以上脱发较少见。
2 相关注意事项[39]
4.1 PLD用药方法和途径
使用5%葡萄糖注射液稀释后静脉滴注,禁用于肌内或皮下注射。取用PLD 时需戴手套,如果药液与皮肤或黏膜发生接触,应立即用肥皂水清洗。PLD不可与其他药物混合使用。
4.2 药物间相互作用
未对PLD行药物相互作用研究,但对于与多柔比星产生相互作用的药物,在联用时需注意。在卵巢癌相关研究中,与紫杉醇和环磷酰胺联用未见额外不良反应。但艾滋病相关卡波西肉瘤的相关研究提示,使用多柔比星会加重环磷酰胺导致的出血性膀胱炎,增强巯嘌呤的肝细胞毒性。
4.3 特殊人群[39]
4.3.1 肝功能不全患者
未对PLD在肝功能不全患者中行药代动力学试验。多柔比星主要由肝脏代谢,经胆汁排泄,对于肝功能不全患者应减少PLD剂量。建议根据以下胆红素水平数值考虑减量:1.2 ~ 3.0 mg/dl,采用常用量的1/2;>3.0 mg/dl时,采用常用量的1/4。
4.3.2 肾功能不全患者
多柔比星主要由肝脏代谢,经胆汁排泄,故肾功能不全患者使用PLD时一般不需要调整剂量,但需严密监测肾功能。人群药代动力学分析提示,肌酐清除率为30 ~ 156 ml/min 者,PLD的药物代谢未见明显异常;肌酐清除率<30 ml/min者,无相关数据。
4.3.3 老年患者
人群药代动力学分析提示,年龄为21 ~ 75岁的患者使用PLD无明显差异。
4.3.4 妊娠和哺乳期患者
PLD禁用于孕妇,建议育龄女性在使用PLD治疗期间和停药后6个月内避孕。目前尚不明确PLD是否经乳汁分泌,哺乳期女性在接受PLD治疗前应停止哺乳。
3 结语
以铂类为基础的联合化疗是多数妇科恶性肿瘤的首选化疗方案,除联合紫杉类药物外,联合PLD 亦是目前常用的临床选择。PLD可以替代紫杉类药物用于卵巢癌的初始化疗,尤其是在复发性卵巢癌治疗中,其更是首选药物之一。PLD亦是治疗晚期/ 持续性/复发性子宫颈癌和子宫体恶性肿瘤常用的有效药物。PLD是不同于原药多柔比星而具有明显药学优势的新型化疗药物,特别适用于对紫杉类药物过敏、周围神经病变和顾虑脱发的患者。PLD除常见的血液学毒性外,HFS亦较为常见,应引起临床重视。PLD应用需掌握其适应证、禁忌证、疗效和不良反应,在争取患者最大获益的同时,保障其用药安全和生活质量。
执笔人:孔北华 尹如铁 李小平 姜 洁 鹿 欣 李秀琴 张国楠 向 阳 刘继红 沈 铿 谢 幸 马 丁
共识专家组成员(以姓氏笔画为序):
万小平 上海市第一妇婴保健院
马 丁 华中科技大学同济医学院附属同济医院
王丹波 辽宁省肿瘤医院
王世宣 华中科技大学同济医学院附属同济医院
王建六 北京大学人民医院
王新宇 浙江大学医学院附属妇产科医院
尹如铁 四川大学华西第二医院
孔北华 山东大学齐鲁医院
吕卫国 浙江大学医学院附属妇产科医院
曲芃芃 天津市中心妇产科医院
向 阳 中国医学科学院北京协和医学院北京协和医院
刘继红 中山大学肿瘤防治中心
李小平 北京大学人民医院
李秀琴 中国医科大学附属盛京医院
杨兴升 山东大学齐鲁医院
杨佳欣 中国医学科学院北京协和医学院北京协和医院
吴小华 复旦大学附属肿瘤医院
吴令英 中国医学科学院北京协和医学院肿瘤医院
汪 辉 华中科技大学同济医学院附属同济医院
沈 铿 中国医学科学院北京协和医学院北京协和医院
宋 坤 山东大学齐鲁医院
张国楠 四川省肿瘤医院
赵 霞 四川大学华西第二医院
哈春芳 宁夏医科大学总医院
姜 洁 山东大学齐鲁医院
徐丛剑 复旦大学附属妇产科医院
高庆蕾 华中科技大学同济医学院附属同济医院
高雨农 北京大学肿瘤医院
郭瑞霞 郑州大学第一附属医院
崔 恒 北京大学人民医院
康 山 河北医科大学第四医院
鹿 欣 复旦大学附属妇产科医院
梁志清 陆军军医大学第一附属医院
程文俊 江苏省人民医院
谢 幸 浙江大学医学院附属妇产科医院
[1] WEISS R B. The anthracyclines: will we ever find a better doxorubicin?[J]. Semin Oncol, 1992, 19(6):670-686.
[2] YANG F, TEVES S S, KEMP C J, et al. Doxorubicin, DNA torsion, and chromatin dynamics[J]. Biochim Biophys Acta, 2014, 1845(1):84-89.
[3] ARCAMONE F, CASSINELLI G, FANTINI G, et al. Adriamycin, 14-hydroxydaunomycin, a new antitumor antibiotic from S. peucetius var. caesius[J]. Biotechnol Bioeng, 1969, 11(6):1101-1110.
[4] MINOTTI G, MENNA P, SALVATORELLI E, et al. Anthracyclines: molecular advances and pharmacologic developments in antitumor activity and cardiotoxicity[J]. Pharmacol Rev, 2004, 56(2):185-229.
[5] MALPAS J S. Chemotherapy in the management of ovarian carcinoma: a review[J]. J R Soc Med, 1979, 72(5):357-361.
[6] GABIZON A, MARTIN F. Polyethylene glycol-coated (pegylated) liposomal doxorubicin. Rationale for use in solid tumours[J]. Drugs, 1997, 54 Suppl 4:15-21.
[7] GABIZON A, CATANE R, UZIELY B, et al. Prolonged circulation time and enhanced accumulation in malignant exudates of doxorubicin encapsulated in polyethylene-glycol coated liposomes[J]. Cancer Res, 1994, 54(4):987-992.
[8] 多美素®(盐酸多柔比星脂质体注射液)[Z].石家庄:石药集团中奇制药技术(石家庄)有限公司,2018.
[9] HASHIZUME H, BALUK P, MORIKAWA S, et al. Openings between defective endothelial cells explain tumor vessel leakiness[J]. Am J Pathol, 2000, 156(4):1363-1380.
[10] MAEDA H, TSUKIGAWA K, FANG J. A Retrospective 30 Years After Discovery of the Enhanced Permeability and Retention Effect of Solid Tumors: Next-Generation Chemotherapeutics and Photodynamic Therapy--Problems, Solutions, and Prospects[J]. Microcirculation, 2016, 23(3):173-182.
[11] VON MOOS R, THUERLIMANN B J, AAPRO M, et al. Pegylated liposomal doxorubicin-associated hand-foot syndrome: recommendations of an international panel of experts[J]. Eur J Cancer, 2008, 44(6):781-790.
[12] CHARROIS G J, ALLEN T M. Rate of biodistribution of STEALTH liposomes to tumor and skin: influence of liposome diameter and implications for toxicity and therapeutic activity[J]. Biochim Biophys Acta, 2003, 1609(1):102-108.
[13] SWAIN S M, WHALEY F S, EWER M S. Congestive heart failure in patients treated with doxorubicin: a retrospective analysis of three trials[J]. Cancer, 2003, 97(11):2869-2879.
[14] ZAMORANO J L, LANCELLOTTI P, MUÑOZ D R, et al. 2016 ESC Position Paper on cancer treatments and cardiovascular toxicity developed under the auspices of the ESC Committee for Practice Guidelines: The Task Force for cancer treatments and cardiovascular toxicity of the European Society of Cardiology (ESC)[J]. Eur Heart J, 2016, 37(36):2768-2801.
[15] CURIGLIANO G, CARDINALE D, SUTER T, et al. Cardiovascular toxicity induced by chemotherapy, targeted agents and radiotherapy: ESMO Clinical Practice Guidelines[J]. Ann Oncol, 2012, 23 Suppl 7:vii155-166.
[16] ANDREOPOULOU E, GAIOTTI D, KIM E, et al. Pegylated liposomal doxorubicin HCL (PLD; Caelyx/Doxil): experience with long-term maintenance in responding patients with recurrent epithelial ovarian cancer[J]. Ann Oncol, 2007, 18(4):716-721.
[17] PIGNATA S, SCAMBIA G, FERRANDINA G, et al. Carboplatin plus paclitaxel versus carboplatin plus pegylated liposomal doxorubicin as first-line treatment for patients with ovarian cancer: the MITO-2 randomized phase Ⅲ trial[J]. J Clin Oncol, 2011, 29(27):3628-3635.
[18] PUJADE-LAURAINE E, WAGNER U, AAVALL-LUNDQVIST E, et al. Pegylated liposomal Doxorubicin and Carboplatin compared with Paclitaxel and Carboplatin for patients with platinumsensitive ovarian cancer in late relapse[J]. J Clin Oncol, 2010, 28(20):3323-3329.
[19] WAGNER U, MARTH C, LARGILLIER R, et al. Final overall survival results of phase Ⅲ GCIG CALYPSO trial of pegylated liposomal doxorubicin and carboplatin vs paclitaxel and carboplatin in platinum-sensitive ovarian cancer patients[J]. Br J Cancer, 2012, 107(4):588-591.
[20] BRUNDAGE M, GROPP M, MEFTI F, et al. Health-related quality of life in recurrent platinum-sensitive ovarian cancer--resu lts from the CALYPSO trial[J]. Ann Oncol, 2012, 23(8): 2020-2027.
[21] GLADIEFF L, FERRERO A, RAUGLAUDRE G D, et al. Carbo pl atin and pegylated liposomal doxorubicin versus carbopl atin and paclitaxel in partially platinum-sensitive ovarian cancer patients: results from a subset analysis of the CALYPSO phase Ⅲ trial[J]. Ann Oncol, 2012, 23(5):1185-1189.
[22] PFISTERER J, SHANNON C M, BAUMANN K, et al. Bevacizu mab and platinum-based combinations for recurrent ovarian cancer: a randomised, open-label, phase 3 trial[J]. Lancet Oncol, 2020, 21(5):699-709.
[23] GORDON A N, FLEAGLE J T, GUTHRIE D, et al. Recurrent epithelial ovarian carcinoma: a randomized phase Ⅲ study of pegylated liposomal doxorubicin versus topotecan[J]. J Clin Oncol, 2001, 19(14):3312-3322.
[24] MUTCH D G, ORLANDO M, GOSS T, et al. Randomized phase Ⅲ trial of gemcitabine compared with pegylated lipo s o mal doxorubicin in patients with platinum-resistant ovarian cancer[J]. J Clin Oncol, 2007, 25(19):2811-2818.
[25] PUJADE-LAURAINE E, HILPERT F, WEBER B, et al. Bevacizumab combined with chemotherapy for platinum-resi stant recurrent ovarian cancer: the AURELIA open-label rando mized phase Ⅲ trial[J]. J Clin Oncol, 2014, 32(13):1302-1308.
[26] POVEDA A M, SELLE F, HILPERT F, et al. Bevacizumab Comb- i ned With Weekly Paclitaxel, Pegylated Liposomal Doxorubicin, or Topotecan in Platinum-Resistant Recurrent Ovarian Cancer: Analysis by Chemotherapy Cohort of the Randomized Phase Ⅲ AURELIA Trial[J]. J Clin Oncol, 2015, 33(32):3836-3838.
[27] 曹冬焱.脂质体阿霉素(多美素®)治疗卵巢癌的中国数据[R].珠海:中华医学会第十四次全国妇产科学学术会议,2019.
[28] COLEMAN R L, GORDON A, BARTER J, et al. Early changes in CA125 after treatment with pegylated liposomal doxorubicin or topotecan do not always reflect best response in recurrent ovarian cancer patients[J]. Oncologist, 2007, 12(1):72-78.
[29] SABBATINI P, MOONEY D, IASONOS A, et al. Early CA-125 fluctuations in patients with recurrent ovarian cancer recei ving chemotherapy[J]. Int J Gynecol Cancer, 2007, 17(3):589-594.
[30] GOSSNER G, COLEMAN R L, MUTCH D G, et al. CA-125 response in patients with recurrent ovarian or primary peritoneal cancer treated with pegylated liposomal doxorubicin or topotecan[J]. Gynecol Oncol, 2006, 103(1):212-218.
[31] TANGUAY J S, ANSARI J, BUCKLEY L, et al. Epithelial ovarian cancer: role of pegylated liposomal Doxorubicin in prolonging the platinum-free interval and cancer antigen 125 trends during treatment[J]. Int J Gynecol Cancer, 2009, 19(3):361-366.
[32] MUGGIA F M, BLESSING J A, SOROSKY J, et al. Phase Ⅱ trial of the pegylated liposomal doxorubicin in previously treated metastatic endometrial cancer: a Gynecologic Oncology Group study[J]. J Clin Oncol, 2002, 20(9):2360-2364.
[33] PIGNATA S, SCAMBIA G, PISANO C, et al. A multicentre phase Ⅱ study of carboplatin plus pegylated liposomal doxoru-bicin as first-line chemotherapy for patients with advanced or recurrent endometrial carcinoma: the END-1 study of the MITO (Multicentre Italian Trials in Ovarian Cancer and Gynecologic Malignancies) group[J]. Br J Cancer, 2007, 96(11):1639-1643.
[34] DU BOIS A, PFISTERER J, BURCHARDI N, et al. Combination therapy with pegylated liposomal doxorubicin and carboplatin in gynecologic malignancies: a prospective phase Ⅱ study of the Arbeitsgemeinschaft Gynaekologische Onkologie Studiengruppe Ovarialkarzinom (AGO-OVAR) and Kommission Uterus (AGO-K-Ut)[J]. Gynecol Oncol, 2007, 107(3):518-525.
[35] SUTTON G, BLESSING J, HANJANI P, et al. Phase Ⅱ evaluation of liposomal doxorubicin (Doxil) in recurrent or advanced leiomyosarcoma of the uterus: a Gynecologic Oncology Group study[J]. Gynecol Oncol, 2005, 96(3):749-752. [36] HARTER P, SEHOULI J, REUSS A, et al. Phase Ⅱ Study Eval- uating PegLiposomal Doxorubicin and Carboplatin Com bination Chemotherapy in Gynecologic Sarcomas and Mixed EpithelialMesenchymal Tumors A PhaseⅡ Protocol of the Arbeits gemeinschaft Gynaekologische Onkologie Study Group (AGOGYN 7)[J]. Int J Gynecol Cancer, 2016, 26(9):1636-1641.
[37] ROSE P G, BLESSING J A, LELE S, et al. Evaluation of pegylated liposomal doxorubicin (Doxil) as second-line chemotherapy of squamous cell carcinoma of the cervix: a phase Ⅱ study of the Gynecologic Oncology Group[J]. Gyne col Oncol, 2006, 102(2):210-213.
[38] VERSCHRAEGEN C F, KAVANAGH J J, LOYER E, et al. Phase Ⅱ study of carboplatin and liposomal doxorubicin in patients with recurrent squamous cell carcinoma of the cervix[J]. Cancer, 2001, 92(9):2327-2333.
[39] CAELYX®(Pegylated Liposomal Doxorubicin Hydrochloride for Injection)[Z]. Toronto: Janssen Inc, 2018.
[40] VON GRUENIGEN V, FRASURE H, FUSCO N, et al. A double-blind, randomized trial of pyridoxine versus placebo for the prevention of pegylated liposomal doxorubicin-related hand-foot syndrome in gynecologic oncology patients[J]. Cancer, 2010, 116(20):4735-4743.
[41] BUN S, YUNOKAWA M, TAMAKI Y, et al. Symptom management: the utility of regional cooling for hand-foot syndrome induced by pegylated liposomal doxorubicin in ovarian cancer[J]. Support Care Cancer, 2018, 26(7):2161-2166.
[42] TEMPLETON A J, RIBI K, SURBER C, et al. Prevention of palmar-plantar erythrodysesthesia with an antiperspirant in breast cancer patients treated with pegylated liposomal doxorubicin (SAKK 92/08)[J]. Breast, 2014, 23(3):244-249.
[43] HONG C H L, GUEIROS L A, FULTON J S, et al. Systematic review of basic oral care for the management of oral mucositis in cancer patients and clinical practice guidelines[J]. Support Care Cancer, 2019, 27(10):3949-3967.
[44] RILEY P, GLENNY A M, WORTHINGTON H V, et al. Interventions for preventing oral mucositis in patients with cancer receiving treatment: oral cryotherapy[J]. Cochrane Database Syst Rev, 2015(12):CD011552.
[45] RILEY P, GLENNY A M, WORTHINGTON H V, et al. Interventions for preventing oral mucositis in patients with cancer receiving treatment: cytokines and growth factors[J]. Cochrane Database Syst Rev, 2018, 11(11):CD011990.
[46] LALLA R V, BOWEN J, BARASCH A, et al. MASCC/ISOO clinical practice guidelines for the management of mucositis secondary to cancer therapy[J]. Cancer, 2014, 120(10):1453-1461.
[47] HE M. Interventions for preventing oral mucositis in patients with cancer receiving treatment[J]. Clin Nurse Spec, 2011, 25(6):284-285.
[48] YAROM N, HOVAN A, BOSSI P, et al. Systematic review of natural and miscellaneous agents for the management of oral mucositis in cancer patients and clinical practice guidelines-part 1: vitamins, minerals, and nutritional supplements[J]. Support Care Cancer, 2019, 27(10):3997-4010.
[49] MCGUIRE D B, FULTON J S, PARK J, et al. Systematic review of basic oral care for the management of oral mucositis in cancer patients[J]. Support Care Cancer, 2013, 21(11):3165-3177.