英文名称 :erythema exudative multiforme heavy sywdrome
中文别名 :Stevens-Johnson综合征;多形性红斑;多型性渗出性红斑;Beader综合征;皮肤粘膜眼综合征;Fissing‐er‐Renda综合征;Neumann综合征;Neumann粘膜溃疡病;重型多形性渗出性红斑综合征;口腔‐粘膜‐皮肤‐眼综合征
重型大疱性多形红斑,又名Stevens‐Johnson综合征,本征病因不明,可能与药物过敏、变态反应和病毒感染有关。因其主要累及口腔、皮肤、眼,故又称“口腔-粘膜‐皮肤‐眼综合征”。
确切病因至今未明,很多因素均能引起:包括药物、遗传、免疫、感染、射线、妊娠及结缔组织疾病等。
1.药物因素
是引起此病最常见的因素,约占50%~55%。这些药物包括磺胺药、非甾体类抗炎药、别嘌呤醇、抗痉挛药、抗疟药、环丙沙星和胆茶碱等,甚至可发生于接种牛痘等。其中比较常见的是磺胺类药物和水杨酸类制剂。
2.感染因素
病毒感染如(腺病毒、单纯疱疹病毒、乙肝病毒、EB病毒、麻疹病毒、天花病毒等),据报道是因为病毒及其相关变异抗原引起宿主的免疫反应起了很大作用。另外,肺炎支原体、小肠耶尔森菌、立克次体等亦可引起Stevens‐Johnson综合征。
3.遗传因素
研究表明,遗传性自身免疫亦是主要致病因素之一。其中HLA与Stevens‐Johnson综合征的关系是当前研究的热点,早在1982年Bartly等就发现HLA‐BW44抗原在SJS白人患者中的阳性率(66.7%)明显高于对照组(20.4%)。近年来,William等首次运用PCR技术在分子生物学水平用非放射性探针检测出HLA水平,用非放射水平在眼表受累的23例SJS白种人群中的比例明显失调。HLA人群中的表达和HLA‐DQB0601分属于HLA‐D型和HLA‐Ⅱ型,二者的水平异常,提示Stevens‐Johnson综合征与遗传免疫有一定的必然联系。最近,Sotozono等人研究发现:Fas配体基因单核苷酸多态性与Stevens‐Johnson综合征呈现强烈的负相关。他们检测了76个Stevens‐Johnson综合征患者和160个正常日本人的四对Fas配体基因多态性,发现其可能与Stevens‐Johnson综合征的发病有关。
4.其他
包括肿瘤(内脏恶性肿瘤,白血病,淋巴瘤等),物理因素(日光,X线照射等),内分泌因素(妊娠,经前期,自身免疫性孕酮皮炎等),接触反应(二硝基氯苯,报春花属植物等),红斑狼疮,结节性多动脉炎,结节病,精神因素,过度疲劳,食物过敏甚至寒冷等均可诱发本病。
为临床少见的皮肤黏膜性眼综合征。据文献报道:德国的年发病率为1.1/百万,法国年发病率为1.2~1.3/百万,意大利的年发病率为0.6/百万,但Chan1990年报道为4.2/百万,而我国目前尚无准确数据统计,但近年文献报道及临床所见此病有增多趋势,儿童及青少年多见,发病季节以秋季为多。大约90%患者均有黏膜受累,依次为颊黏膜、眼表黏膜和肛门生殖器黏膜。
发病机制至今仍未完全明确,目前认为多与基因表达调控异常引起的免疫反应等有关。
1.基因表达调控异常
传统观点认为基因表达调控异常引起的免疫反应在该病的发展中起了很大作用。Nishida等在基础研究中发现,增殖的结膜上皮细胞对核抗原产生的单克隆抗体Ki‐67明显高于正常细胞,并且通过原位杂交技术检测出所有SJS患者增殖结膜基底膜上层细胞中均记录有谷氨酰胺转移酶‐1(TGase1)mRNA,而正常结膜上皮细胞并未见TGasel基因的表达。这证明了谷氨酰胺转移酶‐1的翻译出现在角质细胞的终末分化阶段,并且促进角质细胞的形成。由此,他们推测SJS的活动性炎症产生大量炎性细胞浸润,这些细胞释放相应的炎症细胞因子,诱导TGasel基因的表达,并最终导致结膜上皮角质化。
Nakamura等对结膜上皮凝集素蛋白基因的表达进行了专题研究。他们运用半定量PCR方法检测凝集素蛋白基因的表达,并且通过免疫组化研究凝集素蛋白的分布情况。结果发现病变结膜的凝集素mRNA水平明显低于相应的正常组织,而且,角质化的结膜凝集素蛋白水平也明显低于同类正常组织。基于这一结果,他们认为,凝集素蛋白的正常水平对于防止眼表上皮组织的角质化起着重要作用。
2.细胞免疫
在Stevens‐Johnson综合征的发病机制中,细胞免疫起了重要的作用。Caproni等为评价SJS发病中细胞免疫效应器和CD40/CD40L配体系统的作用,他们将6例SJS患者的活检标本用碱性磷酸酶/抗碱性磷酸酶染色,进行免疫组化检查。使用的单克隆抗体包括CDla、CD4、CD8、CD40、CD40L、CD68、Fas、Fas配体(FasL)和髓过氧化物酶。结果显示SJS皮损中的浸润细胞均以T淋巴细胞和CD68+巨噬细胞为主,并且有大量中性粒细胞浸润;Fas和Fas配体在SJS中表达高。所有组织切片中CD40染色均为强阳性,并有许多CD40L+细胞。他们认为:活化的T淋巴细胞、巨噬细胞和中性粒细胞,可能是SJS疾病谱中导致皮肤黏膜损害的主要触发因子。故CD40/CD40L系统可能是引起Stevens‐Johnson综合征损害的一个重要途径。
3.其他
近几年,随着研究的深入,提出了许多新的观点。Lan等为研究有药物性疱疹病史的患者在有或无致病药物刺激的情况下,外周血单核细胞(PBMCs)分泌的可溶性Fas配体的诊断意义。结果显示患者组用致病药物100μg/ml刺激后外周血单核细胞Fas配体分泌显著(P<0.05)。对照组无明显变化(P>0.05)。组间对照,患者组的外周血单核细胞PBMCs比正常对照组在无药物刺激情况下分泌更多的可溶性Fas配体。这些结果提示PB‐MCs高分泌可溶性Fas配体的个体易患严重的Stevens‐Johnson综合征。
临床上分重、轻两型,一般S‐JS 指重型而言,而轻型被称为“渗出性多形红斑”,当然不论全身症状及局部症状,重型较轻型明显增重。
组织学所见主要为表皮下非特异性纤维素性炎症变化。
1.皮肤病理
Stevens‐Johnson综合征的皮损病理活检常常表现为病变皮肤的表皮大多正常,可有少许淋巴细胞浸润,血管周围组织疏松,真皮浅层可见大量淋巴细胞浸润(图1)。由药物导致的Stevens‐Johnson综合征间质常可见少许嗜酸性粒细胞浸润。
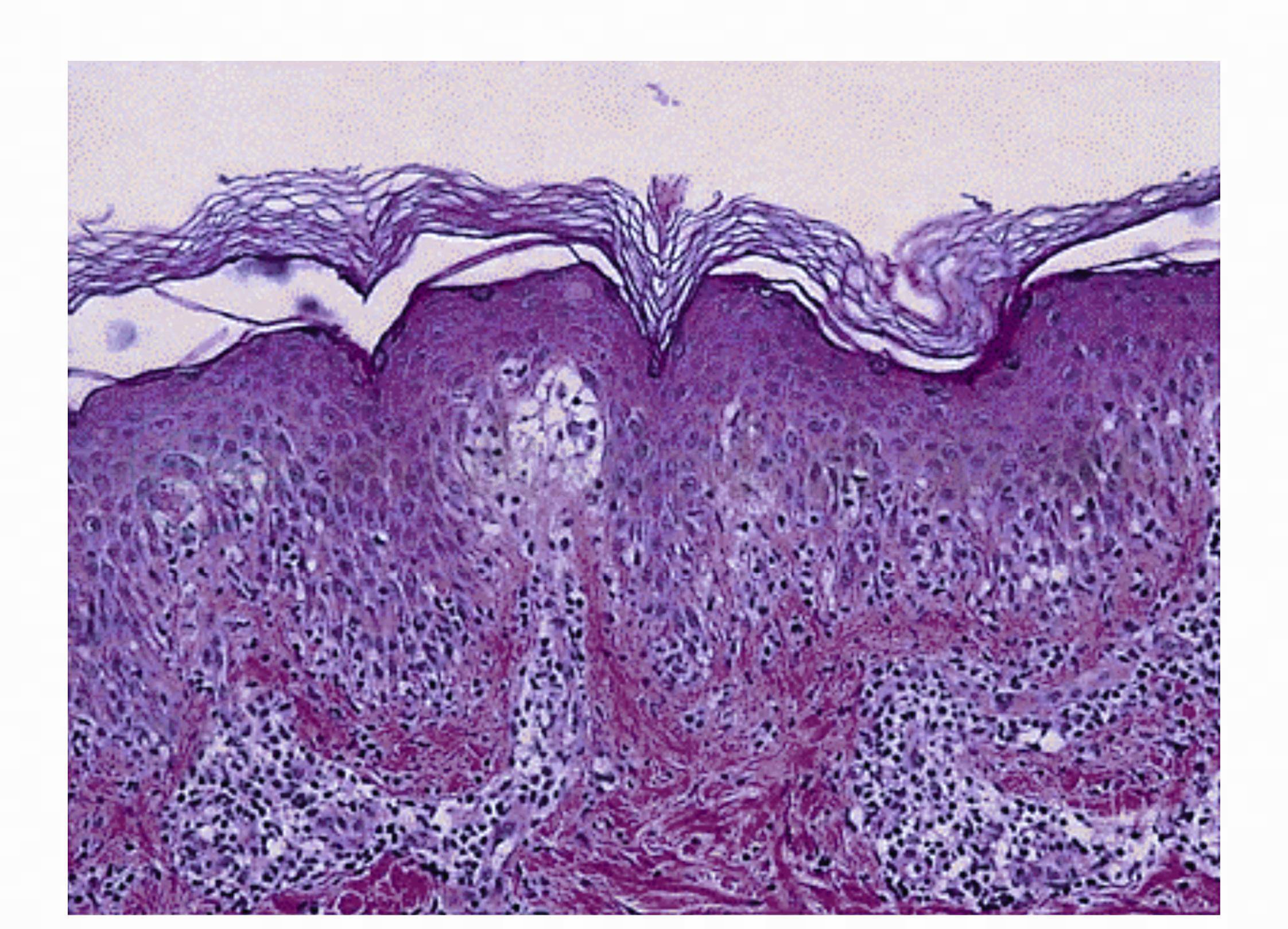
图1
SJS皮肤活检:大量淋巴细胞浸润
2.眼病理
在眼的组织病理学、超微结构和免疫病理学方面,Stevens‐Johnson综合征常表现为一种活动的、免疫介导的炎症,其主要特点是眼附属器如眼睑、结膜受损、腺体的血管炎、血管周围炎、血管壁的免疫复合物沉积、血管基底膜的病理性肥厚和破坏以及伴随T淋巴细胞、巨噬细胞和郎罕氏巨细胞(Langerhans罕cell)的浸润。
Kawasaki等对Stevens‐Johnson综合征患者角结膜连接处组织进行免疫组化研究发现:LFA‐1、CD4、CD8和CD68在此处上皮下细胞浸润明显。并且,HLA‐DR和CAM‐1在上皮细胞表面,上皮下的炎症细胞,上皮下成纤维细胞,血管内皮细胞中均有浸润。IFN‐γ在基底上皮细胞被发现;上皮下细胞及上皮下细胞外基质没有发现IFN‐γ。
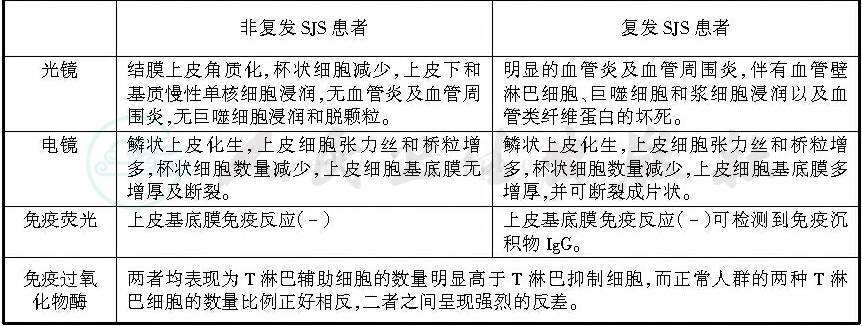
另外,Foster等对非复发和复发Stevens‐Johnson综合征患者分别进行了光学显微镜、电子显微镜、免疫荧光和免疫过氧化酶检查,发现在以上各项检查中的结果明显不同,(见表1)。
表1
实验室检查示血沉加速、白细胞增多、核左移、CRP阳性、α2及γ‐球蛋白增高、补体增高。
①皮质类固醇激素;②支持疗法;③预防和控制继发感染;④中医疗法;⑤皮肤黏膜损害的局部处理。
应尽量避免本病的诱因。
大约有3%的人在应用抗生素治疗会出现轻微的副作用,如短暂的皮疹、念珠菌性阴道炎和胃肠道的不适感。光过敏通常与强力霉素有关,但在氟喹诺酮类药物也可以见到。主要的副作用有Stevens‐Johnson综合征,在接触TMP‐SMX等含磺胺药物的人中10000人可以出现1例;过敏症状;甚至还会引起死亡。













