英文名称 :cerebral salt wasting syndrome
脑性盐消耗综合征(cerebral salt wasting syndrome,CSW)是指在颅内疾病情况下,因肾脏丢失大量的钠盐而导致的低钠血症并伴有细胞外液降低。其发病机制仍未明了,但病因与交感神经过度兴奋及某些利尿因子的作用有关。临床上鉴别SIADH和CSW较困难,鉴别的关键点是血容量状态,并排除其他中介病因(intermediate causes)。治疗的要点是补充血容量,必要时补充盐皮质激素。脑性盐消耗综合征(CSW)首先由Peters等于1950年报道,7年后报道了另一个与中枢神经疾病相关的综合征——SIADH,有些学者一度对是否存在CSW提出质疑,但因为随后报道越来越多,使CSW逐渐成为一个独立的临床状态(现象)[1]。
本征由于下丘脑或脑干损伤引起,其机制主要是下丘脑与肾脏神经联系中断,致使远曲小管出现渗透性利尿,患者血钠、氯、钾均降低,而尿中则含量增高;高平面的脊髓损伤也常导致严重的盐耗损性低钠血症。AVP是AVP受体V1aR、V1bR和V2R的激动剂,其中的AVP抗利尿作用是由V2R介导;AVP与V2R结合,激活相似环化酶,升高细胞内cAMP,激活PKA;继而磷酸化AQP2转位至细胞膜顶部,促进水的重吸收。
神经系统疾病(如SAH)引起脑钠肽(BNP)和其他钠利尿因子大量分泌,加上交感神经兴奋性不足,因肾脏钠消耗和血容量衰减而导致CSW综合征[2-4]。肾脏的交感神经张力是调节肾近曲小管钠和水重吸收和促进肾小球旁器上皮细胞释放肾素的关键因素[5],肾脏的交感神经张力不足引起肾近曲钠小管和水重吸收减少,肾素分泌降低。脑钠肽扩张入球小动脉,收缩出球小动脉,肾小球滤过率增高[6];其次,脑钠肽作用于肾小管,抑制AT-2介导的钠和水重吸收,拮抗AVP的作用[7]。一旦肾钠消耗发生,机体的压力感受器即被激活,AVP释放增多,以减少水的丢失。
钠利尿激素包括三类化合物:利钠肽有ANP、BNP、CNP、胃肠肽有尿苷蛋白(guanylin)、尿鸟苷(uroguanylin)和内源性心甾醇如乌巴因(ouabain)、地高辛(digoxin)和南美蟾毒精(marinobufagenin)。这些物质的共同作用是以内分泌或旁分泌方式促进肾脏排泄钠,调节水钠代谢、血容量与血压。此外,钠利尿激素也是脑组织的神经递质和神经调质。
(一)心钠肽
ANP由28个氨基酸残基组成,来源于含126个氨基酸残基的前体物质——利钠多肽(C-type natriuretic peptide,CNP)裂解 N末端后产生的 C端片段(ANP99-126)。ANP主要是心脏细胞合成与分泌的一种循环激素,主要有γ-hANP、β-hANP和α-hANP三种分子形式。
ANP的分泌受物理因素、体液因素、血流动力学变化和神经因素的调节。心房容量负荷增加或直接牵拉心房,都可促进ANP的释放,引起钠利尿、抑制肾素-血管紧张素-醛固酮、扩张血管和抑制血管平滑肌增殖等作用。
(二)脑钠肽
除ANP外,脑钠素(BNP)亦有利钠、利尿、舒张血管和降低血压作用。容量负荷刺激BNP和ANP分泌,促进心脏耗氧量或氧扩散,BNP和ANP引起钠利尿、水利尿和血管扩张氧张力;钠利尿、水利尿(diuresis)和血浆容量转移引起血容量缩减。
(三)尿苷蛋白和尿鸟苷
饮食钠负荷引起钠利尿的作用不依赖于醛固酮,摄入钠盐后,肠黏膜释放的尿苷蛋白和尿鸟苷激活GC受体,生成的cGMP进入肠腔,刺激氯化物和碳酸氢盐分泌,抑制钠吸收[8]。在肾脏,这些肽类刺激钠和钾排泄,同时排出较多水分。此外,尿苷蛋白和尿鸟苷在中枢神经系统也调节下丘脑功能,影响食欲和行为。
(四)心甾醇
能抑制Na+-K+-ATP酶活性。某些能治疗心衰的植物药可能含有心甾醇(钠利尿第3因子)[9,10]。这类网站可分为强心内戊酯(cardenolide)如乌巴因、地高辛和蟾蜍二烯羟酸内酯(bufadienolide),它们的共同结构特点是含有甾核和内酯环,其受体可能是Na+-K+-ATP酶的α催化亚基,可抑制Na+-K+-ATP酶泵功能[11,12]。Na+-K+-ATP酶广泛存在于体内,因而心甾醇对心肌细胞、平滑肌细胞、上皮细胞和神经元均有作用。
(五)利钠肽与脑耗盐综合征
在外周和中枢神经组织,心甾醇与其他利钠肽相互作用。例如,地高辛可促进ANP分泌[11-19],心衰患者应用地高辛后血浆ANP和BNP升高,而ANP也调节脑组织的心甾醇分泌。CSW患者表现为钠利尿(尿Na+131~250mmol/L)和多尿[每小时(5.5±1.5)ml/kg]特征,Na+的代谢转换与丢失加速,每小时约1.50mmol Na+/kg,而K+的排泄也明显高于正常(约每小时0.18mmol K+/kg),血浆BNP升高,ANP升高或正常,而血浆肾素活性与醛固酮均被抑制或在正常低值范围,说明CSW的钠和钾代谢处于明显的负平衡状态,此与SIADH刚好相反[20-22]。
(一)中枢神经系统疾病
低钠血症是住院患者中最常见的电解质紊乱之一,主要见于蛛网膜下腔出血(subarachnoid haemorrhage,SAH;占56.6%)、中枢神经系统感染(结核性脑膜炎、病毒性脑炎、单纯疱疹性脑炎等)、癌性脑病、经蝶窦手术、颅底或颈椎损伤、不合理的电解质补充和适用利尿剂等(详见病例报告1)。重度低钠血症(血钠≤130mmol/L)的病因有 SIADH(62.9%)、CSW(6.5%),低血容量性低钠血症(21%)和混合型CSW/SIADH(21%)。在102例存活的中度以上脑创伤病例中,12.9%发展为SIADH,(1%)发展为 CSW。但有报道,CSW的发生率高于SIADH[23,24]。
(二)利钠因子及交感神经功能紊乱
CSW的发病机制未明。CSW常见于适用利尿剂后,后者引起低血容量和钠消耗,但排除大量的钠盐的启动机制不明,可能与利钠因子有关,其中可能以BNP最重要。血容量增加,引起心房肌扩张,通过交感神经或增加血管紧张素-2或endoteline使利钠因子大量释放,同时使RAAS抑制,最终导致肾远曲小管钠利尿(natriuresis)。近来发现,在一组神经外科31例蛛网膜下腔出血伴低钠血症的患者中,其原因是血ANP升高而非AVP过多。另一组(9例)颅缝早闭(craniosynostosis)患者在进行颅骨术后1天,ANP和BNP增加3~6倍,并于术后第5天恢复正常,而ADH一直正常,所有患者的尿钠增多而血尿渗透压均正常。交感神经兴奋时,下丘脑或肾上腺髓质是可表达大量BNP,从而引起钠利尿。另一方面,交感神经的反应性异常则加重钠利尿,导致CSW。中枢神经的利钠因子调节水钠代谢和脑脊液生成ANP/BNP与颅内压直接相关,颅内压升高时的钠利尿现象是一种保护性反应,以降低颅内压和交感兴奋所致的血管收缩。BNP还可以显著增加充血性心衰和急性缺血性卒中的风险,而心衰和卒中后,交感兴奋又进一步加剧,BNP分泌更多。此外,CSW还与以下两个因素有关:①严重的细胞外液扩张可降调节肾脏的Na+转运体;②肾上腺素能神经冲动引起压力性钠利尿(pressure natriuresis)。但因为脑组织病变,交感神经的调节功能紊乱,肾脏的交感冲动最终因此而减低,并进一步导致肾血流和肾小球滤过率增加,钠的重吸收降低。
脑水肿引起脑组织容量扩张和颅高压。一般存在两种类型的脑水肿,即血管性脑水肿(vasogenic brain edema)和细胞毒性/细胞性脑水肿(cytotoxic/cellular brain edema)。但是,目前对于创伤性脑水肿(traumatic brain edema)的了解有限,治疗困难。 水孔蛋白-4(aquaporin-4,AQP4)主要由脑组织的星形胶质细胞表达的主要水通道蛋白,而高表达AQP4的星形胶质细胞主要位于脑实质与脑脊液腔或血管的交界处,这提示,AQP4是调节脑组织水代谢的最重要因子。细胞毒性脑水肿时,AQP4缺乏使水进入脑组织的速度减慢,而血管性脑水肿时,AQP4缺乏的作用相反,即水从脑组织泵出的量与速度下降,因此,调节脑组织的AQP4表达是治疗创伤性脑水肿的可能途径[3]。
(三)SIADH与CSW的临床表现异同点
临床上必须鉴别SIADH与CSW,因为治疗方法与预后完全不同,如果诊断与处理错误,将导致严重后果。由于SIADH与CSW的绝大部分表现相同,而实验室检查结果往往是重叠的,故两者的鉴别相当困难。SIADH和CSW均常见于颅内急性病变患者,此时的共同表现包括:①颅内病变;②低钠血症,而尿高渗透压较高,一般尿液尿钠均>20mmol/L;③均无水肿表现;④低尿酸血症;⑤尿酸盐排泄分数增加。但是,两者理论上的唯一不同之处是血容量,SIADH患者的血容量正常或升高,而CSW病例的血容量降低(表1和表2)[25-30]。
表1 SIADH与CSW的异同点

表2 CSW和SIADH患者纠正低钠血症后的血容量比较

注:血容量采用放射性核素稀释法测定
临床上测定中心静脉压(CVP)是判断血容量的最佳指标。如果患者的尿钠排泄>30mmol/L或钠或氯化物的排泄分数>0.5%,一般可确诊为SIADH,但是SIADH患者因水潴留、高血压或应激性儿茶酚胺增多而诱发利钠肽分泌,干扰尿电解质测定,尤其是当尿钠稍微升高时,很难做出正确的鉴别诊断。血细胞比容、BUN、白蛋白升高提示血容量不足和CSW可能,而血清尿酸降低与尿酸盐排泄分数增高可见于SIADH和CSW,其鉴别意义有限[31,32]。正常血容量者 FEurate约为10%,低血容量时降至5%以下,而SIADH和CSW患者一般高于10%。Maesaka等发现,SIADH患者的低尿酸血症在纠正血容量后有所改善,而CSW患者因钠-尿酸转运体功能障碍而无变化。
尿酸排泄分数反映尿酸的转运状态正常人为4%~11%,SIADH和CSW增加至11%以上,纠正低钠血症后SIADH患者恢复至正常(4%~11%),而CSW仍持续性升高(>11%)。因此,可应用FEurate和血清钠的关系鉴别SIADH与CSW(图1和图2)。

图1 SIADH和CSW的尿酸盐排泄分数比较
阴影区为正常范围
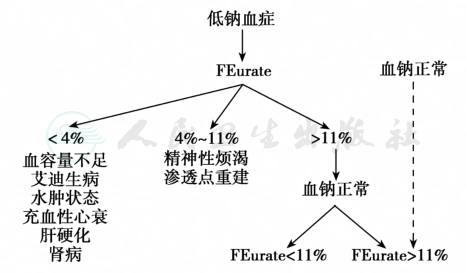
图2 根据尿酸盐排泄分数(FEurate)鉴别低钠血症的病因
CSW的治疗应针对病因。首先补充等渗或高渗钠盐溶液(SIADH应首先限制液体摄入)。SIADH和CSW都需要补充钠盐,但是多数低钠血症不需要使用高渗盐水,当患者可以进食时,盐片(salt tablet)可采用两种方法:首先应将血钠提升到安全水平,其次是应将钠池(Na+pool)和血容量补足。补液的速度要慢,以防止发生脑桥脱髓鞘(pontine myelinolysis)等并发症,一般要求补钠的速度低于0.7mmol/h,血钠水平不超过20mmol/(L·h)。CSW常使血管痉挛性脑缺血的治疗发生困难,血容量降低又常引起脑血流和心排出量进一步下降,血黏度升高。因此,在处理蛛网膜下腔出血等疾病时,必须按照3A治疗的要求(如晶状体和胶体溶液相结合),持续静脉输注液体。对因为颅内疾病引起的CSW,一种简单的办法是补充晶状体电解质和水即可。必要时亦可应用AVP拮抗剂处理低钠血症,皮质醇0.05~0.10mg/次,2次/天的效果较佳,因该药可直接促进肾小管的钠重吸收,但长期应用可引起低钾血症和高血压,偶尔导致肺水肿[33-35]。
研究发现,高渗液体并不能改善脑创伤、颅内高压或脑水肿的长期预后。在高渗负荷下,虽然液体的吸水能力提高,但可能引起高钠血症或导致渗透性血脑屏障开放和高渗溶液外渗而进入脑组织。用高渗盐水(即在通常的补充液体中加入高渗盐溶液)可以作为甘露醇的另一种补充,治疗顽固性颅高压并不能降低脑创伤患者的死亡率。患者在高渗负荷下,减轻脑水肿,降低颅内压,但必须注意防止发生严重的高钠血症或溶质性血脑屏障开放而使大量的水与钠进入脑组织[36]。低钠血症治疗药物有考尼伐坦(conivaptin)、莫扎伐普(mozavaptan)、托伐普坦(tolvaptan)和萨特普坦(satavaptan),其差别见表3。
表3 低钠血症治疗药物比较














