IGF-1缺乏症(IGF-1 deficiency)是由于IGF-1缺乏引起的生长发育障碍综合征,其主要原因是下丘脑和垂体性GH缺乏症以及原发性或继发性GH抵抗综合征。
IGF-1缺乏症为生长障碍的常见病因,引起IGF-1缺乏的主要病因见表4-24-9。
临床上,可将IGF-1缺乏症分为原发性和继发性两类,其中原发性IGF-1缺乏症又分为原发性GH缺乏症与原发性IGF-1缺乏症两种;继发性IGF-1缺乏症的原因在GHRH/GH缺乏,而原发性IGF-1缺乏症是直接因为IGF-1缺乏所致,其特点是GH正常或升高,而IGF-1降低(表4-24-10)。到目前为止,已经发现如下类型:①下丘脑疾病与功能紊乱(如转录因子缺陷与GHRH基因突变);②垂体疾病与功能紊乱(如转录因子缺陷与GHRH受体基因突变)或GH基因突变引起的GH缺乏与GH生物活性降低;③GH受体(GHR)病(包括GHR缺乏和GHR后JAK/STAT/MAPK障碍);④IGF-1合成障碍;⑤IGF-1转运与清除障碍;⑥1型IGF-1受体或受体后缺陷;⑦IGF-1的酸敏感亚基(acid-labile subunit,ALS)突变,表现为血清IGF-1极度降低伴胰岛素抵抗和低骨量,但躯体生长的影响程度相对较轻。
儿童期以后生长激素可明显抑制体重增加,但这种抑制作用是可逆的。相反,GH缺乏者容易发生肥胖。
(一) GH缺乏者补充GH
根据WHO对rhGH(重组的人GH)制剂的规定(somatropin,88/624),常用推荐量为每周0.175~0.35mg/kg,分7次注射;也可每周使用6次或3次。增加GH用量可加速生长,但生长速度只与剂量的对数值呈正比。有人认为即使在生长停止后仍可应用GH,因为GH还具有促进性腺功能和增加骨量等作用。如患者有其他激素缺乏,要注意同时补充,否则GH的疗效难以发挥。
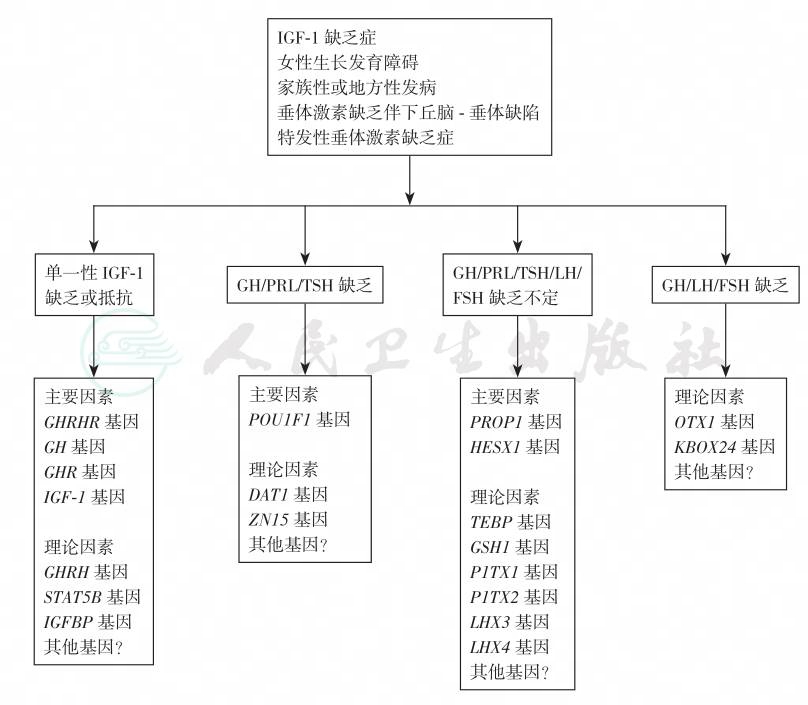
图4-24-2 IGF-1缺乏症的病因
注:GH、GHR、IGF-1和IGF-1R为主要因素;GH/PRL/TSH/LH/FSH为理论因素
表4-24-11 不同时期的IGF-1治疗方案

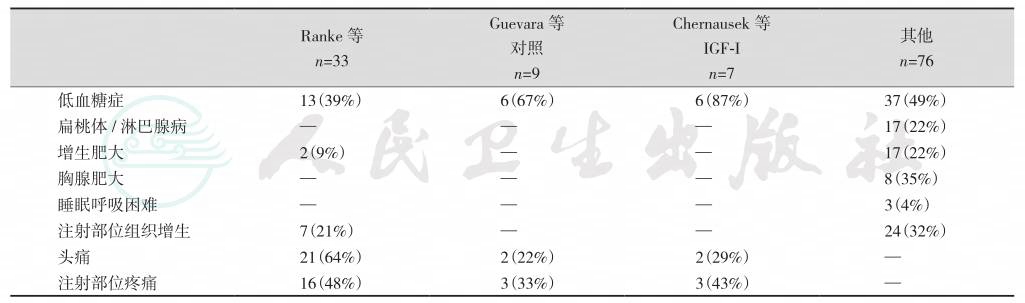
表4-24-12 IGF-1治疗的不良反应
使用GH后,生长增速主要发生于第1年,如疗效差,要想到下列可能性:①制剂效价不符合要求或使用不当;②伴有亚临床甲减等疾病,或合并存在其他全身性疾病;③应用过或同时应用了糖皮质激素制剂;④骨骺已经融合;⑤出现了抗GH抗体;⑥诊断错误。
(二) GH抵抗和IGF-1缺乏者用IGF-1治疗
用重组DNA技术获得的IGF-1(美卡舍明,mecasermin)安全,疗效明显。但静注IGF-1(以分子量计)的降血糖作用为胰岛素的6%,如静注100μg/kg可于注射后15min内发生低血糖症。如改为每小时20μg/kg滴注,一般不发生低血糖症。除主要用于GH抵抗综合征的治疗外,IGF-1还对下列数种临床疾病有治疗作用:①慢性肾衰或糖皮质激素所致的生长障碍;②IUGR;③分解代谢过盛状态,如营养不良症、手术后、烧伤、败血症、恶病质、恶性肿瘤致全身衰竭、AIDS和静脉高营养者;④老年人重度体衰;⑤胰岛素抵抗性糖尿病;⑥1型糖尿病等;⑦纤维肌痛症(fibromyalgia)。但是应禁止使用于竞技目的,由于IGFs有潜在的致肿瘤生长的作用,所以单独长期用于临床治疗的安全性应得到进一步的评估。
原发性IGF-1缺乏症的治疗 原发性IGF-1缺乏症的特点是矮小症,应用重组的人IGF-1的剂量与时间相差很大,效果不一(表4-24-11)。治疗的主要不良反应有低血糖症和淋巴组织增生(表4-24-12)。
1. Domené HM,Hwa V,Argente J,et al. Collaborative Group.Human acid-labile subunit deficiency:clinical,endocrine and metabolic consequences. Horm Res,2009,72(3):129-141.
2. Kreitschmann-Andermahr I,Suarez P,Jennings R,et al. GH/IGF-1 regulation in obesity—mechanisms and practical consequences in children and adults. Horm Res Paediatr,2010,73(3):153-160.
3. Tritos NA,Biller BM. Growth hormone and bone. Curr Opin Endocrinol Diabetes Obes,2009,16(6):415-422.
4. Ester WA,van Duyvenvoorde HA,de Wit CC,et al. Two short children born small for gestational age with insulin-like growth factor 1 receptor haploinsufficiency illustrate the heterogeneity of its phenotype. J Clin Endocrinol Metab,2009,94(12):4717-4727.
5. Backeljauw P,Bang P,Dunger DB,et al. Insulin-like growth factor-I in growth and metabolism. J Pediatr Endocrinol Metab,2010,23(1-2):3-16.
6. Backeljauw P. Diagnosis and management of primary insulin-like growth factor-I deficiency:current perspectives and clinical update. Pediatr Endocrinol Rev,2010,7(Suppl 1):154-171.
7. Kemp SF. Insulin-like growth factor-I deficiency in children with growth hormone insensitivity:current and future treatment options. BioDrugs,2009,23(3):155-163.
8. Fintini D,Brufani C,Cappa M. Profile of mecasermin for the long-term treatment of growth failure in children and adolescents with severe primary IGF-1 deficiency. Ther Clin Risk Manag,2009,5(3):553-559.
9. Chernausek SD. Growth hormone-resistant syndromes:long-term follow-up. Endocr Dev,2009,14:135-142.
10. Cuatrecasas G. Fibromyalgic syndromes:could growth hormone therapy be beneficial? Pediatr Endocrinol Rev,2009,6(Suppl 4):529-533.
11. Guha N,S?nksen PH,Holt RI. IGF-I abuse in sport:current knowledge and future prospects for detection. Growth Horm IGF Res,2009,19(4):408-411.













