类癌(carcinoid)又称嗜银细胞瘤(argentaffinoma),1907年首次由病理学家Oberndorffer提出,由于其特征性的生化异常是5-羟色胺(5-HT)以及代谢产物5-羟吲哚乙酸(5-HIAA)的过量生成,引起皮肤潮红、腹泻、哮喘和心脏瓣膜病变等一组临床综合征(图1),故于1952年又命名为类癌综合征(carcinoid syndrome),其常见的临床表现为阵发性面部潮红、腹泻、右心衰竭、支气管哮喘和呼吸困难等以及尿5-HIAA增高;偶尔亦可表现有体重下降、阵发性出汗和糙皮病样皮损。通常意义上的神经内分泌肿瘤是指类癌和胰腺内分泌肿瘤,这些肿瘤的病因、病理、临床表现、诊断和治疗均有共同之处。
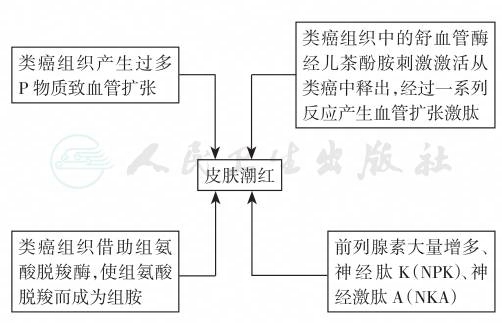
图1 类癌综合征致皮肤潮红的机制
(一)类癌瘤分泌多种生物活性物质
类癌瘤的病因未明,此类肿瘤来源于APUD细胞,这些细胞可起源于胚胎的外胚层、内胚层或中胚层;类癌瘤分泌的生物活性物质很多,如5-羟色胺(5-HT)、5-羟色氨酸(5-hydroxytryptophan)、缓激肽、胃泌素、胃泌素释放肽(gastrinreleasing peptide)、降钙素、胰多肽、ACTH、CRH、GHRH、生长抑素、胰高血糖素和降钙素基因相关肽、AVP(精氨酸加压素)以及神经激动素(neurokinin)等。但是,无论类癌瘤分泌何种激素,其共同特点是都同时产生糖蛋白——铬粒素A(chromogranin A,CgA),因而CgA是类癌瘤的最重要肿瘤标志物(图2)。CgA为一种酸性糖蛋白,含439个氨基酸残基,分子量48kD。CgA裂解后可产生多种活性片段,如血管抑制素(vasostatin)、铬粒抑素(chromostatin)、胰抑素(pancreastatin)等。这些胺类或生物活性肽在细胞内有两种储存形式:①大颗粒致密分泌囊泡,内含CgA及其分解的活性产物;②小颗粒的触突样囊泡。
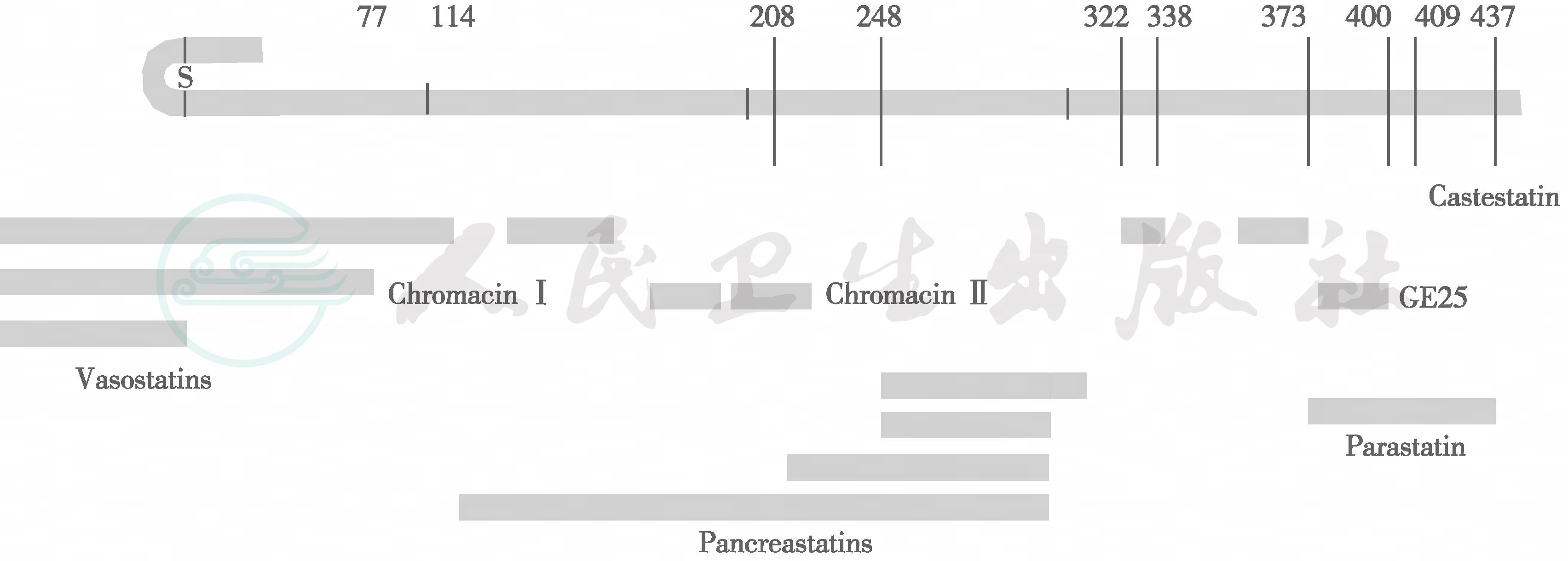
图2 铬粒素A及其相关肽
(二)类癌瘤作为遗传性肿瘤综合征的表现之一
目前研究表明有3种遗传性肿瘤综合征与类癌瘤有关,分别为多发性内分泌肿瘤综合征(MEN-1)、视网膜及中枢神经血管瘤病(VHL病)和神经纤维瘤病1型(NF-1)。
1.MEN-1
患者中95%有甲状旁腺增生或肾上腺腺瘤;2/3的MEN-1患者有胰腺内分泌肿瘤(PETs)。而PETs多半无功能或产生胰岛素和胃泌素。从病理学角度看,MEN-1中的PETs属于前肠的类癌瘤。在MEN-1患者中,类癌瘤经常表现为11q13杂合性缺失和野生型MEN-1等位基因的缺失。
2.VHL病
患者在小脑和视网膜等处可有成血管细胞瘤。VHL基因位于染色体3p25~3p26上,正常情况下,VHL基因是一种肿瘤抑制基因,抑制肿瘤生长,当缺失或突变时易患肿瘤。VHL病的病变有25种之多,其中最常见的特征是视网膜、中枢神经系统和腹腔脏器多发肿瘤,包括小脑血管母细胞瘤(13%~60%)、视网膜多发血管瘤(>50%)、嗜铬细胞瘤(>10%)、脊髓或脊柱血管母细胞瘤(<10%)和肾癌(25%~38%)以及肝、肾囊肿。VHL病合并类癌,罕见。
3.NF-1
少数患者中可发生十二指肠或纵隔类癌。NF-1基因定位于染色体17q11.2,目前NF-1基因协会已公布了276种突变。最常见的症状为黄疸和腹痛,其他症状有体重下降、上消化道出血和急性胰腺炎。推荐对有腹部不适的NF-1患者行胃十二指肠镜检查以明确是否罹患类癌瘤。
根据1963年William等的意见,可分为前肠类癌瘤、中肠类癌瘤和后肠类癌瘤3类(表1)。
表1 类癌瘤的胚胎来源分类
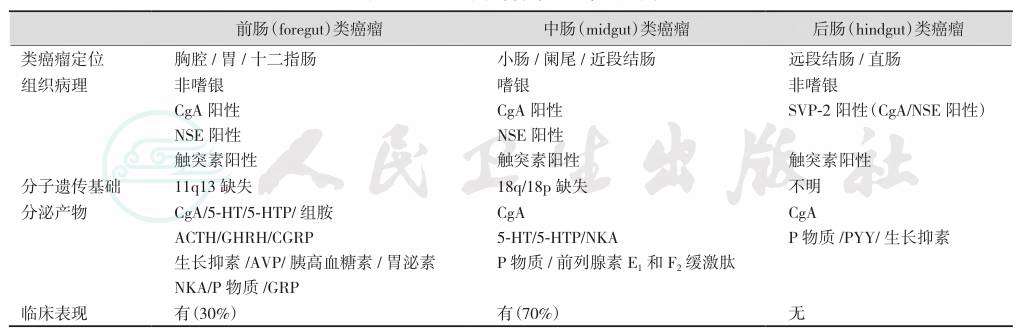
注:CgA:铬粒素A(chromogranin A);5-HT:5-羟色胺(5-hydroxytryptamine);5-HTP:5-羟色氨酸(5-hydroxytryptophan);CGRP:降钙素基因相关肽(calcitonin-gene-related peptide);AVP:精氨酸加压素(arginine vasopressin);NKA:神经激动素(neurokinin);GRP:胃泌素释放肽(gastrin-releasing peptide);NSE:神经元特异性烯醇酶(neuro-specific enolase)
(一) 组织病理分为分化良好和分化不良的类癌瘤
见表2。
表2 类癌瘤病理分类

1.消化道类癌
类癌可以发生在全身的各个部位,包括消化道、呼吸道、纵隔、肝、卵巢、乳腺、阑尾、睾丸、肺、喉、胸腺、支气管、肾(包括马蹄肾)、膀胱、前列腺、化学感受器、直肠后窝、血管、Meckel憩室、颅内和中耳等处,其中消化道最多见,占87%(其中又以阑尾的发生率最高),呼吸道约占10%,其他部位罕见。
消化道类癌发生的部位较广泛,其中最常见的是回肠远端的1/3,其他部位包括小肠、大肠、胃、胰和胆总管。类癌的体积小,直径常在1.5cm以下,一般不超过3.5cm。小肠肿瘤罕见,而神经内分泌肿瘤却相对常见,小肠肿瘤主要有4种:①类癌瘤;②腺癌;③淋巴瘤;④间胚叶肿瘤。
胃类癌瘤可分为3型:①Ⅰ型胃类癌瘤与A型慢性萎缩性胃炎有关,即由高胃泌素血症所致。该型胃类癌瘤通常属良性肿瘤。②Ⅱ型胃类癌瘤常发生于MEN-1和胃泌素瘤患者,呈相对良性。③Ⅲ型胃类癌瘤为散在性肿瘤。其侵袭性最强,也最具转移性,并且与胃泌素浓度无关。其中Ⅰ型最常见,占63%~75%,Ⅱ型最少(0~10%),Ⅲ型占13%~20%。Ⅰ型肿瘤常为多发。肿瘤直径小于1cm者,很少转移,而直径大于2cm的胃肠胰类癌瘤常转移至淋巴结和肝脏。Ⅰ型和Ⅱ型胃类癌瘤直径一般小于1~2cm,且分化良好;而Ⅲ型胃类癌瘤直径一般>2cm,其组织学形式包括分化良好、分化不良和内分泌-外分泌混合瘤(mixed endocrine-exocrine tumor)。
2.支气管-肺类癌
分为典型和非典型两种类型。非典型类癌的预后较差,可能与肿瘤细胞凋亡和浸润活性有关。一般支气管肺类癌细胞凋亡减少,但增殖活性也不高,加上p53基因的功能正常(无突变),故一般呈良性经过。单凭肿瘤细胞的分化程度和形态特征不易估计其预后,如加用神经内分泌细胞标志物(如MIB-1和p53等)免疫组化检查可提高预后估计的可靠性。
3.乳腺类癌
主要见于老年妇女,其生物学行为与乳腺导管癌相似,可用细针活检明确诊断。卵巢类癌罕见。阑尾类癌甚至可转移到盆腔。
4.胸腺类癌
往往有重症肌无力和旁癌综合征表现。部分胸腺瘤患者除重症肌无力、多发性肌炎或神经性肌强直症外,亦可伴有类癌症状。
(二)皮肤潮红
正常情况下,膳食中的色氨酸99%被用于合成烟酸和蛋白质,而类癌患者所摄入的色氨酸一半以上被色氨酸脱羧酶转化为5-色氨酸,进而生成5-HT,并代谢为5-HIAA。有些类癌可以作为MEN的组成部分。类癌细胞在表达单胺氧化酶方面存在显著的不均一性。除自身合成外,肿瘤细胞合成的5-HT前身物还可被非肿瘤细胞用于5-HT的合成。不同胚胎起源(前肠、中肠和后肠)的类癌具有不同的生化、病理及临床特征,来自前肠的类癌(胃十二指肠、胰腺和支气管)为非亲银性,由于缺乏芳香氨酸脱羧酶,故5-HT生成较少,而5-色氨酸含量较高,它们也可产生组胺和各种肽类;来自中肠(小肠、回盲部、升结肠和部分横结肠)的类癌为亲银性和嗜银性,能产生较多的5-HT、缓激肽、前列腺素、P物质和各种肽类;来自后肠的类癌为非亲银性,大多无分泌功能。来自前肠的类癌可表现为各种内分泌肿瘤综合征;来自中肠的类癌较易发展为类癌综合征;来自后肠的类癌在临床上多呈静止状态。
1.皮肤潮红发作的常见诱因
主要有:①物理性、精神性或生物性应激;②感染;③乙醇;④刺激性食物;⑤某些药物,如儿茶酚胺、钙剂和五肽胃泌素等。导致皮肤潮红的直接原因未明,一般认为与血清素和血清素的代谢产物有关,但高血清素血症患者不一定都发生皮肤潮红;用血清素拮抗剂(如赛庚啶、methysergide和酮舍林等)并不能缓解皮肤潮红,而应用生长抑素类似物却可以获效。因此,除血清素外,还可能与速激肽(tachykinin)、神经肽-Y(neuropeptide-Y)、P物质、激肽释放钛、激肽、内皮细胞松弛因子(endotheliumderived relaxing factor,EDRF)和NO等有关。在支气管类癌瘤和胃ECL细胞瘤患者中,组胺是导致皮肤潮红的重要因素。
2. 皮肤潮红的病变特点
常为鲜红色或紫色,为阵发性或突然发作,持续时间可自数分钟或至1~2天,皮肤黑的患者颜色改变多不明显,常伴有局部及眼眶周围水肿、心动过速、血压低、及肺和胃肠的症状。患者常有温、热感,有时只见球结膜的血管扩张。诱发刺激(如疼痛和饮酒等)、体力活动和情绪波动等引起儿茶酚胺释放能诱发发作。皮肤潮红如果阵发数年,则在经常发作的部位出现固定性皮肤改变,即多数毛细血管扩张及轻微紫红色,特别易见于颊部、鼻部、上唇及下颏。类癌通过下列机制使皮肤潮红。
3. 皮肤潮红的表现形式
皮肤潮红有4种表现形式:①突发的弥漫性红斑样皮肤潮红(diffuse erythematous flush):波及的部位是面部、颈部和上胸部;持续的时间1~5分钟;此型多见于来源于小肠、阑尾或近段结肠的中肠类癌瘤(20%~70%)。②恶性皮肤潮红(violaceous flush):类癌瘤的来源与红斑样皮肤潮红相同,持续的时间约数分钟或稍长一些;面部可见血管扩张;此型皮肤潮红多提示其病程较长。③持久性皮肤潮红(prolonged flush):皮肤潮红的发作时间常长达数小时至数天;波及的部位可达全身,并常伴有大量流泪、唾液腺肿大、低血压和面部水肿;此型皮肤潮红最常见于恶性支气管类癌瘤。④块状皮肤潮红:局部皮肤呈亮红色;发作频率不定;主要见于萎缩性胃炎和ECL细胞增生患者,分泌的活性物质为组胺与组胺的代谢产物。由于腹泻致烟酸及其前体色氨酸摄入不足,晚期病例可出现癞皮病。
(三) 类癌瘤活性物质引起长期腹泻与吸收不良
腹泻的发生与多种因素有关。在生物活性物质方面,可能主要与5-HT、速激肽、组胺、激肽释放肽、激肽和前列腺素等有关。常伴有腹痛、腹胀及里急后重,程度轻重不一,亦可有恶心、呕吐、肠梗阻和吸收不良等症状。腹泻1天1次至数次不等,不一定和皮肤潮红同时出现。消化性溃疡较一般人多见。当类癌有巨大肝转移时,肿瘤可因相对缺血、坏死,产生出血,可出现阵发性严重的右上腹痛、右肩痛、发热、白细胞偏高和其他急腹症表现。长期的腹泻可引起吸收不良综合征。经小肠减压等保守治疗,症状可于7~10天内缓解。由于肿瘤的分解代谢作用和严重腹泻,伴消瘦,甚至呈恶病质。
(四) 5-HT分泌过多引起阵发性哮喘和呼吸困难
因5-HT有增强平滑肌收缩作用,故有20%~30%的类癌患者有哮喘和呼吸困难,临床表现与支气管哮喘相同。哮喘可与皮肤潮红同时发生。麻醉或注射肾上腺素可诱发或加重哮喘。
(五) 5-HT导致类癌性心脏病
1.心内膜内皮下新胶原层形成
早期的支气管类癌或房间隔缺损而有由右至左的分流者,心脏受累主要是肝转移瘤所产生的5-HT等物质进入右心所致,故右心瓣膜易受累。肺能使这些物质灭活,故左心不易受累。当肺有类癌组织或有由右至左的分流时,这些物质逃避了肺的灭活而达左心,遂有左心瓣膜病变。心内膜内皮下的新胶原层只见于类癌综合征心血管损害,其诊断特异性几乎为100%,高分辨率B超的发现率约70%。但如果患者已用生长抑素或α-干扰素治疗,则难以发现内皮下新胶原层。内皮下新胶原层是导致严重心肌病的主要原因。另一方面,长期使用芬氟拉明类(芬氟拉明或右旋芬氟拉明)减肥药物者亦可并发类似于类癌综合征的心血管损害,其原因是这些药物可促进血清素和速激肽的分泌。
心内膜纤维化主要侵犯右心瓣膜及心内膜。以肺动脉瓣狭窄、三尖瓣狭窄和闭锁不全最为常见,左心受累较轻,此见于长期类癌综合征患者。
2.心瓣膜狭窄与关闭不全
在组织学上,新胶原层呈斑块样,心内膜明显增厚;斑块内含大量的粘多糖和胶原,散布有较多的成肌纤维细胞和成纤维细胞。可能是血清素、速激肽和IGF-1等上调转化生长因子-β(TGF-β)的表达,而后者促进了内膜下纤维化。因为由肠管或肝脏类癌瘤分泌的生物活性物质可直接进入右心房和右心室,导致内皮下新胶原层的形成和纤维化;而左心房和左心室血液中的生物活性物质已经由肺降解,故其浓度显著下降,引起内皮下新胶原形成和纤维化的几率小;但支气管类癌瘤仍可引起左心房和左心室纤维化。心内膜和心瓣膜呈特异性增厚与纤维化可进一步导致心瓣膜狭窄与关闭不全。晚期可有充血性右心衰,为致死的常见原因。心脏听诊杂音显示为肺动脉瓣狭窄、三尖瓣狭窄和闭锁不全等。
3.低血压/高血压和心力衰竭
通常,患者的血压正常或降低。当皮肤潮红时,可有严重低血压,甚至休克。高血压并不多见,但高血压与严重头痛倾向较多见于原发性支气管类癌而有转移者。水肿可由于心力衰竭、腹泻、蛋白丢失或肝转移瘤等所致。
(六)组织纤维化引起器官损害
除心肌外,其他组织亦可发生纤维化。如腹腔或腹膜后腔纤维化可导致不明原因的腹痛;广泛的动脉纤维化引起顽固性高血压;静脉纤维化可并发肝脾肿大或皮下水肿;阴茎纤维化导致勃起障碍(Peyroie病);关节软骨纤维化的后果是顽固性关节病(类癌性关节病);盆腔纤维化致泌尿道梗阻和反复感染。
由于色氨酸多被用于合成5-HT,患者可表现烟酸缺乏,而出现癞皮病。5-HT能致平滑肌收缩,可使肠过分蠕动产生腹泻及支气管痉挛。
(七)伴癌综合征
此在支气管类癌中最为常见,合成的激素有生长抑素、胰多肽、神经降压素、胃动素、降钙素、β-内啡肽、甲状旁腺素、ACTH及绒毛膜促性腺激素等。许多类癌可分泌两种或两种以上的激素。所以,类癌患者可能有上述某些激素功能亢进的表现。例如,大约有1%的Cushing综合征是因类癌引起的;如类癌分泌GHRH,可出现生长过度或肢端肥大症。
胸腺类癌往往有重症肌无力和伴癌综合征表现。类癌综合征女性易致早产、死产和胎儿生后夭折。胸腺的神经内分泌肿瘤可无症状(1/3),多数位于前纵隔,肿瘤的分泌程度直接影响其生物行为(包括临床表现)。部分胸腺瘤患者除重症肌无力、多发性肌炎或神经性肌强直症,亦可伴有类癌症状,被认为是一种伴癌综合征表现。伴重症肌无力者可检出抗神经肌肉的多种抗体,如抗乙酰胆碱受体抗体、titin抗体、骨骼肌钙释放通道蛋白(skeletal muscle calcium release channel)抗体和电压门控通道(voltage-gated potassium channel,VGPC)受体等。
类癌综合征的临床表现变化多端,在一定程度上可反映类癌所产生激素的量和患者对激素的反应性。临床表现取决于原发肿瘤的大小、部位和是否发生转移等因素。类癌的最好发部位是小肠和上段结肠,这些部位的类癌的类癌综合征表现发生率高(40%~60%),支气管、卵巢和腹膜后的类癌多在早期出现类癌综合征表现,因为其分泌的生物活性物质可直接进入血液循环,而直肠类癌不出现临床表现。中肠来源(小肠、阑尾、近段结肠)的类癌亦很少有临床表现(5-HT等生物活性物质在局部组织和肝灭活,极少进入血液循环),一般只出现局部肿块或局部淋巴结转移。具有典型类癌综合征临床表现的病例往往提示类癌已伴有多灶性肝转移。
小肠类癌发生肝转移时,肝不能对5-HT等活性物质提供足够的灭活能力,引起过多的5-HT进入体循环并引起症状。肺支气管、卵巢和睾丸类癌可直接引流入体循环而产生类癌综合征。阑尾类癌很少是恶性的,故几乎不引起类癌综合征。但个别的无转移的膈、胸腺、胰和胃类癌也可引起类癌综合征表现。类癌瘤向浆膜和肠系膜淋巴结转移,可致肠粘连、固定、牵拉、梗阻和缺血。5-HT是类癌综合征患者的主要病理生理基础。84%的类癌患者血中5-HT或尿5-HIAA增高。
(八)类癌危象
自引入生长抑素类似物治疗以来,类癌危象已很少见。类癌危象的主要诱因是急性应激,如麻醉、血管介入治疗、化疗或感染等。类癌危象一般发生于前肠类癌,尿5-HIAA可骤然增高,临床上表现为严重而普通的皮肤潮红,发热、心动过速、腹泻明显加重并伴腹痛,可有眩晕、嗜睡和昏迷等中枢神经系统症状,以及心动过速、心律失常、高血压及严重低血压等心血管异常。
类癌的治疗主要包括手术切除、肝动脉结扎或栓塞、化疗和药物治疗。
(一)手术和肝动脉结扎或栓塞治疗
根据肿瘤的大小、部位和有无转移决定相应的切除范围和术式。未转移的胃、肠、胰、支气管、胸腺或卵巢类癌可以手术切除治愈。其他如回肠类癌转移至肝,手术切除部分肝和转移癌可缓解症状。如腹部局部纤维化致肠系膜血管闭塞,肠段缺血,切除此坏死肠段可获长期缓解。
90%的肝瘤细胞氧来自肝动脉,50%的正常肝细胞氧来自门静脉系统,故动脉闭塞以减少瘤细胞的氧供应,可致瘤萎缩。方法有肝动脉结扎或栓塞,可使80%~90%的患者症状减轻。如果同时开腹切除回肠原发瘤或坏死小肠,效果更好。有人主张肝动脉栓塞后加化疗对症状缓解比单用一种方法治疗效果更好。肝动脉栓塞的禁忌证是:①肿瘤占据肝脏的50%以上;②血清乳酸脱氢酶(LDH)>425mU/ml;③血清谷丙转氨酶(SGOT)>100U/L;④血清胆红素>34μmol/L。门静脉瘤栓则只有当其使门脉血流离肝逆流时才构成禁忌证。
类癌患者在应激情况下(如手术、创伤、麻醉和乙醇中毒等)或化疗开始时,诊断性诱发试验均可诱发类癌危象,有时可自发发生类癌危象(特别是前肠类癌者)。化疗从小剂量开始可预防类癌危象的发生。对严重类癌综合征,化疗的开始剂量宜小,在常规剂量之下,以免肿瘤溶解,突然释放大量血管活性物质,造成危象。24小时尿5-HIAA超过150mg者一般病情重,要特别防止危象的发生。此类病例为危象的高危人群,化疗剂量应为通常的一半,或先用生长抑素类似物,情况改善后,再用全量化疗。类癌综合征可由于通常标准剂量的化疗无效,遂采用长期较大剂量,从而出现危象致死,应予避免。
(二)生长抑素类似物治疗类癌瘤
奥曲肽和缓释兰乐肽等均是生长抑素类似物,因奥曲肽的初始剂量为0.05mg,每天1~2次,奥曲肽的初始用量为100μg/d,分2~4次皮下注射,根据患者的耐受性及疗效渐加至每天3次,每次200~300μg。个别患者可能需要更高剂量,维持剂量因人而异。如用药数周后仍无效,应改用其他治疗方法。由于这几种药物在肠道吸收差,故需肠外给药。资料显示:使用奥曲肽375μg/d,可使80%以上的类癌综合征患者得到缓解,当奥曲肽用量≥400μg/d时,80%以上患者的皮肤潮红也得到控制;同样,当奥曲肽用量≥400μg/d时,70%以上的患者尿5-HIAA排泄量下降一半以上。对仅有轻至中度症状而又存在危及生命因素的类癌综合征患者,奥曲肽治疗宜从每8h注射100μg开始,因对治疗存在个体差异,及时调整用药剂量满意地控制症状尤为重要,个别患者皮下注射用药量可达3000μg/d以上。奥曲肽治疗明显延长了患者生存期。但长期使用可引起胆汁淤积、脂肪泻、高血糖和心脏传导异常等,因此治疗中要监测胆石形成和血糖等。
奥曲肽是目前治疗类癌危象最有效的药物,因而建议,在诱导麻醉前24~48小时开始使用奥曲肽180~250μg,每6~8小时皮下注射1次;转移性类癌患者在化疗开始前1~2小时也应皮下注射250~500μg,紧急情况下可注射100~500μg。抑肽酶(aprotinin)、酮舍林(5-HT2受体阻滞剂)和色氨酸等的疗效不肯定。其他辅助对症治疗包括补液、补充电解质、应用升血压药和皮质激素等。肺类癌综合征所致的类癌危象治疗特别困难,奥曲肽的用量宜加大,一般为每小时50~100μg,并同时给予组胺H1受体和H2受体阻滞剂。
(三)色氨酸羟化酶抑制剂和组胺拮抗剂抑制治疗类癌瘤
色氨酸羟化酶为色氨酸转变成5-HT所必需,parachlorophenylalamine是色氨酸羟化酶抑制剂,可减少尿中绝大部分的5-HIAA,并使腹泻停止,但对皮肤潮红无效。过敏反应和精神障碍等不良反应较常见。赛庚啶(cyproheptadine)是5-HT和组胺的拮抗剂,4~8mg,每日3次,可有效止泻,但对皮肤潮红无效。推测此类药物抑制瘤的生长是通过阻滞胺类激素的效能来实现的。可刺激食欲致体重增加。二甲麦角新碱(methysergide)亦有类似止泻作用,2~4mg,每日3~4次。
(四)其他药物治疗类癌瘤
1.他莫昔芬(tamoxifen)
是合成的雌激素拮抗剂,部分研究应用显示能改善类癌综合征的症状,每日20~40mg 分次服用,至少2个月,能降低尿中5-HIAA并缩小肿瘤体积,但尚未被公认。
2.干扰素
能改善症状,单独应用α-干扰素时,约40%的患者尿5-HIAA的量减少并且约12%的患者显示肿瘤的生长被抑制;当α-干扰素与奥曲肽联合使用时,有转移的中肠类癌瘤患者5年生存率为57%,而单独使用α-干扰素的5年生存率为37%。α-干扰素能引起肿瘤组织纤维化,所以肿瘤的体积虽无改变,但仍然有效。如果患者对生长抑素类似物治疗的反应差,或发生快速免疫反应(tachyphylaxis),加用α-干扰素后往往有良好疗效,而且可减轻α-干扰素的不良反应。同样,如患者对α-干扰素治疗的反应差,或发生免疫反应,加用生长抑素类似物后亦有良好疗效。α-干扰素的主要不良反应有慢性虚弱综合征、贫血、粒细胞减少和自身免疫疾病等。
3.选择性5-HT 3受体拮抗剂
如患者腹泻明显,可试用选择性5-HT3受体拮抗剂如阿洛斯琼(alosetron)。由美国加州Patty-George Hoag癌症中心执行的持续性IL-2静脉滴注治疗各种恶性肿瘤的疗效评价试验结果表明,612例中,存活率≥37%(其中包括2例类癌患者)。说明IL-2对本病亦可能有效。同样,白细胞介素调节因子-1(IRF-1)也有抗肿瘤增殖作用,可用于类癌的治疗。参莲胶囊据报道对消化道类癌有抑制作用。2~6粒/次,3次/日,可长期服用。
4.生长抑素类似物和靶受体放射治疗
可选用奥曲肽(octreotide LAR),如果效果不佳,重复给予大剂量111In奥曲肽可使类癌体积缩小和5-HIAA排出减少,或改用新的生长抑素类似物pasireotide(SOM230,对奥曲肽抵抗者部分有效),必要时可加用VEGF/VEGFR/PDGFR抑制剂,如依维莫司、舒尼替尼(sunitinib)和贝伐珠单抗(bevacizumab),131IMIBG 治疗研究也显示对60%的患者有效。













