胃肠胰激素分泌肿瘤属于胺前体摄取和脱羧(amine precursor uptake and decarboxylation,APUD)细胞肿瘤,多发生于胰腺,其中又以起源于胰岛β细胞的胰岛素瘤为最常见,约占胰腺内分泌肿瘤的75%,也可见于十二指肠、胃、肝门及胰腺附近。胃肠胰激素分泌肿瘤或细胞增生往往分泌一种或多种激素而有明显的临床表现,引起低血糖、糖尿病及其他代谢异常综合征。
(一)APUD细胞嗜银染阳性
胰腺内分泌肿瘤以单个多见,良性占80%~90%,而胃泌素瘤常为多发性,恶性多见。胰腺肿瘤常小于1.5cm,大而钙化的肿瘤提示恶性;恶性肿瘤常见淋巴结(胰周围淋巴结、十二指肠和肝门淋巴结)及肝内转移,其次是肺和骨骼转移。
Warren曾提出胰腺内分泌肿瘤在光学显微镜下诊断标准:细胞的形态和排列类似于正常胰岛细胞,具有完整包膜并挤压邻近胰组织,直径至少1cm。进一步研究发现,仅带状型胰腺内分泌肿瘤的细胞形态类似于正常胰岛细胞。目前认为,胰腺内分泌肿瘤有3种生长方式:①小梁型(trabecular)、带状型或脑回样型:细胞排列与正常胰岛细胞相似,含有丰富的毛细血管网,网间排列着柱状和立方形细胞;②玫瑰花结样型:细胞围绕毛细血管排列,如同玫瑰花结,这型也称为腺型、小泡型或假腺泡型;③髓状、实质性或弥漫生长型:不管哪种生长方式及产生何种激素,胰腺内分泌肿瘤内血管及结缔组织丰富,可见异型核,可有透明变性、淀粉样变、纤维化和钙化。
APUD细胞嗜银染色呈阳性反应。如醛-硫堇染色主要显示产生胰岛素的β细胞,Hell-Estrom-Hellman银浸染色显示产生SS的δ细胞,Fontana-Masson银浸染法显示肠嗜铬细胞以及Grimelius银浸染法显示胰岛α细胞、G细胞和D1(Ⅳ型)细胞。免疫组织化学可帮助确定胰岛内分泌细胞的类型。单纯的组织学难以确定肿瘤的良恶性,如果胰腺内分泌肿瘤为MEN-1的一部分,则属常染色体显性遗传病,系MEN-1基因突变引起。该基因是一种肿瘤抑制基因,含10个外显子,其突变多样化,突变基因检测是确定病理突变的有效方法。比较性基因杂交(comparative genomic hybridization,CGH)可用于判断DNA的拷贝数和抑癌基因的丢失或MEN-1基因的突变。
临床上,将能从患者血中检测到活性激素或其产物并有典型的激素过高临床表现的肿瘤称为“激素分泌性瘤”;而将无明确激素产生,无激素介导症状的肿瘤称为“非激素分泌性瘤”或“意外瘤”。非功能性胰岛瘤主要有两种情况:①肿瘤含有大量激素前体,但分泌具有生物活性的激素甚微;②肿瘤合成的生物分子未被认识。研究发现,某些非功能性胰岛瘤可分泌PP,虽无临床表现,实属有功能,称“PP瘤”。功能性胰腺内分泌肿瘤根据分泌的主要激素将其命名为激素瘤,如胃泌素瘤和胰岛素瘤等。
(二)根据组织来源分为正位胰腺内分泌瘤和异位胰腺内分泌瘤
胰岛内分泌细胞属APUD系统,在胚胎期与胃肠胰内分泌细胞一样,来源于神经嵴。因此,将胰岛内分泌肿瘤分为正位和异位胰腺内分泌瘤两类。
1.正位胰腺内分泌瘤
目前发现的共有5种:①胰岛素瘤发生于β细胞;②α细胞的胰高血糖素瘤;③δ细胞的SS瘤;④PP细胞的PP瘤;⑤肠嗜铬细胞的释放5-HT的类癌瘤。
2.异位胰腺内分泌瘤
肿瘤释放的激素在正常情况下不能由胰岛释放。例如,胃泌素瘤所分泌的胃泌素正常情况由胃窦G细胞分泌,而非胰岛分泌。异位胰腺内分泌瘤还包括VIP瘤、TSH瘤、ACTH瘤、降钙素瘤和甲状旁腺素(PTH)瘤等。这类肿瘤常为恶性,释放的多肽可有多种。其异位分泌的机制尚不明了。有人认为,胚胎期胰岛内APUD细胞的前体具有合成和分泌多种多肽的功能,正常成熟的APUD细胞含有肽酶,能将大分子的激素前体分子分解为与细胞功能相适应的小肽,而分解为其他肽类的功能受抑制。如果APUD细胞形成肿瘤,则不能生成肽酶且激素前体为原始状态,故不能转变为与细胞正常功能相应的激素,而原被抑制的功能则解抑,从而产生异位激素。
应用常规的组织病理检查可将胰腺内分泌肿瘤分为β细胞性及非β细胞性肿瘤。
(三)根据生物学行为分为良性瘤/潜在恶性瘤/低度恶性瘤/高度恶性瘤/高分化癌/低分化癌/未分化癌
胰腺内分泌肿瘤具有不同的恶性肿瘤发生率。胰岛素瘤95%为良性腺瘤,类瘤均为恶性,胃泌素瘤多为恶性。胃肠胰肿瘤的良、恶性主要取决于肿瘤的生物学行为,而非单纯组织学形态。根据其生物学行为分为良性、潜在恶性、低度恶性和高度恶性。也常根据细胞分化程度分为高分化癌、低分化癌及未分化癌。
胰腺内分泌肿瘤细胞具有摄取胺前体及对胺前体脱羧形成胺的特性。血浆激素测定与免疫组织化学检测是确定激素分泌肿瘤的主要依据。
1.神经内分泌肿瘤具有多激素分泌特点
激素浓度与生物活性不一致的原因可能是:①消化道多肽激素在细胞内合成,一般先经基因转录合成一个大分子的激素前体(激素原),而后经酶裂解并经修饰和酰化而成小分子的具有生物活性的激素分子,此种转录后的加工过程使激素存在明显的异质性(不均一性),即同一激素以一种以上的结构形式存在于体内。如胃泌素根据其羧基末端第7个酪氨酸上有无硫酸基团而分为Ⅰ式或Ⅱ式,并以肽链的长短而又分为G-14、G-17、G-34及巨大胃泌素。其异质性使高浓度激素并不具有相应的生物活力。②激素过多的临床表现,如消化性溃疡和腹泻等,常需较长时间的病理生理演变过程,故肿瘤生长可能远远早于临床征群出现。③激素经过肝脏灭活,致体循环中的浓度与门脉血中的浓度有较大差异。④多数胰腺内分泌肿瘤能产生和分泌多种激素,其中有一种是最重要的,对临床征象有决定意义,但其他伴随激素,尤其是相反作用的激素可不同程度地影响其临床表现及演变过程。⑤激素实际的生物活力在不同个体中常有很大差异,而某一患者的血浆激素浓度不一定等于该激素的体内生物活力。⑥所测激素并非肿瘤分泌的主要激素,故一般主张多项激素同时测定,如胰岛素、胰岛素原、胰高血糖素、胃泌素、PP和SS等,此外,还可选择各种激素促分泌剂(激发试验)来协助诊断。
胰腺神经内分泌肿瘤(pancreatic neuroendocrine tumors,PNET)的种类见表1。
少功能性胰腺神经内分泌肿瘤(rare-functioning pancreatic neuroendocrine tumors)是指有微弱神经内分泌激素分泌功能的神经内分泌肿瘤,且不引起症状的一种临床状态。
2.铬粒素A是神经内分泌肿瘤标志物
免疫组织化学可标记并测出某些特殊的细胞产物。铬粒素A(chromogranin A)对鉴别神经内分泌肿瘤的良、恶性有一定价值。激素原转化酶可能与胰腺内分泌肿瘤的功能特性有关。此外,胃肠胰内分泌肿瘤表达生长抑素(somatostatin,SS)受体。SS受体有5种亚型,在各种胰腺激素肿瘤中有不同的表达,可用于进一步鉴别诊断,并为SS类似物治疗提供依据。铬粒素A、铬粒素B和分泌粒蛋白Ⅱ(secretograninⅡ,SgⅡ)属于弥散性神经内分泌系统(diffuse neuroendocrine system)酸性分泌蛋白家族(acidic secretory protein family)成员,在激素分泌颗粒的形成和分泌中起重要作用。1997年,Mahata等鉴定了一种新的胃肠胰神经肽catestatin。该激素具有强烈抑制儿茶酚胺分泌的作用。人类存在3种catestatin分子类型——G(364)S、P(370)L和R(374)Q,高血压患者的血catestatin水平降低。
表1胰腺神经内分泌肿瘤的分类和临床特点
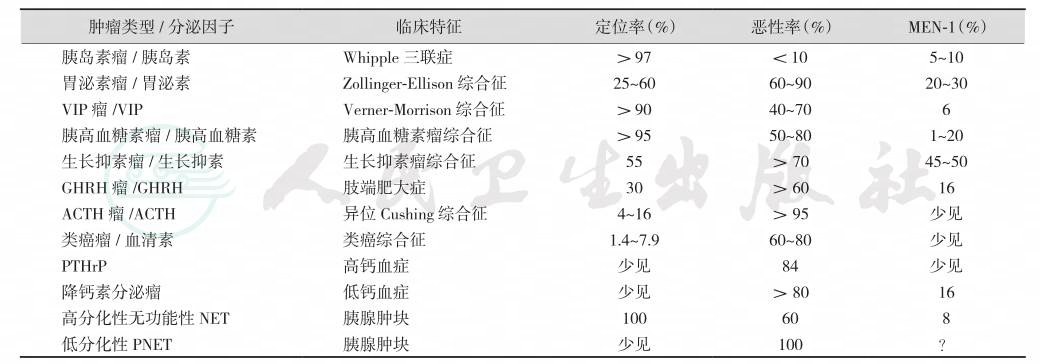
注:VIP:vasoactive intestinal polypeptide,血管活性肠肽;PTHrP:PTH-related peptide,甲状旁腺相关肽;PNET:pancreatic neuroendocrine tumors,胰腺神经内分泌肿瘤
1.抑制激素分泌和改善症状
胃肠胰内分泌肿瘤只有在诊断时已扩散转移或患者情况不能耐受手术时方考虑药物治疗控制病情,或用于术前准备和术后处理。
针对激素分泌过多,可选用调节分泌的抑制剂,如胃泌素瘤致胃酸分泌亢进,可选用抑制胃酸分泌的药物,如H2受体阻滞剂或质子泵抑制剂;二氮嗪可用来抑制β细胞分泌胰岛素;制动剂(hypomotility)如肠氯分泌抑制剂可缓解VIP瘤、胃泌素瘤和SS瘤等所致的腹泻。生长抑素(somatostatin,SS)类似物可治疗除SS瘤以外的大多数胃肠胰激素内分泌肿瘤。它不仅能抑制多种激素和氨基酸递质的释放而控制激素过多分泌症状,而且还可通过肿瘤中存在的SS受体抑制肿瘤内分泌因子,影响信号传导,发挥抗肿瘤增殖作用。但后一作用在常规剂量难以达到。有学者主张与干扰素联用。
目前应用于临床的SS类似物有奥曲肽(octreotide)和思他宁(somatostatin)等。SS类似物的应用扩大了药物治疗指征,部分肿瘤可将药物治疗作为首选方案。SS治疗胃肠胰内分泌肿瘤的常用初始剂量为0.1mg/d,分1~2次皮下注射,渐次增至每次0.2mg,每天3次至临床症状和实验室检查改善后,改用维持量,疗程10~14天。对于胰岛素瘤患者,可能加重低血糖症状,影响环孢素和西咪替丁的吸收,应注意观察。本品的主要不良反应为消化道症状,一般不需要特殊处理。临床可用奥曲肽治疗的内分泌肿瘤见表5。
表5奥曲肽对内分泌肿瘤的治疗作用
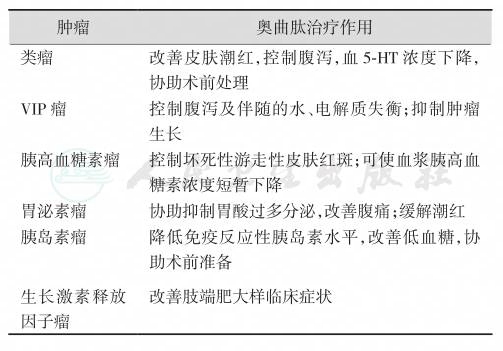
此外,胃肠胰激素分泌肿瘤大多存在SS受体,可利用它与SS多肽及其类似物耦联的核素发挥其导向作用及抗肿瘤作用,如采用放射性核素(111In-DTPA或123I-Tyr3)标记的奥曲肽治疗。
2.化疗
链佐星对于恶性胰岛素瘤,氮烯唑胺对于胰高血糖素瘤和VIP瘤均有一定疗效。链佐星为胰岛β细胞选择性细胞毒性药物,可抑制胰岛β细胞DNA合成,缓解有效率70%左右。常用剂量为每天500mg/m2,连续5天,或每周1.5g/m2,持续6 周,也可加用5-氟尿嘧啶或阿霉素。













