英文名称 :gastroenteropancreatic neuroendocrine neoplasms
神经内分泌肿瘤(neuroendocrine neoplasm,NEN)是一类起源于胚胎神经内分泌细胞、具有神经内分泌标记物、可以产生生物活性胺和/或多肽激素的肿瘤。其中,胃肠胰神经内分泌肿瘤(gastroenteropancreatic neuroendocrine neoplasm,GEP-NEN)原发于胃黏膜、小肠和大肠、直肠或胰腺等,常分为胰腺神经内分泌肿瘤(pancreatic neuroendocrine neoplasm,pNEN)和胃肠道神经内分泌肿瘤(gastrointestinal neuroendocrine neoplasm,GINEN)两大部分。依据胚胎起源,GEP-NEN可以分为前肠肿瘤(胃、十二指肠、胰腺)、中肠肿瘤(空肠、回肠、盲肠、阑尾、升结肠)和后肠肿瘤(左半结肠、直肠)。GEP-NEN能够产生5-羟色胺(5-HT)代谢产物或多肽激素,如胰高血糖素、胰岛素、促胃液素或促肾上腺皮质激素等,出现皮肤潮红、腹痛、腹泻、支气管痉挛和心瓣膜病变等多种复杂临床表现,称为类癌综合征(carcinoid syndrome),临床上出现典型症状者少见。
本病病因尚未阐明。GEP-NEN是一种能产生小分子多肽类或肽类激素的肿瘤,故又称小分子多肽或肽类结构瘤,它除能分泌具有强烈生物活性的5-HT、血管舒缓素和组胺外,还可分泌其他肽类的激素,如促肾上腺皮质激素、儿茶酚胺、生长激素、甲状旁腺激素、降钙素、血管升压素、促性腺激素、胰岛素、胰高血糖素、前列腺素、促胃液素、胃动素等物质。
NEN曾被认为是一种罕见肿瘤,近年来发病率和患病率均显著上升,其中,GEP-NEN约占全身NEN的55%。美国监测、流行病学与最终结果(SEER)数据库数据显示,NEN发病率5.25/10万;日本的资料表明,pNEN的年发病率为2.23/10万;我国最新研究显示,NEN发病率在12年间上升了5倍。GEPNEN可发生于任何年龄,阑尾NEN的发病年龄较轻,平均30岁,其他部位的NEN发病年龄平均50岁左右。pNEN总体发病率≤1/10万,占所有胰腺肿瘤的1%~2%,但过去20年间,pNEN发病率日益升高,可能与影像学、超声内镜检查普及化相关,提高了无症状患者的检出率。据一项我国的回顾性统计分析报道,GEP-NEN中以pNEN最为常见,占49.8%,其次为直肠NEN,占24.3%,阑尾 NEN占 11.1%,其他部位 NEN均未超过10%。
NEN根据所在部位可分为六类。
(一)食管神经内分泌肿瘤
罕见。常发生于食管胃连接处,大多数为高度恶性未分化神经内分泌癌,典型NEN极罕见。肿瘤较大,直径>4cm,呈息肉蕈伞状或溃疡硬化型。
(二)胃神经内分泌肿瘤(gastric neuroendocrine neoplasm,GNEN)
罕见。可分为四型:1型GNEN由自身免疫性萎缩性胃炎继发胃酸缺乏引起,常表现为胃底、胃体多发息肉,多数预后良好(NEN G1)。2型GNEN则是由于胃泌素瘤分泌大量激素导致高胃泌素血症引起,绝大部分患者胃多发性内分泌肿瘤1型(multiple endocrine neoplasia-1,MEN1)合并十二指肠NEN或pNEN。3型GNEN多为散发,无促胃液素升高,可以是 G1、G2或 G3。4型较少见,恶性度较高(NEN G3),生物学行为类似胃腺癌。
(三)小肠神经内分泌肿瘤
相对较多见。占小肠肿瘤的30%~50%,大多由于发现转移灶后寻找原发灶或不经意间发现。原发灶引起的最常见症状为非特异性腹痛,其原因为小肠蠕动障碍、小肠梗阻及肠系膜纤维化引起的肠系膜缺血等。
(四)阑尾神经内分泌肿瘤
较常见。阑尾NEN占阑尾肿瘤50%以上,占胃肠道NEN的20%。多发生于中年人(中位数年龄为40岁)。阑尾可以发生杯状细胞类癌、小管状类癌和混合性腺神经内分泌癌(mixed adenoendoecrine carcinoma,MANEC)。
(五)结直肠神经内分泌肿瘤
结肠NEN的发生率较低,但直肠却是NEN的好发部位之一,占10%~20%。直肠NEN大多表现为直肠息肉,总的转移率为23%。直径<1cm的息肉发生淋巴结转移率为1%~4%;直径>2cm的息肉,以及淋巴血管受侵犯的直肠NEN更易发生转移。
(六)胰腺神经内分泌肿瘤
常见的有胃泌素瘤(gastrinoma),比较罕见的包括胰高血糖素瘤、生长抑素瘤、舒血管肠肽瘤(VIP瘤)等。胃泌素瘤又称佐林格-埃利森综合征(Zollinger-Ellison syndrome,ZES),是由胃酸分泌过多导致严重的酸相关性消化道疾病和腹泻,一般是由十二指肠NEN或pNEN分泌胃泌素导致。VIP瘤是一种罕见、分泌VIP的功能性NEN。95%以上成人VIP瘤发生于胰腺内,儿童VIP瘤可发生于交感神经节和肾上腺。
典型的GEP-NEN常为细小的黄色或灰白色黏膜下结节样肿块,单发或多发,黏膜表面多完整。其形态不一,可呈结节状、息肉样或环状等。少数癌瘤表面可形成溃疡,外观酷似腺癌,常侵入肌层和浆膜层,一部分患者可有多源性NEN存在。
NEN细胞在显微镜下呈正方形、柱状、多边形或圆形。细胞核均匀一致,很少有核分裂象,细胞质内含有嗜酸颗粒。这些细胞能产生大量神经内分泌颗粒,病理免疫组织化学表现可见弥漫性分布高表达的神经内分泌标记物,如突触和嗜铬粒蛋白。此外,一些肿瘤会分泌特定的肽类激素或生物胺,如胰岛素、胰高血糖素、促生长素抑制素(简称生长抑素)、血管活性肠肽、5-HT、促胃液素等,临床表现为激素综合征。
WHO对NEN及 pNEN的分级分别见表1和表2。
表1WHO神经内分泌肿瘤分级(2010年)

引自:实用内科学.第16版.ISBN:978-7-117-32482-3
表22019年WHO第5版胃肠胰神经内分泌肿瘤病理学分类和分级标准
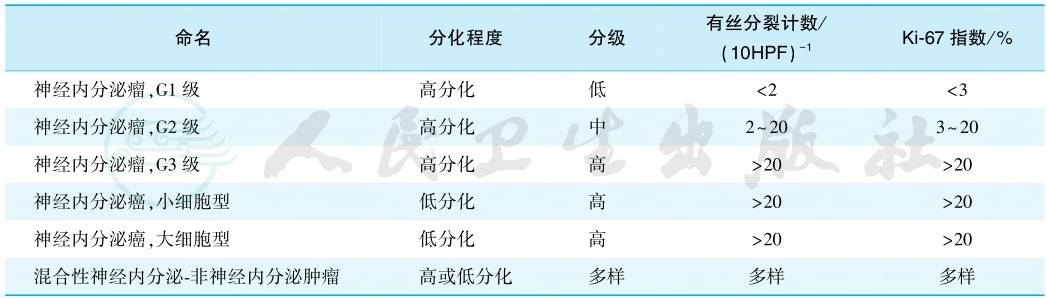
引自:实用内科学.第16版.ISBN:978-7-117-32482-3
NEN可以浸润生长,直接穿透浆膜至周围组织内,亦可发生淋巴转移或血行转移。血行转移以肝脏最为多见,亦可转移至骨、肺、脑及其他部位。
(一)血清嗜铬粒蛋白(chromogranin,Cg)
分为 A、B两型。CgA,是NEN中最常用、最有效的肿瘤标志物,诊断NEN的敏感度和特异度可达70%~90%。血浆CgA诊断NEN水平可能与肿瘤的大小有关,生长抑素类似物(somatostatin analogs,SSA)可降低CgA水平;使用质子泵抑制剂(PPI)、肝肾衰竭、心力衰竭、肝细胞癌、甲状腺髓样癌、慢性胃炎患者血浆CgA有假性升高现象。
(二)各种肽类激素的测定
主要用于功能性GI-NEN的诊断,对于出现各种临床综合征时应考虑相应激素的检测。
(三)5-HT及其代谢产物测定
血5-HT或其代谢产物尿5-HIAA的测定在类癌综合征的诊断中起关键作用。正常人尿5-HIAA排量为2~8mg/d,>10mg/d可肯定为阳性。血5-HT正常值为80μg/L,>130μg/L 为阳性。
(四)激发试验
对于激素水平轻度升高患者,必要时可行激发试验以明确诊断。
1.皮肤潮红激发试验
①将10ml乙醇加入15ml橘子汁中口服,3~5分钟后,约1/3患者出现皮肤潮红;②静脉注射去甲肾上腺素15~20μg,肾上腺素5~10μg。此两种激发试验对诊断有一定的帮助,但有心律失常、心功能不全、哮喘史患者慎用。
2.五肽胃泌素激发试验
可辅助类癌综合征的诊断。方法是:给患者静脉注射五肽胃泌素(0.6μg/kg,30秒内注毕),于注射前和注射后1、3、5、10、15分钟取血测 5-HT。
(一)内镜检查
是GI-NEN首选的检查措施,内镜检查结合病变部位的活检使很多类癌在早期能够被检出。超声内镜扫描不仅可用来诊断类癌,还可评估类癌的浸润深度及是否有淋巴结转移。超声内镜不仅对GNEN具有较好的诊断价值,而且对于pNEN可以在超声内镜引导下行细针穿刺活检。若考虑病变位于小肠,胶囊内镜在发现隐匿的小肠NEN方面具有优势,其不足之处在于胶囊内镜通常无法实现对小肠肿瘤的精确定位。
(二)影像诊断
胃肠道X线造影、超声、CT、血管造影、PET等检查,有助于NEN的定位诊断,寻找原发灶和转移瘤,对根治和延长生存期有重要意义。CT和超声可检出10%的最大直径<1cm的肿瘤,CT对最大直径>3cm的肿瘤检出率为100%,MRI对于原发肿瘤的检出率仅为50%,对于转移灶的检出率为80%。
(三)核医学检查
在GI-NEN定位诊断中具有很好的应用前景。碘-131-间位碘代苄胍(iodine-131-metaio-dobenzylguanidine,131I-MIBG)也可用于胃肠及其他NEN的诊断,敏感度为55%。
(四)推荐采取多途径的辅助检查
GI-NEN主要通过内镜和镜下活检病理组织学和免疫组织化学诊断,超声内镜可以协助局部肿瘤的分期和内镜下的息肉切除,还可以协助术前评估及获取组织学检查。pNEN首选超声、CT、MRI检查明确病灶部位和大小。对于原发灶不明的NEN和初发肿瘤的分期,以及治疗后的随访,立体定向放射外科(stereotactic radi-osurgery,SRS)与PET/CT具有较好的诊断价值。
(一)手术治疗
手术切除原发病灶是最有效的治疗方法。早期手术效果好,即使发生转移,切除大的原发病灶也能减轻和消除症状。
(二)内镜治疗
随着内镜技术的不断进步,内镜治疗占据了越来越重要的地位,其中,越来越多研究表明内镜黏膜下剥离术(ESD)在 GI-NEN中治疗是安全有效的。对1型GNEN、直径≤1cm的十二指肠 NEN及直径<2cm的结直肠NEN可以考虑行内镜下治疗。
(三)一般内科治疗
包括对症支持治疗和控制相关症状。对于激素分泌导致的相关症状,如ZES、类癌综合征或异位皮质醇增多症可分别使用PPI、SSA和肾上腺素受体拮抗药控制相关症状。
1.生物治疗
生物治疗主要包括SSA和干扰素两类。治疗指征:生长抑素主要适用于分化良好、级别较低(G1/G2)和生长抑素受体(somatostatin receptor,SSTR)阳性(G3)的患者;我国专家共识也建议将长效奥曲肽作为有功能或无功能进展期中肠NEN(G1)的一线治疗。干扰素也主要用于G1期和G2期患者的治疗,其中α干扰素(IFN-α)应用最多。美国国立综合癌症网络(National Comprehensive Cancer Network,NCCN)指南推荐首选SSA,进展后加用依维莫司,欧洲神经内分泌肿瘤学会(European Neuroendocrine Tumor Society,ENETS)推荐生长缓慢者首选SSA,生长迅速者首选依维莫司,进展后用化疗或肽受体放射性核素治疗(peptide receptor radionuclide therapy,PRRT)等。
(1)生长抑素及其类似物的应用
生长抑素具有抑制多种激素释放的功能,因而已用于多种内分泌肿瘤的治疗。人工合成的生长抑素八肽类似物奥曲肽,半衰期约100分钟,每日注射3次治疗类癌综合征可获较满意的疗效,可在数分钟内使皮肤潮红消退,数小时内使腹泻停止。奥曲肽对NEN危象亦有很好的疗效,静脉注射剂量为100μg。
(2)干扰素
IFN-α可抑制类癌生长,有效率达40%~50%,15%的肿瘤体积可缩小,主要不良反应为疲劳、类流感症状。
2.化学治疗
总体来说GEP-NEN对化学治疗(简称化疗)的敏感度不高,尤其是高分化的肿瘤,对于有丝分裂率较低的肿瘤来说,化疗有效率通常低于30%。
(1)化疗方案的选择
霉素联合5-氟尿嘧啶(5-FU)和/或表柔比星治疗G1/G2期的pNEN已有较多证据。目前,ENETS及北美神经内分泌肿瘤学会(North American Neuroendocrine Tumor Society,NANETS)均推荐顺铂联合依托泊苷治疗GEP-NEN。
(2)肝脏介入治疗
肝脏血供丰富,是GI-NEN远处转移的主要器官之一,对于NEN肝转移瘤,肝动脉化疗和栓塞治疗展现了很有希望的前景。联合应用肝动脉化疗和栓塞,效果较好,患者最长存活达6年,pNEN肝转移者行该治疗后生存时间为20~36个月。
3.分子靶向治疗
GI-NEN肿瘤细胞均可表达血管内皮生长因子(VEGF)及其受体、血小板衍生生长因子(PDGF)及其受体、成纤维细胞生长因子(FGF)及其受体等促血管生成因子,作用于VEGF受体、PDGF受体等多个靶点的受体酪氨酸激酶(RTK)抑制剂舒尼替尼已经在晚期pNEN中完成了Ⅲ期临床试验,结果证实,与安慰剂比较能显著延长晚期高分化pNEN的无进展生存期(11.4个月vs.5.5个月)。
4.肽受体放射性核素治疗(PRRT)
很多GEP-NEN表达生长抑素受体,当生长抑素受体显像(SRS)提示病灶有放射性摄取时,镥-177(171Lu)标记的长效奥曲肽类似物可作为一种治疗选择。
5.支持疗法
食物富于营养和热量,补充蛋白质,给予足够维生素。避免可诱发皮肤潮红和腹泻的食物,如牛奶制品、蛋类、柑橘等。













