绝经(menopause)指卵巢功能停止所致永久性无月经状态。绝经的判断是回顾性的,停经后12个月随诊方可判定绝经。围绝经期(perimenopausal period)指妇女从生育期的规律月经过渡到绝经的阶段,包括从出现与卵巢功能下降有关的内分泌、生物学和临床特经起,至末次月经后一年。共同的表现是出现月经的不规则,介于40~60岁之间。绝经综合征(climacteric syndrome或 menopausal syndrome,MPS)是指在此时期由于卵巢功能衰退而引起的下丘脑-垂体-卵巢轴功能障碍,出现一系列躯体症状的综合征。
绝经可分为自然绝经(natural menopause)和人工绝经(induced menopause)两种。前者指卵巢内卵泡耗竭,或残余的卵泡对促性腺激素丧失了反应,卵泡不再发育和分泌雌激素,导致绝经。后者是指手术切除双侧卵巢或放疗和化疗等损伤卵巢功能。
近几十年来,妇女寿命延长,我国妇女平均寿命达75岁,而绝经年龄并无改变。因而许多妇女一生中,有1/3的时间在绝经后度过。围绝经期妇女由于卵巢功能逐渐降低,体内雌激素降低,常出现围绝经期症状,严重影响妇女的生活质量。围绝经期为一种自然现象,对机体无大妨碍。但一些患者的症状很重,影响生活。绝经后易并发泌尿生殖系感染、老年性阴道炎、性交疼痛、温度波动过大、感觉异常、精神病样发作、骨质疏松症、糖代谢异常和高血压等。
病理性绝经是由于下丘脑-垂体-卵巢轴病变(性染色体异常、卵巢发育不全、肿瘤、炎症和药物)或全身疾病(甲状腺疾病、肾上腺疾病、贫血、营养不良和免疫缺陷等)所致。人工绝经是基于某些疾病治疗的需要,手术切除或放疗致卵巢功能永久性损害所致。自然绝经是由于卵泡数目逐年减少终至排卵停止,以致绝经。卵细胞数目随增龄呈指数减少,并且这种减少是不可逆性的,源于出生后卵母细胞的消失。少女初潮时,双卵巢卵泡总数约40万~50万个,发育期排卵400~500个,余者归于闭锁。30岁时卵泡数目开始减少,37.5岁时卵泡数目减至25 000个,以后卵泡数目以不可思议的速度减少,接近51岁时只剩余1000个。可以根据卵泡细胞的数目,依照数学模型来预测绝经的年龄。当卵泡消耗殆尽或残留卵泡对促性腺激素不发生反应时,卵泡停止发育,不再合成激素而发生绝经,HPO轴出现相应的变化。
(一)肾上腺和外周组织转化
女性的雌激素来源于以下组织:①卵巢;②皮肤细胞(主要为皮肤成纤维细胞);③脂肪细胞(包括皮下脂肪细胞);④下丘脑;⑤乳腺癌细胞和异位的子宫内膜细胞。当卵泡发育减缓或停止时,雌二醇(E2)减少,循环雌酮(E1)减少的幅度较E2小,因而 E2/E1下降。绝经后,肾上腺是分泌雌激素的主要来源。但由肾上腺或卵巢直接分泌的不多,大部分来自雄烯二酮在外周组织(脂肪、皮肤、肌肉、肝、肠)的转化。绝经后,雌激素的外周平均转化率是有排卵妇女的2倍(转化率2.8%~6.5%),肥胖者更高。E1可还原为E2,因此绝经后雌激素生成从腺内(卵巢)向腺外(外周)转移,雌激素形式从E2向E1转移。绝经后雌酮代谢清除率减少20%,平均生成率为55μg/d;E2代谢清除率下降30%,平均生成率为12μg/d。研究发现,绝经后雌激素受体两种亚型(ERα和ERβ)的表达水平与绝经前有显著的差异,绝经期ERβ表达明显降低,而这两种亚型皆存在于调节生物节律的视交叉上核,提示绝经前后ER亚型的改变可能与围绝经期症状有关。孕激素由卵巢黄体合成,排卵后无黄体形成,则不能合成孕激素。绝经后孕酮水平仅为绝经前卵泡期孕酮水平的30%。老年妇女存在的少量孕酮来自肾上腺。雄激素在女性体内有重要的生理作用。老龄妇女的卵巢和肾上腺雄激素减少对健康有明显影响,特别是心血管功能。因此,绝经后妇女常采用去氢异雄酮或睾酮替代治疗。
(二)绝经后卵巢分泌睾酮增多
虽然女性的血清雄激素水平较男性低20~25倍,但因为雄激素是合成雌激素的前体,所以雄激素在卵泡成熟过程中仍然起了十分重要的作用。老年女性雄激素缺乏可引起性功能和肝功能障碍、情绪低落、肌力不足和骨质疏松。女性30~40岁后睾酮水平降低,绝经时降至绝经前水平的15%左右,绝经后2~5年内进一步下降约60%。因此,适当补充雄激素有益于绝经后女性的健康。
绝经后循环雄激素减少,雄烯二酮生成率为1.6mg/d,为绝经前的50%,睾酮轻度降低,睾酮生成率约为150μg/24h,仅较年轻者低1/3。绝经后卵巢直接分泌的睾酮比绝经前显著增多,其原因为过多的促性腺激素刺激,卵鞘膜细胞、间质细胞和门细胞呈不同程度增生而致雄激素增高,同时缺乏雌激素的对抗,从而某些老年妇女可出现肥胖、多毛甚至男性化表现。游离睾酮较生育期妇女轻度降低,而结合睾酮较绝经前增高50%,结合睾酮的升高主要由于血清中的性激素结合球蛋白(SHBG)增高。绝经后SHBG升高约44%。体外试验发现,IGF-1抑制SHBG生成,随着年龄老化,这种抑制作用逐渐减弱,从而出现SHBG增高。内脏型肥胖更易发生于绝经后女性,但在肥胖女性中并没有明显的激素水平变化,而只表现在体质指数(BMI)与SHBG的明显相关性,两者之间呈负相关变化。绝经后肾上腺脱氢异雄酮(DHEA)和硫酸脱氢异雄酮(DHEAS)明显下降。DHEA生成率为4.91mg/d,为绝经前的35%~40%;DHEAS生成率为(18.3±6.1)mg/d,为绝经前的40%。这些激素的减少是否与绝经或衰老有关尚不清楚。DHEA和DHEAS分泌的明显下降提示肾上腺激素分泌功能已发生改变。
(三)FSH和抑制素调节紊乱
围绝经期可分为三个时期:①Ⅰ期:下丘脑-垂体功能活跃期,FSH开始升高,卵巢对促性腺激素的敏感性降低,性激素合成减少。②Ⅱ期:排卵和黄体功能衰竭,无排卵和存在黄体功能不全,但仍有部分雌激素分泌,致月经失调、功能性子宫出血、子宫内膜增生过度和内膜癌。③Ⅲ期:卵巢卵泡衰竭,卵泡耗竭殆尽,性激素匮乏、绝经。性激素生成转向外周组织和肾上腺。
绝经意味着月经永久性的终止,是卵泡功能衰竭的结果。FSH是反应卵泡活性确切的间接指标。基础FSH水平升高与卵巢的储备力降低有关。卵巢功能衰竭的最早变化是FSH的升高。垂体FSH的释放受卵巢负反馈抑制较LH敏感,卵巢功能下降使垂体FSH分泌增多,文献报道FSH基础值>10U/L是卵巢功能开始衰竭的激素特征。绝经后(>50岁)FSH急剧升高。绝经2~3年时可达最高水平,此时FSH约为正常卵泡期的13~14倍。LH缓慢升高,约为正常卵泡期的3倍,持续5~10年之久。绝经后两种促性腺激素仍呈脉冲性释放,频率与绝经前卵泡期类似,但幅度更大些。幅度增大的原因是下丘脑激素GnRH的释放增加和低雌激素水平引起的垂体对GnRH反应性增强。受雌激素降低的影响,PRL分泌减少,而TSH、GH、ACTH分泌仍正常。抑制素(INH-B)是卵巢颗粒细胞分泌的一种异二聚体蛋白质,峰值主要出现于卵泡早期,调节FSH的分泌。在围绝经期时,分泌减少,使FSH升高;INH-B比基础FSH和E2水平更能直接且灵敏地反映卵巢的储备力。
(四)肾上腺雄激素变化
肾上腺类固醇激素生成的两条基本途径见图1,睾酮和雄烯二酮与受体相互作用的机制见图2。肾上腺皮质的雄激素生成随着增龄而逐年下降,而在绝经过渡期血清DHEAS升高,而绝经过渡期FSH升高,E2下降。
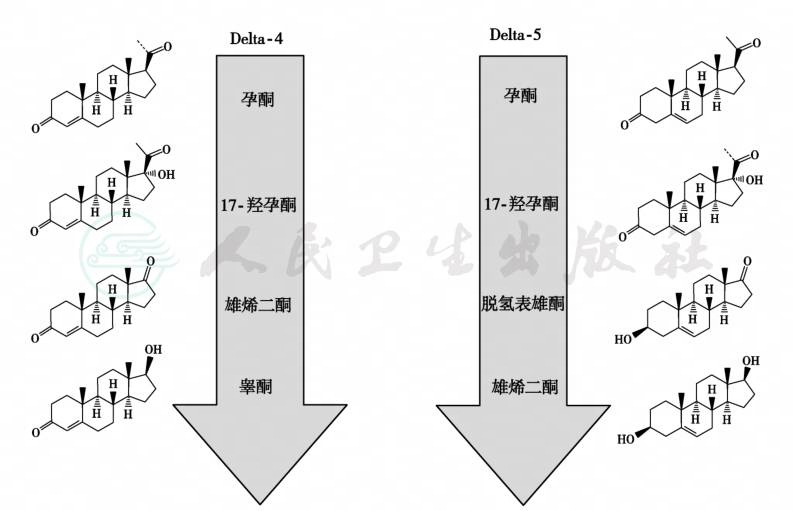
图1 肾上腺类固醇激素生成的两条基本途径
δ-4途径是盐皮质激素、糖皮质激素和雄烯二酮与睾酮的关键代谢途径;雄烯二酮与睾酮在外周组织芳香化为雌激素;δ-5途径是生成去氢异雄酮和去氢异雄酮硫酸盐的关键途径,去氢异雄酮又转化为许多生物活性固醇类物质的底物;类固醇合酶3-β-羟类固醇脱氢酶(或δ4/5异构酶)将δ-5转换为δ-4激素
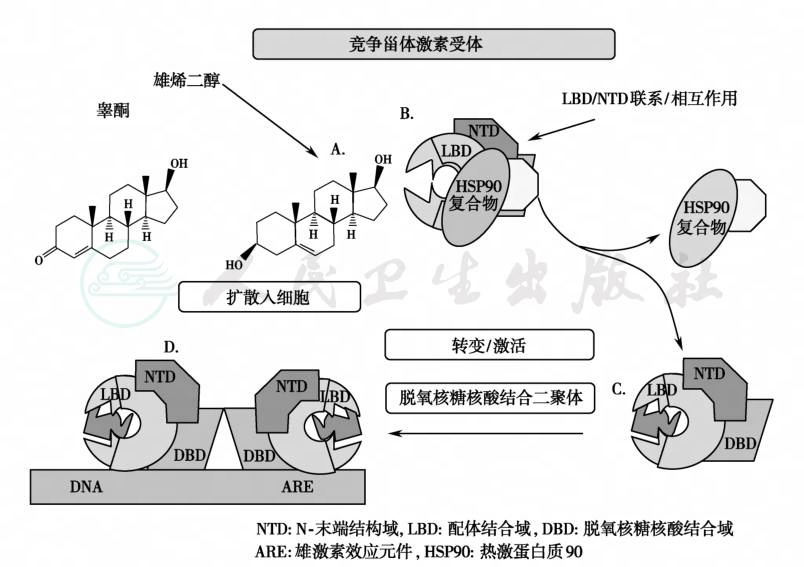
图2 睾酮和雄烯二酮与受体相互作用的机制
睾酮或雄烯二酮相互竞争雄激素受体;A.雄烯二酮与受体的结合亲和力低,如果其浓度很高,可提高结合量;中年女性雄烯二酮浓度高于睾酮1倍,故能与受体的配体结合域(LBD)结合;B/C.与配体结合后的受体复合物从热休克蛋白中解偶联,并与受体的配体结合区形成单体(monimer)而暴露;D.两个单体结合成二聚体作用于DNA雄激素结合元件(ARE),启动靶基因表达
(一)激素检查
1.选择性激素测定
有助于判断卵巢功能状态,FSH>40U/L,提示卵巢功能衰竭。绝经后 FSH>40U/L,LH>30U/L,FSH上升早,上升较LH高,测定血浆FSH、LH和雌二醇水平有助于诊断。如切除子宫保留卵巢手术后的患者,血E2<73pmol/L,同时FSH和LH升高提示卵巢功能已衰竭。正常年轻妇女雌二醇水平与在绝经后妇女中所观察到的雌二醇水平不出现重叠,由于卵巢功能减退,血雌二醇常<73pmol/L。雌酮在绝经前后有明显重叠,因此测量雌酮对了解患者的卵巢功能状态无帮助。绝经后妇女血浆雄烯二酮浓度减少约50%,约为2.1nmol/L,血浆睾酮轻度下降(约0.87nmol/L),60~70岁的妇女血浆DHEA和DHEAS平均水平分别降至6.2nmol/L和0.78μmol/L。绝经后孕酮水平显著降低,约 0.17ng/ml。
2.血清抑制素(inhibin B)
≤45ng//L是提示卵巢功能衰退的最早标志,比FSH更敏感。
3.抗米勒激素(AMH)
AMH≤0.5~1.0ng/L预示卵巢储备功能下降。
(二)特殊检查
1.超声检查
有助于明确某些病理性闭经的病因。盆腔超声检查,测定子宫内膜厚度以确定患者是否存在子宫内膜增生或子宫内膜癌。卵巢B超检查有助于明确某些病理性闭经的病因。
2.阴道脱落细胞涂片
绝经后妇女应用阴道脱落细胞涂片仅能对雌激素状态粗略估计,不能用作指导替代疗法的指标。有1/4的妇女早在绝经前数年,阴道涂片即显示雌激素水平有不同程度的低落。相反,绝经后妇女阴道涂片检查显示有雌激素的影响。评价脱落阴道上皮细胞时,不仅要考虑到雌激素活性的影响,还应想到其他激素(尤其是孕酮和睾酮)、局部阴道炎症、阴道出血或癌症的存在,刮取标本的部位和靶器官(阴道上皮)对雌激素反应的差异等因素也会影响涂片的结果。因此,在绝经后妇女应用阴道脱落细胞涂片分析结果时,应注意:①涂片仅为一种对雌激素状态的粗略测量方法,有时可能完全被误解;②阴道细胞图像不能预测患者是否出现围绝经期的症状和体征;③涂片结果不能用作指导替代疗法的唯一方法;④治疗阴道萎缩前涂片,有助于确定雌激素的用量。
3.分段诊断性刮宫和内膜活检
有绝经后流血者,应作分段诊断性刮宫和内膜活检以除外宫颈病变和子宫内膜癌。刮宫需分别在宫颈、宫体内取材,分别送检查,围绝经期妇女由于无孕酮的拮抗作用,子宫内膜多呈增殖期改变,对外源性孕激素有撤退性出血反应,也可呈萎缩改变。
4.骨密度测定
可确定有无骨质疏松并发症。
(三)鉴别诊断
许多疾病均可引起与围绝经期相似的症状和体征,一般来说,根据其临床表现可作出初步诊断。
1.伴潮热症状的其他疾病
如甲亢、嗜铬细胞瘤、类癌综合征、糖尿病神经病变、烟碱酸过量、结核和其他慢性感染等。上述疾病产生的皮肤潮红不具备围绝经期潮热发作的特点(持续时间、身体上的特殊分布等)。另外,如患者有皮肤潮红症状而无其他围绝经期表现,应进一步做激素测定检查等。
2.异常阴道出血
40~50岁的患者有月经周期延长和月经量减少,可能是绝经期卵巢功能衰退所致,不必行内膜活检,但如果出现月经频发、月经增多或月经间期子宫出血,应检查子宫内膜。常采用内膜活检法和扩宫刮宫法。绝经6个月后卵巢功能活动再发阴道出血,常与器质性病变有关。此外,许多特殊的外阴和阴道病变(如滴虫性阴道炎、阴道念珠菌病)的表现酷似雌激素缺乏引起的外阴阴道炎,常需特殊检查明确诊断。
3.心悸与高血压
围绝经期综合征常伴有心悸、头昏等症状,需与神经症、冠心病、高血压和甲亢等鉴别。若无围绝经期所特有的症状(发作性潮热),应进行较全面的检查,排除器质性疾病的可能。
4.卵巢早衰
如围绝经期综合征发生于40岁前,要想到卵巢早衰可能。对这些患者应做以下的检查:①血FSH≥40U/L,LH反复升高(提示为卵巢早衰);②其他自身免疫性疾病的实验室依据(协助卵巢早衰的诊断);③半乳糖血症的相关检查;④卵巢的影像学检查(排除卵巢肿瘤可能)。
只要卵巢有一定功能,可维持一定程度的阴道出血,一般不需治疗。但少许患者尚存月经功能时,即有潮热症状,需要性激素治疗。对于有围绝经期症状的患者应进行心理咨询,充分解释围绝经期症状属生理性变化,以消除其思想顾虑,减轻其焦虑、忧郁和睡眠障碍等症状。
(一)雌激素制剂
大量的临床试验证实,无论何种形式的雌激素治疗,都能改善生殖道和血管舒缩障碍症状,有效地防治骨质疏松,但有增加静脉血栓、卒中和子宫内膜癌等的风险。雌激素治疗经大型的RCT研究被发现可增加心血管病风险而受到质疑。目前,雌激素主要用于解除血管症状。由于雌激素替代治疗可能带来某些并发症,因此对每一患者用药利弊要进行具体评价。
1.ERT/HRT的绝对禁忌证和相对禁忌证
ERT/HRT的绝对禁忌证:①原因不明的阴道出血;②急性肝脏疾病和慢性肝功能损害;③急性血管栓塞(有或无栓子形成);④神经血管性疾病;⑤近期发生的子宫内膜癌及乳腺癌。ERT/HRT的相对禁忌证:①癫痫发作史;②严重高血压、乳腺囊性纤维性疾病、子宫肌瘤或胶原病;③家族性高脂血症或糖尿病;④偏头痛、慢性血栓栓塞性静脉炎、胆囊疾病、子宫内膜异位症及慢性囊性乳腺炎。偏头痛主要发生于女性,雌激素似乎有独到疗效,但仍需注意雌激素的禁忌证。
E2在体外有一定的抗炎作用,促进NO和前列腺素生成。选择性雌激素受体调节剂刺激ERα和ERβ调节活动功能,AF-1和AF-2膜受体也间接导致基因转录。而且E2的血管保护作用并不需要AF-1的参与,而生殖系统的靶细胞则必须存在AF-1。所以选择性雌激素受体调节剂因为不刺激ER-α-AF-1而具有血管保护作用。
2.使用方法
见表3。
表3 雌激素替代治疗药物与用量
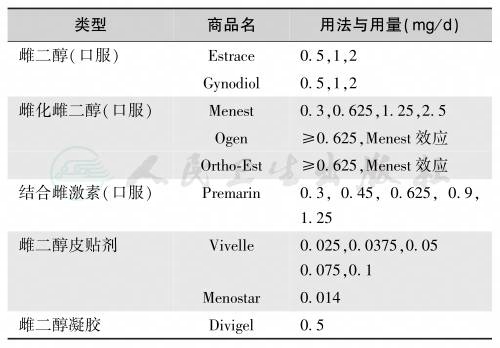
(1)ERT
仅适用于子宫切除不需要保护子宫内膜的妇女。主要为连续用药方式。单纯雌激素周期疗法以结合雌激素0.625mg/d或其他等量雌激素,每月服25天,停药5天。
(2)HRT
单用雌激素引起子宫内膜增生,因而主张雌、孕激素联合使用,适用于子宫完整的妇女,加用孕激素的目的除对抗雌激素促子宫内膜过度生长的作用外,还对增进新骨形成可能有协调作用。血管症状和阴道萎缩仅用小剂量雌激素短期治疗,且疗效并未得到肯定。另外,考虑到阴道局部使用仍然可能进入血液循环,主张改用选择性雌激素受体调节剂如巴多昔芬(bazedoxifene)和雌激素激动剂(estrogen agonist)。
雌激素结合孕激素0.625mg/d或相当剂量的其他雌激素,孕激素用甲羟孕酮2.5~5mg/d。有以下两种服用方式:①雌孕激素序贯应用:适用于年龄较轻,绝经早期,能够接受周期性阴道出血的妇女。模拟生理周期,在用雌激素的基础上每月加用孕激素10~14天。又分为周期性和连续性两种。周期性方案:每月的前25天每天使用雌激素,孕激素通常加用在周期的第12~16天之间,第25天之后雌、孕激素均停用。连续性方案:每天使用雌激素,在每月的第1~14天或每月最后的10~14天之间加用孕激素。②雌、孕激素连续联合应用:适用于年龄较长,不愿有周期性阴道出血的妇女。雌、孕激素每天连续使用。
(3)单用孕激素
当应用外源性雌激素/孕激素治疗时,因为两者的比例不当或存在妇科疾病(如月经紊乱、PCOS、肥胖、低SHBG血症等)仍然可以出现孕激素缺乏,其表现是黄体功能不全、子宫内膜增生甚至子宫内膜癌。肥胖使孕激素缺乏的症状进一步加重,因此PCOS患者在进入围绝经期后,容易发生子宫内膜增生甚至子宫内膜癌。周期性使用孕激素适用于绝经过渡期,如用醋酸甲羟孕酮10mg/d,共用5~7天。连续性短期使用孕激素适用于绝经后症状重,需要用HRT但又存在雌激素禁忌证的妇女。
(4)合用雄激素
可促进蛋白质合成,改善全身状况,拮抗雌激素作用,抑制子宫内膜增长,协同雌激素加强对下丘脑的抑制作用,加强性欲,防治骨质疏松,该方法并不降低雌激素对心脑血管的保护作用,且具有协同和互补作用。临床上适用以下情况:①绝经后单用雌激素围绝经期症状不能缓解者;②绝经前行双卵巢切除的妇女,内源性雌、雄激素均减少者;③骨质疏松明显者;④性功能明显下降者。用法:雌激素配甲睾酮或替勃龙(tibolone)1.25~2.5mg/d,共 21天,重复用药3~6个周期。
(二)其他药物治疗
组织选择性雌激素复合物和地文拉法辛(desvenlafaxine),或者改用非激素类药物,如阿普唑仑、地西泮,加巴喷丁(gabapentin)与可乐定等缓解症状。瑜伽、针刺、运动和磁疗亦有裨益。
1.选择性雌激素受体调节剂
可通过增高内啡肽水平而发挥作用,对子宫内膜无刺激作用。不出现撤退性出血,对下生殖道有轻度雌激素效应,能抑制骨质吸收,减缓骨质疏松症的发生。每次1.25~2.5mg,每天1次,最好每天固定在同一时间服用,用药6周后,症状能明显改善,可连续长期服用。外用SERM适用于糖尿病、肝病、心血管疾病及肥胖的患者,如爱斯妥凝胶(Estradilum):为天然雌二醇透皮吸收制剂。涂于皮肤透皮吸收后,暂时储存于皮下组织中并缓慢释出,用药期间药物血浆浓度平稳,无首关效应,无肝脏损害。每天早晨或晚间涂于上臂、肩颈、腹壁和大腿,禁用于乳腺、外阴部位。雌二醇控释贴片:透皮用药可使雌二醇恒定按生理需要量直接进入血液。可连续或周期性使用,但应每周规范加用孕激素。血管运动症状的非药物治疗方法见表4,血管运动症状的治疗药物见表5。植物SERM似乎有一定作用。
表4 血管运动症状的非药物治疗
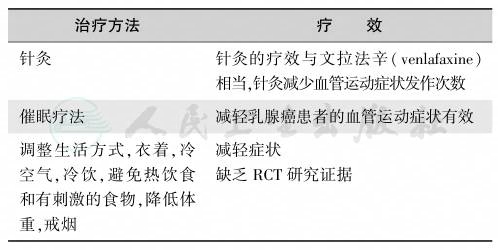
表5 血管运动症状的药物治疗
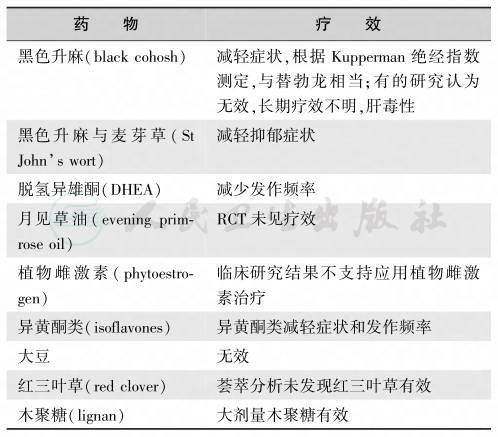
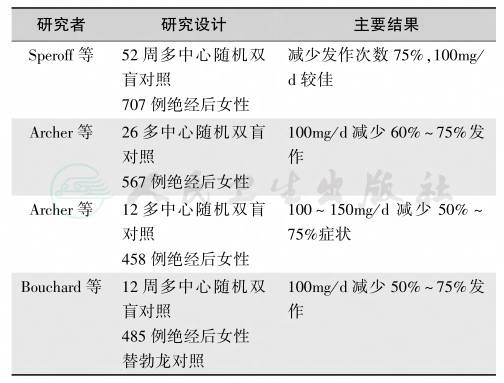
Desvenlafaxine属于血清素-去甲肾上腺素再摄取抑制剂类药物,于2008年被FDA批准用于抑郁症治疗,有关Desvenlafaxine治疗血管运动症状的研究见表6。
表6 Desvenlafaxine治疗血管运动症状的疗效
2.其他药物
HRT禁忌者可采用其他药物控制与围绝经期有关的潮热症状。中枢性降压药可乐定(可乐宁,clonidine)和甲基多巴均有减轻潮热作用,可乐定作用于下丘脑以“稳定”体温调节中枢,也可能直接作用于周围血管,阻断潮热所特有的血管扩张。可用0.1~0.2mg,每天2次,可减轻潮热频率30%~40%。其不良作用为眩晕及口干。围绝经期要注意骨质疏松症的预防,尤其在绝经后的数年内补充钙、维生素D等能减少骨钙丢失,周期性使用二膦酸盐或必要时注射降钙素均有良好的防治效果。













