英文名称 :autoimmune thyroid disease
中文别名 :自身免疫性甲状腺炎
自身免疫性甲状腺病(autoimmune thyroid disease, AITD)又称为自身免疫性甲状腺炎(autoimmune thyroiditis, AIT)是一种多基因多因素性复杂病综合征,主要包括弥漫性毒性甲状腺肿又称Graves病(Graves disease, GD)、慢性甲状腺肿性淋巴细胞性甲状腺炎又称慢性淋巴细胞性甲状腺炎(chronic lymphocytic thyroiditis, CLT)、自身免疫性萎缩性甲状腺炎(autoimmuno-atrophic thyroiditis, AAT)、产后甲状腺炎(postpartum thyroiditis, PPT)、无痛性甲状腺炎(painfulless thyroiditis, PT)和甲状腺相关性眼病(thyroid-associated ophthalmopathy, TAO),弥漫性甲状腺肿伴甲亢又称为自身免疫性甲亢(autoimmune hyperthyroidism, AIH)。
甲状腺组织特别容易发生自身免疫性病变的原因很多,可以分为3类。
1.遗传因素:如HLA-DR、细胞毒性T淋巴细胞相关因子(cytotoxic T lymphocyte-associated factor, CTLA-4)、CD40、蛋白酪氨酸磷酸酶(protein tyrosine phosphatase 22, PTPN22)、Tg、促甲状腺激素测定(thyroid stimulating hormone, TSH)受体基因等;
2.环境因素:如碘摄入过多、锶缺乏、药物、感染、应激、吸烟、环境污染等;
3.内源性因素:如青春期发育、妊娠、分娩、绝经、衰老、心理精神异常、女性等。
AITD是常见的器官特异性自身免疫性疾病。是对甲状腺自身抗原的自身免疫反应而引起的一种甲状腺淋巴细胞炎症应答,属于抑制性T淋巴细胞功能缺陷所导致。其结果往往造成甲状腺功能的异常。发病率占总人群的5%。与其他所有的自身免疫性疾病相似,AITD的发病除了免疫机制之外,也与个体的遗传易患性和环境因素密切相关。
Hashimoto甲状腺炎(HT)和Graves病是最常见的两种器官特异性自身免疫性疾病,其临床表现符合自身免疫性疾病的基本特征,即:①甲状腺淋巴细胞浸润;②抗甲状腺抗体阳性;③常常与其他自身免疫性疾病重叠;④发病存在较强的家族遗传背景和女性发病特点;⑤免疫性实验动物可模拟自身免疫性甲状腺炎和 Graves病。甲状腺特异性抗原——甲状腺球蛋白(Tg)、甲状腺过氧化物酶(TPO)和TSH受体(TSH-R)是数十年前就鉴定了的三种甲状腺自身抗原,继而又发现NIS和pendrin蛋白也有强烈的抗原性,并在Hashimoto甲状腺炎和Graves病患者中检测到较高的相应抗体水平。
(一)甲状腺自身免疫动物研究
甲状腺自身免疫的基础研究结果主要来源于小鼠动物实验。应用Tg加Freund完全佐剂和鼠抗原呈递细胞或树突细胞可诱导出实验性自身免疫性甲状腺炎,实验中,细胞分泌的细胞因子可分别诱导Th1、Th2或Th17介导的免疫反应。Th1细胞主要分泌IFN-γ和IL-12,Th2细胞主要分泌 IL-4与 IL-10,而 Th17细胞分泌IL-17。Th1和Th17细胞浸润至甲状腺,引起慢性炎症,最后导致甲状腺细胞死亡(图2-4-15-1)。CD4+T细胞是浸润至甲状腺的主要细胞类型,这种细胞含有功能不均一T效应细胞(Teff)与Treg亚群表达CD25(IL-2受体α),因而是引起甲状腺炎的关键因素。另一方面,Treg细胞表达Foxp3,故属于维持周围免疫耐受的功能细胞,其分泌的IL-10和TGF-β诱导了免疫耐受。同样,Treg细胞使循环抗原的激活被抑制,防治发生自身免疫反应;但当小鼠在出生3天切除胸腺和放射处理后,诱导出多器官自身免疫性病变,原因是动物缺乏自然Treg细胞。
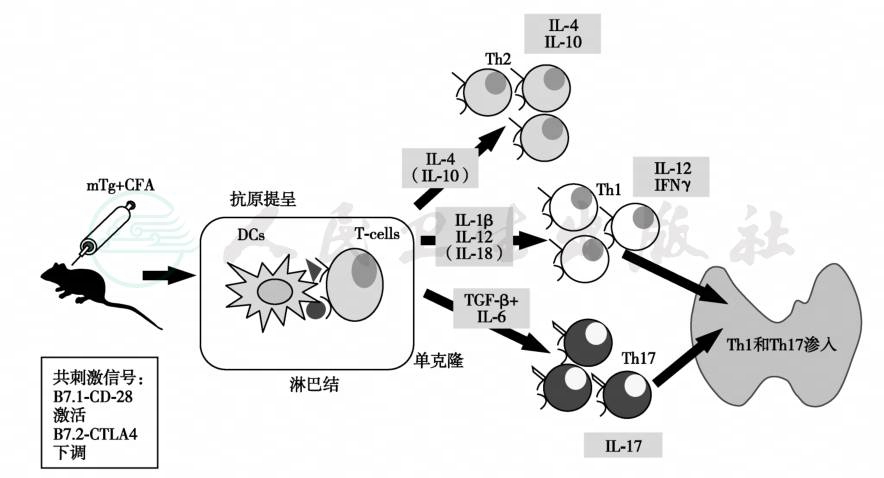
图1实验性自身免疫性甲状腺炎的发病过程
鼠Tg(mTg)加完全Freund佐剂(CFA)免疫动物;辅助免疫信号包括B7-1和B7-2。B7-1(CD80)激活B细胞和单核细胞,与T细胞表面的CD28蛋白结合后,为T细胞提供辅助免疫信号;抗原呈递细胞表达的B7-2(CD86)与Tx细胞表面的CTLA-4结合则下调免疫反应。EAT:实验性自身免疫性甲状腺炎;DCs:树突细胞;IFN:干扰素;IL:白细胞介素;TGF:转型生长因子
(二)甲状腺自身免疫人体研究
1.甲状腺自身免疫耐受缺失
甲状腺自身免疫耐受缺失是发生自身免疫性甲状腺病的关键,根据克隆筛选理论,在胎儿发育早期,多数自身反应性T细胞(auto-reactive T-cell)由胸腺进行阴性筛选清除(即中心性耐受),少数未被清除的自身反应性克隆移行至周围组织,这些细胞受周围耐受机制的调节,但对抗炎刺激物仍无反应(无反应性,anergy)。如果这种自身免疫耐受缺失,即可引起自身免疫反应。自身免疫耐受缺失涉及遗传背景和环境因素之间的复杂相互作用。
2.遗传因素
自身免疫性甲状腺病在家系中高发,同卵双生子的发病率远高于异卵双生子和非家族成员26%~28%,但未能达到100%,说明环境因素也起了重要作用。全基因组分析发现,自身免疫性甲状腺病的易感基因分为非特异性免疫相关基因和家族性特异性基因两类,其中的免疫相关基因分为免疫相关基因和调节性T细胞基因两组(表1)。
3.环境因素
环境因素刺激甲状腺自身免疫反应。食物因素、污染因素主要作用于免疫细胞数量水平,感染因素、治疗干预与药物因素和应激等主要与个体的自身免疫性甲状腺病发展相关(表2)。
(三)甲状腺自身免疫反应假说
曾提出的甲状腺自身免疫反应假说很多,其中较公认的有先天性免疫激活(innate immune activation,亦称危险假说,danger hypothesis)、胎儿微嵌合(fetal microchimerism hypothesis)和卫生保障假说(hygiene hypothesis)。
1.先天性免疫激活假说
细胞死亡过程产生的内源性分子亦称危险(损害)相关分子群(anger/damage-associated molecular pattern,DAMP)可诱导先天性免疫反应,DAMP包括基因组DNA、基因组DNA片段、热休克蛋白、高迁移率B1组蛋白(high mobility group B1 protein)、尿酸、胶原和透明质酸等。甲状腺细胞的Toll样受体可识别DAMP,激活先天性免疫反应。例如,基因组DNA进入细胞质后被DNA感受体(DNA sensor)辨认,上调MHC基因和其他分子表达,诱发先天性免疫反应。这一自噬过程也能释放细胞质MHC-Ⅱ上的多种抗原。
表1与AITD关联的免疫相关基因与家族性特异性基因
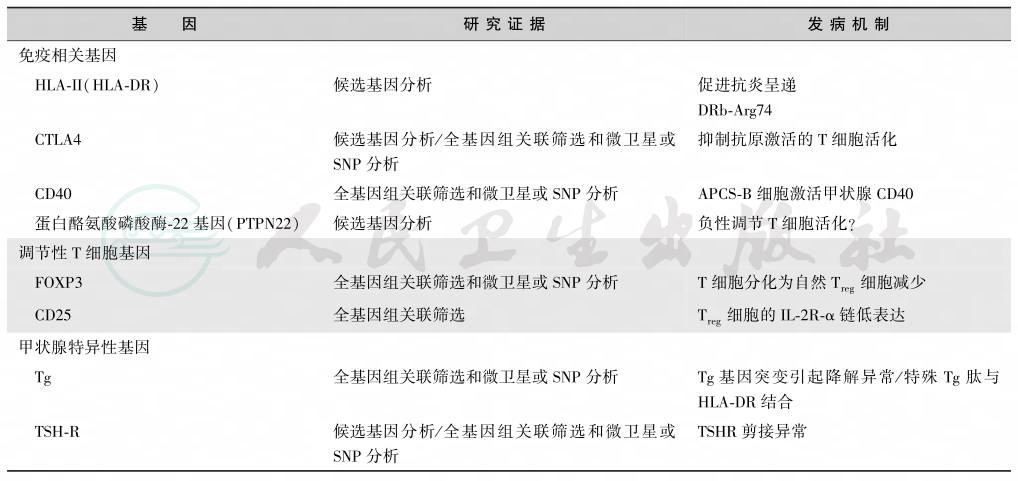
表2自身免疫性甲状腺病发病的环境因素

由上可知,危险假说的要点是认为甲状腺滤泡细胞本身属于一种抗原呈递细胞,但是未能在实验性Graves病得到证实。不过改用非经典共表达MHC-Ⅱ与TSHR的成纤维细胞代替APC后,或者应用TSHR表达质粒免疫后,或应用腺病毒表达TSHR亚基感染后,可满意地复制出Graves病动物模型,说明该种自身免疫性甲状腺病必须以TSHR作为自身抗原才能成功。
2.胎儿微嵌合假说
胎儿细胞常常在妊娠早期(4~5周)进入母体的血液循环系统。胎儿微嵌合假说认为,自身免疫性甲状腺病的发生与CD4+T淋巴细胞、CD8+T淋巴细胞、B淋巴细胞、单核细胞、巨噬细胞、NK细胞、CD34+生血干细胞、CD34+/CD38+原始干细胞、间质细胞、内皮前身细胞有关。胎儿细胞可在母体存活达27年之久,进入胸腺后形成成熟细胞,这些细胞或细胞的某些蛋白能破坏免疫耐受功能,或能损害宿主的自身抗原特异性免疫调节细胞。因而,产后的自身免疫功能恶化。支持该假说的依据是:①女性Hashimoto甲状腺炎和Graves病患者的胎儿微嵌合现象明显高于非自身免疫性甲状腺病者;②在健康女性和Graves病女性的血液内可找到男性细胞;③实验性自身免疫性甲状腺炎小鼠模型中,母体甲状腺内积聚有较多的胎鼠免疫细胞;④胎儿微嵌合母亲-胎儿均呈甲状腺自身免疫标志物HLADQA1∗0501-DQB1∗0201和 DQB1∗0301阳性反应;⑤病例对照研究发现,多次妊娠是AITD的风险因素,但也有反对意见。
3.卫生保障假说
高社会经济地位家庭的儿童接触感染的机会少,但更容易发生自身免疫性甲状腺病。比较俄罗斯Karelia人与芬兰人的自身免疫性甲状腺病流行病学资料发现,Karelia学龄儿童自身免疫性甲状腺抗体明显高于芬兰人。
(四)AITD的标志物
AITD的遗传学病因复杂,包括主效基因和次效基因两个部分。在病理学上,狭义的AITD是指甲状腺内淋巴细胞浸润和甲状腺滤泡破坏;而广义的甲状腺炎仅指甲状腺内淋巴细胞浸润,包括桥本慢性淋巴细胞性甲状腺炎等传统的甲状腺炎和Graves病。亚急性淋巴细胞性甲状腺炎是一种特殊类型的甲状腺炎,其病因可能与自身免疫有关。慢性淋巴细胞性甲状腺炎为甲状腺器官特异性自身免疫病,甲状腺有淋巴细胞、浆细胞浸润,甲状腺肿伴自身抗体阳性是AITD的主要表现,而原发性甲状腺功能减退为其终末结局。
表1自身免疫性甲状腺炎的分类

自身免疫性甲状腺疾病是在遗传背景下,因环境因素的作用而使免疫细胞调控失衡,自身免疫的细胞逃逸了正常的免疫耐受监控从而引起免疫损伤,而细胞和体液介导的反应则与组织损伤有关。因机体的遗传易感性不同,而使自身免疫性甲状腺病有一个广阔的谱带,有着不同的临床表型,从仅能在循环中检出甲状腺自身抗体到发生自身免疫性甲状腺炎和Graves病,后两者之间可有交叉带。
在病理学上,狭义的自身免疫性甲状腺炎是指甲状腺内淋巴细胞浸润和甲状腺滤泡破坏;而广义的甲状腺炎仅指甲状腺内淋巴细胞浸润,包括桥本慢性淋巴细胞性甲状腺炎等传统的甲状腺炎和弥漫性甲状腺肿伴甲亢;这样一来,自身免疫性甲状腺炎可以替代自身免疫性甲状腺病。
甲状腺多呈不同程度的弥漫性、对称性肿大,或伴峡部肿大。甲状腺滤泡上皮细胞增生,滤泡间以T淋巴细胞浸润为主,伴少量B细胞和浆细胞。眼浸润性突眼者的球后组织中常有脂肪浸润,纤维组织增生,粘多糖和糖胺聚糖(glycosaminoglycan, GAG)沉积,透明质酸增多,淋巴细胞及浆细胞浸润。眼肌纤维增粗、纹理模糊,肌纤维透明变性、断裂及破坏,肌细胞内粘多糖亦增多。胫前黏液性水肿病变皮肤切片在光镜下可见蛋白样透明质酸沉积,伴多数带颗粒的肥大细胞,吞噬细胞和内质网粗大的成纤维细胞浸润;电镜下见大量微纤维伴粘蛋白及酸性GAG沉淀。骨骼肌、心肌有类似上述眼肌的改变,但较轻。
各种甲状腺疾病的治疗可归纳为以下五种措施:①抗甲状腺药物治疗;②手术治疗;③甲状腺激素制剂治疗;④放射性核素(主要为131I)治疗;⑤其他治疗。
[抗甲状腺药物治疗]
广义的抗甲状腺药物包括硫脲类衍生物、咪唑类衍生物、碘剂、β受体阻滞剂、过氯酸盐和锂盐等。其中应用最多的是硫脲类和咪唑类衍生物。
(一)硫脲类/咪唑类制剂
硫脲类和咪唑类药物的主要优点是:①疗效较肯定;②不引起永久性甲减;③使用方便、经济和安全。但是,抗甲状腺药物治疗的疗程较长,长程治疗需1~2年,有时需长达数年,而且治愈率较低,停药后复发率较高,并存在继发性失效可能;少数病例可发生严重肝损害或出现粒细胞减少症甚至粒细胞缺乏症等严重不良反应。硫脲类主要有甲硫氧嘧啶(甲基硫氧嘧啶,methylthiouracil,MTU)及丙硫氧嘧啶(丙基硫氧嘧啶,propylthiouracil,PTU);咪唑类药物主要有甲巯咪唑(methimazole,MMZ)和卡比马唑(carbimazole,CMZ)。两类药物的作用机制基本相同,均可被甲状腺逆浓度差“捕获”而聚集在甲状腺内,都可抑制甲状腺激素合成,如抑制Tg及酪氨酸残基碘化,抑制单碘或二碘酪氨酸的偶联缩合反应,抑制免疫球蛋白生成、淋巴因子和氧自由基释放,使TSAb下降。其中PTU还抑制甲状腺内及外周组织5’-脱碘酶活性,减少T4向T3的转换。
抗甲状腺药物的主要适应证是:①作为病情轻、甲状腺呈轻~中度肿大的Graves病基本治疗;②用于Graves病患者年龄在20岁以下,或孕妇、年迈体弱,或合并严重心、肝、肾疾病而不宜手术者;③用于Graves病患者甲状腺手术前准备或作为放射性131I治疗前后的辅助治疗;④亚临床型甲亢或术后复发而不宜再次手术或不宜用131I治疗者。
(二)碘剂/β-受体阻滞剂/过氯酸盐/锂盐
1.碘剂
碘化钾(potassium iodide,KI)和饱和碘化钾液(saturated solution of potassium iodide,SSKI)中的无机碘离子可抑制碘在甲状腺的转运、有机结合和甲状腺激素分泌。还可使甲状腺组织的血流减少,组织变得坚实,有利于手术施行。目前碘剂主要用于甲状腺手术(尤其是Graves病)的术前准备,甲亢危象的抢救和放射性碘治疗后的某些反应等。碘剂不宜用于甲状腺毒性腺瘤和毒性多结节性甲状腺肿的治疗。作甲状腺131I(或123I,或99mTc)摄取率或核素扫描检查,或放射性碘(radioactive iodine,RAI)治疗前亦应禁用碘剂一段时间。缺碘所致的非毒性甲状腺肿用碘剂治疗,一方面可补充碘的不足,另一方面可望肿大的甲状腺缩小或结节消失。
碘化食盐是防治缺碘性甲状腺疾病的法定方法,但由于只注意到地区甚至国家人群的缺碘总趋势和宏观情况,补碘也带来一些不良反应,其中最主要的是碘甲亢和毒性结节性甲状腺肿。偶尔发生碘相关性甲状腺炎。但只要补充得当,加强观察、注意防治的个体化原则,这些都是可以避免的。碘液(通常用KI)也可用于新生儿甲亢(母亲患Graves病所致)的防治。放射性碘(RAI)治疗甲亢已经越来越受到人们的重视,在美国和欧洲的大部分国家,RAI已成为甲亢的最主要治疗措施。RAI治疗是利用甲状腺高度摄取和浓集碘的能力及131I释放出的β射线对甲状腺的毁损效应,破坏滤泡上皮而减少甲状腺激素分泌。此外,RAI也可抑制甲状腺内淋巴细胞的抗体生成,降低TSAb浓度,加强治疗效果。RAI治疗具有简便、安全和疗效迅速等优点。RAI治疗的主要缺点是患者要接触放射线,除近期可发生放射性甲状腺炎或一过性甲亢外,远期的主要并发症是永久性甲减。RAI治疗禁用于妊娠期和哺乳期妇女。
2.β-受体阻滞剂
甲亢者常有β-肾上腺素能受体功能亢进表现,应用β-受体阻滞剂可明显减轻甲亢的大部分症状,除可增强抗甲状腺药物的治疗作用外,还可抑制T4转换为T3,消除部分精神神经症状。非选择性β-受体阻滞剂(如普萘洛尔,propranolol)的疗效肯定,改善甲亢初治期症状的近期疗效显著。本药可与其他抗甲状腺药物合用,但遇有哮喘、严重心功能不全者,应慎用或改用选择性β1-受体阻滞剂(如阿替洛尔、美托洛尔等)。
3.锂盐
当锂离子在体内,尤其是在甲状腺内达到一定浓度时,具有与碘剂相似的Wolff-chaikoff效应,其作用机制尚未完全阐明。另一方面,摄入过量锂盐(如用锂盐治疗某些精神性疾病)亦可导致甲状腺肿,其原因未明。甲亢危象时,可用于阻止甲状腺激素的合成和释放。
4.过氯酸钾
很少用于甲亢治疗。本药的不良反应大,目前偶用于碘甲亢的治疗,因为此时的甲状腺对硫脲类或咪唑类抗甲状腺药物具有抵抗性。
[手术治疗]
甲状腺次全切除术的治愈率达70%以上,但可引起多种并发症,有的病例于手术多年后复发或发生甲减。
(一)手术治疗适应证
在一些国家,近年来已很少考虑首先用手术治疗甲亢,而在我国和其他一些国家,手术治疗的比例仍较高。甲状腺手术已相当规范成熟,在遇有下列情况时,可选用手术治疗:①中度或重度甲状腺肿大,长期服药无效,停药后复发,或不愿长期服药者;②甲状腺肿或伴有压迫症状者;③胸骨后甲状腺肿伴甲亢者;④存在恶性病变或疑为恶性病变者,不论有无结节均应手术切除。微创手术已应用于甲状腺结节的治疗多年,效果良好。这种内镜手术不留手术瘢痕,受到女性患者的欢迎。
(二)手术治疗禁忌证与并发症
手术治疗的禁忌证主要有:①较重或发展较快的浸润性突眼者;②合并较重的心、肝、肾、肺疾病,不能耐受手术者;③妊娠早期(第3个月前)及晚期(第6个月后);④轻型可用药物治疗者或亚急性或慢性甲状腺炎伴甲亢者;⑤术前准备不充分或术前准备失败者;⑥继发性甲亢或伴瘤综合征性甲亢者;⑦TSH受体缺陷或甲状腺激素抵抗者。术前准备不充分或术前准备失败者勉强手术可诱发甲亢危象,亚急性或慢性甲状腺炎伴甲亢为一过性表现,TSH受体缺陷或甲状腺激素抵抗者手术治疗将导致永久性甲减,术后如发生甲减需终生用L-T4替代治疗。甲状腺手术的主要并发症有创口出血、感染、呼吸道梗阻、喉上及喉返神经损伤、暂时性或永久性甲减。
[甲状腺激素治疗]
甲状腺疾病使用甲状腺激素制剂有三个主要目的:①补充替代治疗:使甲状腺激素浓度维持在正常水平;②抑制性治疗或诊断性治疗:通过甲状腺激素治疗,达到进一步明确诊断和取得更佳治疗效果的目的;③阻滞-替代治疗:作为抗甲状腺药物治疗的辅助方案,调整下丘脑-垂体-甲状腺轴的关系,防止某些并发症(如突眼或医源性甲减等)的发生。
(一)甲状腺激素补充/替代治疗
使用一定剂量的甲状腺激素制剂,补充甲状腺激素缺乏。补充替代治疗主要用于临床型甲减、甲减危象、甲状腺炎或亚临床型甲减患者。
1.L-T4
几乎仅考虑用L-T4口服。L-T4的半衰期为7天,吸收缓慢而完全,每日晨间服药一次即可维持较稳定的血浓度。不考虑使用碘塞罗宁(L-T3)、L-T4/L-T3混合剂的原因是口服L-T4不易导致医源性甲亢(高T3综合征),亦不致引起血中甲状腺激素的过度波动。
2.甲状腺粉片
也常用,但制剂的甲状腺激素含量差异较大,而且片剂中所含的T3/T4比值高于生理状态;加上经消化吸收,Tg水解后释出的以及在外周组织转换而来的T3,使T3/T4比值进一步升高。这些均不符合机体代谢和稳定甲状腺功能的需要,故不良反应较多。
3.注意事项
应用甲状腺激素时要特别注意以下几点:①从小剂量开始:无论有无并发症,均需从小剂量开始。如L-T4常用初始剂量为25~50μg/d,每2~3周递增1次。长期维持用量约每日 1.4~1.6μg/kg(75~150μg/d)。 如用甲状腺粉片,可按甲状腺粉片60mg约相当于100μg的L-T4比例给予。②剂量个体化:根据治疗目的、病情轻重、治疗反应、患者年龄、生活环境及劳动强度等确定个体的最佳用量,替代治疗必须强调基础剂量的个体化。用最小剂量达到纠正甲减而不产生明显不良反应的目的。一般在遇有青春发育、应激、腹泻、吸收不良,使用某些药物(如糖皮质激素、利福平、卡马西平、氢氧化铝、苯妥英钠等)时,应适当增加用量。妊娠期的用量约需增加30%~50%,外周型甲状腺激素不敏感综合征者需用较大剂量才能奏效,而老年人或合并冠心病者的用量宜小。③调整剂量:不能太勤,一般每2~3周变更一次。调整剂量的依据可能主要是临床治疗反应,在未达到稳定替代剂量前,TSH、T3、T4均仅供参考。在达到理想效果后,可用血TSH作为评价指标(一般需2~6个月)。④不良反应:长期替代治疗要特别注意体重和心功能的追踪观察,并防止因甲状腺激素过量所致的骨质疏松或冠心病恶化等的发生。
(二)甲状腺激素抑制治疗与诊断性治疗
1.甲状腺结节功能评价
T3抑制试验可用于观察和评价甲状腺结节对T3的反应性(75~100μg/d,5~7天)。如结节摄取131I被抑制,说明为TSH依赖性结节,反之则为自主功能性结节。鉴别结节有无自主功能对选择最佳治疗方案是十分重要的。
2.抑制自身抗原释放
放射性碘治疗后,为减少放射线引起的自身抗原释放,也常加用糖皮质激素和L-T4。
3.甲状腺结节治疗
在甲状腺结节的诊断与处理方面,可用L-T4作为抑制性治疗或诊断性治疗。如核素扫描示“热”结节,血TSH下降,可用L-T4来追踪病情,观察治疗反应。对疑为放射性甲状腺结节患者,如甲状腺呈弥漫性肿大,这种结节可先用L-T4治疗一段时间,并追踪观察结节变化,如证实为多发性结节性甲状腺肿,可考虑手术治疗。术后用L-T4治疗可收到较好效果。
4.预防甲状腺癌复发
甲状腺癌术后,也常用L-T4来抑制TSH的分泌,防止因TSH刺激甲状腺组织增生而导致复发。甲状腺激素抑制性治疗的血TSH目标值为0.1~0.5mU/L。一般弥漫性肿大的效果优于结节性肿大,随机对照研究发现,甲状腺激素不能使甲状腺结节的体积变小,且停药后即复发。如效果不明显,应及时停用。
(三)甲亢的替代-阻滞治疗
在抗甲状腺药物治疗的同时应用甲状腺激素制剂的疗法称为替代-阻滞治疗(replacement-blocking therapy,RBT),临床上一度广泛流传,据称具有预防发生药物性甲减与突眼、抑制免疫等作用,但没能得到临床观察的证实。少数患者在使用抗甲状腺药物后,容易发生药物性甲减,加用甲状腺激素制剂后可防止发生甲减,减少就诊频率。因此,该疗法用于儿童Graves病的治疗有一定益处。另有研究发现,Graves病治愈后,单用甲状腺激素制剂可能有预防Graves病复发的作用。目前仅用于儿童型Graves病的长程治疗,不宜作为一般Graves病的常规治疗。
[131I治疗]
(一) 131I治疗甲亢
放射性131碘治疗甲亢(尤其是Graves病)具有迅速、简便、安全、疗效明显等优点,一些国家将放射性碘治疗视为Graves病甲亢的首选方式。放射性131I治疗主要适应于中度甲亢而年龄>25岁的Graves病,或对抗甲状腺药物过敏而不能继续使用,或长期治疗无效,或治疗后复发者;或合并心、肝、肾疾病等不宜手术,或术后复发,或不愿手术者。Graves病患者伴无功能性甲状腺结节时,应先作结节FNA,如确定为恶性或疑为恶性结节应早期手术治疗。如术后残留有聚碘组织或TSAb阳性,可行RAI治疗。但妊娠、哺乳期妇女(131I可透过胎盘,进入乳汁)、年龄<25岁的Graves病、严重心肝衰竭或活动性结核、甲状腺极度肿大并有压迫症状、重症浸润性突眼、甲亢危象和甲状腺摄碘不能或摄碘功能低下者禁用RAI治疗。
(二) 131I治疗有摄碘功能的甲状腺瘤
手术后进行放射性131I治疗可摧毁残留的微小肿瘤灶或转移灶。改用重组的人TSH(rhTSH)先刺激甲状腺(包括含TSH受体的癌细胞)及PET扫描来对转移灶进行定位与追踪,方法可靠,灵敏度高。但是,即使用TSH达到最大刺激,甲状腺癌细胞的摄碘能力也要比正常甲状腺低得多,约1/3患者的甲状腺几乎无摄碘功能,因此主张应用大剂量131I。如果发现残留的甲状腺癌组织或转移灶,通常可施以131I 1850~2220MBq(50~60mCi),如果是有功能的转移癌则剂量加倍。
转移性分化良好的甲状腺癌可用131I治疗。但其前提是需要有TSH的强有力刺激。为了达到该目的,常停用L-T4,使血TSH升高,但患者易发生甲减。应用rhTSH的优点是不发生甲减,接受的131I剂量减少,而且使131I在甲状腺肿瘤组织中的存在时间延长。
[其他治疗]
蔡文佳等超声引导下经皮无水酒精注射(PEI)治疗甲状腺囊肿44个病灶。疗效显著,安全可靠,虽然存在出血风险,术前严格把握适应证,出血后妥善处理不会造成严重的后果。周伟等对3例单发甲状腺微小乳头状癌行超声引导下经皮激光消融术(PLA)治疗。均采用局部麻醉,成功进行PLA治疗,未发生严重并发症;超声引导下PLA治疗是一种安全、有效、可行的方法。
刘晓岭等对甲状腺微小乳头状癌9例患者,11个病灶行超声引导下射频消融治疗(RFA)。结果发现:①RFA可作为治疗无淋巴结转移的甲状腺微小乳头状癌的一种安全、有效的方法;②由于RFA微创、安全、有效,对于影像学高度怀疑甲状腺病灶恶性可能,即使无病理学诊断支持,仍是RFA的适应证之一;③本组病例RFA后是否存在癌组织残留及淋巴结微转移等问题,有待更长时间的随访资料。应规范RFA适应证,RFA治疗后诊断为PTC的患者应积极手术治疗,由于RFA治疗后局部粘连和水肿较明显,手术应由有经验的外科医师施行。超声引导下经皮微波消融治疗单发甲状腺乳头状微小癌25例,安全可行,效果可靠,具有一定的临床应用价值。50枚甲状腺结节行超声引导下甲状腺结节经皮射频、微波等热消融,治疗安全性高,创伤小,可控性强,疗效确切,具有临床应用潜质。超声引导下经皮激光消融术是治疗甲状腺良性结节的安全有效方法,治疗后结节体积可逐渐缩小,在一定程度上对甲状腺功能并无明显影响。随着研究和探索的深入与拓展,PTC及其区域淋巴结转移也开始成为热消融治疗关注的对象。PTC的预后较好,如能证明新型的治疗技术和治疗方式不导致其预后恶化,那么以热消融为代表的现代微创治疗新技术将具广阔的开发和应用前景。













