英文名称 :hepatopul monary syndrome
肝肺综合征(hepatopulmonary syndrome,HPS)是指肝功能不全引起的肺血管扩张、气体交换障碍导致低氧血症及一系列病理生理变化和临床症状的肝病终末期严重并发症。
HPS的概念最早用以描述肝硬化肺部并发症所致的氧合功能受损,近年关于慢性肝病、门静脉高压症与肺血管畸形间相关性的观点逐渐被接受。HPS以肺血管扩张为其主要特点,导致动脉血氧合功能下降,临床上主要表现为呼吸困难和发绀。慢性肝病、肺血管扩张和肺泡-动脉血氧分压差(A-aDO2)上升为HPS三大主征。
HPS最常见于各种病因所致的肝硬化,也可发生于非肝硬化的门脉高压症,甚至无肝硬化、无门脉高压的急、慢性病毒性肝炎。慢性肝病患者中4%~47%有HPS,肝硬化患者的发病率为4%~30%,发病率的差异主要是由于采用的诊断标准不同所致。
HPS多见于肝硬化患者,包括肝炎后肝硬化、酒精性肝硬化、胆汁型肝硬化及其他各种肝硬化。50%等待肝移植的HPS患者存在肺血管扩张。慢性乙型肝炎患者肺部血管改变较常见,约15%~20%伴有肺部血管扩张。肝硬化伴HPS者的死亡率明显高于无HPS者,这可能是低氧血症加重肝脏损害的结果。研究认为,HPS的产生和发展是多种因素作用的结果,HPS时肝功能受损,各种血管活性物质在肝脏的灭活减少或生成增加,使肺内扩血管与缩血管物质比例失调,肺血管对其敏感性改变,从而导致肺血管扩张。另外,门静脉高压使肠通透性障碍,发生细菌易位及内毒素血症,进而导致一氧化氮(NO)、内皮素-1(ET-1)、一氧化碳(CO)、肿瘤坏死因子-α(TNF-α)等扩血管因子产生。
1.分流的产生
(1)肺外分流:
主要有两条途径:①门静脉-肺静脉分流:血液通过门静脉,由食管静脉丛、纵隔静脉到达肺静脉,从而使肺静脉血液由氧合血变成混合血,造成心排血量增大,此为肝硬化患者氧合功能下降的重要原因;②胸膜交通支:肝硬化患者胸膜表面多存在扩张的动静脉吻合交通支,其数量甚至比肺内扩张的毛细血管还要多,并可延伸至肺血管床远端,成为肺血液绕行的主要途径,部分尸检可见肝硬化伴低氧血症者胸膜或胸膜下血管呈蜘蛛痣样改变。
(2)肺内分流:
可见于以下情况:①肠源性血管活性物质不能被肝脏及时灭活,从而导致扩血管物质如胰高糖素、血管活性肠肽、前列腺素、血管紧张素Ⅱ、5-羟色胺等囤积,肺血管内皮对肠源性血管活性物质敏感性也可能增加;②非肠源性血管活性物质如心房钠尿肽、P物质、TNF、血小板活化因子等增加;③缩血管物质减少或被抑制。在这些因素共同作用下,毛细血管前交通支开放,肺内动、静脉右向左分流形成。
2.NO与HPS
目前NO是HPS发病机制中研究最多的血管扩张因子,其主要通过激活可溶性鸟苷酸环化酶(sGC),使环磷酸鸟苷(cGMP)浓度升高,导致血管扩张。HPS时肝脏生成NO增多,而NO在肝硬化高动力循环状态中起关键作用。研究显示,HPS患者呼气时NO浓度较正常人明显升高,但在肝移植术后多能得以纠正,应用亚甲基蓝(sGC抑制剂)或左旋硝基精氨酸甲酯(L-NAME,NO及其酶抑制剂)后低氧血症也可短暂纠正。
NO的合成依赖NO合成酶家族(NOS),肺内存在诱导型(iNOS)和内皮型(eNOS)两种NOS。前者由炎症细胞因子和内毒素诱导产生,存在于平滑肌细胞、单核细胞和巨噬细胞等;后者存在于内皮细胞中。研究表明,肝硬化时eNOS过表达和过刺激或iNOS诱导增强,均可导致全身NO产生增多。HPS肺组织及肺血管多为eNOS活性增强,而iNOS活性无明显变化,故门静脉高压时肺内主要由eNOS作用产生NO。同时,eNOS所致低氧血症、过度通气、A-aDO2增加、对去氧肾上腺素(新福林)反应降低等,都可被NOS抑制剂所抑制。HPS肺内eNOS活性增强与ET-1血浆水平升高、肺内eNOS合成增多有关。另外,肝功能受损时肠源性内毒素增加,刺激某些细胞因子如TNF-α、IL-1、IL-6、IFN-α等分泌增多,均可诱导iNOS表达,且内毒素与细胞因子间的协同作用可导致NO合成增多。
3.ET-1
ET-1是一种由血管内皮细胞产生的血管收缩因子,以旁分泌和自分泌形式发挥作用,通过相应的G蛋白耦联受体与许多血管活性物质相互作用,其主要亚型有ETA和ETB受体。ET-1的血管活性作用包括血管收缩和血管舒张,存在于血管平滑肌细胞上的ETA受体介导血管收缩,而存在于血管内皮细胞上的ETB受体激活后通过增加eNOS活性使内皮细胞释放NO从而导致血管扩张。血浆ET-1浓度直接影响血管收缩与扩张,低浓度时血管收缩,高浓度时血管扩张。肝硬化时肝脏灭活功能减退,肝内ET-1浓度增加,侧支循环开放使门静脉血直接流入体循环,进而使体循环ET-1浓度升高。通常情况,ET-1由血管内皮细胞产生后先与血管平滑肌细胞内ETA受体相结合,产生缩血管作用,而在肺内,ET-1与ETB受体结合成为体内清除ET-1的主要方式。肝脏受损时,ET-1进入肺循环先与血管内皮细胞表面的ETB受体结合。肝前性门静脉高压症,不管是胆管性还是非胆管性,高动力循环状态和血管阻力增加均可引起肺内ETB受体表达增加,从而使肺对ET-1的增加更敏感。肺循环ET-1的增加激活eNOS,产生过多NO,从而导致HPS。
4.CO与血红素加氧酶-1(HO-1)
CO作为一种重要的第二信使,也在肺血管扩张中起重要作用。内源性CO主要有HO催化分解血红素,以及在氧化耦联基础上依赖辅酶NADPH的微粒体脂质过氧化两条途径。HO同工酶有HO-1、HO-2、HO-3,其中HO-1主要存在于单核巨噬细胞系统和网状上皮细胞内。CO同样通过激活sGC引起血管平滑肌舒张。iNOS通过诱导产生NO,而HO-1则通过诱导产生CO,二者均可使血管扩张从而导致或加重HPS。
5.巨噬细胞与TNF-α
肺血管内巨噬细胞(PIM)包括肺泡巨噬细胞、肺间质巨噬细胞、肺支气管壁巨噬细胞及胸膜腔巨噬细胞。正常情况下尚未发现肺组织内PIM存在,但肝硬化患者及实验动物模型中发现PIM。肝脏功能下降,肺成为清除细菌和毒素的主要场所,单核细胞黏附、聚集于肺血管内,分化成为PIM,吞噬功能增强,从而清除血液中的肠道菌群和内毒素。目前研究表明,TNF-α诱导巨噬细胞聚集从而引发HPS仅适用于胆汁型肝硬化。
6.雌激素
肝硬化时雌激素灭活减少,生成增多,体内雌激素水平升高,周围毛细血管扩张。Yol等研究发现,内源性及外源性雌激素均可引起肺内血管扩张,动脉血氧分压随血清雌激素的增高而减小,同时血NO水平也升高;抗雌激素治疗可降低雌激素和NO水平,减轻肺血管扩张和低氧血症。然而,雌激素对HPS时肺血管扩张和低氧血症形成的直接作用机制尚不清楚,可能与增加肺内NOS水平有关。
7.降钙素基因相关肽(CGRP)
CGRP是一种强大的血管扩张因子,肺内血管壁、各级支气管壁上的神经内分泌细胞及神经上皮样小体均可分泌CGRP,其通过与受体结合发挥扩血管作用。肝硬化患者CGRP含量明显升高。相关研究显示,HPS时血浆CGRP含量显著高于肝硬化患者,且与ET-1水平呈正相关,与动脉血氧分压(PaO2)呈负相关,提示CGRP可能协同ET-1的扩血管作用,参与HPS肺血管扩张和低氧血症。
主要表现为肺脏毛细血管前水平的动静脉交通支增多,胸膜蜘蛛痣样血管瘤形成,毛细血管扩张。根据血管扩张的情况可分为两型:Ⅰ型为弥漫型,表现为肺内血管弥漫广泛扩张,并进一步可分为轻度和重度,轻度表现为弥漫的轮廓清晰的蜘蛛痣样血管异常;重度则表现为海绵状或者斑块状血管异常。Ⅱ型为局限型,仅表现为局部的动静脉瘘、动静脉短路的形成。
肝肺综合征的主要原发结构改变是肺毛细血管前、后血管扩张,使混合静脉且快速,甚至直接进入肺静脉,同时由于低氧血管收缩机制受损也导致血管张力缺失或减低。动脉低氧血症在肺内有三个决定因素:肺泡通气‐灌注失衡,肺内分流增加和氧弥散下降;其中通气‐灌注最主要,基本上反映了弥散‐灌注缺损;相反,门‐肺静脉交通作用并不大(图1)。但临床上也观察到一些现象,如有些患者尽管在吸入100%纯氧后,其PaO2有显著增加,可>40kPa(>300mg),但其存在的肺内分流也显著增高(可达≥20%的心排血量)。严重患者在吸入室内空气时,对氧的弥散损害,比PaO2下降更明显,对这些现象的解释是由于灌注增加而有利于吸入纯氧提高PaO2,而其他因素不变。虽然毛细血管内血容量可能增加,但氧的弥散也受影响,部分是由于高流量使红细胞的转运时间缩短,因而产生弥散‐灌注失衡。CO弥散下降则可能是由于在扩大的肺微血管的中央主流中,肺泡和红细胞间的距离增加,以致不能使CO和血红蛋白完全平衡;无论如何,肺的气体交换状态仍然和低氧血症的三个机制并存,但其作用地位则分别和疾病的严重程度相关。
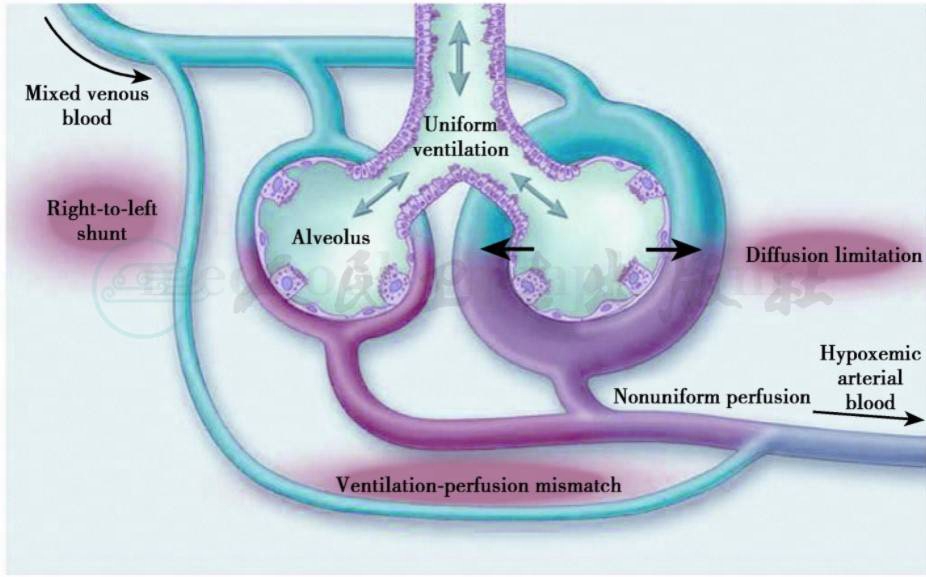
图1动脉低氧血症在肺内决定因素
1.动脉血气分析:
HPS时肺泡氧分压下降,肺内弥散功能下降,导致血氧分压下降(PaO2<80mmHg)和血氧饱和度下降(SaO2<90%)。直立位时,PaO2下降>10mmHg,A-aDO2上升15~20mmHg。呼吸室内空气和100%氧气时变化有所不同,A-aDO2较PaO2更敏感,可作为HPS的主要诊断依据。
2.增强经胸超声心动图造影(CE-TTE):
CE-TTE是HPS的首选筛查方法,也是肺内血管扩张检测的金标准。肺毛细血管的正常直径<8μm。生理盐水产生的直径 > 10μm的微泡,一般无法通过肺毛细血管床。因此,在右心微泡显影3个或以上心动周期后,左心可见微泡显影,提示肺内血管异常扩张。心内分流(如卵圆孔未闭合或房间隔缺损)右心房微泡显影1~2个心动周期内即可在左心房显影。经食管超声心动图可根据气泡到达左心房的途径(通过房间隔或肺静脉),区分心内分流与肺内分流。
3.99mTC-MAA肺灌注扫描:
正常情况下,99mTC-MAA颗粒直径为20~50μm,不能通过肺泡毛细血管。当肺血管扩张时,其可通过肺循环到达脑和肾脏。然而,肺灌注扫描不能区分心内分流与肺动静脉分流,对于成人轻、中度HPS检测的灵敏度低于CE-TTE。但是,MAA肺灌注扫描对于检测儿童轻度肺内血管扩张的灵敏度可能高于CE-TTE。对于合并其他肺部疾病(慢性阻塞性肺疾病、特发性肺纤维化或肝性胸水)的HPS患者,99mTC-MAA肺灌注后的脑摄取异常(吸收>6%),有助于鉴别肺内血管扩张与非血管性肺实质病变引起的低氧血症。因此,MAA扫描可用于合并心肺疾病的HPS相关低氧血症的检查。
4.HPS肺血管造影:
分为两型:Ⅰ型为弥漫性前毛细血管扩张,呈弥散分布的蜘蛛样、海绵状或污渍样影像,吸100%氧气可使PaO2升高,多见于HPS初期和中期;Ⅱ型为断续的局部动脉畸形或交通支,呈孤立的蚯蚓状或团块状影像,吸100%氧气对PaO2无影响,多见于HPS晚期。肺血管造影不能显示小的周围动静脉畸形,可能造成假阴性,故不作为筛查首选。
5.胸部CT检查:
HPS患者胸部CT示肺远端血管扩张,有大量异常的末梢分支,甚至波及胸膜血管,可提示HPS存在,但无特异性。胸部CT可排除其他造成低氧血症的原因,如肺气肿、肺纤维化等。
1.原位肝移植(OLT)
OLT仍被视为HPS严重低氧血症唯一有效的治疗方式。HPS合并进行性低氧血症(PaO2<60mmHg)可作为肝移植的适应证。报道显示,肝移植可明显提高HPS患者的生存率,降低死亡率,明显改善患者氧分压、氧饱和度和肺血管阻力。据报道,HPS患者OTL术后5年生存率为76%,这与非HPS的OTL患者相比无明显差异。近年发现,OLT后患者肺内分流和杵状指可得到改善,甚至可能完全逆转肺内分流。HPS患者能否接受肝移植,关键在于麻醉过程中能否进行安全氧合。有人认为,吸入纯氧有反应,肝功能稳定,动脉氧合功能近期无下降的患者应首选肝移植。合并肺纤维化的患者为肝移植手术禁忌证。
2.经颈内静脉肝内门体分流术(TIPS)
门静脉高压症被认为是导致内生型NO增多的主要原因,进而导致HPS,控制门静脉高压可改善HPS症状。对等待OLT的患者,TIPS可降低围手术期死亡率,提高手术安全性。报道证实,TIPS可降低门静脉高压,改善HPS患者氧合作用,PaO2和A-aDO2均可明显改善,患者呼吸困难症状明显好转。但也有报道TIPS对HPS患者气体交换障碍不起改善或恶化的作用。对于自发性下腔静脉-门静脉分流或Abernethy畸形的患者,置入下腔静脉支架或结扎先天性门体分流血管可有效治疗HPS。
3.肺血管栓塞术
如HPS患者肺血管造影表现为弥漫性肺血管扩张,则肺血管栓塞术不易使之完全闭塞,疗效较差。对于Ⅱ型表现为断续的局部动脉畸形或较大动静脉交通支者,栓塞术较易获得成功,尤其是对严重缺氧和吸纯氧反应较差的患者和肝移植术后缺氧未见明显改善者疗效更佳。“圈状弹簧”栓塞术用来减轻或根治肺内分流取得良好效果。
4.NO合成抑制剂
NO合成抑制剂主要以抑制肺内NO水平升高为主。但因HPS的发病机制目前仍尚未阐明,各种药物的临床疗效也不能肯定。CBDL小鼠实验发现,亚甲蓝可抑制NO的合成。临床试验中,服用亚甲蓝的HPS患者PaO2从用药前的50mmHg升高至用药后的70mmHg。
5.氧疗(高压氧舱、机械通气)
氧疗适用于轻型、早期HPS患者,可增加肺泡内氧浓度和压力,有助于氧弥散。HPS后期患者使用呼吸机加压给氧疗效较差,如造成气胸反而会加重其低氧合状态。
6.其他药物治疗
HPS的药物治疗研究进展缓慢,应用大蒜素、普萘洛尔(心得安)、雌激素、吲哚美辛(消炎痛)、阿司匹林及其他环氧化酶抑制剂治疗HPS,都有小宗病例报道显示有效,但仍缺乏大规模临床试验证实。另有报道,1-(5-氧化己基)3-7-二甲基黄嘌呤(乙酮可可碱)可抑制TNF-α和巨噬细胞对NO的作用,从而防止高动力循环状态和HPS的产生。
结合指南认为,OLT仍被视为HPS严重低氧血症唯一有效的治疗方式。除了氧治疗(休息、运动及睡眠),尚无治疗HPS的药物被证明有效或获得美国食品药品监督管理局批准。(TIPS)对于成人HPS的疗效尚不明确。少数情况下,弹簧圈栓塞术可改善个别HPS患者的氧合情况。建议使用脉搏血氧仪进行连续血氧监测。随着技术的发展也期待更好的基础研究在HPS方面有所突破。
积极控制原发病,避免出现肺部感染等,定期监测肝功能等,如出现呼吸系统症状如气短等不适应及时就诊。













