英文名称 :high altitude heart disease
高原性心脏病(high altitude heart disease,HAHD)的发现及对这一高原特殊疾病名称的确立,都源自我国学者自20世纪50年代起所做的巨大贡献,对高原病及心血管病均具有双重里程碑意义。国外学者是以后才逐渐认识同类高原低氧性肺动脉高压心脏疾病的。
1955年我国四川省人民医院的吴德诚和刘永儒首先报道了一例出生于拉萨(海拔3658m)的汉族男婴,11个月,在拉萨出现水肿、尿少、呼吸困难、发绀。胸部X线检查心脏呈球形增大,心电图示右心室肥厚。该患儿辗转2个月始从拉萨低转至成都,但经治无效死亡。尸检发现肺动脉弥漫性扩大,肺小动脉有多发性新鲜血栓,右心显著肥大扩张。作者认为该例患儿从病理上排除了先天性或其他器质性心脏病,从而第一次被命名为“高原性心脏病”,即小儿高原性心脏病(pediatric high altitude heart disease,PHAHD),认为属于急性肺心病的范畴。
1965年吴天一等正式报告在青藏高原的一组22例成人高原性心脏病病例,男性21例,女性1例,4例发病在海拔3402~3750m,18例在4150~4888m。18例为平原地区人移居高原后2~9年发病,4例为中海拔高原(2000~2500m)居住者,包括1名藏族人,在迁往海拔4200m以上2~12年后发病,全组平均发病时间为5年3个月。主要临床症状为呼吸困难、心悸、胸闷、疲乏、咳嗽。全部病例均有不同程度的右心衰竭,出现颈静脉怒张、肝大、腹水及皮下水肿等。实验室检查有红细胞增多,Hb平均211g/L(170~245g/L)。X线检查肺门扩大、肺纹增粗、肺动脉段凸出,右心或全心扩大。ECG示垂悬型心电位、顺钟向转位、电轴右偏、肺性P波、右心室肥厚及右束支传导阻滞。由于临床上有明显的肺动脉高压征象及均有右心衰竭,故命名为“成人高原性心脏病”(adult high altitude heart disease,AHAHD)。
此后在青藏高原有一系列大量的临床病例报告,总数近万例,积累了丰富的临床学和病理生理学资料。
流行病学的研究可进一步确定高原心脏病在青藏高原的客观存在及其流行规律,以及发病的危险因素,为防治提供依据。
(一)患病率
1.小儿高原心脏病地理分布及发病情况
本病虽然曾由不同作者冠以不同名称,造成一定紊乱,但病理性质完全相同,即由高原低氧引起显著肺动脉高压,右心肥大,右心衰竭。据此特征,本病不仅发生于我国青藏高原,尚发现于美国科罗拉多州、南美秘鲁及玻利维亚。可以说,全世界高原地区婴幼儿及儿童均可罹患。
根据笔者在青藏高原的观察,小儿高原心脏病的发病有以下三种情况:
(1)父母系平原人,移居高原后所生育并留居高原的小儿,占总病例数的73%,其儿童人群患者率为2.5%。
(2)小儿出生于平原后由父母携往高原,占总病例数的17%,儿童人群患病率为1.6%。
(3)小儿随父母从中等高度高原(2000~3000m)移居到更高高原(3000m以上至5000m)生活,占总病例数的10%。
除平原汉族后代外,藏汉混血儿,个别藏族小儿也有发病者。特别当居住海拔过高、并发呼吸道感染、营养不良、贫血等诱因加重低氧血症而出现严重肺动脉高压时,更可促发本病。除1岁以内婴幼儿常见外,2~13岁的儿童也有发病者。
笔者曾连续八年(1978~1985)在青藏高原不同海拔高度对移居及世居人群进行了高原病的流行病学调查,诊断基于中华医学会的诊断标准,自然人群普查率达82.5%~97.3%,共查儿童(出生后至14岁)15 251人,小儿高原心脏病的人群患病率见表1。
表1 青藏高原儿童高原心脏病的人群患病率调查

*世居民族以藏族为主,尚包括高原蒙古族、土族、回族和萨拉族
由表1可见,移居汉族儿童患病率较高,并随海拔增高而增高,但高原世居儿童亦可发病。因此涉及高原所有儿童的公共健康问题。
2.成人高原心脏病
为了探讨成人高原心脏病的人群分布,吴天一等从1984~1993年,在青藏高原人群进行了一项成人高原心脏病流行病学研究。系调查自然人群普查率在90%以上,总计调查藏族世居者2314人,汉族移居者2719人,年龄 15岁以上。居住于中度(2267~2980m)、高度(3128~3968m)和极高度(4006~5226m)三个海拔范围。诊断基于中华高原医学会的标准。结果人群患病率于世居藏族为1.21%,而移居汉族为5.57%(P<0.01)。移居汉族持续居住海拔3500m以上多年者患病率是藏族的5倍。尽管藏族有很低的患病率,但证明成人高原心脏病确实存在于这一土生高山人类群体。
(二)易感因素
1.高度
海拔3000m以下成人高原心脏病罕见。患病率随海拔升高而增高,海拔2980m为1.05%,4128~3968m为3.75%,4006~5226m为1.83%。
2.性别
男性多见。在玛多(4300m),本病的患病率于汉族男性为7.77%,女性为1.76%,于藏族男性为1.78%,女性为0.56%。男性约为女性的4倍。性别差别受若干因素影响,如月经期妇女的行经有如“自然放血”起预防红细胞增多的作用,此外或与女性激素对通气的刺激有关。
3.年龄
秘鲁的研究提出年龄是发病的主要因素,因为年龄所依赖的红细胞增多是基于年龄所依赖的通气(功能)丧失及动脉低氧血症,大部分病例发生于中老年。然而,生理学的研究在藏族未见静息通气、血细胞比容(Hct)与年龄间有何相关,在年龄与记分间也无相关性。由此认为在藏族,年龄并非一个明显的易感因素,这一点在高原藏族与安第斯居民间有重要区别。
4.民族
成人高原心脏病在汉族比藏族常见。为了对比藏族和安第斯印第安人,吴天一等(1998)应用 Monge(1992)的同一标准,即Hb>213g/L、SaO2<83%来判定本病,并与其报告相同海拔高度(4300m,玛多),结果藏族患病率仅0.91%,而居住在赛罗·德·派斯科(4300m)的秘鲁克丘亚印第安人患病率高达15.6%,有极显著差异(P<0.001)。这与藏族肺动脉压和红细胞值都维持在近于海平面的正常值范围内有关,这也表现遗传适应对高原心脏病发病的影响。
5.居住期限
成人高原心脏病的发生通常需要一定的高原居住时间。一个健康汉族持续居住高原到发病约需15~20年,而藏族发病通常要35~40年。而汉族年轻工人在海拔4500m以上只需较短数年甚至在海拔5000m一年即可发生。因此居住海拔高度、性别及遗传背景是影响成人高原心脏病发生早晚的因素。
6.吸烟
已观察到吸烟与本病间的关系,在汉族男性,吸烟者患病率是不吸烟者的3倍。其机制尚不清楚,但可能烟的产物造成为小气道功能障碍和导致小叶中心肺气肿,从而减低肺泡通气,而加重低氧血症。
7.职业
有趣的事实是本病与职业有关。在同等海拔高度,不论藏、汉,也不论男女,机关工作者包括干部、教师和政府官员,其成人高原心脏病的患病率约为农、牧民的2~3倍。提示高原居民的居住区如城市化和工业化,则将是一个危险因素。
最后,随着我国西部大开发,大量人群从平原进入青藏高原,无疑高原心脏病的患病率势必增高。而且,在中国,青藏高原总人口约为1200万,一个粗略估测约4%~5%的高原居民患有高原心脏病或相当于有25~30万病人,因此高原心脏病是一个严重影响高原居民健康的疾患,必须引起高度关注。
李经邦等1966年在病理上对51例死于“高原不适应症”(即PHAHD)的婴幼儿尸检材料做了分析,发现主要特征为肺动脉圆锥突出,肺动脉主干扩张,肺动脉分支内膜增生,中层增厚、弹力纤维增生、断裂,血栓形成,右心房、室高度肥大扩张,心肌广泛变性、坏死、瘢痕形成,认为是高原缺氧引起的肺动脉高压和心肌损伤的结果。1974年林治平和吴天一报道了在青藏高原海拔2231~4780m所见的286例小儿高原性心脏病,根据11例尸检主要病变在肺动脉及右心、肺小动脉肌层显著增厚,右心室高度肥厚(图1,图2),故明确指出本病系高原低氧引起的一种肺动脉高压症。
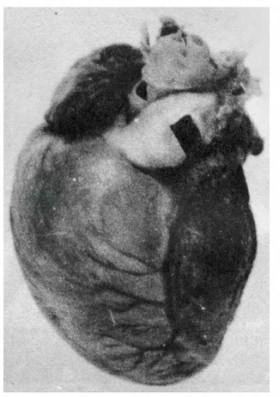
图1 小儿高原性心脏病尸检标本
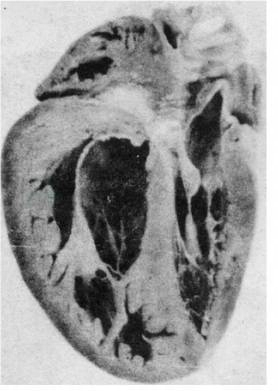
图2 小儿高原性心脏病
成人的尸检病理资料较少,主要病变亦为肺小动脉肌层显著增厚,右心室高度肥厚或全心增大,肺动脉常有血栓形成,有一例因左心房巨大血栓而突然死亡。其他为充血性心力衰竭的病损(图3)。
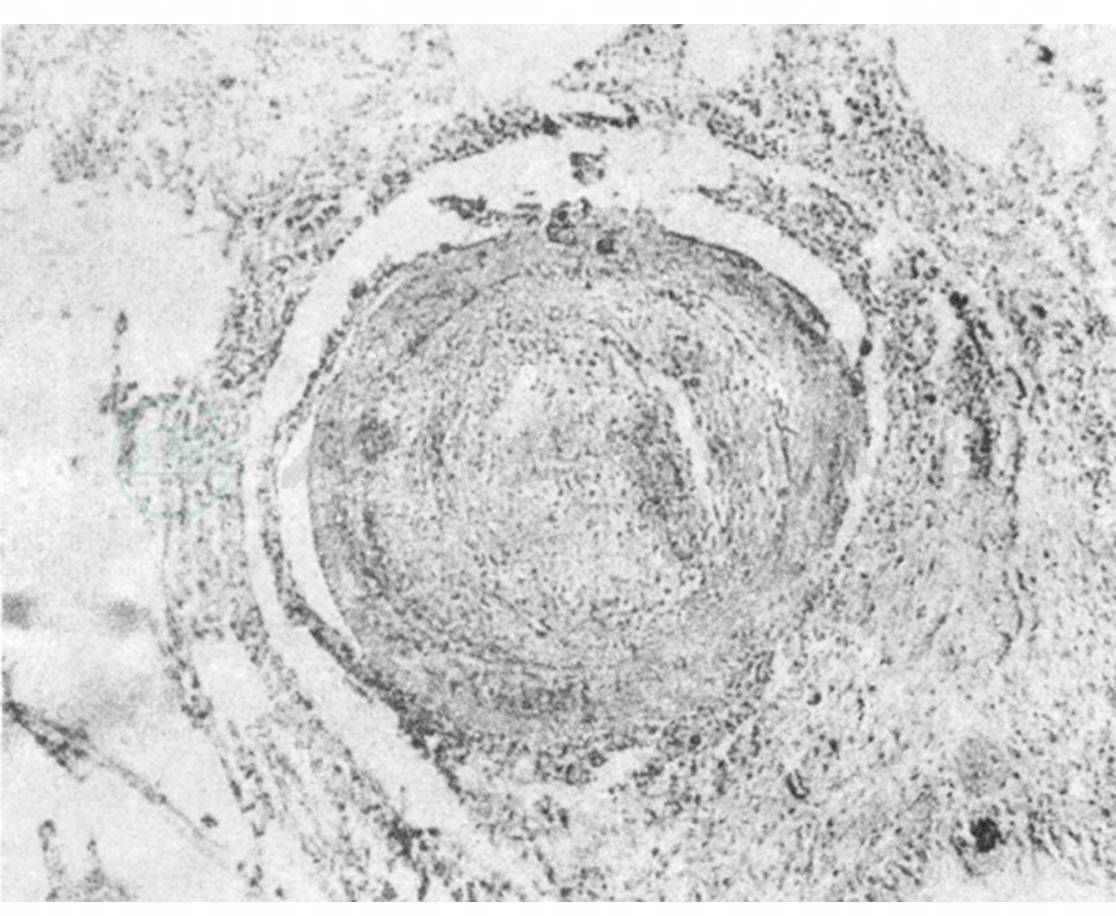
图3 一名42岁汉族男性高原性心脏病患者,肺小动脉肌层显著增厚,并有血栓形成
(一)高原低氧性肺动脉高压是基本的发病机制
1.PHAHD的高原肺动脉高压
人类胎儿在胎盘内处于低氧环境(PaO2低于30mmHg,约相当于海拔7 500m),同时,肺呼吸尚未建立,肺部血流经动脉导管入体循环,此时其肺小动脉肌性增厚,称为“胎儿型”肺小动脉。但在海平面出生后,处于常氧环境,肺呼吸建立,动脉导管逐渐关闭,肌性肺小动脉在数周内消退,转化为肌层菲薄的“成人型”肺小动脉,PAP下降至正常水平。而在高原出生后,婴幼儿仍处于低氧环境,其“胎儿型”肺小动脉退化延迟,约须经数月或更长,PAP仍保持较高水平,右心室依然肥厚,称为小儿“高原心脏(high altitude heart)”,有的甚至退化不全(incomplete regression),PAP持续增高,而发生PHAHD。
此外,平原人,特别是汉族移居高原者,母亲在高原妊娠时,经多普勒技术测定子宫动脉及髋动脉血流量与世居藏族相比明显为低,使汉族胎儿多易发生宫内发育迟缓(intrauterine growth restriction,IUGR),出生时其脐带血氧饱和度也明显低于藏族新生儿。这类汉族新生儿常为低体重儿(<2 500g),其出生后明显的低氧血症使“胎儿型”肺小动脉向“成人型”转化延迟,这种肌肉型肺小动脉及肺细小动脉的异常肌化是形成严重肺动脉高压的形态学基础。而当吸入低氧气体时,其PAP迅速明显增高,证明此类患儿肺小动脉对低氧的易感性而产生明显HPVR。PHAHD时肺小动脉肌层肥厚和肺细小动脉出现异常肌化,导致严重肺动脉高压,MPAP在33~47mmHg,平均为44mmHg,返回海平面后经3~6个月才逐渐恢复正常。
2.AHAHD的高原肺动脉高压
选取心导管资料对肺循环的研究证明AHAHD与居住同高度的健康人相比,有轻或中度的肺动脉高压。杨之等1985年报告6例男性汉族患者均在称多(海拔3950m)当地医院行右心导管术,有4例表现肺动脉高压,其MPAP为4.1kPa(30.8mmHg)。吴天一等1999年观察18例患者中有5例(27.8%)呈现肺动脉高压。1例MPAP明显升高[10.0/4.8kPa(6.4kPa),75/36mmHg(48mmHg)],余4例为轻度。 上述患者在海拔3 719~4280m发病,但右心导管术是在海拔2261m,鉴于肺动脉压力于低转后迅速下降,提示肺血管收缩是肺高压的主要因素,但吸氧并未能使肺动脉压降至正常,说明尚有肺血管解剖学变化参与了肺阻力增高。AHAHD的PAP虽较PHAHD患儿为低,但持续的肺高压,特别当运动或并发呼吸道感染时,PAP将明显增高,日久必将引起右心损害。
(二)红细胞增多及相关分子机制
HAHD的另一个相关的致病因素为红细胞增多,而肺高压与红细胞增多间又形成相互促进的密切关系。人类群体居住在高原受到自然选择的压力,HAHD被认为是对高原应激缺乏/丧失了适应,从而产生大量循环血的红细胞及高含量血红蛋白来代偿低氧。由于低氧性肺血管收缩及重建,而红细胞过度增生导致的高血黏稠度增加了血管阻力,促使肺动脉压进一步增高。
近年的研究已证实不同的高原人群对慢性低氧的反应存在差异,而这些人群中只有一部分人是对HAHD的易感者。而这些易感者可能与其基因成分有关。Mejia等曾在安第斯对48名HAHD(CMS)及56名对照组进行了一组基因学研究,观察一系列候选基因包括红细胞生成素(erythropoietin,EPO)、红细胞生成素受体(erythropoitin-receptor,EpoR)、低氧诱导因子-1α(hypoxic-inducible factor 1 alpha,HIF-1α)、von Hippel-Lindau病肿瘤抑制物(VHL)、羟基赖氨酸酶域1、2、3(prolyl hydroxylase domain 1,2,3,PHD1,PHD2,PHD3)及其他基因,结果没有发现这些候选基因的多态性与红细胞过度增多有何相关。
不过根据一项全基因测序研究,发现VEGF及其他9个基因在HIF调控下成为正选择的候选基因。因此这些基因也可能是HAHD相关的候选基因。目前发现某些基因如内皮素1(Endothelin-1,ET-1)、血管紧张素转换酶(ACE)基因多态性、内皮细胞生长因子A(VEGFA)和一氧化氮合酶(Nos)等基因在低氧性肺动脉高压的调控上起重要作用,已显示出一些与HAHD相关的分子生物学的亮点。
综合国内报道文献,HAHD的主要辅助检查结果如下:
(一)血液学
白细胞数多正常,计数>10×109/L以上者占43.2%~45.4%,常与合并呼吸道感染有关。成人患者常出现高原红细胞增多症(high altitude excessive polycythemia,HAPC),红细胞计数(6.8~9.5)×1012/L,血红蛋白190~280g/L。小儿红细胞增多者仅占10%左右,相反有22%~50%呈不同程度的贫血。
(二)胸部X线表现
PHAHD与AHAHD也有所不同,在婴幼儿心脏常呈球形增大或全心扩大,搏动减弱,常与心肌炎或心包积液影像相似,易误诊,需加注意(图4),随着年龄增长,其心脏特征向成年改变过渡(图5)。AHAHD主要表现为右心室增大、肺动脉段突出、肺动脉圆锥膨隆,有的甚至呈动脉瘤样凸起。突出之肺动脉段常见搏动增强,但未见肺门舞动。右肺下动脉干扩张(高原地区成人应以≥16mm为标准),也有中心肺动脉扩张而外围分支细少,形成“残根状”者。部分肺门影扩大,肺纹增多、粗重或呈网状。心脏扩大占66.3%~95%,主要是右心增大,心尖上翘或圆突,也有以右心为主的全心扩大,单纯表现为左心增大者甚少。上腔静脉影多增宽。
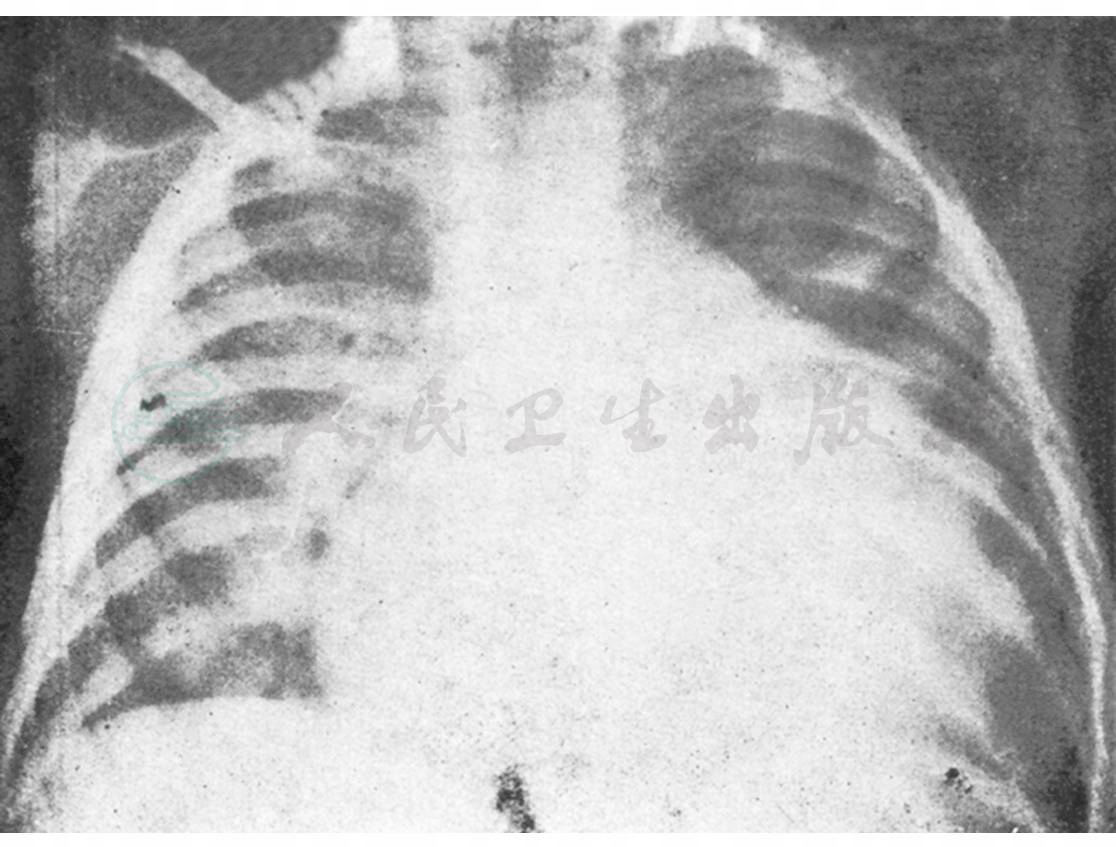
图4 6月龄小儿高原性心脏病X线胸片表现
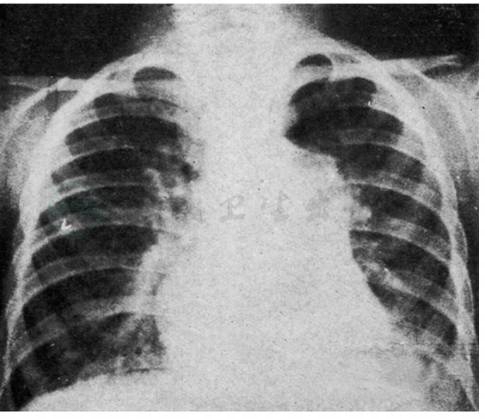
图5 6岁小儿高原性心脏病X线胸片表现
肺动脉段突出,右心室增大。
(三)心电图及心电向量图
主要特征为电轴右偏,极度顺钟向转位(V5R/S≤1),肺性P波(3.2%~29.3%)或尖峰形P波(27.3%~29.2%),右心室肥厚或伴有心肌劳损(33.5%~100%)(图6),右束支传导阻滞(完全或不完全性,占4.9%~26.8%),仅少数呈双侧心室肥厚。也可出现下述值得注意的变化:①V1~V3呈QS型,酷似心肌梗死,而待病情好转或转往低地区可转为rs或rS型;②出现S1S2S3图形,一般反映右心室肥厚;③“假性”电轴左偏,实际也是QRS电轴极度右偏,右心室肥厚的一种表现;④ST-T段改变,常见于Ⅱ、Ⅲ、aVF及右胸前导联,有的T波倒置,颇似“冠状T”;⑤少数有期前收缩,P-R间期或Q-T间期延长、低电压等。

图6 14月龄小儿高原性心脏病心电图表现
窦性心律,电轴右偏,肺性P波,右心室肥厚,明显顺钟向转位。
(四)超声心动图
AHAHD的超声心动图主要特征为:右心室流出道增宽,平均宽径(36.9±5.7)mm,右心室内径增大,平均(27.7±5.4)mm,左/右心室内径比值减小,为1.98±0.6,右心室/左心房内径比值增大,为1.82±0.8。
(五)血气分析
动脉血氧饱和度(SaO2)明显低于同海拔高度的正常人。动脉血氧分压(PaO2)降低而动脉血二氧化碳分压(PaCO2)增高,此与HVR钝化有关。pH多正常或轻偏酸,虽有通气低下,但由于血浆碳酸氢盐含量增高而加以代偿。
(六)肺功能
李英锐等在拉萨(海拔3 658m)对30例AHAHD患者进行肺功能测定,患者均汉族男性,年龄20~56岁(平均34.6岁),移居高原2~38年(平均16.1年),均符合中华医学会诊断标准,且均有心脏肥大及不同程度心力衰竭。对照组40例,汉族男性,19~58岁(平均34.5岁)移居拉萨1~36年(平均16.0年),经检查无心、肺疾病及高原病史。两组均入院检测,应用电子肺量计测定肺功能。结果显示:①AHAHD患者的肺容量(VC):12例正常而18例反有明显增高,对照组各项肺容积均较平原正常预计值扩大20%~80%,示肺容积相应扩大,AHAHD组过度扩大者则较对照组显著扩大(P<0.05),而未扩大者则较对照组显著降低(P<0.01)。②肺通气:对照组通气流速各项指标均较平原正常预计值增高20%~80%,示通气流速加快,与VC增大都是高原习服的表现,以获取更多的氧;患者组无论肺容积扩大与否,与对照组相比最大呼气中段流率(MMEF)及用力肺活量(FVC)的V50、V25均有明显降低(P<0~0.01),最大通气量(MBC)、V75也降低,但统计学差异不明显。对其中返回成都平原5例在5天内复查肺功能,以上指标均恢复大致正常,提示并非肺疾病引起,而提示可能与对高原低氧应激代偿过度有关。同时患者组的残气率过多、通气量及通气流速减低,因此无论肺容积增大与否,仍然导致PIO2降低、弥散功能降低及肺摄氧减少。③肺换气:患者组摄氧量较对照明显降低,从PaO2值判定,对照组为轻度低氧血症,而患病组为中度低氧血症,两组PaCO2分别为(26.36±1.68)mmHg及(28.14±1.98)mmHg,均在正常范围内。④氧耗量及基础代谢:患病组耗氧量、产热量及基础代谢(BMR)较对照组均明显增高。由于摄氧减少而耗氧量增加,严重损害其氧储备,长期低氧血症形成,将在AHAHD发生和发展中可能起重要作用。
(一)向低处转移
小儿高原性心脏病在高原就地治疗疗效不佳,预后较差,有较高病死率,故应坚决将患儿及时转往低海拔处,在低转过程,特别从高海拔偏远地区向低海拔或平原低转,如果只有父母携带将具有很大危险,一旦发生病情恶化,处于束手无策,患儿往往死于途中。必须有医护人员护送,有良好的交通工具、急救药品和充足的氧气,沿途严密观察病情。
成人高原心脏病目前尚无特效治疗,对于病情较重且在高原就地治疗无明显效果,病状不断发展者,最有效的方法仍然是将患者转往平原地区,低转至平原并不再返回高原,对早期患者也是可靠的预防,可以防止病情进一步发展。但实际上不尽可取,因不少患者由于家庭、社会和经济的原因,特别是那些高原世居者仍需留居高原,或者在平原好转后又返回高原他的家,这是一些需要特殊应对的患者。
(二)氧疗
是首要的治疗措施,并要求早期、及时和充分供氧,以纠正低氧血症,这在PHAHD效果尤为明显,氧流量依病情决定,病情稳定后仍以经湿化的氧予持续低流量吸入。对AHAHD患者宜用间歇性供氧,治疗可提高血液氧合及部分降低肺动脉压。但在高原就地吸氧只能暂时减轻症状,特别对AHAHD并不理想。高压氧治疗可用于重症严重缺氧患者,但长期应用也无明显疗效。
(三)预防和控制感染
HAHD患者极易并发各种感染,尤其是上、下呼吸道感染,这在PHAHD极为普遍而且是致命性的,因感染后呼吸道缺氧更严重,肺动脉压更行增高、心力衰竭易于发生或很快加重甚至不可逆转。故预防和控制感染是一项关键性治疗,应选择强有力的抗生素,或者联合用药,疗效不佳须及时调整用药,但注意过敏和毒性反应。
(四)强心药物
有心功能不全或已有心力衰竭者应尽早选用快速洋地黄制剂,常用地高辛口服或去乙酰毛花苷(西地兰)静脉注射,20世纪在青藏高原较普遍地应用毒毛花苷K,疗效快速、稳定,一般在用药10天后心力衰竭可获得控制。在心力衰竭稳定后改为口服地高辛,然而在高原应用洋地黄制剂必须注意的是,高原心肌缺氧下对洋地黄的耐受性减低,另外高原多处水质过硬和含钙较高,用平原常规剂量有时也易出现中毒反应,必须加以注意。对心力衰竭并有水肿者,宜用利尿剂,其间注意水电平衡。
(五)放血疗法
对伴有显著红细胞增多症的患者,可行放血术,单独放血或同时输入等容量液体(等容血液稀释),而后者可能更为可取,因其改善症状的时间更长。然而,我们观察到偶尔在放血术后数日至数周出现了“反跳”现象,其时血红蛋白值又明显增高。放血疗法也只是权宜之计。
(六)降低肺动脉高压药物
α-受体抑制剂酚妥拉明(phentolamine mesilate)有降低肺高压的作用,但不稳定。目前认为硝苯地平(nifedipine)是降低高原肺高压较有效的药物,常先选用控释片口服,首剂10mg,后可20mg/d,应注意禁忌证,与氧疗并用,则可提高疗效。吴天一等对在青海海拔3 000m以上发病的AHAHD患者112例,应用枸橼酸西地那非片(sildenafil citrate tablets),每日25~50mg,疗程15~20日,有明显的降低肺动脉高压的作用,改善心功能,而极少副作用,值得采用。
(七)改善低氧通气药物
醋酸甲羟基孕酮(medroxyprogresterone acetate)可增加通气提高血氧分压(PaO2)而降低血二氧化碳分压(PaCO2)由此使血细胞比容(Hct)降低和改善若干症状,但有时在男性患者出现性欲减低,而被拒绝应用。
(八)中药/藏药
近年来,中药/藏药对HAHD的防治显示有较好的作用,如红景天(Rhodiola Eoccinea)在高原可改善睡眠,而高原睡眠低氧血症常很明显,该剂则可提高血氧合作用。其他如丹参、人参(红参性平为佳)及唐古特青兰等也有某些防治作用。
在我国,随着西部大开发及青藏高原的建设发展,从平原来到高原的人日益增多,而且逐步向高海拔区居住,尽管对高原病的防治工作获得了加强,然而机体对低氧的反应是生理规律,而且人群中存在对低氧易感的个体,尤其是在高原出生的婴幼儿或从平原移居高原2岁以下的儿童,是一个特殊的最易发生低氧损伤的群体。低氧性肺动脉高压不论在儿童和成年人中均极常见,其中重度的和持续的肺高压将发展为高原性心脏病,目前除了向低地转移外,高原就地治疗尚难取得明显效果,因此对HAHD的系统研究特别是有效防治尚需进一步深入。
面对PHAHD的严峻挑战,高原医务人员逐步提高了认识,积累了经验,在防治上有几个关键问题必须高度关注。
1.低体重儿
在高原出生的汉族新生儿中低体重儿的发生率较高,即体重低于2500g,据吴天一等在果洛(海拔3750m)地区的调查,对42例汉族新生儿其母亲在该地至少生活2年以上,另32例藏族新生儿均为当地世居者后代。藏族新生儿平均体重为(3448±48)g,汉族新生儿平均体重为(3014±42)g,较藏族明显为低(P<0.05),汉族低体重儿发生率为19%,藏族为3%。经随诊2年,汉族低体重儿中有5例(12%)发生PHAHD,其中3例死亡,而藏族低体重儿中无1例发生PHAHD者。汉族低体重儿的宫内发育不良,肺小动脉的肌性结构更重并在出生后退化极为延滞,从而形成严重的肺动脉高压。高原低体重儿是发生PHAHD的一个重要危险因素。
2.改善婴幼儿的营养状态
PHAHD患儿常有营养不良及贫血,先天不足和后天消化道功能低下,30%左右有腹泻,夜间哭闹不安,体能消耗很大,不少患儿面黄肌瘦,十分衰弱。因此改善哺乳及饮食营养极为重要,必要时少量多次输血或输入血浆、白蛋白等。
3.孕妇的低氧习服状态
孕妇的高原低氧习服优劣直接影响到新生儿的健康状态。移居高原的汉族孕妇中有一部分处于习服不良状态,其心血管功能较低,通气水平低下,在妊娠期有明显的低氧血症,对胎儿的供氧及营养提供不足,从而导致宫内发育迟缓(IUGR),由此形成高原低体重新生儿。如果孕妇有心血管问题、高血压、过劳、吸烟等因素,或有妊娠前子痫或有过流产史者,则其胎儿的IUGR呈高发生率,特别是有妊娠期贫血的孕妇。一项在海拔2220~4850m地区的观察发现,孕妇的贫血程度和海拔的高度与新生儿体重呈负相关。因此在妊娠前后提高孕妇的习服水平和改善营养状态是另一个预防PHAHD的关键因素。
4.汉族孕妇以到平原分娩为佳
最有效的预防是汉族孕妇,特别是在海拔3000m以上的孕妇,最好在预产期前6个月返回平原,并在平原分娩,这样会有许多安全因素;此外,如能待到小儿2岁以后再一起去高原,则较理想,实施多年来证明,这一措施已使PHAHD发病明显减少。













