睡眠呼吸暂停(sleep apnea,SA)指睡眠时间歇性发生的口鼻呼吸气流消失持续10秒以上。SA可分为阻塞型、混合型及中枢型三种。阻塞型睡眠呼吸暂停(obstructive sleep apnea,OSA)指上气道完全阻塞,呼吸气流消失但胸腹呼吸运动仍存在;中枢型睡眠呼吸暂停(central sleep apnea,CSA)指呼吸气流及胸腹部的呼吸运动均消失;混合型睡眠呼吸暂停(mixed sleep apnea,MSA)兼有二者的特点,一般先出现CSA,接着为OSA。三者常出现在同一患者的睡眠过程中,但以其中一种为主。上气道部分塌陷时,呼吸气流虽未彻底消失,但通气量已不能满足机体需要,称为低通气(hypopnea),其定义为呼吸气流下降至基础值的20%~50%,且伴血氧饱和度(SaO2)下降4%以上或觉醒,临床后果及诊治与SA相同(图1),常与OSA合并。睡眠呼吸暂停低通气综合征(SAHS)指由于睡眠时频发呼吸暂停及/或睡眠通气不足导致低氧血症和睡眠紊乱,从而引起的一系列病理生理改变及日间不适症状。以阻塞型睡眠呼吸暂停低通气综合征(OSAHS)最为常见,占90%以上,其次为中枢型睡眠呼吸暂停低通气综合征(CSAHS),混合型睡眠呼吸暂停低通气综合征(mixed sleep apnea hypopnea syndrome,MSAHS)在成人中少见。临床上将AHI超过5次/h,但无症状的个体称为阻塞型睡眠呼吸暂停低通气者,而并非“综合征”患者。上气道阻力综合征(upper airway resistance syndrome,UARS)是由于入睡后上气道阻力异常增加所致的睡眠障碍性疾病。患者以白天嗜睡为主要症状,系因夜间频繁觉醒,睡眠质量下降所致。呼吸气流并无减低,血氧正常。
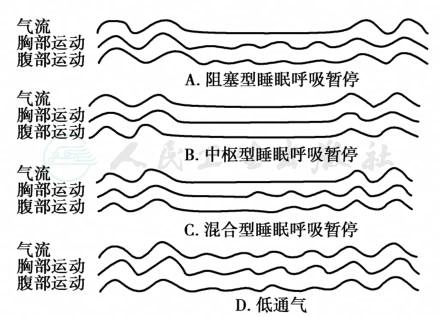
图1 睡眠呼吸暂停与低通气分型
A.阻塞型睡眠呼吸暂停:呼吸气流消失但胸腹呼吸运动仍存在;B.中枢型睡眠呼吸暂停:呼吸气流及胸腹呼吸运动均消失;C.混合型睡眠呼吸暂停:呼吸暂停过程中先出现CSA,接着为OSA;D.低通气:呼吸气流幅度降低但未完全消失。
(一)阻塞型睡眠呼吸暂停的易患因素及发生机制
睡眠呼吸暂停并非一独立的疾病,而是多种病变的一种共同病理表现,其发生是多种因素共同作用的结果(表1)。全面了解这些易患因素,对指导进一步的治疗有帮助。例如,对部分存在上气道解剖狭窄者(表2),外科手术治疗可能取得良效。OSA发生的关键在于睡眠时咽气道的塌陷。气道阻塞的部位可以在鼻咽部、口咽部或喉咽部,80%以上的患者为口咽和喉咽部的联合阻塞。引起上气道阻塞的原因既有解剖上的异常,又有功能上的缺陷。它们都是通过增加咽气道的可塌陷性、影响其开放与关闭的力量对比而发挥作用(图2)。
(二)中枢型睡眠呼吸暂停的病因及发生机制
发生中枢型睡眠呼吸暂停时,中枢呼吸驱动暂时丧失,气流及胸腹部的呼吸运动全部消失,胸膜腔内压为零。CSA与呼吸控制功能失调的关系较为明确(表3,图3)。
表1 阻塞型睡眠呼吸暂停的易患因素

表2 可诱发OSA的上气道解剖异常

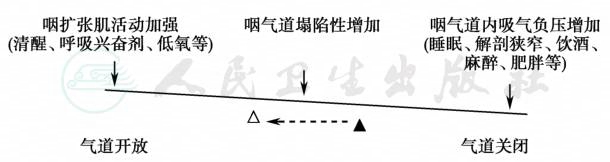
图2 咽气道塌陷性增加的发生机制
咽气道的开放与塌陷取决于以上各力量的平衡,从上图可见三角形支点右侧使上气道闭合的力量主要为气道负压,支点左侧使上气道开放的力量主要为咽扩张肌的活动,咽腔内在塌陷性增加(支点左移)时,也易发生睡眠呼吸暂停。
表3 可引起中枢型睡眠呼吸暂停的疾病

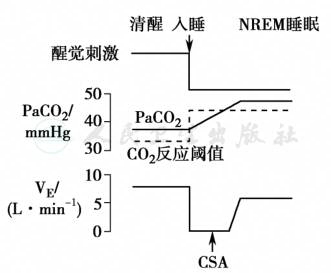
图3 中枢型睡眠呼吸暂停与呼吸控制功能失调的关系
在欧美等发达国家及地区,SAHS的成人患病率为2%~4%,中国香港中年男性SAHS的患病率为4.1%。国内多家医院的流行病学调查显示有症状的SAHS的患病率在3.5%~4.8%,且南北差异不明显。男女患者的比率为2∶1~4∶1,进入更年期后,女性的发病率明显升高。老年人睡眠时呼吸暂停的发生率增加,但65岁以上的重症患者减少。
(一)上气道解剖结构异常
上气道机械性狭窄对睡眠中上气道的塌陷和闭合起到重要作用,而上气道解剖结构的狭窄则是发生机械性狭窄的病理学基础。CT和MRI等影像学检查显示OSAS患者咽部的口径和容积均小于对照组。上气道任何部位或水平的狭窄,如鼻腔肿瘤、鼻甲肥大、鼻中隔偏曲、扁桃体肥大、软腭肥大下垂、舌体肥大等都可以发生睡眠呼吸暂停。咽部是上气道阻塞的好发部位。可以单独发生在咽部的一个水平或同时发生在两个以上水平。上气道塌陷部位会随睡眠的不同分期和睡眠的体位不同而发生变化。肥胖与OSAHS发生密切相关,主要是由于脂肪在咽部气道周围的沉积形成对气道挤压的缘故。上气道狭窄的直接影响是气道内气流加速和跨腔压增加,构成上气道闭合和塌陷的力学基础。
(二)睡眠对上气道的影响
OSAHS患者在清醒状态下尽管存在上气道狭窄,但并不打鼾和发生呼吸暂停。正常人清醒时上气道阻力和流速关系曲线与睡眠时无明显差别;而OSAHS患者清醒与睡眠状态则存在显著不同。提示OSAHS患者在睡眠状态下上气道功能发生了很大变化。OSAHS患者保持咽腔开放的重要机制在于上气道扩张肌吸气相收缩活动增加和张力增高,而在睡眠状态全身肌肉活动和神经肌肉反射减弱(包括上气道扩张肌)。上气道扩张肌肉张力减低、上气道腔内径减小,咽腔侧壁顺应性增加。睡眠状态时OSAHS患者上气道扩张肌对于胸腔负压和气道阻力增加的反射减弱或消失,REM期更为明显。由于保持上气道开放力量降低或消失,在胸腔负压作用下更容易发生塌陷和闭合。发生睡眠呼吸低通气和呼吸暂停时,高气道阻力、低氧和高二氧化碳的刺激使呼吸肌缩力明显增强,无疑会大幅度增加胸内和上气道的腔内负压,促成上气道塌陷。同时睡眠呼吸暂停的发生还与咽腔扩张肌同膈肌收缩不同步、配合不协调有关。
(三)气道呼吸力学的改变
研究表明引起OSAHS患者上气道关闭的因素有很多,解剖学因素固然是一个重要的方面,但更重要的还是功能性改变,因此应当重点研究引起上气道关闭的功能因素和机制。上气道的开放与关闭由以下几方面因素决定:管腔内压(intraluminal pressure)、管腔外压(extraluminal pressure)、跨壁压(transluminal pressure)和管壁的顺应性(compliance of luminal wall)等。呼吸过程中上气道的腔内压主要决定于吸气肌的收缩力。其收缩力越大,管腔内压力越低,腔内压越低管腔越容易塌陷或闭合。管腔外压力由颌面部器官和组织的重力与围绕在气道周围的脂肪沉积构成,腔外压力越大,管腔越容易塌陷和闭合。跨壁压是管腔外压力与管腔内压力之差,跨壁压越大管腔越容易塌陷。上气道的开放与闭合主要是跨壁压与管壁顺应性相互作用的结果。管壁的顺应性决定于管壁自身的张力。上气道扩张肌收缩力减低或松弛会使管壁顺应性增加,气道趋向狭窄。环绕上气道的组织对上气道黏膜的牵拉力也是对抗胸腔负压,保持气道开放的一种力。管腔狭窄会使腔内流速加快,速度越快腔内压力越低,跨壁压越大,管腔越容易闭合。顺应性增加形成的上气道狭窄、阻力增加及通气不足会反射性地引起呼吸肌收缩力的增强,出现上气道内压异常减低和跨壁压异常增高,最终发生上气道的不完全或完全闭合。咽部黏膜的表面张力具有阻止上气道重新开放和促成、维持咽腔气道塌陷的作用。一旦发生气道完全闭合,则会维持于呼气相和吸气相的全过程。咽部黏膜层的增厚是反复发生的压力变化和打鼾损害的结果。
临界压(critical pressure,Pcrit)是上气道完全闭合瞬间吸入气流为零时咽部气道内的压力(腔内压)。用以定量表示上气道倾向于闭合的趋势和严重程度,其大小与上气道阻塞部位以上和以下(胸内)的压力,及上气道阻力等因素相关。正常人清醒时Pcrit<-41cmH2O,睡眠时为-13cmH2O;OSAHS患者清醒时为-40~-17cmH2O。发生睡眠低通气和呼吸暂停时分别为-1.6cmH2O和2.78cmH2O,明显高于正常人。
(四)上气道顺应性对OSAHS的影响
上气道顺应性是决定患者上气道管腔压的重要因素,咽部是一个缺乏骨和软骨支持的管腔型器官,决定了它具有较高的顺应性和易塌陷性。清醒状态下OSAHS患者上气道顺应性正常或低于正常水平,睡眠状态时上气道顺应性增加,在高的跨壁压和吸气负压作用下极易闭合和发生呼吸暂停。除上气道扩张肌相关的神经肌肉因素外,上气道血流灌注状态对上气道的顺应性也有影响。
(五)神经肌肉因素
上气道的开放有赖于上气道的通畅程度,包括咽部扩张肌功能正常和神经肌肉反射功能正常。而咽腔狭窄者咽腔的开放则很大程度上依靠扩张肌收缩来维持,任何程度的扩张肌收缩活动减弱或消失都会明显增加上气道的阻力,导致上气道进一步狭窄和塌陷。CSA的发生主要是由于脑干呼吸控制中枢障碍致使呼吸冲动发放障碍和紊乱,具体细节目前尚不完全清楚。男性、高龄、低碳酸血症者易发生CSA,此外发现慢性充血性心力衰竭患者容易发生CSA。
患者睡眠时呼吸暂停短则10秒,长则2分多钟。首先,长时间反复发生呼吸暂停低通气可导致间断低氧血症,血氧饱和度可降到60%~80%。严重低氧可引起儿茶酚胺、肾素-血管紧张素和内皮素分泌增加,微血管收缩,血管内皮细胞损害,胸内压大幅度波动,内分泌功能紊乱,自主神经调节功能失调,血流动力学和流变学改变,微循环异常,使组织器官缺血、缺氧加重而导致多系统器官损害。同时,反复发生重度呼吸暂停也会引起CO2潴留和呼吸性酸中毒。其次,由于睡眠过程中不断出现睡眠中断,睡眠质量下降,因而白天嗜睡,严重时出现各种神经、精神症状。再次,睡眠重度打鼾,上气道阻力增加,患者张口呼吸,会引起咽喉部慢性感染。此外,呼吸暂停时胸膜腔内负压增加,引起或加重胃食管反流。
频发的SA可引起严重的血气异常及睡眠紊乱,从而累及全身各个系统。近年来,SA引起的自主神经系统功能紊乱对心血管系统的损害也引起了广泛的重视(图4)。
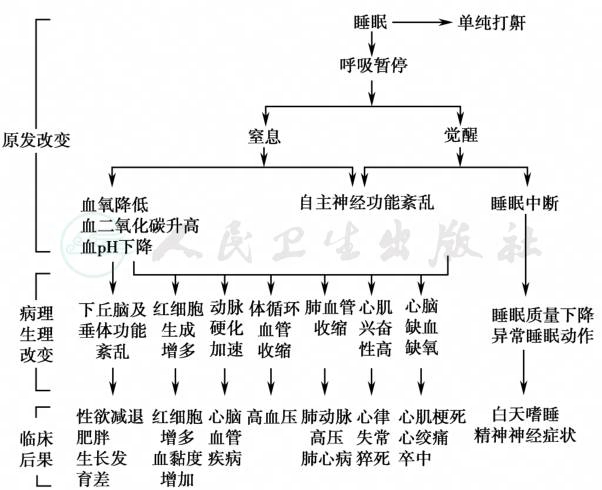
图4 睡眠呼吸暂停的病理生理改变
(一)筛查
可通过问卷进行,结合已明确的主要危险因素、体格检查、临床症状等,给出危险性评估结果。如STOPBang问卷,通过打鼾、乏力、目击的呼吸暂停、血压、体重指数、年龄、颈围、性别共8个项目,评价危险性。对于危险性较高者,需进一步检查明确。
(二)多导睡眠监测(PSG)
标准的PSG包括至少7个参数,包括脑电图、眼电图、颏肌电图、心电图、口鼻气流、胸腹呼吸运动、血氧饱和度(SaO2),还应监测患者体位、腿动等,需有技术人员参与,必要时进行干预。可根据患者实际情况进行:①整夜PSG监测:诊断OSAHS的标准手段,需不少于7小时的睡眠,客观评估患者夜间不良事件与疗效,鉴别诊断其他睡眠障碍性疾病等;②夜间分段PSG:前2~4小时进行PSG,之后进行2~4小时的持续气道正压通气(continuous positive airway pressure,CPAP)压力调定,可减少检查和治疗费用;③午后小睡的PSG监测:可用于白天嗜睡明显者,需保证有2~4小时睡眠(包括REM和NREM)。
(三)便携式睡眠监测(PM)
需至少包括口鼻气流、SaO2、胸腹运动等参数。可用于:①临床症状严重且提示有呼吸暂停,需尽快治疗,且无法进行标准PSG者;②无法在睡眠实验室进行监测;③已明确诊断,用于疗效随访。由于PM未记录睡眠分期、体位和呼吸相关觉醒,监测结果阴性时仍不能除外OSAHS。
(四)其他通气测定方法
直接监测通气用咬口或面罩收集呼出气,不易耐受,且影响自然睡眠状态。间接监测通气包括定性和半定量两种方法。定性方法应用热敏电阻或快速CO2分析仪监测呼出气体。半定量方法采用磁强计或呼吸感应性体容积描记仪。胸腹呼吸运动可用膈肌电图、经膈压测定和呼吸感应性容积描记仪监测。监测的内容主要有PaO2、PaCO2和SaO2。
(五)相关检查
如体格检查包括身高、体重、颈围、血压(睡前和醒后血压)、评定颌面形态、鼻咽部的检查,心、肺、脑、神经系统检查等,血常规,动脉血气分析,肺功能检查,影像学检查(如上呼吸道三维CT重建),心电图或动态心电图、高危因素(如甲状腺功能)相关检查,合并症相关检查等。
(六)嗜睡评估
1.主观评价
现多采用ESS嗜睡量表(表5),评价白天嗜睡程度。
表5 ESS嗜睡评分量表

注:最近几个月以下情况打瞌睡的可能,如没做过,试着填上它可能给你带来多大影响。
2.客观评价
有条件可进行多次睡眠潜伏期试验(MSLT)。通过让患者白天进行一系列的小睡来客观判断其白天嗜睡程度的检查方法。每2小时测试1次,每次小睡持续30分钟,计算患者入睡的平均潜伏时间及异常REM睡眠出现的次数,正常成年人睡眠潜伏期为10~20分钟,如果平均睡眠潜伏期<5分钟为嗜睡,5~10分钟为可疑嗜睡,>10分钟为正常。
(一)病因治疗
甲状腺功能减退是SA肯定的病因之一,甲状腺素替代治疗后SA常可减轻或消失。半数心力衰竭患者可出现SA,以CSA为主,经药物治疗心功能改善后,CSA可以好转。
(二)氧疗
对于绝大多数SAHS患者,氧疗并无必要;有氧疗指征者,也应与气道持续正压通气结合进行,以免单纯吸氧延长SA持续时间而引起CO2潴留、加重睡眠紊乱。
(三)一般治疗
指导患者养成良好的睡眠习惯,获得足够的睡眠时间及最好的睡眠质量。减肥、戒烟、戒酒、慎用镇静安眠药物、侧卧位睡眠及应用鼻黏膜收缩剂滴鼻保持鼻道通畅,对轻症患者及单纯打鼾者可能有效。
(四)药物治疗
甲羟孕酮(安宫黄体酮)、乙酰唑胺具有呼吸兴奋作用,均曾被试用治疗CSAHS,但由于疗效差、副作用大,现已少用。目前尚无药物对SA有肯定疗效。
(五)口器治疗
主要有下颌移动装置及固舌装置,是针对喉咽部狭窄的治疗手段。前者通过前移下颌骨使舌体前移而扩大上气道,后者直接牵拉舌体而防止舌根后坠。对轻、中度SAHS患者或不耐受CPAP治疗者可试用。
(六)手术治疗
手术治疗主要基于两个目的:①绕开睡眠时易发生阻塞的咽气道,建立第二呼吸通道。②针对不同的阻塞部位,去除解剖狭窄、扩大气道。由于其有创性及疗效有限,除一些具有手术适应证者、年轻轻症患者或CPAP治疗失败者外,手术治疗对大多数OSAHS患者不作为首选;对CSAHS患者无效。主要术式有气管切开造口术,腭垂咽软腭成形术(uvulopalatopharyngoplasty,UPPP),扁桃体、腺样体切除术,鼻中隔偏曲矫正、鼻息肉摘除、鼻甲切除等鼻部手术及针对喉咽部解剖狭窄的手术如颌骨前徙术、舌骨悬吊术、舌成形术。近年来,植入能够刺激舌下神经的起搏器通过舌根前移而改善睡眠呼吸暂停取得一定效果,已经获得美国FDA的批准。
总之,治疗OSA的手术复杂多样,必须仔细进行术前检查,严格选择手术适应证,必要时联合应用多种术式分期进行。
(七)持续气道正压通气治疗
无创正压通气(noninvasive positive pressure ventilation,NPPV)是指无须建立人工气道(如气管插管和气管切开等),在上气道的结构和功能保持完整的情况下实施的气道内正压通气。NPPV包括持续气道正压(continuous positive airway pressure,CPAP)、双水平气道正压(bilevel positive airway pressure,BPAP)和自动气道正压(auto-titrating positive airway pressure,APAP)等多种通气模式。1981年澳大利亚的睡眠呼吸疾病专家Sullivan教授等首次成功应用CPAP治疗OSAHS,1985年以后随着人机连接界面的不断改进,CPAP应用得到推广;1991年美国匹兹堡大学的睡眠呼吸疾病专家Sanders教授研发的BPAP呼吸机问世,能够有效提供通气支持、改善CO2潴留,拓展了无创正压通气的应用领域。1993年能够根据上气道阻力变化而自动调节呼吸机压力的APAP应用于临床,大大提高了患者的舒适度。近年来,随着计算机和自动控制技术的发展,在以上基本模式的基础上,多种新的无创通气技术相继问世,在提高使用舒适度、增加长期依从性和开拓适应证等方面取得了重要进展。(图5)
(1)无创气道正压通气的主要模式
CPAP是指在自然呼吸状态下,吸气相和呼气相持续输送一定的正压形成“气体支架”使上气道保持开放。CPAP只需设置一个固定压力,通常在4~20cmH2O。是最早研发并应用于临床治疗OSAHS的无创正压通气模式,目前仍然是大多数OSAHS患者的首选呼吸机模式。除OSAHS外,CPAP也可用于治疗中枢型睡眠呼吸暂停/陈-施呼吸(central sleep apnea with Cheyne-Stokes breathing,CSA-CSB)、某些肥胖低通气综合征(obesity hypoventilation syndrome,OHS)、部分OSAHS合并慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)即重叠综合征和治疗相关中枢型睡眠呼吸暂停(treatment-emergent central sleep apnea,T-ECSA)患者的治疗。CPAP简单易用、相对价廉,但不适合用于CO2潴留较重者,也不能根据患者的需要而自动调整压力水平和潮气量的大小。
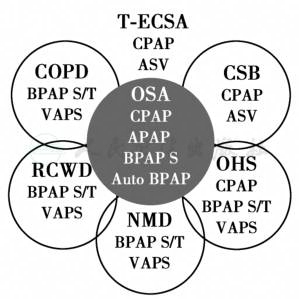
图5 用于治疗OSA的多种无创通气技术
T-ECSA:重叠综合征和治疗相关中枢型睡眠呼吸暂停;CPAP:无创呼吸机选择;ASV:适应性伺服通气;COPD:慢性阻塞性肺疾病;BPAP S/T:自主触发时间控制模式;VAPS:容量保证压力支持通气;CSB:陈-施呼吸;OSA:阻塞型睡眠呼吸暂停;APAP:自动气道正压;BPAP S:自主触发模式;Auto BPAP:自动双水平气道正压;RCWD:限制性胸廓疾病;OHS:肥胖低通气综合征;NMD:神经肌肉疾病。
BPAP通过分别设置和调整吸气压(inspiratory positive airway pressure,IPAP)和呼气压(expiratory positive airway pressure,EPAP)改善上气道阻塞。IPAP和EPAP之间的压力差即压力支持(pressure support,PS,PS=IPAP-EPAP)是保证足够潮气量的基础。通过扩大压力差来增强吸气力量支持和肺泡通气量,从而降低CO2水平,同时减轻呼吸肌负荷。EPAP可维持呼气相的上气道开放、改善阻塞型睡眠呼吸暂停、增加功能残气量、防止肺泡萎陷。BPAP可提供3种通气治疗模式。①自主触发(BPAP-S)模式:患者自主呼吸触发IPAP和EPAP的转换。BPAP-S模式需在治疗前分别设置IPAP和EPAP,在压力滴定时分别调节IPAP和EPAP的水平。②自主触发时间控制(BPAP-ST)模式:即在自主触发的基础上加入备用呼吸频率。患者可自主触发IPAP/EPAP的转换,如果在一定的时间内无自主呼吸,呼吸机将按照预设的备用呼吸频率补足呼吸频率。BPAP-ST模式除设置压力外,还应设置等于或稍低于睡眠中自主呼吸频率的备用呼吸频率和适当的吸气压力上升时间。③时间控制(BPAP-T)模式:该模式需设置呼吸频率和IPAP时间即IPAP/EPAP及吸气、呼气压力水平。无论患者呼吸状况如何,呼吸机均以固定的呼吸频率、固定的吸气/呼气比例或固定的IPAP/EPAP切换时间送气。BPAP可用于OSAHS的治疗,但其更重要的应用指征是慢性肺泡低通气,该类患者常伴CO2潴留,尤以睡眠时为重。与CPAP相比,BPAP治疗OSAHS的依从性并无明显差异。对于某些CPAP治疗失败者可试用BPAP。BPAP-ST模式使用不当造成过度通气时可能诱发中枢型呼吸暂停。BPAP-S模式通常用于CPAP滴定压力达到≥15cmH2O仍不能有效消除阻塞型呼吸事件或不能耐受高CPAP而出现严重呼气困难、吞气、窒息感的OSAHS患者。BPAP-ST模式主要用于限制性胸廓疾病、神经肌肉疾病(neuromuscular disease,NMD)和OHS患者,或因呼吸中枢驱动减低需要辅助通气患者,或合并日间呼吸衰竭的COPD患者,也可用于CSAS,特别是伴CO2升高的CSAS和T-ECSA患者。但无论哪一类型的CSAS,首先应治疗基础病。BPAP-S模式已达到最大压力支持(或最大耐受度)而未能维持足够通气或仍然存在呼吸肌疲劳可以应用BPAP-ST模式。但呼吸支持频率的设定应避免影响人机同步性。BPAP-T模式单独应用机会不多,但对可能出现呼吸骤停而又不能长期插管机械通气如急性进展性NMD患者提供有限的保护。
APAP根据探测到的气流量(呼吸暂停或低通气)、气流波形(气流受限)、震动(鼾声)和/或气道阻力在预设的最大和最小压力之间自动调整压力水平,保证上气道开放所需的最低有效治疗压力。APAP用于无充血性心力衰竭、无明显肺疾病、无非阻塞性呼吸事件所致夜间氧饱和度降低及无CSAS的中重度OSAHS患者,适于仰卧、REM睡眠、饮酒和服用镇静促眠药物相关的OSAHS的治疗。APAP可用于辅助进行非PSG下无人工值守的自动压力滴定,提供确定家庭CPAP最适治疗压力的参考值,也可用于OSAHS的长期家庭治疗。
其他新型无创正压通气模式包括:①自动双水平气道正压(auto BPAP)模式,根据睡眠中出现的各种呼吸事件,在所设置的EPAP和IPAP范围内分别自动调整EPAP和IPAP以保持气道开放。需设置最大IPAP、最小EPAP、最大和最小压力支持或固定压力支持。对压力敏感者或对CPAP和APAP的高压力不耐受者可能从Auto BPAP中获益,长期使用的依从性与CPAP相似,可能提高舒适度。②自动三水平呼吸(auto-trilevel PAP)模式,在呼气相前期输送压力相对较低的EPAP,呼气末适当提高EPAP,形成IPAP、EPAP和呼气末EPAP三个压力水平。有限的研究表明,该技术对于同步去除残存的阻塞型呼吸暂停和纠正高碳酸血症可能较BPAP更有效。③适应性伺服通气(adaptive servo-ventilation,ASV)模式,是以某一时间窗内峰流速或分钟通气量的90%为目标通气量,实时自动调整压力支持水平以达到目标通气量。当通气和气流降低时压力支持增加,而通气和气流升高时压力支持减少,具有稳定通气的作用。需设置固定EPAP或最大和最小EPAP、最大和最小压力支持及备用呼吸频率。EPAP保持气道开放以消除阻塞型呼吸暂停,压力支持在最大和最小之间与气流自动适应,使不稳定的呼吸幅度和节律趋于稳定,避免过度通气和低碳酸血症导致的中枢型睡眠呼吸暂停。目前已知ASV不适于治疗左室射血分数≤45%的CHF伴CSA-CSB的患者,但对左室射血分数>45%的CHF伴CSA-CSB者、CSAS、T-ECSA及阿片类所致CSA有一定疗效,但因对COPD、限制性肺疾病及NMD患者有加重CO2潴留的风险,不提倡使用。ASV的主要优势在于稳定通气,在治疗CSAS和T-ECSA方面,与BPAP-ST相比可进一步降低AHI,但对上气道完全闭合的中枢型呼吸暂停,呼吸机触发的压力支持常不能有效输送足够的气流或潮气量,需要提高EPAP水平以开放上气道。④容量保证压力支持通气(volumeassured pressure support,VAPS)模式,可通过自动调整压力支持的水平来保证设定的潮气量或肺泡通气量。当潮气量或肺泡通气量低于目标值时则提高压力支持,反之则降低压力支持。需根据目标潮气量或体重估算的肺泡通气量,预设EPAP、最大和最小IPAP、备用呼吸频率及IPAP时间或最小和最大压力支持。VAPS主要用于治疗COPD、NMD或OHS等CAH患者。其优势在于无论患者的呼吸努力、气道阻力和肺顺应性如何变化均可保证预设的目标潮气量,特别是REM睡眠的通气量。与BPAP-ST相比可进一步提高有效通气量、降低PaCO2,从而改善CO2潴留,但在改善睡眠质量方面二者无明显差异。
无创正压通气呼吸机的其他辅助功能包括延时升压功能、呼气相压力释放技术及呼吸事件自动追踪管理系统等可以提高舒适度,为临床决策提供依据。
(2)人机连接界面分类及应用
人机连接界面是无创通气人与呼吸机连接的界面。人机连接界面选择或佩戴不佳会导致不适及漏气,引起频繁觉醒、睡眠片断化,因治疗压力降低而影响呼吸机治疗效果和依从性,甚至治疗失败。必须认真选配人机连接界面,以达到漏气量最小、舒适度最好、安全性最佳、使用最方便的目标。
人机连接界面的类型包括:①鼻罩:覆盖并包绕整个鼻部,经鼻腔输送压力。简单易用、耐受性好,但容易经口漏气。②鼻枕:以两个鼻垫插入并封闭鼻孔,经鼻腔输送压力。与面部皮肤的接触面积最小,轻巧、易于接受、可避免漏气对眼睛的刺激,不影响患者佩戴时阅读。插入式鼻垫本身可引起鼻腔不适,压力较大时的直接作用对鼻黏膜刺激较大,患者入睡后易因鼻枕移位而漏气。③口鼻罩:同时覆盖口和鼻,患者可经口和/或经鼻呼吸,避免经口漏气。对于鼻腔阻塞、压力足够但仍张口呼吸而严重漏气的患者有益,但因与面部皮肤接触面积大,容易漏气且舒适性较差,还可造成幽闭恐惧。影响患者饮水、交流,与鼻罩相比,对疗效和依从性影响更大。④全脸面罩:遮罩整个面部。可作为缓解由于佩戴其他人机连接界面而造成鼻梁皮肤损伤的替代。因接触面部皮肤面积更大,更易漏气,舒适性也更差。⑤口含罩(mouth piece):蝶形软片置于唇齿间,密封罩夹固于唇外,经口腔输送压力。优势是不阻挡视野,防止口漏气和鼻周皮肤损伤。但易口干,特别需要加强湿化。可能出现鼻漏气。
目前已出现了各种品牌、样式和大小的人机连接界面,选择应该个体化。结合每个患者的面部情况、皮肤敏感性、治疗模式和压力高低按需选择不同款式和型号的人机连接界面。专业测量卡尺会有所帮助,但最可靠的方法还是患者充分试戴的体验。口鼻周围皮肤完好和上下齿列完整是佩戴鼻罩和/或口鼻罩的基础。压力滴定或开始NPPV治疗时大部分患者更愿意选择鼻罩,后续治疗中鼻罩的应用也最为普遍,通常是患者NPPV治疗的首选。习惯张口呼吸者鼻罩并非禁忌,最初治疗时可考虑口鼻罩或加用下颌托带,数日后张口改善即可更换为鼻罩。幽闭恐惧症、胡须浓密的患者更倾向使用鼻枕。选择鼻枕时鼻垫尺寸应足够大才能保证密封性。对于NPPV治疗期间严重鼻充血或张口呼吸而经相应治疗无效的患者可考虑使用口鼻罩。多个上齿缺如者须佩戴义齿使用口鼻罩。全脸面罩限于在医师指导下用于特殊患者。口含罩仅为其他面罩的补充,除非特殊情况如面部解剖结构异常、不能经鼻呼吸或NMD患者。极少数幽闭恐惧症患者也可能选择口含罩。NMD患者选择面罩时应充分考虑呼吸机故障、停电或呕吐等特殊情况下无法独自摘除面罩而引起的窒息风险,口鼻罩可能增加这种机会,而鼻罩更易经口漏气,导致有效通气量减少并使睡眠片段化,所以应仔细选择。
(3)湿化器可内置或外接于主机,分为冷湿化和加温湿化
冷湿化不具备加温功能,湿化效果有限。加温湿化器通过加热板使储水盒中水温升高,可维持吸入气的适宜温度和较大湿度、减轻黏膜干燥而提高舒适感。实验表明令人满意的温度为26~28℃,相对湿度为70%~80%。除加温湿化器外,还可以选择加温湿化管路,以防止气体在输送过程中因降温而在管路中冷凝,进一步提高湿化效果。加温湿化特别适用于干燥环境和经口漏气或鼻充血的患者。应当根据气候、环境、室内温湿度、使用压力水平及患者的感受来调节加温湿化水平。为防止冷凝水倒灌入患者呼吸道,呼吸机应放置在低于患者头部的水平,还可以下调加温湿化挡位、使用管路隔热套或加温管路,减少冷凝水的形成。尽管加温湿化可否提高NPPV治疗的接受性和长期治疗的依从性尚无定论,但对经口漏气、鼻充血或口鼻干燥患者在压力滴定及长期治疗过程中肯定建议使用。
(4)无创正压呼吸机治疗OSA压力滴定和参数设置
合适的治疗压力是保证治疗成功的关键,应用NPPV前需进行压力滴定。压力滴定是指通过逐渐调整压力,寻找并确定维持上气道开放所需最低有效治疗压力即最适压力的过程。该压力可消除所有睡眠期及各种睡眠体位下的呼吸暂停、低通气、呼吸努力相关性觉醒和鼾声,并维持整夜睡眠中氧饱和度在正常水平,恢复正常睡眠结构。最适压力并非一绝对数值,可在一个较小范围内动态变化。压力滴定的主要目的是为长期家庭无创通气治疗提供最适压力。技术人员整夜值守进行PSG下人工压力滴定是确定最适压力的标准程序。重度OSA患者还可以实施分段压力滴定(同一夜中前半夜PSG诊断分析,后半夜压力滴定),非PSG下的APAP自动压力滴定目前已广泛用于无重要合并症的中重度OSA患者。
在开始压力滴定前首先应详细询问患者的病史,包括睡眠史、既往史、过敏史、用药史和治疗史,评价有无合并症和并发症,认真回顾多导睡眠图,必要时进行胸部影像学、肺功能和动脉血气分析。对患者进行有关睡眠呼吸疾病、家庭无创正压通气压力滴定和治疗的教育,使患者了解治疗指征、作用原理和可能存在的不适与缓解方法。其次,帮助患者试戴面罩、适应压力。面罩应达到最大的舒适性和最小的漏气量。滴定期间,当观察到任何明显的非故意漏气或患者感觉到面罩不适,应当调整或更换面罩。根据患者具体情况选择适宜的NPPV设备、确定初始治疗模式及压力。滴定后还应当向患者介绍NPPV呼吸机的组件、使用意义、依从性和清洁保养注意事项等。
整夜或分段人工压力滴定使用标准PSG系统和与之连接的CPAP、BPAP或多模式滴定设备在正规睡眠中心或睡眠实验室中完成。自动压力滴定则使用APAP在睡眠实验室或家中进行。均应由具备一定经验的技师按照滴定规则执行操作,经睡眠医生检查审核滴定结果、选择合适的压力水平并出具滴定处方。
人工压力滴定是指在睡眠实验室应用PSG同时连接CPAP、BPAP或多模式压力滴定设备,根据睡眠过程中出现的呼吸事件逐步调整压力,以确定维持上气道开放所需的最低有效治疗压力的过程。为设定长期使用CPAP时的固定压力、使用BPAP时的IPAP和EPAP或使用APAP时的压力范围而提供依据。
(5)治疗依从性与随访
加强对长期家庭NPPV治疗者的跟踪随访是发挥最大疗效、改善患者远期预后的关键。由经培训的专业人员对NPPV治疗依从性、有效性和安全性进行密切临床观察和随访,包括面对面访谈、下载治疗数据,也可以通过远程医疗系统来实现。治疗后第1周、第1个月和第3个月及时随访,此后每半年或1年规律随访。通过询问原有症状的改善和存在的不良反应,以及下载NPPV实际使用时间、残存AHI、漏气量和潮气量来评价治疗效果和依从性。NPPV治疗前和治疗中的教育、选择合适的治疗模式及面罩、理想的压力滴定结果和合理的参数设置、早期和规律地主动随访、及时干预处理不良反应和不适感觉可提高治疗依从性。
OSAHS是一种多因素疾病,根据个体化特征,选择多种治疗方式联合应用将使得疗效显著提高。在精准医学的背景下,借助生物标志物、蛋白及基因组学研究结果、疾病表型分析等,可有效预测治疗手段的个体化疗效,有助于提高治疗的成功率和患者的依从性。物联网医学(Medical Internet of Things,MI-oT)借助物联网这一新兴信息技术,通过感知层实时采集信息,融合网络传递、汇集并处理信息,最后与医疗行业专业应用技术结合,可实现健康诊断、评估、干预、预警及紧急救治等。将物联网医学应用于OSAHS的全程管理,可贯穿疾病风险预测、预防、个体化诊断治疗、个体参与等多个环节,将为精准医学的实施提供极大的帮助。上海市呼吸病研究所和复旦大学附属中山医院曾共同建立首个“云加端物联网医学睡眠实验室”,患者或社区医疗机构用户端的监测数据经传感器和网络实时上传至医学中心,形成报告并反馈诊疗意见。同时借助物联网医学平台的大规模数据存储功能,进行海量信息深度加工和挖掘,可为OSAHS患者提供精细、动态、智能的疾病全程管理。













