英文名称 :plastic bronchitis
塑型性支气管炎(plastic bronchitis,PB)是一种较为少见的呼吸系统疾病,其特点是黏稠的内生性异物堵塞气管、支气管从而导致一系列的临床症状。早在公元2世纪Galen观察到患者咳出了一些支气管形状的物质,他推测可能是“肺动脉或者静脉”,后来的研究者证实为气道内的分泌物。
本病分为原发性和继发性,其病因未明。临床上以继发性多见,约占80%,原发性较少,约占20%。文献报道认为继发性常与以下疾病相关:①心脏病:先天性心脏病、风湿性心脏病、充血性心肌病等;②镰状细胞病;③肺部疾病:肺结核、支气管扩张、肺炎、慢性阻塞性肺部疾病、肺癌、哮喘、尘肺、曲菌病等;④其他:尿毒症、Ⅰ型糖尿病、流行性出血热、嗜酸性粒细胞增多症、白喉、类风湿关节炎等。Seear认为一部分病人与先天性心脏病Fangtan手术后有关。笔者将检索的国外报道塑型性支气管炎52例相关主要病种分类于表1。
塑型性支气管炎发病机制尚未明确,真实的发病率难以准确的获得,常存在诊断不足的问题。只有在患者咳出支气管形状的塑型物、支气管镜检查和尸检时才得以确诊。
塑型性支气管炎的塑型物中含有大量的黏蛋白,与正常呼吸道黏膜产生的黏液聚合物不同,其黏蛋白之间是交叉相连的而非线性连接的,其中仅含有少量的纤维蛋白。不同的学者对于本病分型有不同的见解。Seear根据塑型物的病理特点,把疾病分成两个类型,Ⅰ型炎症细胞型,Ⅱ型非炎症细胞型。Ⅰ型通常与支气管疾病有关,这一类型的组织学特点是上皮细胞炎症,临床表现通常是急性的而非慢性的。Ⅱ型多出现于发绀型的先天性心脏病和肺部淋巴管畸形,病理组织中缺乏炎症细胞,临床表现通常是慢性、反复的而非急性的。Brogan按照与塑型性支气管炎关联疾病的角度分为三个类别:过敏/哮喘相关、心脏疾病相关和特发性。而Rubin则认为,哮喘严重发作时气道黏液栓塞是由于分泌腺高反应性(secretory hyperresponsiveness)所导致,不能算真正意义的塑型性支气管炎。Madsen提出的疾病分析方法首先基于关联疾病,如致病因素不清楚才通过塑型物的病理特点进行分型。仅仅针对塑型物进行病理分型,并无助于患者的诊断、治疗和预后。
综合现有病例报道和小型的案例研究,可能与塑型性支气管炎关联的疾病包括:肺部疾病、心血管疾病、淋巴系统解剖异常、特发性和多因素性。根据证据的等级分为以下三个类别。
1.已被证实有关联性的疾病
具有Fontan循环的先天性心脏病、肺部淋巴管解剖异常、A型流行性感冒病毒或曲霉感染导致的肺炎。
2.可能具有关联性的疾病
吸入毒气(例如:芥子气)、镰状细胞病急性胸部综合征(sickle cell acute chest syndrome,SCACS)、严重的哮喘急性发作。
3.关联性未获证实的疾病
囊性纤维化、慢性阻塞性肺疾病、支气管扩张、细菌性肺炎。
(一)胸片
无特征。肺纹理增粗,部分或全肺叶肺不张,气胸,纵隔气肿,胸积液;间质性肺炎的X线征。(图1,图2)
(二)CT检查
特征性。肺纹理增粗,气管纹理致密影,部分或全肺叶肺不张,气胸,纵隔气肿,胸积液。(图3~图8)
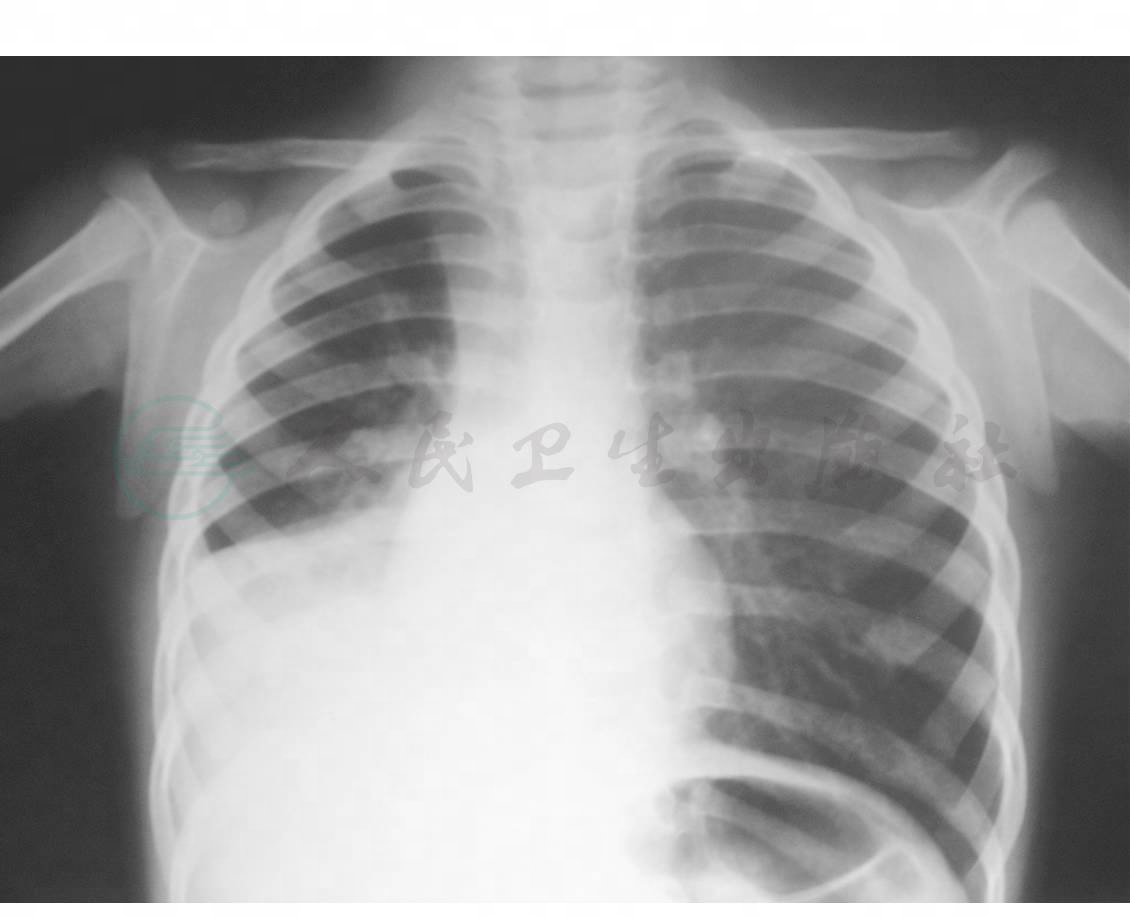
图1 塑型性肺炎X线胸片表现
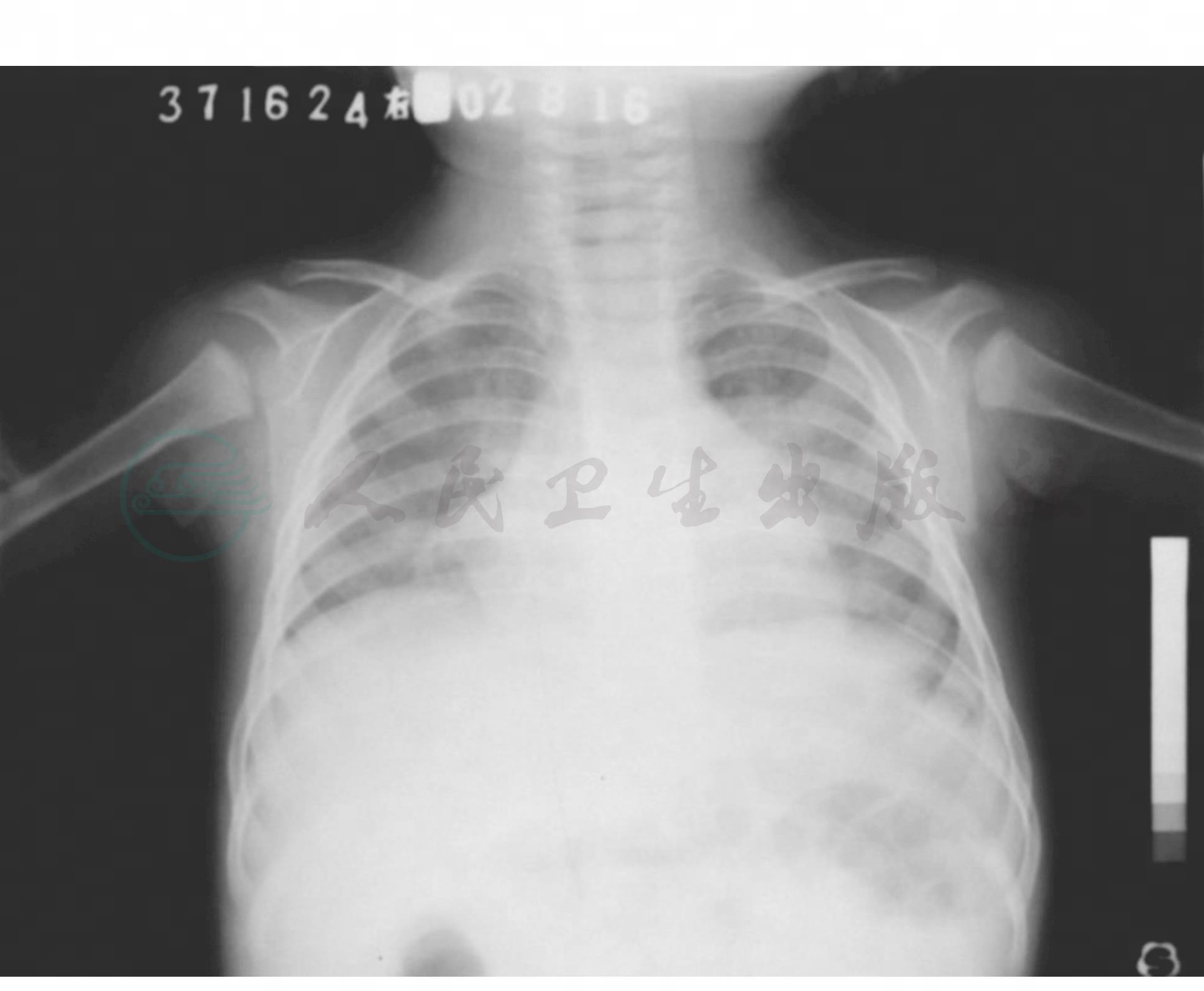
图2 塑型性肺炎X线胸片表现
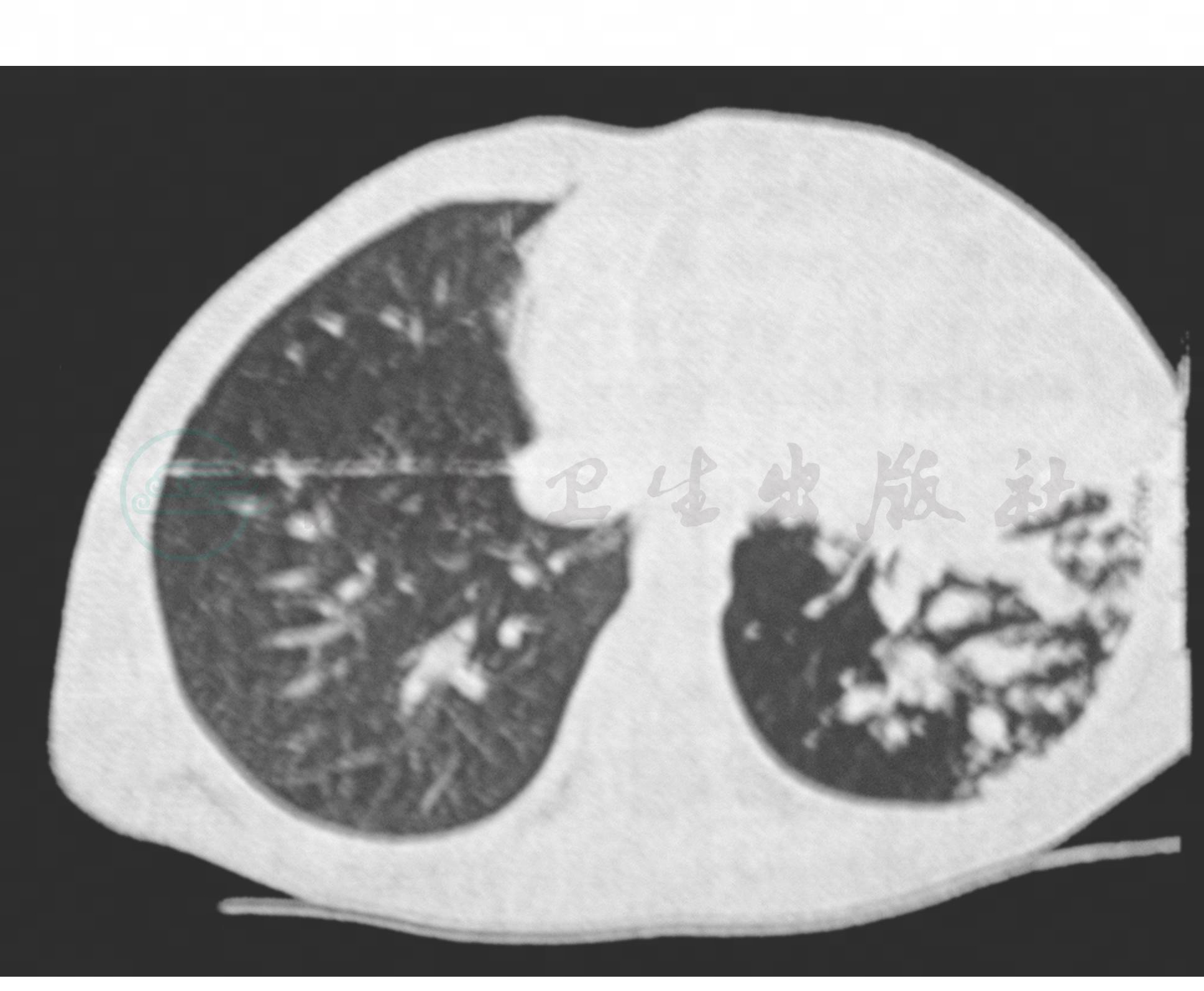
图3 塑型性肺炎CT表现
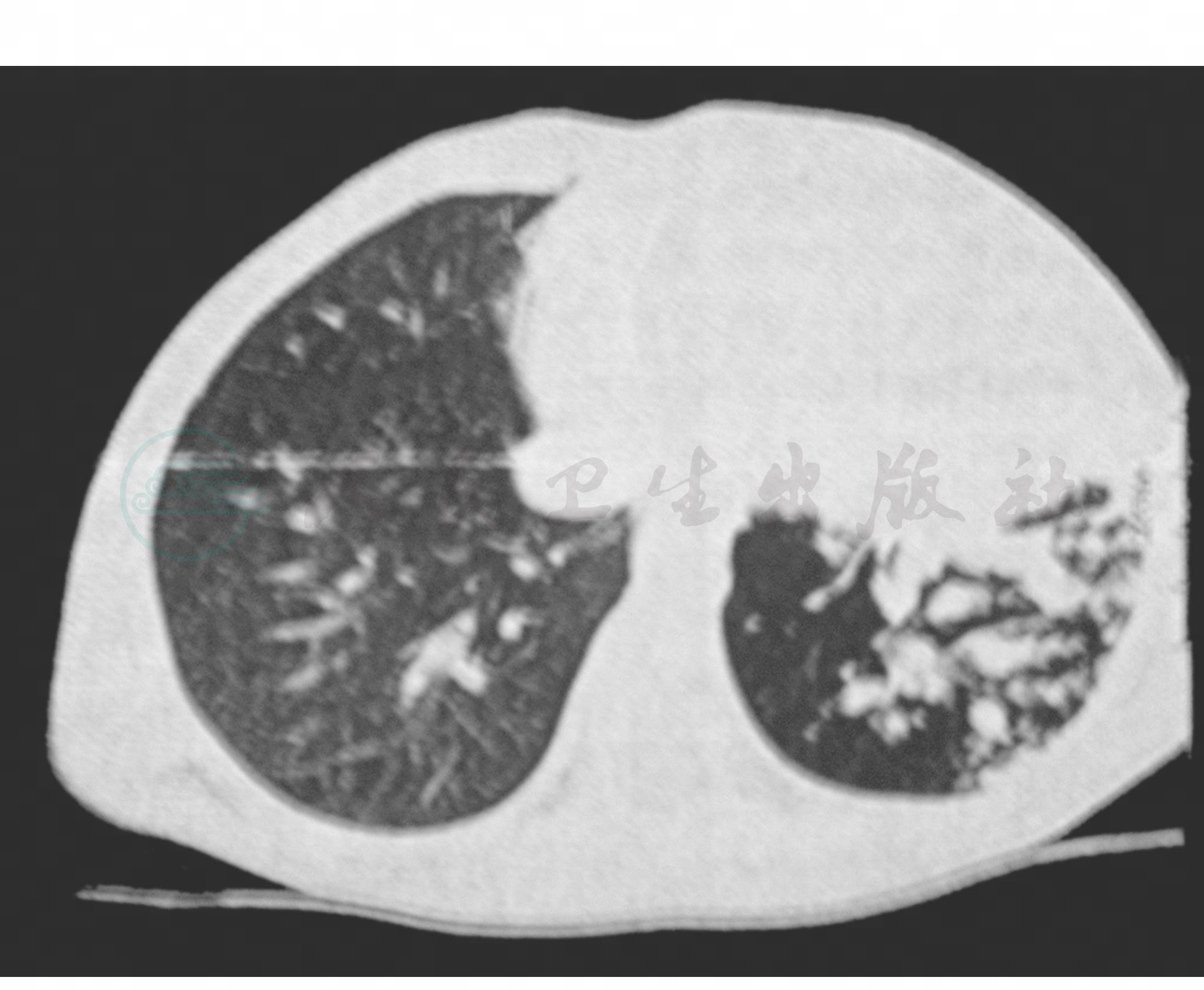
图4 塑型性支气管炎CT表现
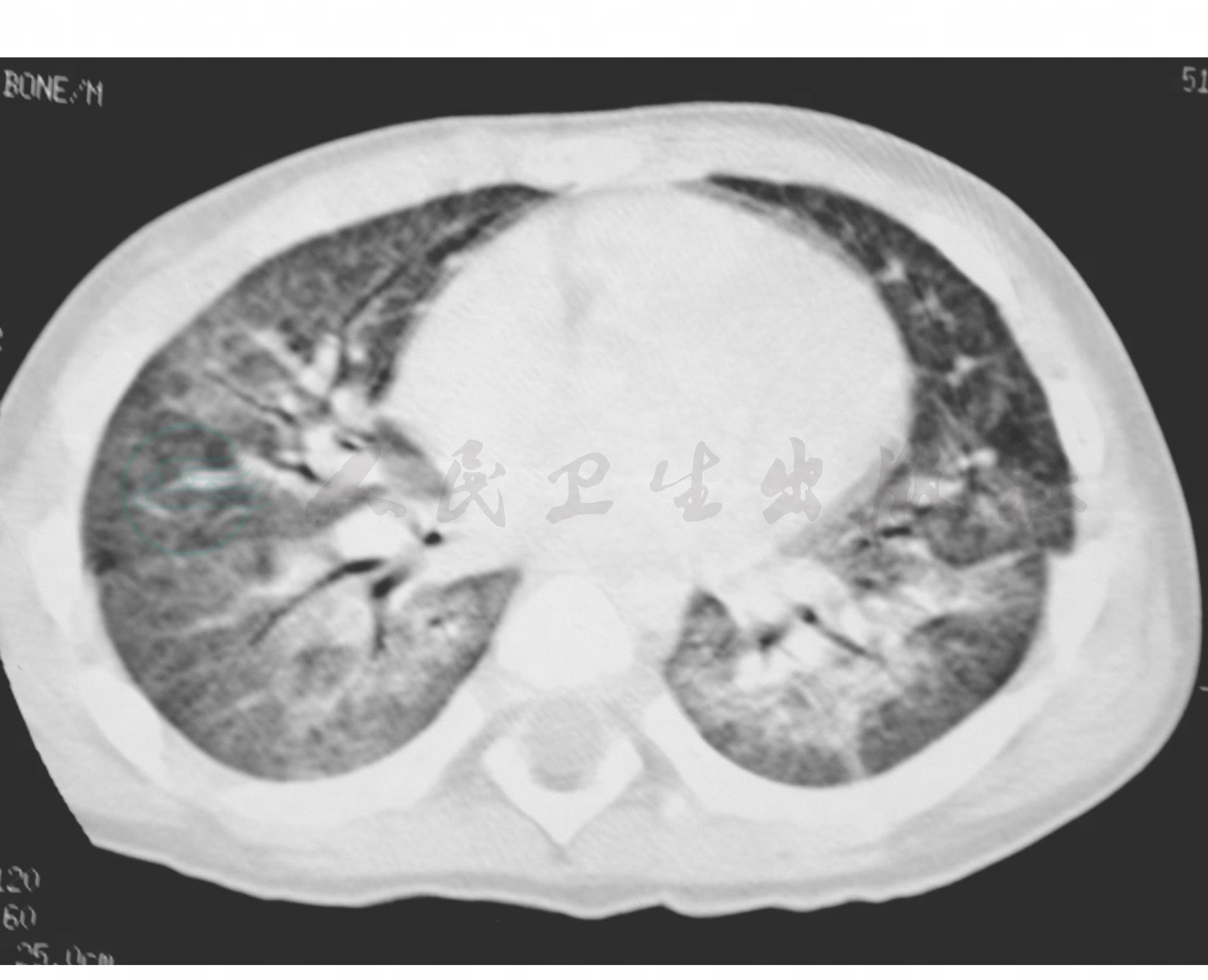
图5 塑型性支气管炎CT表现
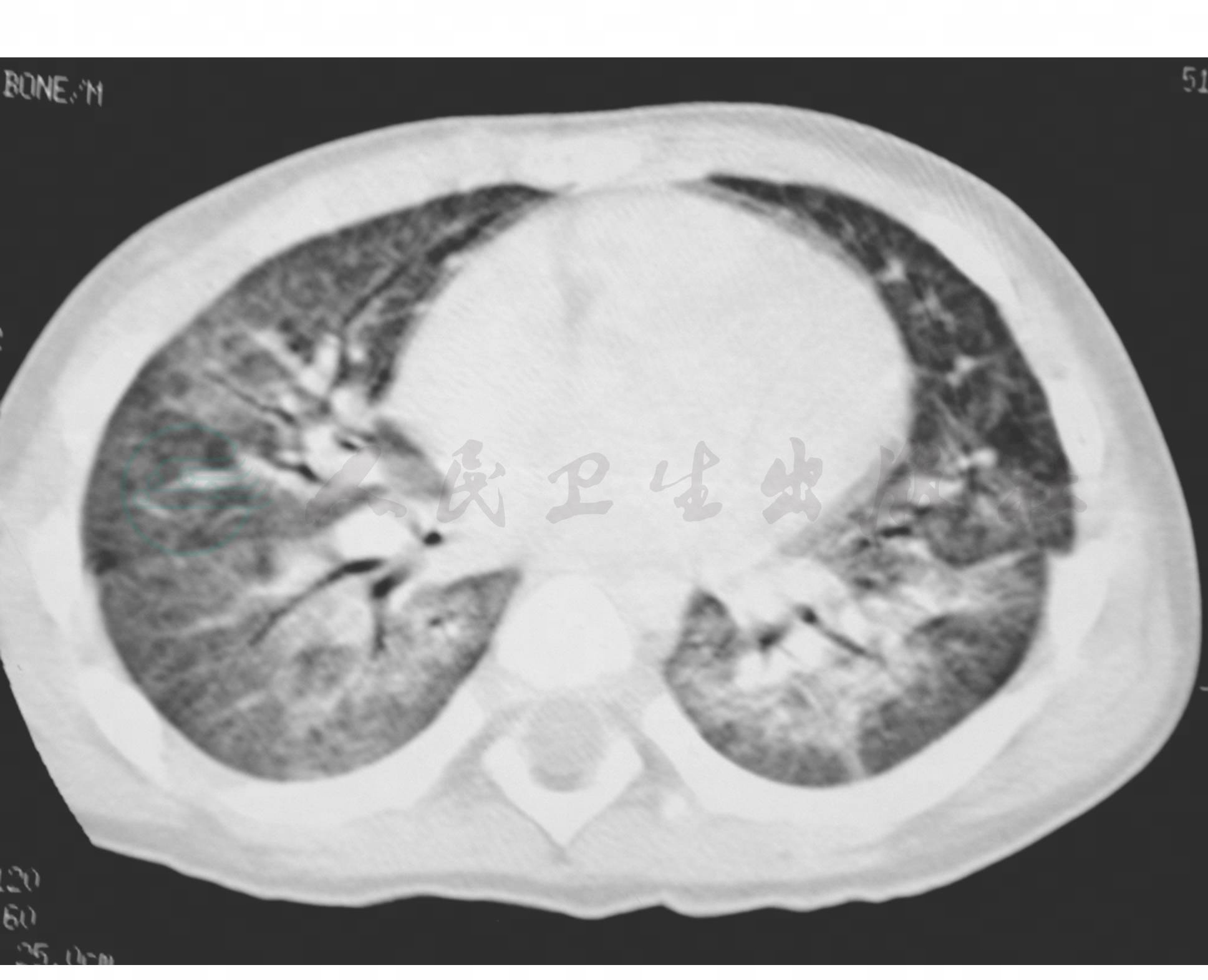
图6 塑型性支气管炎CT表现
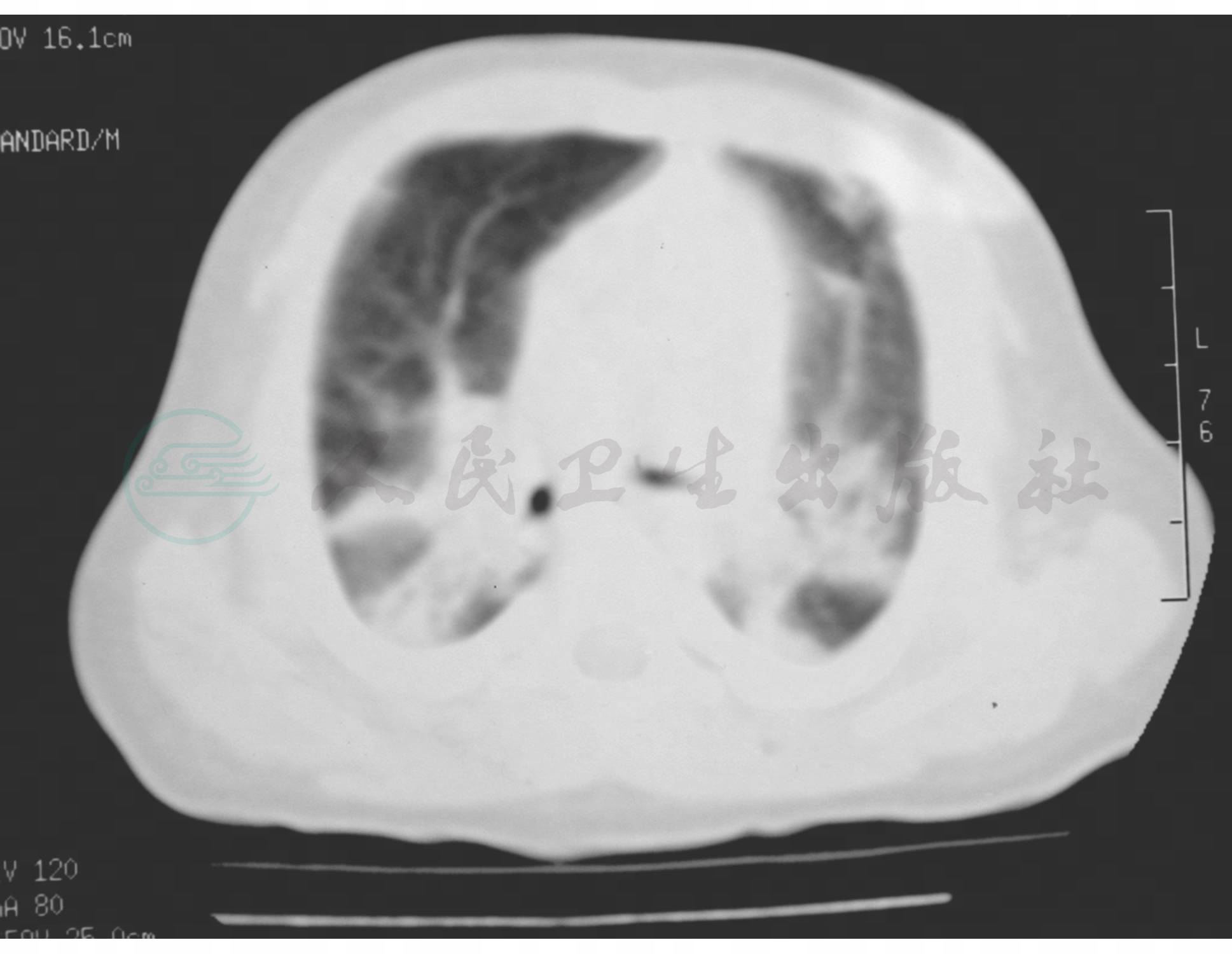
图7 塑型性支气管炎CT表现
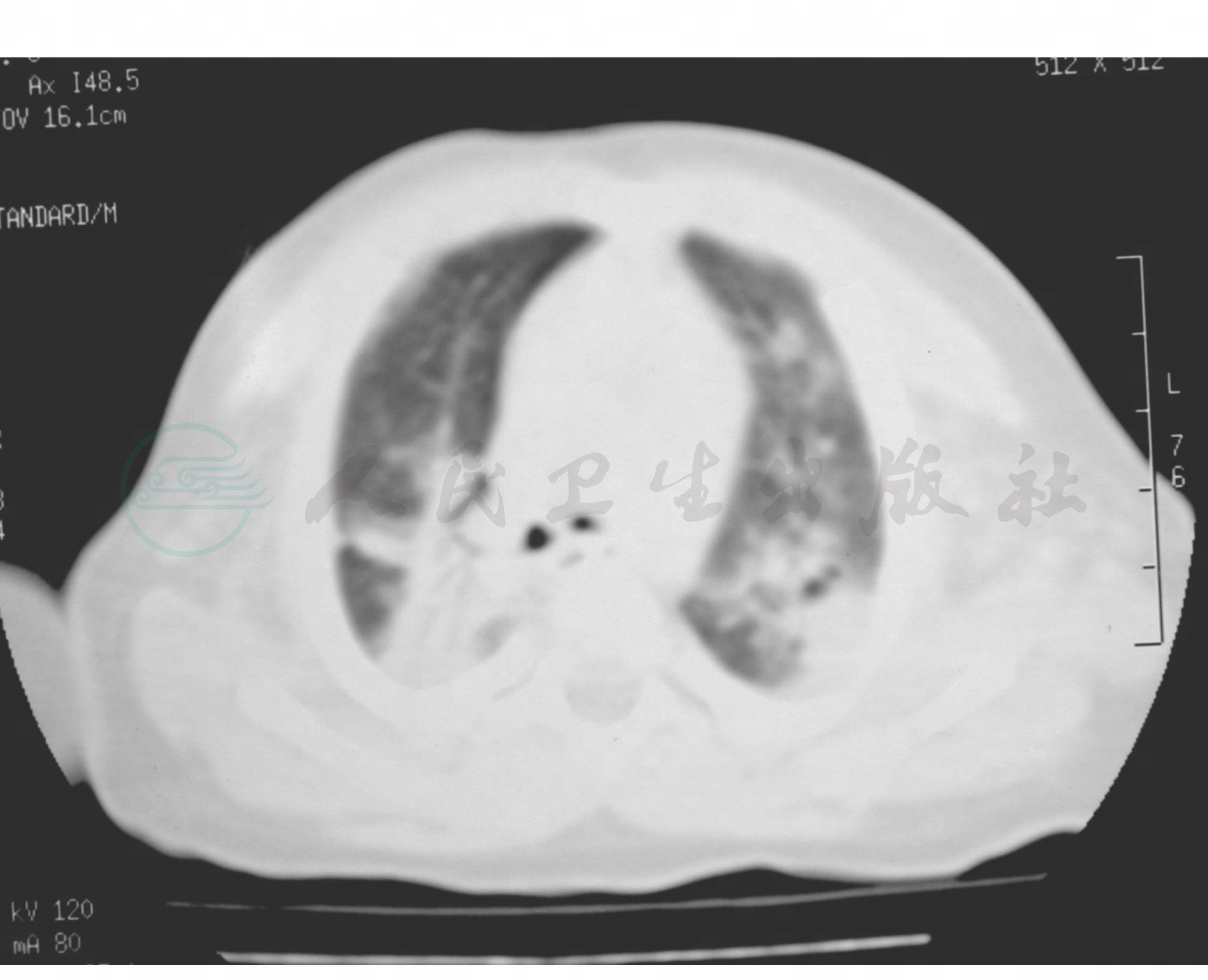
图8 塑型性支气管炎CT表现
(三)支气管镜检查
特征性。内源性异生物呈条块状,呈支气管塑型。未展开时外观看像脓痰,将其泡在生理盐水中展开可见支气管状塑性。
(四)病理组织学检查
大体可见条块状,支气管塑型;Ⅰ型气道腔内生异物光镜下所见的主要成分为黏液蛋白、纤维素和大量嗜酸性和中性粒细胞浸润,推测Ⅰ型的发病应与炎症和过敏反应相关;Ⅱ型气道腔内生异物光镜下所见的主要成分为黏液蛋白和纤维素,有少量或完全没有炎症细胞浸润,镜下所见为一片均质伊红染色。
大体标本:冻胶状支气管树样物质(图9)。
Ⅰ型低倍镜下病理标本所见:大量纤维素样渗出物质和炎性细胞浸润(彩图10)。
Ⅰ型高倍镜下病理标本所见:大量脓细胞、纤维素和坏死组织(彩图11,彩图12)。
Ⅱ型低倍镜所见的主要成分为黏液蛋白和纤维素,有少量炎症细胞浸润(彩图13)。
Ⅱ型高倍镜下病理标本所见:纤维素样物质呈均质嗜伊红染色(彩图14)。
电镜图见图15~图20。
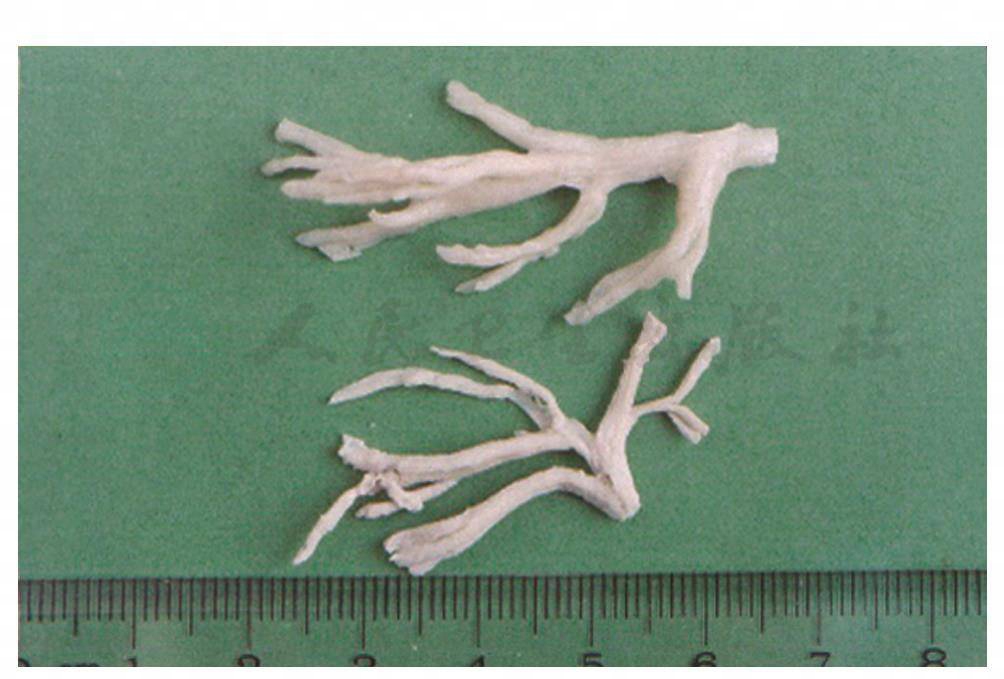
图9 塑型性支气管炎内源性异生物大体标本
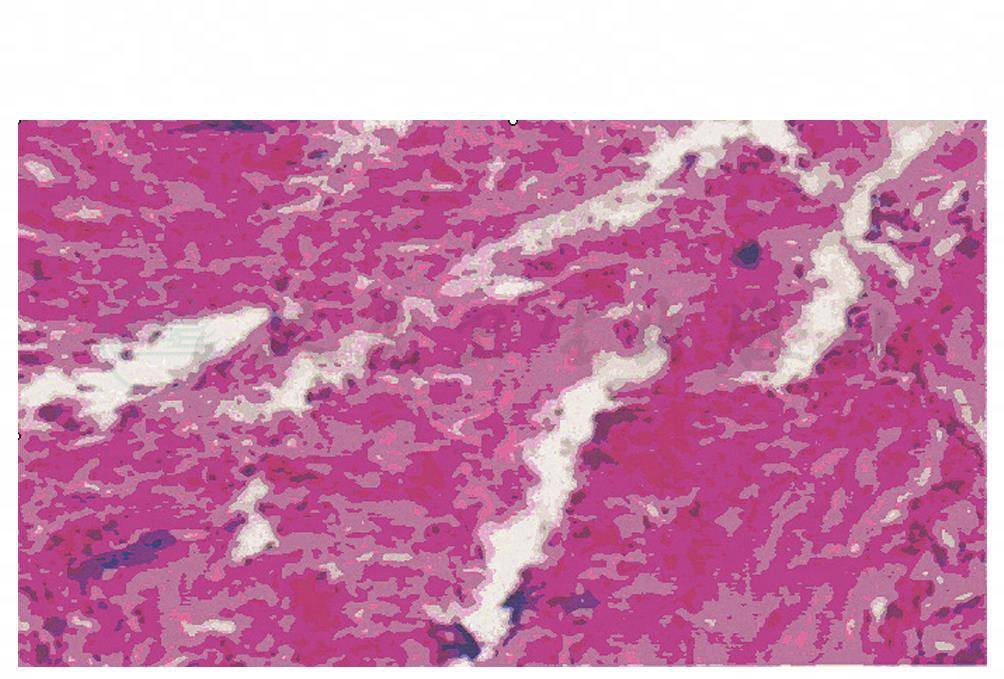
图10 Ⅰ型塑型性支气管炎低倍镜下的病理改变
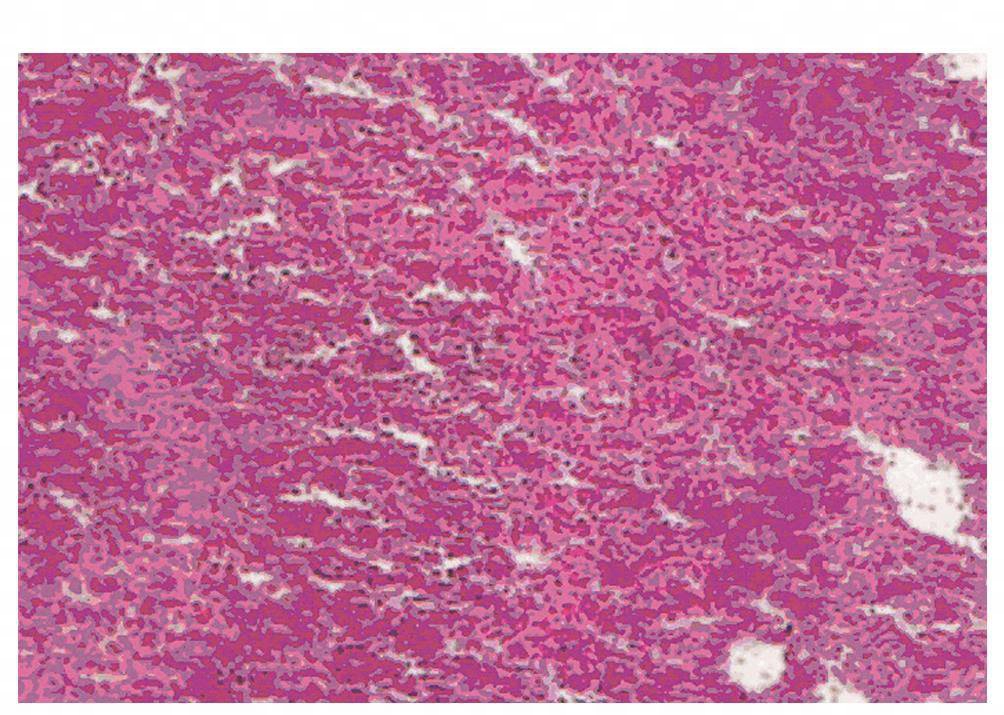
图11 Ⅰ型塑型性支气管炎高倍镜下的病理改变
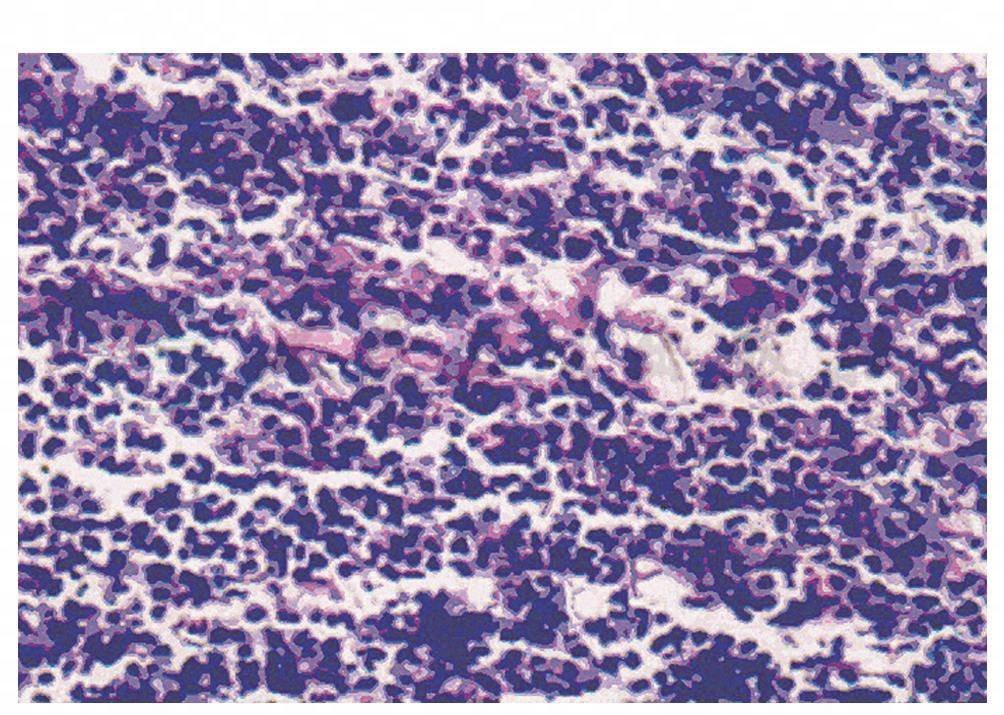
图12 Ⅰ型塑型性支气管炎高倍镜下的病理改变
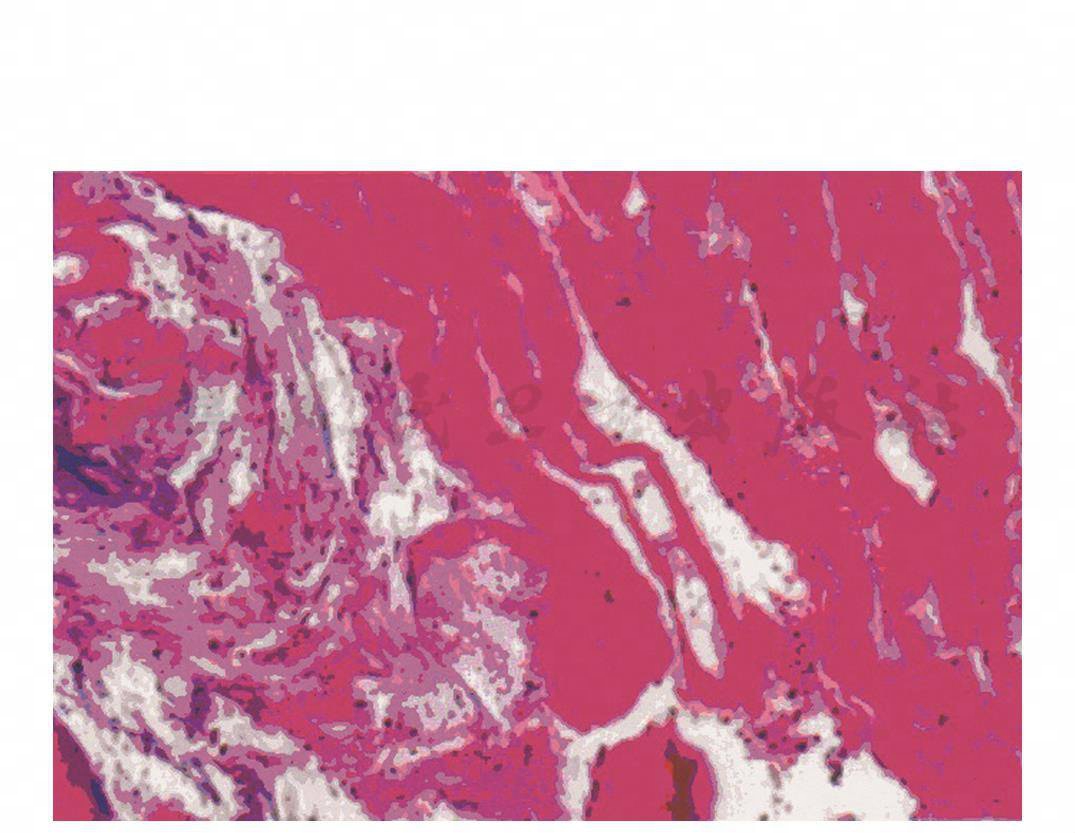
图13 Ⅱ型塑型性支气管炎低倍镜下病理改变
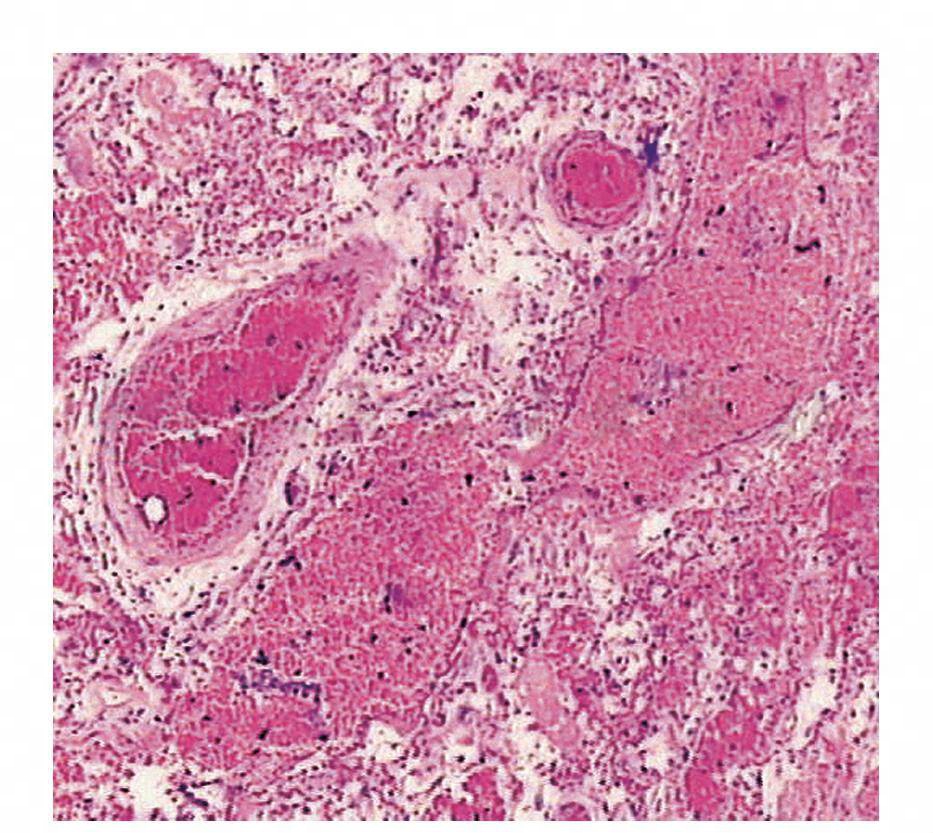
图14 Ⅱ型塑型性支气管炎高倍镜下病理改变
治疗主要包括原发病的治疗和气道梗阻的处理。
(一)原发病的治疗
1.先天性心脏病的手术治疗和改善心功能。
2.选择性地堵闭异常的胸部淋巴管。
3.胸导管结扎。
(二)气道梗阻的处理
1.物理治疗
常规的气道护理、清理气道分泌物是安全和有效的处理方式。每日常规高频振动肺部理疗刺激患者咳嗽或使用咳嗽辅助装置可协助患者排出气道内的塑型物,并预防塑型物重新聚集。
2.药物治疗
由于塑型性支气管炎的发病率很低,而患者在使用某一可能有效的药物同时还使用了很多其他的治疗方式,使得药物治疗的效果难以得到客观和准确的判断。基于少量的病例报道和小型的病例研究,以下的药物被认为可能有效。
(1)口服低剂量的大环内酯类抗生素:
通过阻止细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK)1和2活化,降低黏蛋白的产生,从而降低塑型性支气管炎的严重程度。
(2)雾化吸入肝素:
肝素本身不能溶解塑型物,但可以发挥抗炎作用,减少黏蛋白分泌,阻止纤维蛋白途径的组织因子激活,降低血管通透性。
(3)口服或全身糖皮质激素:
对嗜酸性粒细胞炎症导致的塑型性支气管炎可能有效。
(4)雾化吸入组织纤溶酶原激活物(tissue plasminogen activator, tPA):
对于病情不稳定无法耐受支气管镜检查和治疗的患者,雾化吸入tPA 0.7~1mg/kg,每4小时一次。但应注意,tPA对呼吸道有刺激性,可能导致患者出现呼吸困难、咯血,同时该药物非常昂贵。目前美国正在开展关于本药物的2期临床试验。
(5)以下的药物在塑型性支气管炎的治疗中有应用,但疗效未获得证实:
①雾化吸入β受体激动剂;②阿法链道酶;③黏液溶解剂,例如乙酰半胱氨酸;④祛痰剂,例如愈创木酚甘油醚;⑤非大环内酯类抗生素;⑥雾化吸入高渗盐水。
3.经支气管镜取出
支气管镜有可弯曲支气管镜和硬质支气管镜两种。可弯曲支气管镜操作灵活、创伤小,是诊断塑型性支气管炎的重要手段,同时可以开展治疗,取出塑型物解除呼吸道梗阻。建议尽量选择配有2.0mm操作通道的可弯曲支气管镜,以便有足够的负压对塑型物进行吸引。但对于儿童患者,还需要考虑到其年龄特点,可以选择外径为2.8mm、3.5mm配有1.2mm操作通道的可弯曲支气管镜。术前根据患者的年龄特点、病情分级,按照支气管镜介入手术的要求做好术前检查和准备、术中和术后监护。
(1)麻醉
1)局部麻醉:
对于病情稳定,不需要高级生命支持的成人和儿童患者可以使用利多卡因局部黏膜麻醉,辅以全身镇静、镇痛药物,例如咪达唑仑、芬太尼等。
2)全身麻醉:
使用硬质支气管炎方法,病情危重需要高级气道辅助通气,塑型物取出难度大,配合能力差的患者需要采用全身麻醉的方式。
(2)支气管镜进入途径
1)硬质支气管镜:
使用直接喉镜暴露声门,直接插入。
2)可弯曲支气管镜:
可根据患者需要呼吸支持方式的不同,选择经口、经鼻、经面罩、经喉罩和经气管插管进入。使用喉罩既能保障有效的呼吸支持又不占用气道,尤其适合对通气有较高要求的儿童患者。
(3)取出方式:
原则是先处理病变较轻的一侧,操作中要注意保障患者的通气,如出现血氧不稳定或迅速下降可先暂停操作,充分通气后再继续。
1)经硬质支气管镜:
从声门区逐渐往下导入支气管镜探查,找到塑型物后,直视下用异物钳以适当的力度将其钳出,一次难以完整取出的需多次钳取,直至直视下没有异物残留。较小的塑型物可使用生理盐水冲洗、负压吸引清理干净。如遇黏膜出血,用肾上腺棉球压迫止血。
2)经可弯曲支气管镜:
①负压吸引,一些小的和嵌入支气管腔比较松动的塑型物可以直接通过负压吸引取出。取出时动作要轻柔,以免远端的塑型物断开。配有2.0mm操作通道的可弯曲支气管镜可获得更大的吸力,但在儿童患者受限于气道的直径问题,部分患者只能选择外径较小的配有1.2mm操作通道的可弯曲支气管镜。②钳取:使用活检钳、异物钳对塑型物进行钳取。但由于塑型物比较脆,成功率往往不高,需要反复多次钳取。③冻取:塑型物富含水分,且容易断开,使用二氧化碳冷冻设备对其进行冻取是非常理想的方式。但受限于冷冻探头的外部直径,仅能用于配有2.0mm操作通道的可弯曲支气管镜。④刷取:使活检刷插入塑型物的中间,轻轻旋转、搅动使毛刷充分地黏住塑型物,然后小心地把支气管镜连同毛刷一起撤出呼吸道。
由于炎症导致的塑型性支气管炎通过治疗关联疾病和取出塑型物解除呼吸道梗阻,预后通常较为理想。而由于发绀型先天性心脏病导致的塑型性支气管炎预后则较差,患者常死于呼吸衰竭和中心气道梗阻。Madsen等的统计结果发现,炎症细胞型的塑型性支气管炎死亡率为6%~50%,而非炎症细胞型的塑型性支气管炎死亡率为28%~60%。













