CHB的病理学特点是:不同程度的汇管区及其周围炎症,浸润的炎症细胞以单个核细胞为主,主要包括淋巴细胞及少数浆细胞和巨噬细胞,炎症细胞聚集常引起汇管区扩大,并可引起界板肝细胞凋亡和坏死形成界面炎,旧称碎屑样坏死。小叶内肝细胞变性坏死及凋亡,并可见毛玻璃样肝细胞,肝细胞坏死形式包括点灶状坏死、桥接坏死和融合性坏死等。病毒持续感染、反复的炎症病变活动导致细胞外基质过度沉积,呈现不同程度的汇管区纤维性扩大、纤维间隔形成。马松三色染色(Masson trichrome staining)及网状纤维染色有助于肝纤维化程度的评价。肝纤维化的进一步发展,可引起肝小叶结构紊乱,肝细胞结节性再生,形成假小叶结构,即肝硬化。病毒清除或抑制,炎症病变消退,组织学上肝纤维化及肝硬化可呈现不同程度的逆转。根据Sheuer评分,肝组织炎症可分为0~4级(G0~4),肝纤维化程度可分为0~4期(S0~4)(表1)。也可采用Metavir评分系统。
表1 慢性肝炎组织学分级分期标准

注:PN.碎屑样坏死;BN.桥接坏死。
1.治疗的目标
最大限度地长期抑制HBV复制,减轻肝细胞炎性坏死及肝纤维化,延缓和减少肝衰竭、肝硬化失代偿、HCC及其他并发症的发生,从而改善生活质量和延长生存时间。在治疗过程中,对于部分适合的患者应尽可能追求CHB的临床治愈,即停止治疗后持续的病毒学应答、HBsAg消失,并伴有ALT复常和肝脏组织学的改善(表2及图1)。
表2 临床治愈和绝对治愈临床特征的比较
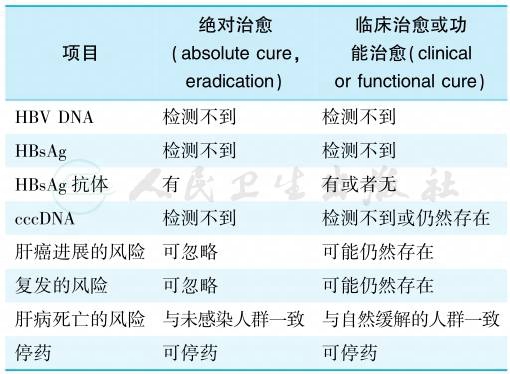
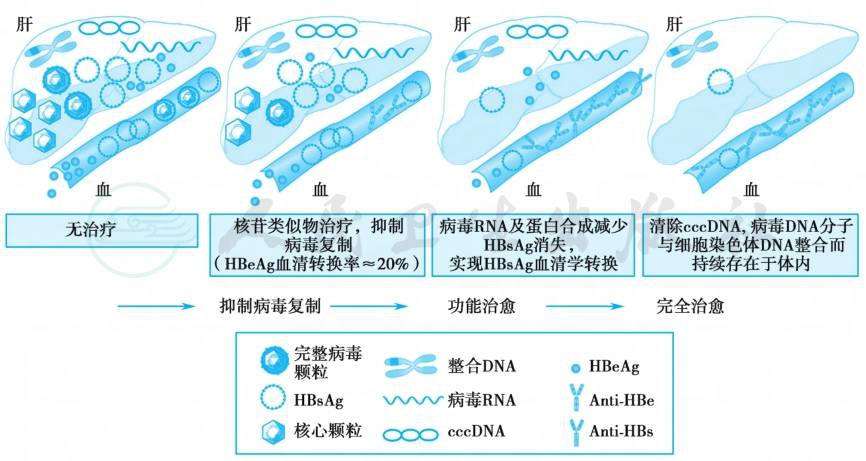
图1 不同治疗终点的血清学和病毒学特征
2.抗病毒治疗的一般适应证
依据血清HBV DNA、ALT水平和肝脏疾病严重程度,同时需结合年龄、家族史和伴随疾病等因素,综合评估患者疾病进展风险,决定是否需要启动抗病毒治疗;动态评估比单次检测更有临床意义。血清HBV DNA阳性的慢性HBV感染者,若其ALT持续异常(>ULN)且排除其他原因导致的ALT升高,建议抗病毒治疗。
导致ALT升高的其他原因包括:其他病原体感染、药物性肝损伤、酒精性肝炎、非酒精性脂肪性肝炎、自身免疫性肝病、全身系统性疾病累及肝脏等。同时,也应注意排除应用降酶药物后ALT的暂时性正常。
存在肝硬化的客观依据,只要可检测到HBV DNA,均应进行积极的抗病毒治疗。对于失代偿期肝硬化者,若HBsAg阳性就建议抗病毒治疗。
血清HBV DNA阳性、ALT正常患者,如有以下情形之一,则建议抗病毒治疗:①肝组织学存在明显的肝脏炎症(≥G2)或纤维化(≥S2);②ALT持续正常(每3个月检查1次,持续12个月),但有肝硬化/肝癌家族史且年龄>30岁;③ALT持续正常(每3个月检查1次,持续12个月),无肝硬化/肝癌家族史,但年龄>30岁,肝纤维化无创诊断技术检查或肝组织学检查,存在明显肝脏炎症或纤维化;④有HBV相关的肝外表现。
血清HBV DNA阳性、ALT持续异常(>ULN)且排除其他原因所致者,建议抗病毒治疗。对于血清HBV DNA阳性的代偿期乙型肝炎肝硬化患者和HBsAg阳性失代偿期乙型肝炎肝硬化患者,建议抗病毒治疗。
3.α干扰素治疗
我国已批准普通α干扰素(2a,2b和1b)和聚乙二醇干扰素α(PegIFN-α)用于治疗慢性乙型肝炎。普通α干扰素的剂量为3~5MU,每周3次或隔日1次,皮下注射,一般疗程至少为6个月。PegIFN-α-2a的剂量为每次180μg,PegIFN-α-2b的剂量为每次1.0~1.5μg/kg,均为每周1次,皮下注射,疗程均为1年。PegIFN-α相较于普通IFN-α能取得相对较高的HBeAg血清学转换率、HBV DNA抑制及生化学应答率。
(1)PegIFN-α初治单药治疗:
多项多中心随机对照临床试验显示,HBeAg阳性CHB患者采用PegIFN-α-2a或国产PegIFN-α-2b治疗48周(180μg/周),停药随访24周,HBV DNA<2 000IU/ml的发生率为30%,HBeAg血清学转换率为30.75%~36.3%,HBsAg转换率为2.3%~3%,停药3年HBsAg清除率为11%。PegIFN-α-2a治疗HBeAg阴性慢性HBV感染者48周,停药随访24周,HBV DNA<2 000IU/ml的发生率为43%,停药随访48周时为42%;HBsAg消失率在停药随访24周、3年、5年时分别为3%、8.7%和12%。
PegIFN-α治疗24周时,HBV DNA下降<2log10IU/ml且HBsAg定量>2×104IU/ml(HBeAg阳性者)或下降<1log10IU/ml(HBeAg阴性者),建议停用PegIFN-α治疗,改为NA治疗。PegIFN-α有效患者的疗程为48周,可以根据病情需要延长疗程,但不宜超过96周。
(2)PegIFN-α与NA联合治疗:
对NA经治CHB患者中符合条件的优势人群联合PegIFN-α可使部分患者获得临床治愈。治疗前HBsAg低水平(<1 500IU/ml)及治疗中HBsAg快速下降(12周或24周时HBsAg<200IU/ml或下降>1log10IU/ml)的患者,联合治疗后HBsAg阴转的发生率较高。
(3)α干扰素抗病毒疗效的预测因素:
具有以下因素的HBeAg阳性CHB患者接受PegIFN-α治疗,HBeAg血清学转换率更高。①HBV DNA<2×108IU/ml;②高ALT水平;③基因型为A或B型;④基线低HBsAg水平;⑤肝组织炎症坏死G2以上;⑥基线核心抗体定量检测(qAnti-HBc)定量高水平;⑦基线信号转导及转录激活蛋白4(STAT4)为rs7574865。PegIFN-α治疗12周时的HBV DNA水平、HBsAg定量及其动态变化,可用于预测干扰素疗效。α干扰素治疗的监测和随访、α干扰素的不良反应及其处理、α干扰素治疗的禁忌证等,可参见《慢性乙型肝炎防治指南(2019年版)》。
4.核苷(酸)类似物抗病毒治疗
目前批准用于慢性乙型肝炎治疗的核苷(酸)类似物有6种,包括拉米夫定(lamivudine,LAM)、阿德福韦 (adefovir,ADV)、恩替卡韦(entecavir,ETV)、替比夫定(telbivudine,LdT)、替诺福韦(tenofovir,TDF)和丙酚替诺福韦(tenofovir alafenamide,TAF)。初治患者应首选强效低耐药药物(ETV、TDF、TAF)治疗。不建议ADV和LAM用于HBV感染者的抗病毒治疗。正应用非首选药物治疗的患者,建议换用强效低耐药药物,以进一步降低耐药风险。应用ADV者,建议换用ETV、TDF或TAF;应用LAM或LdT者,建议换用TDF、TAF或ETV;曾有LAM或LdT耐药者,换用TDF或TAF;曾有ADV耐药者换用ETV、TDF或TAF;联合ADV和LAM/LdT治疗者,换用TDF或TAF。
采用ETV、TDF或TAF治疗,HBeAg阳性CHB患者治疗1年若HBV DNA低于检测下限、ALT复常和HBeAg血清学转换后,再巩固治疗至少3年(每隔6个月复查1次)仍保持不变,可考虑停药,延长疗程可减少复发。HBeAg阴性CHB患者,建议HBsAg消失且HBV DNA检测不到后停药随访。
代偿期乙型肝炎肝硬化患者,推荐采用ETV、TDF或TAF进行长期抗病毒治疗,或采用PegIFN-α治疗,但需密切监测相关不良反应。失代偿期乙型肝炎硬化患者,推荐采用ETV或TDF长期治疗,禁用干扰素治疗,若有必要可以应用TAF治疗。
核苷(酸)类似物治疗的监测和随访:
(1)治疗前相关指标基线检测:
①生物化学指标主要有ALT、AST、胆红素、白蛋白等;②病毒学和血清学标志物主要有HBV DNA定量和HBsAg、HBeAg、抗-HBe;③根据病情需要,检测血常规、血清肌酐水平、血磷水平、肾小管功能等;④肝脏无创纤维化检测如肝脏硬度值测定;⑤当ETV和TDF用于肌酐清除率<50ml/min患者时均需调整剂量;TAF用于肌酐清除率<15ml/min且未接受透析的患者时,无推荐剂量;其余情况均无须调整剂量。治疗过程中密切关注患者治疗依从性问题。
(2)少见或罕见不良反应的预防和处理:
NA总体安全性和耐受性良好,但在临床应用中确有少见、罕见严重不良反应的发生,如肾功能不全(服用TDF、ADV)、低磷性骨病(服用TDF、ADV)、肌炎/横纹肌溶解(服用LdT)、乳酸酸中毒等(服用ETV、LdT),应引起关注。
(3)耐药监测及处理:
随着强效低耐药药物的应用,NA长期治疗出现耐药发生率大幅降低。如果在治疗过程中出现HBV DNA定量较治疗中最低值升高>2log10IU/ml,排除依从性问题后,需及时给予挽救治疗,并进行耐药检测。
5.HBV感染者的随访管理
慢性HBV携带者一般不推荐抗病毒治疗,但需要每3~6个月进行随访。非活动性HBsAg携带者也不推荐抗病毒治疗,但建议每6个月进行随访。
对治疗结束后停药患者,不论患者在抗病毒治疗过程中是否获得应答,在停药后3个月内应每月检测1次肝功能、HBV血清学标志物及HBV DNA;之后每3个月检测1次肝功能、HBV血清学标志物及HBV DNA,以便及时发现肝炎复发及肝脏功能恶化。AFP和超声影像学每3~6个月检查一次。对于肝硬化患者,应每3个月检测AFP和腹部超声显像,必要时做CT或MRI以早期发现HCC。
6.特殊人群的治疗
(1)HBV/HIV合并感染患者的治疗:
不论CD4+T淋巴细胞水平如何,只要无抗HIV暂缓治疗的指征,均建议尽早启动抗反转录病毒治疗(antiretroviral therapy,ART)。HIV和HBV合并感染者应同时治疗2种病毒感染,ART方案NA选择推荐TDF或TAF+LAM或恩曲他滨(emtricitabine,FTC)。治疗过程中需对HBV相关指标进行监测。对于HIV和HBV合并感染者,不建议选择仅含有1种对HBV有活性的NA的方案治疗乙型肝炎。
(2)应用化疗和免疫抑制剂治疗的慢性HBV感染者:
起始治疗前应常规筛查HBsAg、抗-HBc。HBsAg阳性者应尽早在开始使用免疫抑制剂及化学治疗药物之前或最迟与之同时应用NA抗病毒治疗。HBsAg阴性、抗-HBc阳性患者,若HBV DNA阳性,也需要进行预防性抗病毒治疗;如果HBV DNA阴性,可每1~3个月监测ALT水平、HBV DNA和HBsAg,一旦HBV DNA或HBsAg转为阳性,应立即启动抗病毒治疗。HB-sAg阴性、抗-HBc阳性患者,若使用B细胞单克隆抗体或进行造血干细胞移植,HBV再激活风险高,建议预防性使用抗病毒药物治疗。应用化学治疗和免疫抑制剂的CHB或肝硬化患者,NA抗病毒的疗程、随访监测和停药原则与普通CHB或肝硬化患者相同。处于免疫耐受和免疫控制状态的慢性HBV感染患者,或HBsAg阴性、抗-HBc阳性,需要采用NA预防治疗的患者,在化学治疗和免疫抑制剂治疗结束后,应继续ETV、TDF或TAF治疗6~12个月。对于应用B细胞单克隆抗体或进行造血干细胞移植的患者,在免疫抑制剂治疗结束至少18个月后方可考虑停用NA。NA停用后可能会出现HBV复发,甚至病情恶化,应随访12个月,其间每1~3个月监测HBV DNA。
(3)肝移植患者:
患者因HBV相关疾病进行肝移植时,应合理选用抗HBV方案,减少移植肝再感染HBV的风险。其具体方案主要取决于再感染的主要风险因素,即移植前的HBV DNA定量水平。如移植前HBV DNA定量阴性,则意味着再感染风险低,可在术前尽早使用强效低耐药的NA,预防HBV再激活,术后无须加用乙型肝炎免疫球蛋白(HBIG)。如移植前HBV DNA阳性,则意味着再感染风险高。术前尽早使用强效低耐药的NA以降低HBV DNA水平;术中无肝期应静脉注射HBIG;术后除了长期应用NA,还应联合应用低剂量HBIG持续0.5~1年,此后再继续单用NA。
(4)HBV/HCV合并感染患者的治疗:
所有HBsAg阳性者都应筛查抗-HCV,如为阳性,则需进一步检测HCV RNA定量。HCV RNA定量阳性者均需应用直接抗病毒药物(direct acting agents,DAA)治疗。此类患者有发生HBV再激活的风险,因此在应用抗HCV治疗期间和停药后3个月内,建议联合ETV、TDF或TAF抗病毒治疗并密切监测。HBsAg阴性、抗-HBc阳性者应用DAA治疗丙型肝炎过程中也有HBV再激活的风险,建议每月监测血清HBV DNA定量和HBsAg,若出现阳转,建议应用抗病毒治疗。
(5)儿童患者:
儿童HBV感染者常处于免疫耐受期,通常不考虑抗病毒治疗。对于进展期肝病或肝硬化患儿,应及时抗病毒治疗,但需考虑长期治疗安全性及耐药性问题。我国已批准TAF用于青少年(≥12岁,且体重≥35kg)。PegIFN-α-2a可应用于≥5岁CHB儿童。ALT升高的HBeAg阳性CHB儿童患者可选用有限疗程的普通干扰素-α或PegIFN-α-2a治疗以实现HBeAg血清学转换,也可选用ETV、TDF或TAF治疗。普通干扰素-α用于儿童患者的推荐剂量为每周3次,每次300万~600万U/m2,最大剂量不超过1 000万U/m2,推荐疗程为24~48周;PegIFN-α-2a每次剂量180μg/173m2,疗程为48周。
(6)妊娠相关情况处理:
育龄期及准备妊娠女性均应筛查。对于HBsAg阳性者需检测HBV DNA。对于有抗病毒治疗适应证患者,可在妊娠前应用PegIFN-α治疗,以期在妊娠前6个月完成治疗。在治疗期间应采取可靠的避孕措施。若不适合应用PegIFN-α或治疗失败,可采用TDF抗病毒治疗。对于妊娠期间首次诊断CHB的患者,其治疗适应证同普通CHB患者,可使用TDF抗病毒治疗。妊娠前或妊娠期间开始服用抗病毒药物的CHB孕产妇,产后应继续抗病毒治疗,并根据病毒学应答情况,决定是继续原治疗方案,还是换用其他NA或PegIFN-α继续治疗。抗病毒治疗期间意外妊娠的患者,若正在服用TDF,建议继续妊娠;若正在服用ETV,可不终止妊娠,建议更换为TDF继续治疗;若正接受干扰素治疗,建议向孕妇和家属充分告知风险,由其决定是否继续妊娠,若决定继续妊娠则要换用TDF治疗。血清高水平HBV DNA是母婴传播的高危因素,妊娠中后期如果HBV DNA定量>2×105IU/ml,建议在与患者充分沟通,在其知情同意的基础上,于妊娠第24~28周开始抗病毒治疗,应用TDF或LdT。应用TDF时,母乳喂养不是禁忌。免疫耐受期口服NA的孕妇,可于产后即刻或服用1~3个月后停药。停药后17.2%~62%的患者可能发生肝炎活动,且多发生在24周内,应加强产后监测。可于产后4~6周时复查肝脏生物化学指标及HBV DNA,如肝生物化学指标正常,则每3个月复查1次至产后6个月,如为乙型肝炎活动,建议抗病毒治疗。
(7)男性患者抗病毒治疗相关生育问题:
应用干扰素-α治疗的男性患者,应在停药后6个月方可考虑生育;应用NA抗病毒治疗的男性患者,目前尚无证据表明NA治疗对精子的不良影响,可在与患者充分沟通的前提下考虑生育。
(8)HBV相关HCC患者:
HBV DNA阳性的HCC患者接受抗HBV治疗可减少HCC术后的复发,提高总体生存率。若HBsAg阳性,建议应用ETV、TDF或TAF进行抗病毒治疗。无禁忌者,也可使用干扰素-α治疗。
(9)肾功能损伤患者:
推荐ETV或TAF作为一线抗HBV治疗药物,或可根据患者情况选用LdT进行抗病毒治疗,不建议应用ADV或TDF。对于存在肾脏损伤高危风险的CHB患者,应用任何NA抗病毒过程中均需监测肾功能变化。已应用ADV或TDF的患者发生肾脏或骨骼疾病或存在高危风险时,建议改用ETV或TAF。
7.肝衰竭的治疗
病因治疗、内科综合治疗、免疫调节治疗、促进肝细胞再生、微生态调节治疗等。
(一)管理传染源
HBsAg携带者和乙型肝炎患者不能捐献血液、组织器官。除不能从事饮食业、托幼机构等国家明文规定的职业或工种外,可照常工作和学习,但应定期进行医学随访。患者的洗漱用具、剃须刀等应与健康人分开。医疗机构在诊断出急性或慢性乙型肝炎时,应按规定向当地疾病预防控制中心报告。
(二)切断传播途径
除加强对献血员筛查外,对血液制品应做HBsAg检测,严格掌握输血及血液制品的适应证,对各种医疗器械和用具应实行严格消毒,提倡使用一次性的注射器、检查和治疗用具,防止医源性传播。服务行业所用的理发、刮脸、修脚、穿刺和文身等器具也应严格消毒。注意个人卫生,不和任何人共用剃须刀和牙具等用品。对HBsAg阳性的孕妇,应避免羊膜腔穿刺,并缩短分娩时间,保证胎盘的完整性,尽量减少新生儿暴露于母血的机会。
(三)保护易感人群
接种乙型肝炎疫苗是预防HBV感染的最有效方法。乙型肝炎疫苗全程需接种3针,按照0、1、6个月程序,即接种第1针疫苗后,间隔1个月及6个月注射第2及第3针疫苗。新生儿接种乙型肝炎疫苗要求在出生后24小时内接种,越早越好。接种部位新生儿接种部位为上臂外侧三角肌或大腿前外侧中部肌内注射,儿童和成人为上臂三角肌中部肌内注射。
单用乙型肝炎疫苗阻断母婴传播的阻断率为87.8%。对HBsAg阳性母亲的新生儿,应在出生后24小时内尽早注射HBIG,剂量应≥100IU,同时在不同部位接种10μg重组酵母或20μg中国仓鼠卵巢(CHO)细胞乙型肝炎疫苗,在1个月和6个月时分别接种第2和第3针乙型肝炎疫苗,可显著提高阻断母婴传播的效果。
新生儿乙型肝炎疫苗的接种剂量:①重组酵母乙型肝炎疫苗每针次10μg,不论母亲HBsAg阳性与否;②重组中国仓鼠卵巢(CHO)细胞乙型肝炎疫苗,每针次10μg或20μg,HBsAg阴性母亲的新生儿接种10μg;HBsAg阳性母亲的新生儿接种20μg。对成人建议接种3针20μg重组酵母乙型肝炎疫苗或20μg重组CHO细胞乙型肝炎疫苗。对免疫功能低下或无应答者,应增加疫苗的接种剂量(如60μg)和针次;对0、1和6个月程序无应答者可再接种1针60μg或3针20μg乙型肝炎疫苗,并于第2次接种乙型肝炎疫苗后1~2个月时检测血清抗-HBs,如仍无应答,可再接种1针60μg重组酵母乙型肝炎疫苗。接种乙型肝炎疫苗后有抗体应答者的保护效果一般至少可持续30年,因此,一般人群不需要进行抗-HBs监测或加强免疫,但对高危人群或免疫功能低下者等可监测抗-HBs,如抗-HBs<10mIU/ml,可再次接种1针乙型肝炎疫苗。
(四)意外暴露后HBV预防
在意外接触HBV感染者的血液和体液后,可按照以下方法处理:在伤口周围轻轻挤压,排出伤口中的血液,再对伤口用0.9%氯化钠溶液冲洗,然后用消毒液处理。血清学检测应立即检测HBV DNA、HBsAg、抗-HBs、HBeAg、抗-HBc、ALT和AST,并在3和6个月内复查。已知抗-HBs阳性(抗-HBs≥10mIU/ml)者,可不进行处理。如未接种过乙型肝炎疫苗,或虽接种过乙型肝炎疫苗,但抗-HBs<10mIU/ml或抗-HBs水平不详者,应立即注射HBIG 200~400IU,同时在不同部位接种1针乙型肝炎疫苗(20μg),于1个月和6个月后分别接种第2针和第3针乙型肝炎疫苗(20μg)。













