小肠黏膜占整个消化系统黏膜表面积的90%,而癌症发病率仅占2%左右。小肠腺癌是最常见的小肠恶性肿瘤之一,约占小肠肿瘤的33%,近年发病率呈上升趋势。小肠腺癌多位于十二指肠乳头周围、空肠和回肠。由于小肠黏膜富含淋巴管,故能够通过绒毛与邻近的黏膜腔相连,因此大多数的小肠腺癌在做出诊断时往往已经发生转移。
小肠腺癌的病因不明,长期克罗恩病(Crohn病)可以发生腺癌(发生率3%~60%),部位以回肠为主,克罗恩病的癌变危险性比正常对照人群高出300~1000倍,可能与黏膜完整性破坏及异常免疫应答和潜在的微生物感染有关。
临床观察发现,65%的十二指肠腺癌发生于Vater壶腹周围区域,22.5%发生于十二指肠乳头近侧的壶腹上部,亦以降部为主。壶腹部癌发生率高的原因未明,但壶腹区域标志着前中原肠交接部位,很可能此交接区域黏膜对发生疾病的抵抗力不如十二指肠的其他部位。也有人认为,十二指肠和空肠近端的腺癌或许与胆汁中的某些胆酸(如脱氧胆酸、原胆酸等)在细菌作用下的降解产物与致癌作用有关。另外,近期欧洲多中心的研究表明,其发生可能与饮酒、高脂饮食和某些职业有关,而与吸烟无关。
小肠腺癌是一种少见疾病,随着年龄增长发病率增加,平均发病年龄为50~70岁。黑种人发病率高于白种人,男性高于女性。美国是小肠腺癌发病率最高的国家,且发病率呈上升趋势,由1973年的0.57/10万增长到2004年的0.73/10万。
(一)大体病理形态
1.环状浸润的腺癌
亦称为狭窄型,病变沿肠管横轴环形生长,最后形成环形病变,易引起肠道的狭窄梗阻。
2.息肉状的乳头状癌
较多见,向肠腔内突出,易引起肠套叠,并可逐渐浸润肠壁造成环状狭窄。
3.溃疡型癌
随着病变向深层发展时,黏膜出现糜烂,继而破溃,形成溃疡。此型易引起慢性消化道出血甚至穿孔引起腹膜炎。亦可能在穿孔前,邻近肠管间已经粘连,故穿破后与之相通形成内瘘。
(二)组织学分型
小肠腺癌的组织学分为高分化腺癌、中分化腺癌、低分化腺癌以及黏液腺癌。黏液腺癌分化较好,能分泌黏液。但由于黏液中含有蛋白水解酶,能够溶解癌组织中的胶原纤维、蛋白多糖等,有利于癌细胞浸润和转移,故黏液腺癌恶性程度高、转移早。
(三) 临床病理分期
按照Astler Coller修订的Duke分期法,小肠腺癌分为四期六级:A:癌肿限于黏膜层及黏膜下层,无淋巴结转移;B1:癌肿浸润固有肌层,无淋巴结转移;B2:癌肿穿透固有肌层,无淋巴结转移;C1:癌肿浸润固有肌层,区域淋巴结转移健康搜索;C2:癌肿穿透固有肌层,区域淋巴结转移;D:远处转移(包括血行转移、腹主动脉旁淋巴转移、腹腔种植及广泛浸润邻近脏器组织)。
小肠腺癌原发于小肠黏膜,由黏膜经黏膜下向肌层、浆膜层发展同时向周围扩展。小肠腺癌侵犯肠管的长度一般仅4~5cm,很少超过10cm,其发病机制还未完全明确。研究表明与结肠癌的腺瘤-腺癌序列相似,小肠腺瘤是常见的癌前疾病,特别是家族性腺瘤性息肉病(FAP)患者中,十二指肠腺癌的危险度增加300倍。
分子机制研究表明,几乎20%的患者与出现DNA错配修复基因的高级别卫星不稳定性有关,一些患者中出现了MARCKS基因突变而导致MARCKS蛋白表达缺失,表明MARCKS基因失活是导致小肠腺癌的重要因素。Sutter报告6例小肠腺癌中有5例存在K-ras基因第12密码子的点突变。Hidalgo发现5%~10%的腺癌细胞有p53蛋白过表达,且表达强度与小肠癌的分化程度、浸润、转移及预后明显相关。
(一)实验室检查
1.血常规检查
现小细胞性贫血。
2.大便潜血试验
小肠肿瘤可有50%的患者出现大便潜血阳性,大便潜血实验不仅有助于肿瘤的发现,而且有助于出血的判断和医疗方案的选择,应列为常规。
3.小肠肿瘤标记物和分子生物学检查
血清CEA、淋巴细胞分类和计数以及血细胞镜检形态分析,对于鉴别小肠腺癌、平滑肌瘤、淋巴瘤以及白血病的小肠表现有一定价值。但对于小肠腺癌而言,CEA极少上升,除非有肝或远处转移。
4.血清胆红素检查
十二指肠壶腹部肿瘤可出现血清结合胆红素增高。
(二)选择性腹腔动脉造影
小肠腺癌的造影表现变化不一,可表现为丰富的肿瘤血管,肿瘤染色伴引流静脉早显和颜色增生,也可能无明显的血管及肿瘤染色,但常有瘤周围动脉受侵犯。对于腺癌、肉瘤及其他肿瘤有分辨意义,可判断外科切除的可能性及了解血管异常情况。
(三)消化道钡剂造影
消化道钡餐检查阳性率较低,需口服大量钡剂,且通常因受小肠襻重叠影像干扰结果判断。口服法或导管法低张十二指肠造影可以清楚地显示十二指肠损害的黏膜像及其性质。对于十二指肠肿瘤颇有诊断价值,正确率为53%~62.5%,全消化道气钡双对比造影可以观察黏膜的细致结构及其异常改变,对小肠癌诊断有一定帮助。有经验的医师能查出较早期的病变。病变部位黏膜皱襞破坏消失,管壁僵硬,蠕动消失。
(四)CT及MRI
小肠腺癌CT可表现为不规则软组织肿块,向腔内外生长,增强后肿块呈轻至中度强化影,局部肠壁不规则或环形增厚,肠腔狭窄,少数小肠腺癌仅单纯表现为局限性肠壁增厚。有时坏死的肿块内有气体或造影剂进入,则提示有溃疡形成。MRI表现为肠壁明显增厚及突向肠腔内的软组织肿块影,肠腔环形狭窄,T1WI上呈等低信号,T2WI上呈略高信号,中心坏死在T1WI上呈低信号,T2WI上呈明显高信号,增强扫描后病灶呈均匀或不均匀强化,中心的坏死灶不强化。
(五)胶囊内镜
胶囊内镜可在门诊完成,是一种无创性检查方法,可使临床医生清楚地看到整个小肠。但是若小肠腺癌已导致不全梗阻,则有发生胶囊内镜嵌顿的风险。
(六)小肠镜
十二指肠腺癌可用十二指肠镜检查,确诊率为90%~100%。单气囊及双气囊小肠镜均可用于小肠腺癌的诊断,是小肠腺癌诊断的“金标准”。表现为小肠腔内的隆起性病变,质地较硬,部分呈溃疡型,表明伴有污苔,周边黏膜呈结节状,质地硬易出血,可伴有肠腔狭窄(见图1)。小肠镜不仅可确定肿瘤位置、大小,还可取活检以确诊,为外科手术提供依据。但对黏膜下肿瘤,可能活检为阴性,应予以注意。台湾学者报道在小肠镜发现的小肠肿瘤中,小肠腺癌占18%,其次为小肠淋巴瘤占7%。
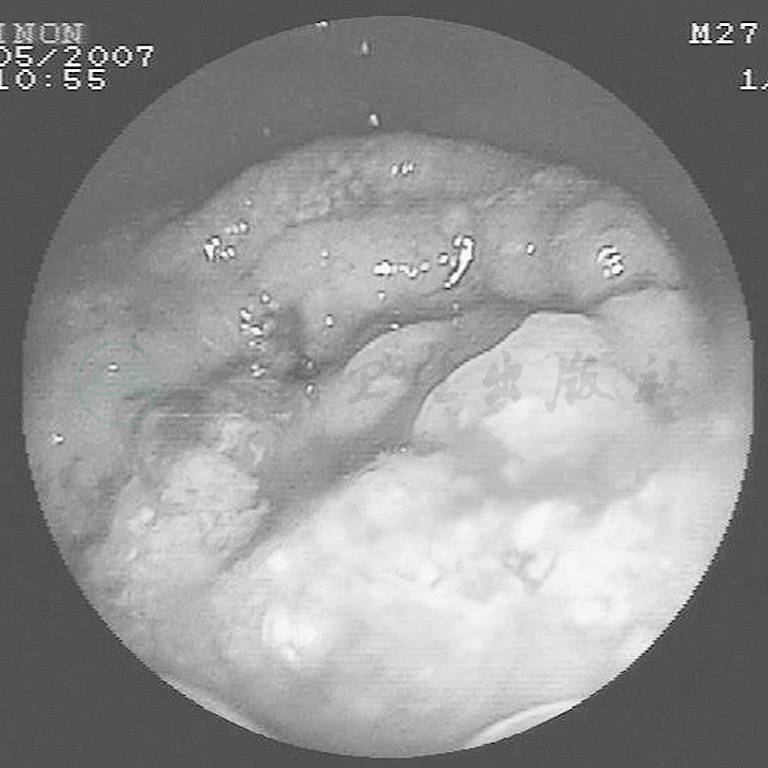
图1 小肠腺癌的小肠镜下表现
手术切除是小肠腺癌的首选治疗方案,术中是否能够完全切除肿物及阳性淋巴结数目是影响预后的主要因素。其他方案包括姑息性化疗及靶向治疗。
(一)手术治疗
1.根治术
如无远处转移,转移性淋巴结未侵及系膜根部大血管,可行根治术。十二指肠腺癌宜行胰十二指肠切除术,可达到根治目的。而空、回肠腺癌应在该段肠管的血管根部(肠系膜上动静脉分出该段血管的起始部)结扎,清除该段肠系膜,并清扫肠系膜上动静脉旁淋巴脂肪组织。为了清除区域淋巴结,小肠可做较广泛切除,肠管两端各距肿块边缘不少于10~15cm,末端回肠应进行根治性右半结肠切除术。
2.姑息性切除术
如有远处转移,应尽可能切除原发病灶及侵犯的肠管,术后给予辅助治疗。
3.短路手术
如肿瘤已固定于腹主动脉或下腔静脉上,无法分离仅能作姑息性的短路手术。如十二指肠完全梗阻者行胃空肠吻合术,但胆总管下段和十二指肠乳头梗阻者应行胆总管空肠Roux-Y式吻合术。
4.术后化疗
一般采用联合化疗方案。如丝裂霉素C(MMC)、氟尿嘧啶(5-FU)和长春新碱联合(VCR)(MFV)方案,3周为一周期,2~3周期为一个疗程或环磷酰胺(CTX)、长春新碱(VCR)、甲氨蝶呤联合(MTX)(COM)方案,5周后重复,2周期为一个疗程。辅助性化疗证据不充分,有学者提出可能导致肿瘤分化不良、结节粘连和更高的复发率。
(二)姑息性化疗
小肠腺癌对放疗不敏感,对化疗亦不敏感。化疗主要用于无法手术的患者。最佳的化疗方案还有待确立。大多数采用氟尿嘧啶,单独使用或与其他药合用,不应答者可采用伊立替康,二者合用可使1/2的患者中位无病进展期达到5个月。东方肿瘤协作组研究表明,联合使用氟尿嘧啶、多柔比星、MMC的有效率为18%,中位生存期大约8个月。
(三)靶向治疗
Overman等分析了54例不同分期的小肠腺癌患者候选癌基因蛋白的免疫表型和分子机制,71%和96%的患者表达EGFR和VEGFR,但抗EGFR和抗VEGFR在小肠癌中的作用有待进一步证实。













