自体造血干细胞移植相关并发症按照其发生时间可分为移植早期并发症和移植远期并发症。移植早期并发症包括消化道反应、感染、口腔黏膜炎、出血性膀胱炎、间质性肺炎等;远期并发症包括生长发育障碍、性腺功能不全、移植后第二肿瘤等。其中,感染既可以发生在预处理后短期骨髓抑制期间,也可以发生在移植后长期的骨髓重建和恢复过程中。
(一)感染
由于患者在预处理到回输后骨髓重建期间需经历一段持续、深度的骨髓抑制和免疫抑制时期,感染成为最常见的移植相关并发症之一,发生率为50%~60%,也是移植相关死亡的主要原因。移植相关感染主要与预处理造成消化道黏膜屏障损害、骨髓抑制和深静脉置管等因素相关,可在预处理后短期粒细胞缺乏期间发生,也可在移植后1~2年的长期骨髓造血和免疫重建过程中发生。感染可发生在身体任何部位,常见感染部位包括口腔、肠道、呼吸道、肛周等,严重者可发生败血症,甚至危及生命。严重感染导致的死亡约占移植相关死亡的30%~50%。
主要致病病原体包括细菌、病毒和真菌。致病菌中常见的革兰氏阴性菌有大肠杆菌、铜绿假单胞菌和肺炎克雷伯杆菌等;近年来,表皮葡萄球菌、金黄色葡萄球菌等革兰氏阳性菌感染有增多趋势。常见病毒感染包括:水痘-带状疱疹病毒、巨细胞病毒以及乙型肝炎病毒再激活等。如未接受抗乙型肝炎病毒治疗,近2/3乙型肝炎病毒携带患者在移植后发生乙型肝炎病毒再激活。预处理后免疫功能抑制期间乙型肝炎病毒在肝细胞内大量复制,移植后免疫功能逐渐恢复,免疫细胞攻击受感染的肝细胞,导致严重肝脏损害,甚至发生急性重型肝炎。白色念珠菌、曲霉菌、隐球菌等是常见真菌病原体。
(二)口腔黏膜炎
口腔是化放疗相关毒性发生的常见部位,主要表现为消化道黏膜炎和继发感染。口腔黏膜炎(oral mucositis,OM)是移植后常见的近期并发症,发生率可达70%~100%。其发生主要与细胞毒药物代谢产生的自由基损伤口腔黏膜以及移植后中性粒细胞减少期间口腔黏膜局部感染相关。放疗造成唾液腺损害降低口腔自我防护作用,也是造成移植后口腔黏膜局部感染的重要原因。口腔黏膜炎的主要临床表现为口腔黏膜疼痛、进食减少等,严重者需肠外营养支持。为防止口腔并发症的发生,推荐预处理治疗前10~14天进行正式的口腔评估及牙科检查:龋齿的适当治疗、义齿的正确装配及出现严重牙周病时拔牙;在治疗期间保持口腔卫生,每日多次使用灭菌注射用水、生理盐水或碳酸氢钠溶液漱口,应用超软牙刷刷牙每天至少两次,以及在不造成创伤的情况下,建议有使用牙线技术经验的患者每天使用牙线。不推荐常规使用抗菌和杀菌药物预防口腔并发症。
(三)间质性肺炎
间质性肺炎(interstital pneumonia,IP)是以肺实质、肺泡炎和间质纤维化为病理改变,以活动性呼吸困难、胸片显示弥漫性阴影以及限制性通气功能障碍、弥散功能降低和低氧血症为主要临床表现的一种疾病。间质性肺炎是移植后早期严重的致死性并发症之一,多发生于移植后30~100天,发生率为10%~40%,如不及时治疗病死率可达85%~100%。与间质性肺炎相关的因素包括:①感染,特别是巨细胞病毒(cytomegalovirus,CMV)感染,其他少见致病原包括单纯疱疹病毒、带状疱疹病毒、腺病毒、念珠菌、曲霉菌或肺孢子菌;②移植物抗宿主反应;③强烈的放疗或化疗;④年龄较大;⑤巨细胞病毒血清学阳性或输注巨细胞病毒阳性的血液制品等。
间质性肺炎的临床表现无特异性,部分患者先有发热,早期无咳嗽或仅轻度咳嗽;部分患者突发干咳,继而胸闷、憋气,进行性呼吸困难。体格检查:双肺听诊常无干湿啰音,或偶可闻及少许干啰音。辅助检查:肺功能检查提示限制性通气功能障碍或弥散功能障碍;影像学表现为双肺间质性改变,最初于肺底及肺门最明显,可呈段、叶或弥漫性间质改变或结节性浸润,以弥漫性改变最为常见;血气分析显示低氧血症常早发现于影像学改变;肺活检提示肺间质水肿伴不同程度纤维化,以淋巴细胞为主的炎性细胞浸润,肺泡内有纤维蛋白渗出,感染性间质性肺炎还可以见到巨细胞病毒包涵体等病原学改变。
间质性肺炎的预防措施包括:预防巨细胞病毒感染、及早发现高危人群和早期给予预防性治疗。对于血清巨细胞病毒抗体阳性者静脉注射免疫球蛋白可以防止巨细胞病毒再激活。对巨细胞病毒有抑制作用的药物有高剂量无环鸟苷、丙氧鸟苷和膦甲酸钠,无环鸟苷剂量在500mg/(m2·d)时能降低或延迟巨细胞病毒感染的发生,且骨髓毒性较小,可以在造血干细胞移植后预防性应用。丙氧鸟苷和膦甲酸钠有明显的骨髓毒性,且膦甲酸钠有肾毒性,一般不建议预防性用于造血干细胞移植的患者。
(四)出血性膀胱炎
出血性膀胱炎(hemorrhagic cystitis,HC)是造血干细胞移植后常见的一种并发症,以血尿伴尿频、尿急和排尿困难为主要临床表现,尿细菌培养阴性。各移植中心报道的出血性膀胱炎发生率差异较大,文献报道为3%~35%,自体造血干细胞移植较异基因造血干细胞移植出血性膀胱炎发生率低,给予积极的预防措施可降低出血性膀胱炎的发生率。
造血干细胞移植过程中出血性膀胱炎的发生与预处理方案中应用环磷酰胺等化疗药物、移植后病毒感染等因素密切相关。按出血性膀胱炎发生的时间可分为早发型和迟发型:预处理后3天内发生为早发型,3天后发生为迟发型。早发型出血性膀胱炎主要与应用高剂量环磷酰胺有关,环磷酰胺代谢产物丙烯醛从肾脏分泌后直接作用于膀胱黏膜上皮造成损伤,环磷酰胺与白消安或全身照射联合应用可增加出血性膀胱炎的发生率。迟发型出血性膀胱炎多与巨细胞病毒等病毒感染以及异基因造血干细胞移植后移植物抗宿主反应相关。
根据血尿程度将出血性膀胱炎分为5级:0级,无血尿;Ⅰ级,镜下血尿;Ⅱ级,肉眼血尿;Ⅲ级,肉眼血尿伴血块;Ⅳ级,肉眼血尿伴血块和尿道梗阻。Ⅰ~Ⅱ级为轻度,Ⅲ~Ⅳ级为重度。
预处理过程中积极的预防措施能避免出血性膀胱炎的发生,预防措施包括:①水化、利尿、碱化尿液,一般在环磷酰胺输注前4小时至输注结束后24小时大量静脉补液,2 500~3 000ml/(m2·d);静脉或口服碳酸氢钠,维持尿pH在7~8;给予呋塞米利尿,同时注意补钾维持电解质平衡。②应用硫羟基复合物,如α-巯基乙基磺酸钠盐(美司钠,Mesna)。美司钠静脉应用后快速从肾脏排出,进入膀胱与环磷酰胺代谢产物丙烯醛结合,形成稳定的硫醚,从而拮抗丙烯醛对膀胱黏膜的损伤。③预防巨细胞病毒等病毒感染。
轻度出血性膀胱炎经积极对症处理后大多能治愈,重度出血性膀胱炎应采取综合治疗措施,包括:①持续水化利尿,碱化尿液,保证平均尿量150ml/h以上;②应用止血药,血小板明显低下者输注血小板;③膀胱灌注冲洗,该方法操作简单、起效快,可在床旁进行,膀胱灌注前列腺素对于部分重度出血性膀胱炎有一定疗效,应在出血性膀胱炎症状一出现立即开始应用;④解痉镇痛对症治疗;⑤病毒性出血性膀胱炎发病迟、病情严重,在上述治疗基础上应同时积极抗病毒治疗;⑥对于极少数重度难治性出血性膀胱炎,可考虑膀胱镜下清除血凝块、电凝止血或膀胱切除术,但上述方法副作用大,不作为常规治疗选择,尤其是造血干细胞移植过程中伴有血小板减少、中性粒细胞减少的患者,不适合应用上述治疗方法。
(五)肝窦阻塞综合征
肝窦阻塞综合征(sinusoidal obstruction syndrome,SOS)又称肝静脉闭塞性病(hepatic venoocclusive disease,HVOD),是造血干细胞移植后的一种严重的肝脏并发症。由于高剂量化/放疗等原因导致肝小叶中央静脉、小叶下静脉和血窦内皮细胞损伤,导致肝内小静脉和血窦的非血栓性狭窄闭塞,同时伴有小叶中心肝细胞的不同程度坏死。肝窦阻塞综合征的主要临床表现包括高胆红素血症、疼痛性肝肿大、体重增加、腹水,伴凝血功能异常和肝功能异常。严重者可发展成肝衰竭及多器官功能衰竭,病死率高,为30%~80%。一项纳入24 920例造血干细胞移植患者的研究结果显示,肝窦阻塞综合征的中位发生率为13.7%(0~62.3%),清髓性预处理异基因造血干细胞移植后肝窦阻塞综合征的发生率为10%~15%,减低剂量强度预处理异基因造血干细胞移植或自体造血干细胞移植后肝窦阻塞综合征的发生率较低,为 < 5%。
肝窦阻塞综合征的发生机制尚未完全明确,可能与预处理所致的血管内皮细胞损伤、细胞因子激活及凝血机制改变等因素有关。肝小静脉及窦状隙内皮经化/放疗损伤后在局部形成高凝状态,释放组织因子,激活外源性凝血途径。既往研究发现移植后肝窦阻塞综合征的发生涉及许多细胞因子的变化,其中以肿瘤坏死因子-α(tumor necrosis factor-alpha,TNF-α)最显著。在自体造血干细胞移植过程中,细胞毒药物、放疗、感染等因素引起巨噬细胞和网状内皮细胞激活,释放大量TNF-α、IL-1等细胞因子,导致血管内皮通透性增加,同时TNF-α引起出血坏死,直接损伤内皮细胞,严重者导致多器官功能衰竭。
肝窦阻塞综合征的实验室检查无特异性指标,主要表现为肝功能和凝血功能异常,血清学和腹水CA125均升高。影像学检查对于诊断肝窦阻塞综合征特异性较低,但与其他临床表现结合有助于评估疾病的危险分层、严重程度及治疗反应。增强CT可见特征性改变:增强期肝动脉增粗扭曲,肝脏可有轻度不均匀强化;门脉期可见“地图状”改变、肝静脉显示不清,下腔静脉、门静脉周围“晕征”或“轨道征”;延迟期肝内仍可见斑片影及地图样低密度区。
肝窦阻塞综合征根据病程发展可分为急性期、亚急性期和慢性期。急性期:多有明显的肝损伤,黄疸和脾大较少见或轻度脾大;亚急性期:以肝肿大和腹水为主要表现,可伴急性发作;慢性期:以门静脉高压为主要临床表现,肝硬化、脾大明显,并伴有顽固性腹水。少数患者可出现食管胃底静脉曲张破裂出血、肝性脑病及肝肾综合征等严重并发症。
肝窦阻塞综合征根据严重程度可分为轻、中、重3级(表1)。一般轻度肝窦阻塞综合征可继续观察;中度肝窦阻塞综合征可在进行适当液体平衡治疗并除外肝/肾毒性药物因素情况下观察2天,如果肝窦阻塞综合征临床表现持续或进展,则应开始治疗;重度肝窦阻塞综合征无论是否伴有多器官衰竭均应立即开始治疗。多数轻、中度肝窦阻塞综合征患者经2~3周治疗后病情可缓解,而重度肝窦阻塞综合征预后差,病死率高达80%~90%。
表1肝窦阻塞综合征临床分级
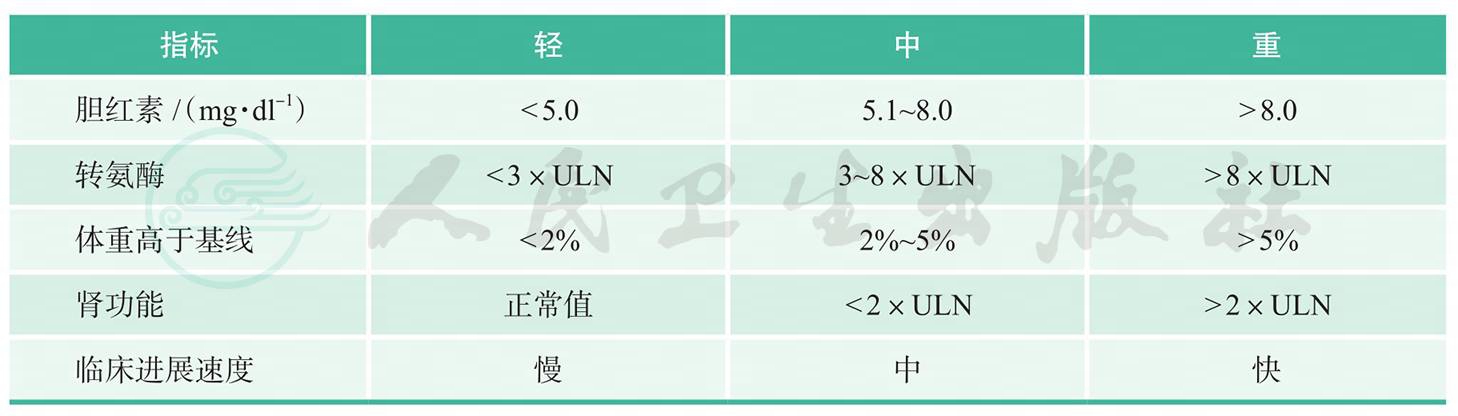
注:ULN:upper limit of normal,正常值上限。
引自:肿瘤内科原理与实践.第1版.ISBN:978-7-117-33943-8.主编:
早期发现、及时治疗是治疗肝窦阻塞综合征的关键。欧洲骨髓移植登记处(European registry of bone marrow transplantation,EBMT)推荐的一线治疗包括:①限制水钠摄入或应用利尿药;②通过输注白蛋白、血浆和红细胞(血细胞比容 > 30%)来维持血容量及肾灌注;③首选治疗推荐去纤维蛋白多核苷酸Defitelio;④其他药物如重组纤溶酶原、抗凝血酶Ⅲ、前列腺素、糖皮质激素、谷胱甘肽/维生素E、N-乙酰半胱氨酸、重组人可溶性血栓调节蛋白等,由于相关研究样本较少或结论不统一,尚不推荐;⑤对症治疗措施:镇痛、抽吸胸/腹水、血液透析/超滤、机械通气;⑥部分重症患者可考虑经颈静脉肝内门腔静脉分流术(transjugular intrahepatic portosystemic shunt,TIPS)以及肝移植。
移植前肝功能异常、活动性肝炎、放化疗、抗生素治疗、铁负荷及预处理强度、合并症等均与肝窦阻塞综合征的发生有关。肝窦阻塞综合征发病具有一定遗传易感性,乙酰肝素酶(heparanase,HPSE)基因多态性与儿童异基因移植后肝窦阻塞综合征的发生相关。此外,亚甲基四氢叶酸还原酶(methylenetetrahydrofolate reductase,MTHFR)基因多态性、血色病C282Y等位基因杂合子、IL-1β-511基因多态性均见报道与增加肝窦阻塞综合征发病风险相关。因此,在移植前进行相关基因型检测有助于评估肝窦阻塞综合征发病风险,必要时可给予高危患者预防性治疗措施。
其他移植相关肝脏毒性还包括预处理导致的药物性肝损伤和骨髓抑制期间发生感染性胆管炎等。几种肝脏疾病可同时发生,需要鉴别肝损伤的原因并给予相应治疗。
(六)移植相关血栓性微血管病
移植相关血栓性微血管病(transplantation associated thrombotic microangiopathy,TA-TMA)是以微血管性溶血性贫血、血小板减少、微血管血栓形成和多器官功能衰竭为主要临床表现的临床综合征,是造血干细胞移植后罕见的严重并发症之一。移植相关血栓性微血管病的发病率报道不一,总体发生率为0.5%~76%,异基因造血干细胞移植和自体造血干细胞移植后移植相关血栓性微血管病的发生率分别为5%~70%和3%~20%。其发生时间可在移植后早期,也可晚至移植后8个月。目前该病缺乏有效的治疗方案,病死率高达60%~90%。移植相关血栓性微血管病主要与血管内皮细胞损害造成的溶血性贫血、微循环中血小板消耗和纤维蛋白沉积有关。在移植过程中,高剂量化疗、放疗、感染及移植物抗宿主反应等因素造成血管内皮细胞损伤,内皮微颗粒释放,激活血小板功能,导致微血栓形成,出现相关临床表现。
移植相关血栓性微血管病的临床表现存在高度异质性,可表现为无症状的亚临床状态,也可呈暴发性表现。主要表现为微血管病性溶血性贫血、外周血红细胞碎片、畸形红细胞增多以及消耗性血小板减少。典型者还有微血栓导致的脑和/或肾功能异常以及发热。实验室检查可发现凝血功能异常,如纤维蛋白原水平下降、纤维蛋白降解产物(fibrin degradation products,FDP)水平增高等;血生化可显示血清乳酸脱氢酶升高。
移植相关血栓性微血管病的诊断尚无统一标准,目前主要依据国际工作小组(international work group,IWG)标准和血液和骨髓移植临床试验网络(Blood and marrow transplant clinical trials network,BMT-CTN)毒性委员会共识标准。IWG标准:①外周血破碎细胞 > 4%;②新出现的或进行性血小板减少症(血小板计数 < 50×109/L或较前减少 ≥ 50%);③血清乳酸脱氢酶突然、持续升高;④血红蛋白下降或输血量需要增加;⑤血清结合珠蛋白减低。BMT-CTN标准是:①外周血涂片中每高倍镜视野至少出现2个破碎红细胞;②血清乳酸脱氢酶升高;③无法用其他原因解释的肾功能异常(血肌酐升高为正常2倍以上或肌酐清除率减少50%)和/或中枢神经系统异常;④直接、间接Coombs试验阴性。然而各研究标准均存在局限性,不同指标达到诊断标准的时间不同,若待全部指标均满足诊断标准后再给予以治疗,则可能延误最佳治疗时机,因此仍需要寻找具有早期诊断意义的生物标志物协助诊断。
移植相关血栓性微血管病缺乏公认的有效治疗手段,治疗性血浆置换(therapeutic plasmapheresis,TPE)、移植物抗宿主反应(graft-versus-host disease,GVHD)预防药物调整、去纤苷、利妥昔单抗和依库珠单抗(eculizumab)等是可以考虑的治疗方案。现有治疗对该病患者的总体预后均较差,早期诊断、尽早治疗,有助于改善预后。
(七)神经系统并发症
神经系统并发症常发生在移植后急性期,但也可以在移植后数月至数年内发生,包括中枢神经系统(central nervous system,CNS)并发症和周围神经系统并发症。前者包括脑血管病变、中枢神经系统感染、代谢性脑病、药物相关毒性反应和移植物抗宿主病等;后者包括神经根病、周围神经病和肌病等。既往研究结果显示,移植后一年内中枢神经系统并发症的发生率为8%~56%,而周围神经系统并发症的发生率小于5%。化放疗毒性、骨髓抑制后继发感染、出血以及异基因造血干细胞移植等因素与移植后神经系统并发症密切相关。
1.药物相关中枢神经系统并发症
造血干细胞移植过程中应用高剂量化/放疗预处理、免疫抑制剂和某些抗生素等药物可导致神经系统并发症。与中枢神经系统毒性相关的化疗药物包括环磷酰胺、阿糖胞苷、氟达拉滨和白消安等,环磷酰胺可致认知功能损害,阿糖胞苷可引起小脑功能障碍和行为异常,氟达拉滨可导致脑白质病变,白消安可透过血脑屏障导致癫痫发作。此外,顺铂、长春新碱和沙利度胺等药物常与周围神经毒性相关。
2.脑血管病变
移植后常见的脑血管病变主要为颅内出血和脑梗死。回顾性研究结果显示,脑血管病变与移植后高死亡率相关。移植后血小板减少可引起颅内出血、出血性脑梗死;感染性疾病可导致动脉炎性损伤;高血压也是颅内出血相关的重要因素;此外,免疫功能紊乱、血栓栓塞性病变等均可导致脑血管意外的发生。既往研究发现,存在严重血小板减少的患者即使接受了足够的预防性血小板输注仍有可能出现颅内出血。
3.中枢神经系统感染
移植后中枢神经系统感染的发生率为2.0%~4.9%,可发生在移植后全血细胞减少阶段或免疫功能恢复过程中,对于接受异基因造血干细胞移植的患者,还可发生于免疫抑制剂治疗或移植物抗宿主病的时期。致病微生物包括细菌、病毒、真菌和寄生虫。其中,常见的中枢神经系统病毒感染为疱疹病毒,尤其是人类疱疹病毒6(human herpes virus type 6,HHV-6)多见于报道。常规预防性应用阿昔洛韦抑制潜在的巨细胞病毒活化,可显著减少巨细胞病毒脑炎的发生。此外,爱泼斯坦-巴尔病毒(Epstein-Barr virus,EBV)病毒相关的移植后淋巴增殖性疾病也可影响中枢神经系统。多数病毒性脑炎患者可出现精神状态改变,如意识障碍、嗜睡甚至昏迷,部分患者发生癫痫发作、行为障碍或局灶性神经功能缺失,特征性的磁共振成像(MRI)表现以及脑电图有助于诊断。中枢神经系统最常见的真菌感染是曲霉菌感染,其次为念珠菌感染和毛霉菌感染,仅依靠临床症状和影像学表现难以确诊和鉴别,明确诊断有赖于组织病理学检查和真菌培养。真菌性脑脓肿的治疗可选择伏立康唑或脂质体两性霉素B等。
4.肿瘤相关中枢神经系统并发症
移植后患者中枢神经系统并发症可与原发肿瘤颅内复发或第二肿瘤有关。患者常出现颅内占位引起的颅内高压症状,如头痛、呕吐等,也可出现意识改变或局灶性神经功能障碍,肿瘤破裂出血需与脑血管意外相鉴别,影像学检查有助于诊断,确诊依赖于组织活检病理。移植前是否有中枢神经系统受累可提供重要的病史依据。移植后长期生存者,尤其是预处理接受过全身照射的患者发现颅内占位需高度警惕第二肿瘤,如恶性胶质瘤、星形细胞瘤、脑膜瘤和淋巴造血系统肿瘤等。
神经系统并发症的早期发现与及时干预和治疗对于降低治疗相关死亡率,改善患者预后具有重要意义。除密切观察患者移植前后神经精神症状外,完善的辅助检查有助于明确诊断和指导治疗,主要包括:①血液检验:血常规、肝肾功能、电解质、血糖和病原微生物检测等;②脑脊液检验:常规、生化、细胞学和病原学检测等;③影像学:脑和脊髓MRI、CT和颅内血管造影等;④神经电生理检查:脑电图和肌电图等;⑤病理活检等。
(八)远期并发症
常见的移植相关远期并发症包括:移植后第二肿瘤、生殖毒性、心血管毒性、儿童生长发育障碍、甲状腺功能减低和无血管性骨坏死等。
1.第二肿瘤
移植后第二肿瘤主要为移植后淋巴增殖性疾病(post-transplant lymphoproliferative disorders,PTLD)、骨髓增生异常综合征(myelodysplastic syndromes,MDS)、白血病和实体瘤。多数移植后淋巴增殖性疾病发生在移植后最初的数月,而白血病和实体瘤则多于移植后数年才发生。与自体造血干细胞移植相比,异基因造血干细胞移植后患者第二肿瘤的发生率更高。来自多个造血干细胞移植中心的研究结果显示,82%的移植后淋巴增殖性疾病发生在移植后1年内,高峰发生时间为移植后1~5个月,生存一年以上的患者第二肿瘤的发病率为5/10万。移植后继发第二肿瘤虽然发病率较低,但作为移植后远期并发症之一仍时有发生,影响患者的远期生存和生活质量,应引起重视。
2.生殖毒性
精子生成和卵泡生长成熟过程中进行高速有丝分裂使其对化疗敏感,因此许多化疗药物具有性腺毒性,影响患者疗后性功能及生殖能力,其中以高剂量烷化剂为著。高剂量化疗后的性腺功能减退取决于年龄、性别、预处理方案和既往接受过的治疗。对于男性而言,化疗过程中,由于快速分化的精原细胞受到细胞毒药物损伤而导致无精症风险及性腺发育不全风险增高。在女性中,高龄、含烷化剂的预处理方案及联合全身照射导致卵巢衰退的发生率升高。随着越来越多的移植后患者获得长期生存甚至治愈,生殖系统并发症对患者生活质量带来的影响越来越引起重视。生育保留技术和辅助生殖技术的发展使受治疗导致生殖毒性的患者仍有机会保留生育能力。
3.心血管毒性
造血干细胞移植后心血管并发症较为少见,通常应用蒽环类药物和纵隔放疗是抗肿瘤治疗引起心血管系统远期并发症的主要原因。已明确预处理方案中应用高剂量环磷酰胺与移植后心脏毒性风险升高相关。一些其他因素,例如移植早期液体超负荷和电解质紊乱,也增加心脏毒性的发生风险。既往研究发现,许多移植后患者进行运动负荷试验结果显示存在心脏功能不全;此外,接受造血干细胞移植的患者发生动脉系统血管意外的概率也较正常人群明显上升,可能与异基因造血干细胞移植后长期应用免疫抑制剂或移植后内分泌紊乱相关。移植前即存在的心血管事件高危因素,如肥胖、高血压、糖尿病、血脂异常等也增加晚期动脉系统血管意外事件的发生风险。因此,在造血干细胞移植治疗前应对患者进行心脏风险因素评估,移植后长期生存的患者也应密切监测心血管疾病的发生情况。













