英文名称 :hereditary antithrombinⅢdeficiency
中文别名 :先天性或家族性抗凝血酶Ⅲ缺乏症
HAT‐ⅢD呈常染色体显性遗传,OMIM编号107300,ATⅢ基因位于1q23~25,全长为19kb。ATⅢ基因包含7个外显子和6个内含子。HAT‐Ⅲ遗传缺陷的类型分为两大类:Ⅰ型HAT‐Ⅲ遗传缺陷为数量性遗传缺陷,表现血浆中AT‐Ⅲ抗原含量和活性水平皆低于正常水平50%,引起Ⅰ型HAT‐Ⅲ遗传缺陷的原因在于:①1号染色体长臂缺失所致ATⅢ基因的完全性缺失;②ATⅢ基因的部分缺失;③ATⅢ基因的单一碱基缺失、插入导致基因转录和翻译的缺陷;④ATⅢ基因的单一碱基对变异,导致AT‐Ⅲ的加工、分泌异常或细胞内外迅速的降解引发的缺陷。Ⅱ型HAT‐Ⅲ遗传缺陷为质量性遗传缺陷,表现为血浆中出现了功能异常的AT‐Ⅲ,导致AT‐Ⅲ的活性低于正常水平的50%,但AT‐Ⅲ抗原量基本正常,引起Ⅱ型HAT‐Ⅲ遗传缺陷的原因在于:ATⅢ基因的单一碱基对变异,导致AT‐Ⅲ功能性和结构性改变;根据ATⅢ基因的变异对AT‐Ⅲ功能和结构的影响方式,将Ⅱ型AT‐Ⅲ分子变异分为3类,即反应中心位点的变异(reactive site,RS),肝素连接位点的变异(heparin binding site,HBS)和多效性变异(pleiotropic efect,PE)。
1965年Egeberg等首先报道本病。估计发病率为1/2000或1/5000。本病在欧美的发病率接近于血友病。近年来采用较敏感的肝素辅因子试验对4000名苏格兰献血者的调查,发病率为1/350,其中大多无临床症状,上述结果提示正常人群中包括部分ATⅢ生化异常者,并不一定有血栓危险性,因为在静脉血栓患者中仅4%为ATⅢ缺乏症患者。
ATⅢ基因位于1号染色体长臂(1q23~25)。在单倍体染色体基因组中为单拷贝,含7个外显子,DNA全长14kb。采用人肝RNA启动子延伸分析法已获ATⅢmRNA起始位图谱。ATⅢ转录起始于5'端距ATG启动编码子72bp处。3'端距终末编码子49bp处,含AATAAA序列。该序列下游224bp处为酶解或多聚腺苷酸作用位点。基因表达有组织特异性,但对其调控机制为顺式调控序列或逆式调控因子,尚不了解。已发现两个调控元件,但在5'区中不能发现常见的TATA、CCAAT或GC等调控元件。
遗传性ATⅢ缺乏症是常染色体显性遗传性疾病。男女患病机会相等,以杂合子多见;杂合子ATⅢ水平40%~70%。父母患本病则子女发病可能性约59%。诊断需基于对患者全病史及家系的了解。阴性家族史者不能除外自发变异的先天性缺乏症。当蛋白试验结果不能肯定时,以单倍体分析法测定其等位基因的变异将有助于遗传病诊断。同时做家系调查,以便对来自同一祖先的变异抑或基因突变提供鉴定依据。由于遗传性ATⅢ缺乏症为单基因疾病,采用基因多态性作单倍体分析图,已鉴定出50余种多态性变异。可是有许多家系的ATⅢ分子缺陷尚不明确。
对年轻血栓患者、复发性血栓或家族好发倾向者,是否值得进行实验室筛选,尚无统一意见。这是因为具有此三项临床特征的静脉血栓患者中仅30%可查出属ATⅢ或蛋白C或蛋白S缺乏。反之,ATⅢ或蛋白C或蛋白S缺乏者中仅13%呈现上述三项临床特征。英国血液学会建议对年龄40~45岁静脉血栓、复发性静脉血栓或血栓性静脉炎、不寻常部位的血栓、明显血栓家族史者或反复习惯性流产者进行病因调查。低ATⅢ活性水平有诊断价值。单纯免疫学试验是不够的。依靠三类试验可将ATⅢ缺乏症分型:①免疫学试验测血浆ATⅢ抗原;②交叉免疫电泳试验测定异常分子。在存在肝素下出现慢峰则提示ATⅢ-肝素结合部位变异;③功能试验,包括ATⅢ肝素辅因子活性试验和渐进性ATⅢ抑制试验。辅因子活性试验是本病的最佳筛选试验,所有缺乏症均表现出异常。试验基于血浆加肝素后的FⅩa或凝血酶的灭活状况(肝素辅因子活性),培养时间缩短至低于30秒能提高检测灵敏度。渐进性ATⅢ抑制试验是基于缺乏肝素加速条件下ATⅢ的蛋白酶抑制活性与靶物蛋白酶之间的互相反应。该试验能筛选出ATⅢ肝素亲和力受损的患者,表现为ATⅢ渐进性抑制活性正常,但肝素辅因子活性低下。
ATⅢ缺乏症分型:ATⅢ缺乏症变异型已知50余种,分类方法尚未完善,可分为两型(表1)。
表1 ATⅢ缺乏症分型
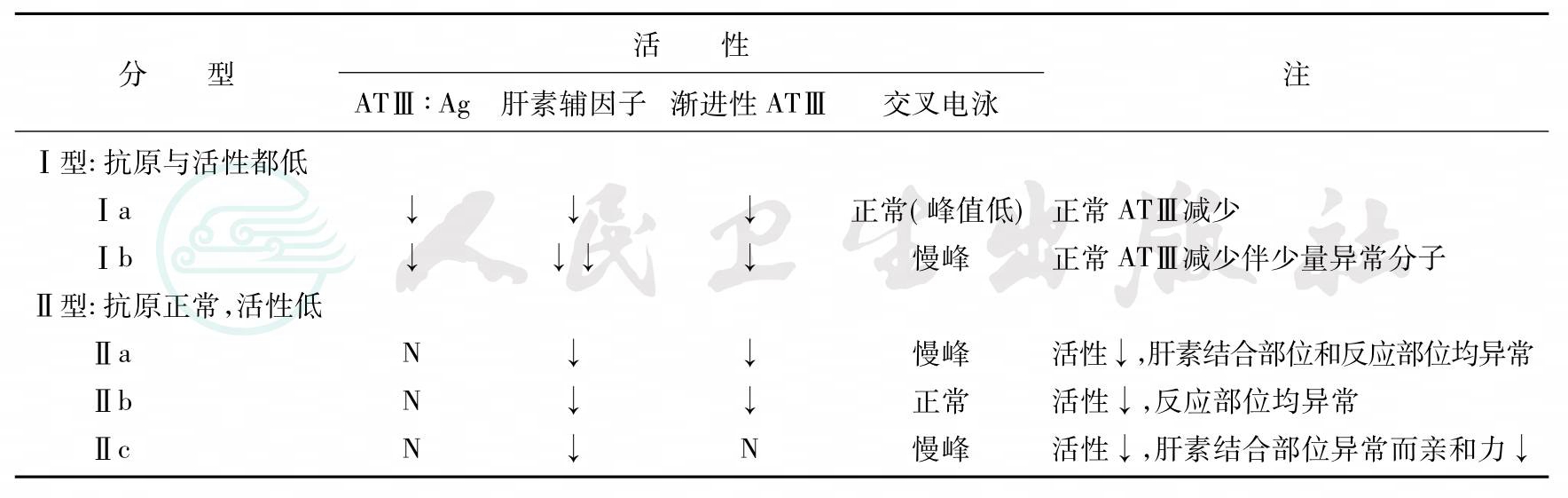
1.Ⅰ型ATⅢ缺乏症
属经典型缺乏症。患者不能合成ATⅢ,故血浆ATⅢ抗原和活性都降低。Ⅰa型测不到变异蛋白,交叉免疫电泳泳动及峰形正常,但峰值减低。Ⅰb型伴少量变异蛋白,故抗原性与活性的减少不成比例,抗原水平高于活性水平。交叉免疫电泳出现慢峰。这些变异蛋白与肝素的亲和力减低和凝血酶无反应。分子病基础Ⅰa型少数为大基因缺失或重排导致无功能等位基因。多数Ⅰ型患者为外显子区的点状改变,如单个碱基替代、插入或缺失,而造成:①翻译框架迁移;②过早生成终止编码子;③产生不稳定蛋白;④影响RNA加工过程等机制参与分子病形成过程。
2.Ⅱ型ATⅢ缺乏症
本型血浆中半数ATⅢ为变异蛋白,故抗原量正常但活性减弱。交叉免疫电泳中见慢峰(分子量增高),与肝素形成的复合物无活性。某些功能缺陷者的分子结构缺陷性质尚未明确。
Ⅱa型:能试验显示ATⅢ肝素结合部位及ATⅢ反应部位均有异常。
Ⅱb型:仅反应部位异常。
Ⅱc型:仅肝素结合部位异常。
Ⅱa及Ⅱb型变异体都产生无功能蛋白,主要是由于单个碱基替代,使反应部位功能异常。例如ATⅢNorth Wick Park Arg393→Cys。
Ⅱc的单个碱基替代使ATⅢ肝素结合部位功能异常,如ATⅢToyama,精47→半胱氨酸而无肝素加速ATⅢ活性。ATⅢRouen- 1精47→组及ATⅢRouen- 2精47→丝使肝素亲和力减低。Ⅱc型仅肝素结合部位(辅因子)活性减低者的血栓发生倾向低。
ATⅢ缺乏症并发血栓,可采用的药物是肝素、口服抗凝、ATⅢ替代治疗及雄激素制剂。
1.肝素
是并发静脉血栓急性期的主要治疗手段,某些大面积血栓栓塞急性期病例需考虑溶栓治疗。普通肝素的有效抗凝需维持APTT时间1.5~2倍延长。无血栓并发症的ATⅢ缺乏妇女,妊娠早期或分娩期普通肝素抗凝剂量使APTT延长10秒。常采用肝素皮下注射6250U,2/d,分娩日停肝素,在产后48~72小时恢复使用肝素,之后改为口服抗凝并维持口服抗凝3个月。低分子肝素可按照体重每日1次皮下注射给药,不用监测或采用血浆抗Ⅹa活性作监测。肝素治疗本身可使血浆ATⅢ水平轻度下降,但不致因此引起血栓。ATⅢ水平减低对肝素治疗有抵抗者(血栓见延伸)或无反应者,有指征合并应用ATⅢ浓缩剂1000~5000U/周,肝素长期使用,尤其妊娠妇女有并发骨质疏松的报道。
2.口服抗凝
华法林口服抗凝,常在肝素治疗同时或后期给药,以抵消华法林治疗初1周内诱发的短暂高凝期。华法林治疗诱发短暂高凝的原因为,依赖维生素K的抗凝蛋白——蛋白C,因其半衰期最短而最先被华法林抑制,之后才发生其他促凝蛋白活性被抑制。华法林通过胎盘,故妊娠早期(6周内)及分娩期妇女禁用,以避免致畸或产妇分娩期出血。此时应该用肝素抗凝。可在妊娠第三期采用华法林直到妊娠36周或分娩前1周再转为肝素治疗。分娩后经肝素过渡到改为口服抗凝治疗。这种设计的治疗方案可以避免肝素使用期过长致骨质疏松并发症。华法林抗凝强度采用凝血酶原时间的国际标准比值(INR)作监测。首次发作或妊娠后的血栓,维持INR值2.0~3.0(即1~2倍延长),复发性血栓病则维持INR值3.0~4.0(2~3倍延长),治疗至少3~6个月。
3.ATⅢ替代治疗
冷冻血浆替代,因输注容量极大而使用受限。ATⅢ浓缩剂国外已有商品,虽经高温灭活HIV及肝炎病毒,但与一般生物制剂应用原则相似,给药前需权衡利弊。各种商品ATⅢ制品都含某些无功能分子,需以功能试验监测疗效,使血浆ATⅢ水平维持80%~120%。输注ATⅢ0.75~0.8U/kg体重可升高血浆水平1%。ATⅢ生物半衰期t1/2为61~92小时,故ATⅢ缺乏妇女的一般输注量1000~1500U,1次/周,同时合并肝素12 500~15 000U可增强抗栓疗效,但肝素可使ATⅢ半衰期缩短。妇女分娩期可增至ATⅢ1000U,每天或隔天输注。
4.雄激素
遗传性ATⅢ缺乏者使用达那唑(danazol)、司坦唑醇(stanozolol)、羟甲烯龙(oxymetholone)等雄激素制剂可升高血浆ATⅢ水平,也有作者报道同时升高依赖维生素K的促凝因子的血浆水平而无应用前景。故作为常规推广应用尚需对照试验来证实其安全性。
遗传性ATⅢ缺乏症无症状者无需预防性抗凝治疗,因回顾性分析资料均表明本病血栓并发率及死亡率均不高,但是因各家系的血栓发生率有所不同,目前对15~40岁ATⅢ缺乏者,处血栓高危期,如妊娠、手术,则主张给予抗凝预防血栓并发症。手术期应用ATⅢ浓缩剂或低剂量肝素皮下给药,都有不少成功的报道。













