老年人急性白血病发病率近年有逐渐增高趋势,以急性髓系白血病为常见,占全部AML的50%以上,其中有24%~56%的患者为继发骨髓增生异常综合征、骨髓增殖性肿瘤等。由于老年AML多存在预后不良的因素,如高龄、其他脏器的并发症多、继发白血病、不良的染色体核型发生比例高,以及接受治疗的患者比例较低等原因,造成老年AML疗效较差。传统化疗治疗老年人AML完全缓解率一般在50%左右,3年、5年的生存率很少能超过20%。老年ALL是一个相对少见的疾病,约占所有成人ALL的16%~31%。和年轻患者不同,老年ALL也具有与老年AML相似的危险因素,而且Ph染色体和/或BCR/ABL融合基因阳性病例的比例可达50%,决定了老年ALL预后较差。但随着对老年患者特定关注以及低毒、靶向治疗药物的不断发展,老年白血病的疗效得到显著改善。
对于急性白血病,目前临床并行使用法英美(FAB)分型和世界卫生组织(WHO)分型。
1. FAB分型
(1)AML:FAB协助组将AML分为M1~M6,后来又增加了M0和M7,它们分别是M0(急性髓细胞白血病微分化型)、M1(急性粒细胞白血病未分化型)、M2(急性粒细胞白血病部分分化型)、M3(急性早幼粒细胞白血病,APL)、M4(急性粒 -单核细胞白血病)、M5(急性单核细胞白血病)、M6(急性红白血病)、M7(急性巨核细胞白血病)。
(2)ALL:按原始淋巴细胞的大小及形态学分成L1型、L2型和L3型。
2. WHO分型 WHO分型结合了形态学、免疫表型、细胞遗传学、分子学特点及临床特征,强调了细胞遗传学分型以及基因特征对预后及治疗的重要性(详见表1,表2,表3)。
表1WHO有关AML分类
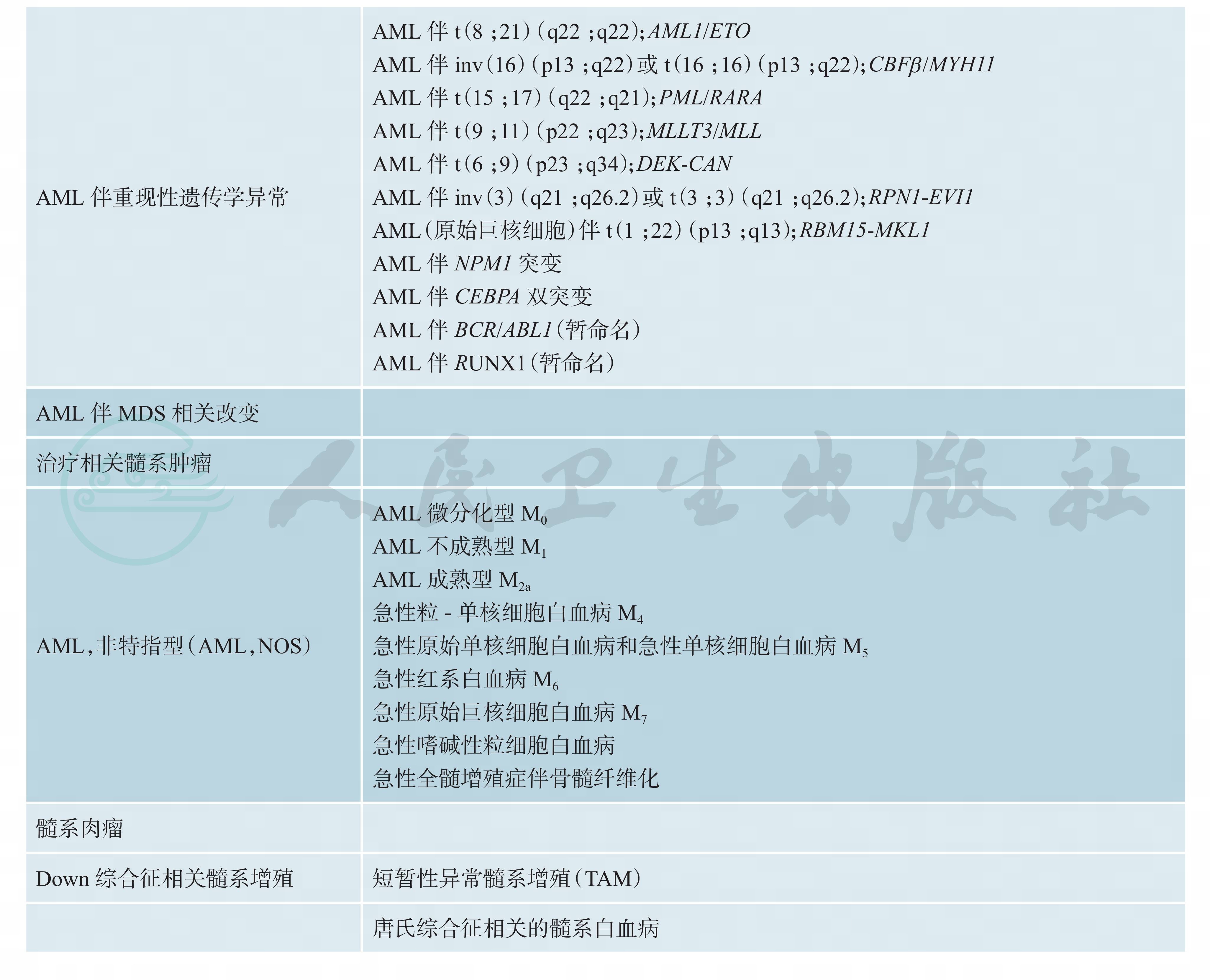
引自:老年医学(第3版).第3版.ISBN:978-7-117-34686-3.主编:
表2WHO有关ALL分类

引自:老年医学(第3版).第3版.ISBN:978-7-117-34686-3.主编:
表3WHO2016:系列未明AL分类

引自:老年医学(第3版).第3版.ISBN:978-7-117-34686-3.主编:
1. 血象 多数病例外周血有不同程度的血红蛋白及红细胞减少,贫血大多数呈正常细胞性,少数患者血片上红细胞大小不等,可找到幼红细胞。约50%的患者血小板 < 60×109/L,晚期血小板往往极度减少。大多数患者白细胞增多, > 10×109/L者称为白细胞增多性白血病,也有白细胞计数正常或减少,低者可 < 1×109/L,称为白细胞不增多性白血病。血涂片分类检查可见数量不等的原始细胞和幼稚细胞,常由此而提示诊断。
2. 骨髓象 是诊断AL的主要依据和必做检查。FAB分型将原始细胞 ≥ 骨髓有核细胞(ANC)的30%定义为AL的诊断标准,WHO分型则将这一比例下降至 ≥ 20%。急性白血病初诊时骨髓中有核细胞极度增生或明显增生,分类中最主要的特征是被累及的血细胞系列有原始和幼稚(早幼稚)细胞大量增生,而正常造血细胞如幼红细胞和巨核细胞则明显受抑制。少数患者骨髓增生低下,称为低增生性急性白血病。
3. 细胞化学 主要用于协助形态学鉴别各类白血病。常见白血病的细胞化学反应见表4。
糖原染色(PAS)除可用于鉴别三种细胞类型白血病外,尚可用于鉴别急性红白血病(M6型)与巨幼细胞贫血,前者往往呈强阳性反应,后者反应不明显。
表4常见AL的细胞化学鉴别

引自:老年医学(第3版).第3版.ISBN:978-7-117-34686-3.主编:
4. 免疫表型检查 根据白血病细胞表达的系列相关抗原,确定其来源。急性混合细胞白血病包括急性双表型(白血病细胞同时表达髓系和淋系抗原)和双克隆(两群来源于各自干细胞的白血病细胞分别表达髓系和淋系抗原)白血病,急性白血病免疫学分类参照WHO 2016分类标准(表5)。
表5WHO 2016白血病免疫分类系统

引自:老年医学(第3版).第3版.ISBN:978-7-117-34686-3.主编:
5. 细胞遗传学和分子生物学 白血病常伴有特异的染色体和基因改变。WHO 2016白血病分类建议不仅包含形态学和免疫学信息,同时包含了细胞遗传学和分子学特征(MICG)。细胞遗传学和分子学信息不仅提供疾病诊断预后信息,同时提供潜在的治疗靶点。例如AML-M3有t(15;17)(q22;q21),该易位是15号染色体上的PML(早幼粒白血病基因)与17号染色体上RARA(维A酸受体基因)形成PML/RARA融合基因。这是M3发病及用全反式维A酸及砷剂治疗有效的分子基础。此外,Ph染色体和/或BCR/ABL融合基因是老年ALL(尤其是前体B-ALL)较常见的细胞遗传学异常,其断裂点位置可能与慢性粒细胞白血病不同。Ph染色体和/或BCR/ABL特异性靶向药物酪氨酸抑制剂纳入治疗方案,显著改善伴Ph染色体和/或BCR/ABL融合基因的ALL预后。随着对白血病分子标志的认识深入,愈来愈多的靶向特异性药物引入白血病治疗,例如FLT3、IDH1/2突变抑制剂。特异性分子标志同时可作为治疗后残留病的监测指标。
6. 其他检查 血清尿酸浓度增高,特别在化疗期间。尿酸排泄量增加,甚至出现尿酸结晶。患者发生DIC时可出现凝血象异常。血清乳酸脱氢酶(LDH)可增高。
出现CNSL时,脑脊液压力升高,白细胞数增加,蛋白质增多,而糖定量减少。涂片中可找到白血病细胞。
急性白血病的治疗目标是彻底清除体内的白血病细胞,同时使正常造血功能得以恢复。急性白血病治疗手段,包括联合化疗、造血干细胞移植、诱导分化、促凋亡、生物靶向治疗等,联合化疗是目前最主要手段,但目前常用的化疗药物,除肾上腺糖皮质激素外几乎都有抑制造血功能的不良反应,并且对肝、肾、胃肠道也有毒性作用,所以用药时要严密观察,随时调整剂量。同时必须加强支持治疗,防治感染和出血,以保证化疗的顺利进行。
老年人本身及白血病细胞的生物学的特性决定其化疗与青壮年急性白血病化疗不同。
首先随着年龄增长,人体各脏器功能不断下降,正常造血细胞的质量和数量亦渐下降,同时药物代谢能力降低,老年患者对长期全量化疗的耐受性明显减低,化疗后易骨髓抑制、全血细胞减少,易并发致命的感染、出血。其次老年患者常伴发其他系统疾病,对化疗药物的毒性耐受减低,感染易感性增加,迫使减量或停止化疗,直接影响抗白血病治疗的疗效。同时,老年人急性白血病细胞的某些生物学特性与青年患者不同,老年患者中有较高比例的预后不良的染色体异常,表达耐药基因的较为常见。此外研究发现老年急性白血病细胞与青年患者比较,更趋于造血干细胞分化的早期原始阶段,处于细胞增殖期的组分较少,骨髓中残存的正常造血细胞甚少,影响化疗后造血恢复,而且老年患者更容易从对标准治疗不敏感的骨髓增生异常综合征转为继发性白血病。上述众多因素导致老年急性白血病化疗缓解率低,化疗相关死亡率高,缓解后复发概率高。老年患者治疗目的既希望提高生存,亦需改善生活质量,降低并发症等。
多项回顾性及前瞻性研究显示,针对 > 65岁老年AML,接受标准7+3方案为主的诱导化疗疗效显著优于支持对症治疗,即使纳入合并症化疗组依然具有更好的总生存。老年AML治疗突破依赖于高效低毒的分子靶向药物。2017年以后FDA陆续批准了8种AML治疗药物,开启了AML靶向治疗时代,新治疗方式出现和循证证据的积累不断推动老年AML临床治疗更新。
急性淋巴细胞白血病儿童更多见,老年患者占急性淋巴细胞白血病不足20%。儿童ALL通过联合化疗治愈率高,成人及老年ALL患者生存显著差于儿童患者,复发显著高于儿童患者。部分成人患者通过异基因干细胞移植改善生存,但仅有少量老年患者有条件接受干细胞移植,老年ALL患者诊断后5年生存率总体不足25%,随着对ALL生物学特性的进一步研究,酪氨酸激酶抑制剂、抗体类药物以及CAR-T细胞的应用显著改善部分老年患者预后。表8列举目前国际上已批准AML、ALL治疗新药。
表8FDA陆续批准AML、ALL治疗药物
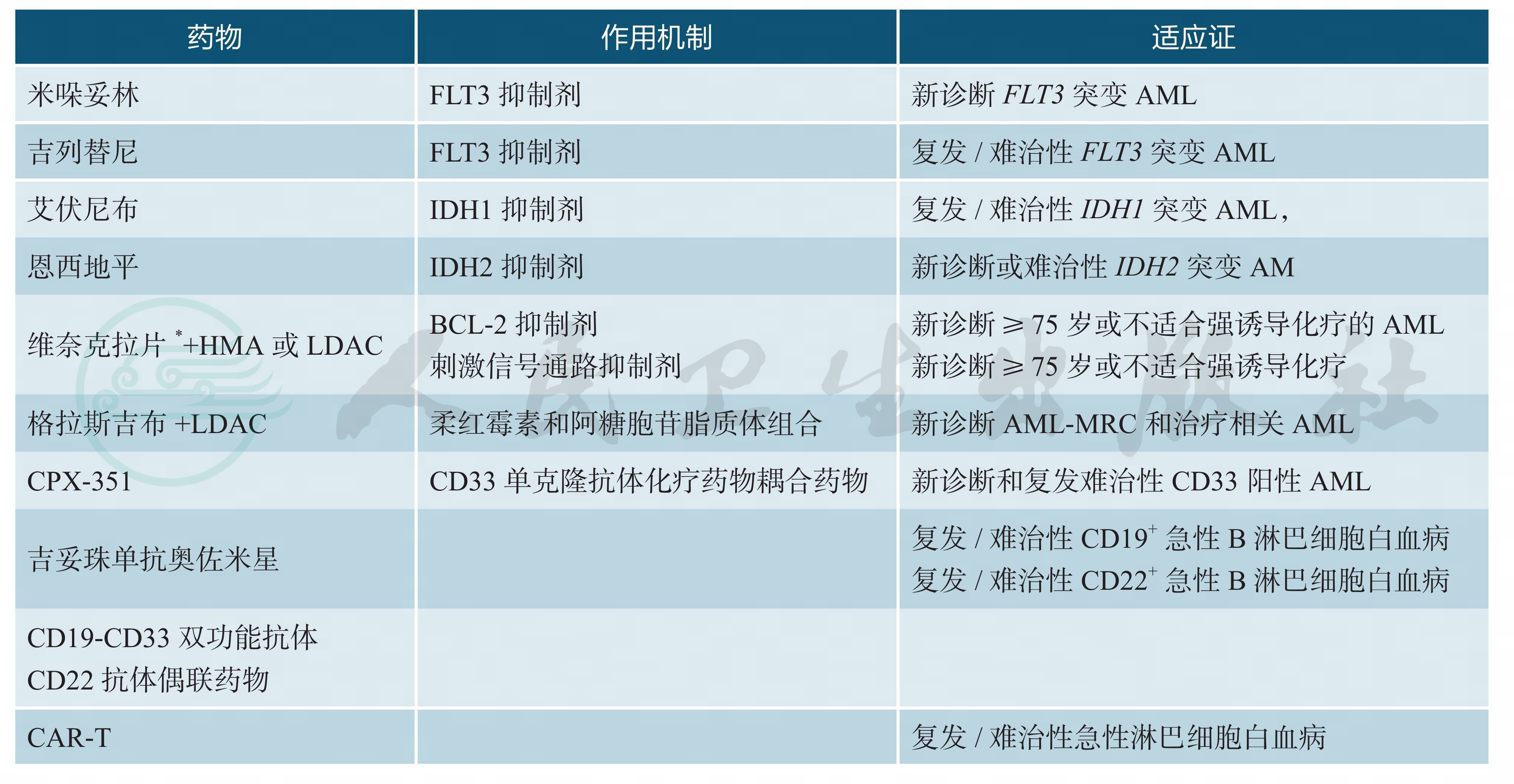
*中国已上市
引自:老年医学(第3版).第3版.ISBN:978-7-117-34686-3.主编:
老年急性白血病治疗方法宜个体化,根据白血病类型、病情程度和客观条件灵活掌握。NCCN(美国国立综合癌症网)2021年AML指南建议针对60岁以上老年患者,使用体能状态,预后不良特征(如不伴有预后良好的细胞遗传学或分子标记的新诊断AML、治疗相关AML、前期血液疾病史)以及合并症来指导治疗方案选择。身体机能状态良好能够耐受强化疗并且预后中-低危老年患者应考虑诱导强化治疗方案;对于预后不良或者无法耐受强烈化疗的患者采用靶向治疗或低强度化疗。老年综合评估是对合并症情况评估的补充,并逐渐成为更好的功能状态预测工具。
1. 支持治疗 对老年急性白血病患者支持治疗显得更为重要,包括血制品输注、抗生素应用及必要时采用羟基脲控制白细胞数,此外还有应用造血生长因子如粒细胞-巨噬细胞集落刺激因子(GM-CSF)、粒细胞集落刺激因子(G-CSF)、红细胞生成素(EPO)等,对老年白血病患者更有积极意义。
2. 化学治疗
(1)急性髓系白血病的治疗
1)标准剂量诱导缓解治疗:目前临床上应用较多的诱导治疗方案仍是以蒽环类药物联合阿糖胞苷(即3+7方案)为主,最常用的是IA方案和DA方案,去甲氧柔红霉素(IDA)8~12mg/(m2·d)或柔红霉素(DNR)45~60mg/(m2·d)×3 天,阿糖胞苷(Ara-C)100mg/(m2·d)×7 天。此外还有以高三尖杉酯碱与阿糖胞苷组成的HA方案是国内常用于AML的诱导缓解治疗的另一方案。但研究表明在这些方案中老年白血病患者疗效明显不如年轻患者,治疗失败的主要原因为毒性相关死亡和白血病耐药。因此如何提高疗效和降低治疗相关毒性就成为学者研究的重点。鉴于蒽环类药物的心脏毒性,现在已有脂溶性柔红霉素(DNX)进入临床试验,随机比较了DNX与DNR联合阿糖胞苷方案治疗老年急性髓系白血病,结果显示缓解率、治疗相关死亡率方面与传统化疗药物相关,但能明显降低复发率。
2)降低剂量的诱导缓解治疗:由于毒副作用相对较少,目前有相当比例的学者采用减低剂量的化疗治疗老年 AML。常用的有减量的 DA 方案[DNR 30mg/(m2·d)×3 天,Ara-C 100mg/(m2·d)×7 天]、小剂量Ara-C方案[Ara-C 20mg/(m2·d)×14~21天];以CAG为代表的预激方案[Ara-C 10mg/m2 q12h皮下注射,第 1~14天;阿柔比星 10mg/d×8天;G-CSF300μg/(m2·d)×14天(WBC > 20×109/L 时停药)],还有小剂量高三尖杉酯碱和小剂量阿柔比星方案等。
3)新药的应用:还有一些新的治疗药物可选择。例如DNA甲基转移酶抑制剂地西他滨(decitabine)、阿扎胞苷。地西他滨20mg/(m2·d)×5天诱导,总体反应率为25%左右,中位生存期7.7个月,且部分染色体核型不良的患者也取得完全缓解,延长了总生存期。阿扎胞苷75mg/(m2·d)×7天治疗患者中位生存期10.4个月,相比经典治疗(支持治疗、LDAC、强烈诱导化疗)患者中位6.5个月显著延长;对于高危细胞遗传学异常老年AML患者阿扎胞苷治疗亦显著延长生存期;对于阿扎胞苷治疗未能获得完全缓解的患者同样生存获益。此外也有小剂量地西他滨联合减低剂量化疗如CAG、小剂量HA、小剂量IA等方案治疗老年白血病的相关的临床研究,初步显示可获得50%~60%的完全缓解率。
氯法拉滨(clofarabine,CaFDA)是第二代核酸类似物。主要有CaFDA联合Ara-C方案和CaFDA单药方案,治疗后缓解率较高,副作用也可以接受,但总体生存率与其他诱导方案相比并未得到明显改善。
2017年后FDA批准多种药物用于AML治疗,包括老年AML治疗。
格拉斯吉布为Hhog通路抑制剂,针对 > 55岁新诊断AML或高危MDS患者,2:1随机对照试验显示,格拉斯吉布+LDAC相比单纯LDAC具有更高的缓解率(17% vs 2.3%,P=0.014 2),中位OS为8.8个月vs 4.9个月(P=0.004),亚组分析显示细胞遗传学中低危患者获益明显(中位OS为12.2个月vs 4.8个月(p=0.000 8))。
维奈克拉为Bcl-2抑制剂,目前已批准用于 > 75岁或不适合强化疗的成人AML诱导治疗。三期临床数据显示,针对前述患者,维奈克拉联合阿扎胞苷相比单纯阿扎胞苷组,诱导缓解率为66.4% vs 28.3%,并且达到完全缓解时间明显缩短(1.3个月vs 2.8个月),中位OS为14.7个月vs 9.6个月,同时残留病MRD转阴比例显著增高(23.4% vs 7.6%),各项指标维奈克拉联合阿扎胞苷均显著优于单纯阿扎胞苷治疗组。进一步亚组分析显示,中-高危细胞遗传学、原发或继发AML患者均可自维奈克拉联合阿扎胞苷获益。IDH1/2突变亚组CR/CRi为75.4% vs 10.7%,FLT3突变亚组为72.4% vs 36.4%,NPM1突变亚组为66.7%vs 23.5%,P53突变/缺失组为55.3% vs 0。2021年NCCN指南推荐维奈克拉联合去甲基化药物作为老年或不适合强化疗患者的优先治疗方案,包括存在IDH、FLT3突变患者。
部分新型分子靶向药物已用于成人AML的治疗。艾伏尼布(Ivosidenib)(AG-120)为口服IDH1抑制剂,针对难治复发合并IDH1突变AML患者的Ⅰ期疗效和安全性数据显示,500mg/d单药口服治疗,完全缓解CR/完全缓解伴部分血液学未恢复CRh比例为30.4%,中位缓解持续时间为8.2个月。针对新诊断、不耐受强化疗且伴有IDH1突变的患者,纳入34例患者,26例(76%)为继发性AML,16例(47%)既往因血液疾病接受至少1疗程的去甲基化药物。中位年龄76.5岁,采用艾伏尼布500mg/d单药口服治疗,CR/CRh反应率为42.4%,其中CR率30.3%,中位缓解持续时间未达,61.5%、77.8%获得CRh及CR患者1年后维持缓解。中位随访23.5个月,总体中位OS为12.6个月。14例患者中9例获得IDH1突变清除。常见不良反应包括腹泻、乏力、恶心、纳差。18%患者出现分化综合征,9%出现3级以上分化综合征。艾伏尼布500mg/d联合标准3+7 DA/IA方案诱导化疗,入组62例,中位年龄62.5岁,18例继发AML,4例(22%)既往接受HMA治疗,中-高危细胞遗传学核型92%,总体缓解率(CR/Cri/CRp)77%,1年OS为78%。
恩西地平为IDH2口服抑制剂,恩西地平Ⅰ/Ⅱ期临床数据显示,214例R/R AML患者中位年龄68岁,接受100mg/d,连续28天为一周期恩西地平治疗,总体反应率38.8%,CR率19.6%,10.3%接受异基因SCT,中位获得CR时间为3.7个月,中位反应持续时间5.6个月,中位OS 8.8个月,既往是否接受强化疗对恩西地平疗效无明显影响。获得CR患者中位OS为19.7个月。3/4级不良反应主要为胆红素升高(10%)、血小板减少(7%)、分化综合征(6%)。Ⅰ/Ⅱ期临床数据包括39例新诊断老年AML伴 IDH2突变患者,中位年龄77岁,23例(59%)存在前驱血液系统疾病,中位接受6周期恩西地平治疗,总体反应率30.8%,CR率18%。中位OS为11.3个月,CR患者中位OS未达。常见治疗相关不良反应包括胆红素增高、恶心、乏力、纳差、皮疹。8例患者出现3/4级AE,但无3/4级感染出现。恩西地平100mg/d联合标准3+7 DA/IA方案诱导化疗,入组93例,中位年龄63岁,35例继发AML,17例(49%)既往接受HMA治疗,91%为细胞遗传学中高危患者,总体缓解率(CR/Cri/CRp)74%,1年OS为76%。
CPX-351为柔红霉素和阿糖胞苷脂质体组合,已批准用于成人新诊断伴多系病态造血以及治疗相关AML的诱导及巩固治疗。Ⅲ期临床试验中纳入309例,60~75岁新诊断的高危或继发AML,相比3+7 DA方案[DNR60mg/(m2·d)×3天],CPX-351治疗老年AML诱导缓解率47.7%,中位总生存9.6个月,均显著优于DA方案组(33.3%、6个月),以移植为删失节点,CPX-351中位OS未达,DA方案组为10.25个月,治疗相关死亡显著降低。
米哚唑啉:FLT3-TKD或FLT3-ITD突变抑制剂,RATIFY研究中纳入 < 60岁新诊断AML伴FLT3-TKD或FLT3-ITD患者,诱导采用3+7 DA联合米哚唑啉(50mg每日二次,第8~21天)或安慰剂,巩固采用4周期大剂量阿糖胞苷(HDAC,3g/m2 q12h,第1、3、5天)联合米哚唑啉(50mg每日二次,第8~21天)或安慰剂,维持治疗12周期,28天/周期,米哚唑啉(50mg每日二次,第1~14天)或安慰剂。米哚唑啉治疗组患者4年OS达51.4%,明显优于安慰剂对照组44.3%(P=0.009);中位OS分别为74.7个月、25.6个月。德国AMLSG16-10研究进一步扩大患者年龄范围,采用DA 3+7 联合米哚唑啉治疗新诊断FLT3-ITD突变的AML患者,61~70岁86例,18~60岁198例。76%患者获得CR/CRi,不同年龄组效果相似。58%CR患者接受HCT,其他患者接受HDAC巩固。55%HCT、56%HDAC患者巩固治疗后米哚唑啉维持治疗,维持治疗中位持续9~10个月。年龄对EFS无影响,与历史对照相比,米哚唑啉维持患者EFS显著优于历史对照(HR,0.41;95% CI,0.27~0.62;P=0.000 02)。最佳人群为CR1期HCT患者,尤其是移植后米哚唑啉维持患者。
吉妥珠单抗(GO,奥佐米星):CD33表达见于90%以上的AML患者,吉妥珠单抗为结合卡奇霉素的人源化CD33单抗。法国随机、开放标签Ⅲ期ALFA-0701研究,纳入280例AML患者,随机分为标准治疗组和加用GO治疗组,旨在了解一线化疗中添加低单次剂量的GO是否可以在改善AML患者的预后的同时而不增加毒性。研究主要终点为无事件生存期(EFS),次要终点为无复发生存(RFS)、总生存(OS)和安全性。研究结果证实在标准方案上加用GO可显著延长新诊断AML患者的EFS和OS,ELN预后中-低危患者均获益,但高危患者疗效无显著差异。
4)缓解后治疗:由于老年患者耐受性较差、并发症多,不能耐受反复的强化巩固治疗,限制了强化疗和干细胞移植的应用。既往研究显示无论采用什么样的缓解后治疗,老年AML的总体生存期一般 < 12个月。随着去甲基化药物HAMS出现,越来越多数据显示以HAMS为基础的维持治疗方案可延长老年AML生存期。针对老年患者缓解后治疗应当依据诱导治疗方案类型、诱导治疗的应答情况以及预后分层特点,结合患者身体状况综合抉择。包括临床试验、异基因SCT、蒽环联合阿糖胞苷、中剂量阿糖胞苷、FLT3或IDH突变靶向药物单独或联合、HAMS维持、支持对症治疗等。缓解后HMA药物维持治疗使老年患者生存获益,尤其是无法耐受强化疗巩固治疗患者。HOVON97三期随机对照研究纳入116例 > 60岁接受2疗程强烈化疗获得CR患者,中位年龄69岁,体能状态评分 < 3。缓解后56例接受阿扎胞苷50mg/(m2·d)皮下注射,连续5天,4周为一疗程,共12疗程或出现疾病进展,82%至少接受4疗程,62%完成12疗程。60例无维持治疗。中位随访3.5年,阿扎胞苷维持治疗组显著降低疾病复发以及缓解期死亡(HR 0.62,95% CI 0.41~0.95,P=0.03),12个月RFS分别为64%vs 42%。但患者OS两组无差异。QUAZAR AML-001研究是口服AZA(CC-486)用于AML维持治疗的全球多中心随机对照研究。共纳入460例诱导治疗后90天内获得CR/CRi的AML患者,中位年龄68岁,1:1随机至CC-486或安慰剂组。CC-486维持治疗300mg/d,连续14天,28天为一周期,同时予以最佳支持治疗。结果显示CC-486组中位OS 24.7个月,显著高于安慰剂组14.8个月(P=0.000 9)。
5)难治复发患者治疗:异基因干细胞移植为唯一治愈手段,但老年患者能够接受干细胞移植可能性低,即使接受干细胞移植老年患者总体获益有限。针对RR-AML老年患者建议参加临床试验,突变基因筛查力求找到靶向治疗药物,采用最佳支持治疗延长生存。
(2)急性淋巴细胞白血病的治疗
1)诱导缓解治疗:老年人治疗方案与青壮年方案大致相同,但疗效较差。剂量以青壮年方案剂量的1/2~1/3为宜。由长春新碱(VCR)和泼尼松(P)组成的VP方案,是ALL的基础用药。在VP方案上加柔红霉素(DNR)或左旋门冬酰胺酶(L-ASP)可分别组成VDP方案或VLP方案,四药同时应用则组成VDLP方案,是目前ALL常采用的诱导方案。在VDLP方案基础上加用其他药物,包括环磷酰胺(CTX)或阿糖胞苷(Ara-C)可提高部分ALL的缓解率。
2)诱导缓解后治疗:与AML治疗不同的是,对于ALL患者完全缓解后应继续治疗的观点被普遍接受。一旦患者达到完全缓解,之后就应进行强化和维持治疗。老年患者完全患者后的最佳治疗方案及治疗持续时间目前仍不明确。多数机构采用在一个疗程中使用多种药物联合治疗并维持2年以上的方案,即完全缓解后经6个月的较强治疗(强化或巩固治疗,如高剂量甲氨蝶呤、Ara-C、6-巯基嘌呤和L-ASP),之后给予大约18个月的较低强度的门诊维持治疗方案(口服6-巯基嘌呤和甲氨蝶呤片)。
3)Ph+ALL的治疗:酪氨酸激酶抑制剂(TKIs)问世前预后极差,常规化疗诱导缓解率50%~90%,但复发率高,多数患者在缓解后1年内复发,中位生存时间8~16个月,5年总体生存率不超过20%。异基因干细胞移植为Ph+ALL唯一治愈手段,但老年患者无法从干细胞移植获益。随着一代TKI伊马替尼问世,随之而来二代达沙替尼、尼洛替尼、氟马替尼、三代普纳替尼的出现,采用化疗联合TKIs不仅显著提高诱导缓解率,同时显著延长患者生存期。化疗联合TKIs对Ph+ALL进行诱导治疗CR率高达90%~95%,异基因干细胞移植联合TKIs的治疗也可使无事件生存率进一步提高。对于老年Ph+ALL患者,强化疗耐受性差,干细胞移植可能性小,在TKI使用基础上可酌情减低化疗剂量,减少血细胞降低和感染的风险。意大利GIMEMA一项研究采用伊马替尼联合泼尼松治疗老年Ph+ALL患者,中位年龄69岁,所有患者均获得CR,中位生存20个月。该数据为后续无化疗方案研究提供重要启示,例如采用更强的二代或三代TKI、联合免疫治疗等。目前国内市场二代TKI包括达沙替尼、尼洛替尼和氟马替尼,二代TKI抑制BCR-ABL;激酶活性作用均显著高于伊马替尼,并且能够克服部分伊马替尼耐药。达沙替尼为ABL/SRC双靶点抑制剂,部分研究显示其可通过血脑屏障,理论上比伊马替尼更适合用于Ph+ALL的治疗。意大利GIMEMA协作组采用达沙替尼140mg/d联合泼尼松治疗53例新诊断Ph+ALL,中位年龄54岁(24~76岁),诱导治疗周期84天。结果显示随着治疗时间延长,患者主要分子学反应率逐步提高,诱导治疗结束后57%患者获得MMR。仅60%患者缓解后结束接受巩固强化治疗,但20个月无复发生存RFS达到51%。随后多项研究显示达沙替尼联合低强度化疗或单纯皮质类固醇药物在老年Ph+ALL患者获益。欧洲白血病协作组EWALL-PH-01研究纳入71例患者,中位年龄69岁(59~83岁),采用达沙替尼联合长春新碱、地塞米松诱导治疗,缓解后巩固治疗提高化疗强度,仅10%患者接受异基因干细胞移植。总血液学CR 96%,分子学CMR为24%,5年RFS、OS分别为28%、36%。尼洛替尼联合化疗治疗Ph+ALL数据有限,医科院血液病医院采用尼洛替尼整合入成人ALL联合化疗治疗30例患者全部获得血液学CR,累积CMR为83.3%,4年RFS、OS分别为45%、54%。氟马替尼在ALL中治疗情况缺乏相关数据。普纳替尼为口服三代TKI,对BCR-ABL激酶抑制作用显著高于一代及二代TKI,并且能够克服包括T315I在内绝大多数激酶结构域突变。MD安德森数据显示,76名中位年龄为47岁新诊断Ph+ALL患者,采用普纳替尼联合hyper-CVAD诱导化疗,完全缓解患者接受每日30mg或15mg普纳替尼维持治疗,联合每月1次VP方案化疗,共维持缓解后2年,15名患者CR1期接受异基因干细胞移植。初始计划普纳替尼剂量为45mg/d,因普纳替尼相关栓塞性心血管事件,入组37例患者后普纳替尼剂量调整,第二周期开始普纳替尼剂量为30mg/d,获得CMR后普纳替尼剂量进一步降低至15mg/d。结果显示3年无事件生存率为70%,最常见的 3或 4级不良事件包括感染(n=65,86%)、转氨酶升高(n=24,32%)、胆红素升高(n=13,17%)、胰腺炎(n=13,17%)、高血压(n=12,16%)、出血(n=10,13%)和皮疹(n=9,12%)。6名患者死亡,3名患者(4%)死于感染,1名(1%)死于出血,2名患者死于与早期普纳替尼使用相关的心肌梗死,方案修订后均未发生死亡。结果显示在没有异基因移植情况下,该方案也能获得持久缓解。GIMEMALAL1811研究中采用普纳替尼联合皮质类固醇激素作为老年或不耐受强化疗患者的一线治疗,入组42例患者,中位年龄69岁(27~85岁),1疗程CR高达95%,累积CMR为45.8%,1年OS为87.5%。
现有临床研究证实TKI药物在Ph+ALL治疗中占有重要作用,无论化疗方案组成、化疗不同阶段,TKI与化疗的联合使用是治疗成功基石。单纯TKI联合激素药物诱导缓解率尽管很高,但是分子学缓解深度以及耐药的发生依然成为关注的重点。目前研究显示,老年或无法耐受强化疗患者在诱导治疗阶段可采用TKI联合毒性较小的方案,例如长春碱类、皮质类固醇激素,减少严重骨髓抑制发生,减少严重感染出血,降低诱导相关死亡,使患者快速、安全地获得血液学完全缓解,有机会进一步接受包括干细胞移植在内的巩固强化治疗。
目前TKI种类较多,何为最佳的一线TKI选择?不同TKI缺乏头对头随机对照研究,MD安德森中心不同时期达沙替尼、普纳替尼联合hyper-CVAD一线治疗Ph+ALL患者的配对数据分析显示,普纳替尼组长期疗效优于达沙替尼治疗,3年 EFS、OS分别为 69% vs 46%(P=0.04)、83% vs 56%(P=0.03)。IPTW分析显示普纳替尼治疗组诱导21天流式MRD转阴率、诱导缓解后完全细胞遗传学反应率、主要分子学反应率以及治疗3个月的完全分子学反应率均显著高于达沙替尼组。IPTW分析进一步证实普纳替尼治疗组具有更长的EFS(P=0.003)及OS(P=0.001)。MD安德森中心Jabbour教授针对一代、二代、三代TKI联合hyper-CVAD治疗Ph+ALL的荟萃分析,显示普纳替尼联合治疗具有更佳的长期疗效,CMR显著高于一代、二代TKI的联合。
4)免疫治疗:急性B淋巴细胞白血病的免疫治疗发展迅猛,主要包括CD3-CD19双功能抗体(贝林妥欧单抗,blinatumomab)、CD22抗体偶联药物以及CAR-T细胞治疗。
贝林妥欧单抗为基因工程制备双特异性抗CD19和CD3抗体,通过抗体将CD3+T细胞定向富集至CD19+B细胞,并刺激T细胞增殖活化,杀灭CD19+B细胞。在形态学复发以及清除残留病治疗的有效性和安全性获得数据支持。在R/R CD19+B-ALL患者,采用贝林妥欧单抗连续输注28天为一周期,每周期间隔2周,CR/CRh比率为69%,安全性良好,独特不良反应包括细胞因子综合征以及脑病。与常规挽救化疗相比贝林妥欧单抗疗效显著增高。Ph+ALL治疗中贝林妥欧单抗亦发挥明显优势。在Ⅱ期ALCANTARA研究中,贝林妥欧单抗治疗45例难治复发Ph+ALL患者,无论既往TKI使用情况,16名(36%)达到CR(有14名患者达到CMR)。同时,10名存在T315I突变患者有4例(40%)获得CR,总体中位OS为7.1个月,RFS为6.7个月。贝林妥欧单抗与标准挽救化疗相比,针对R/R Ph+ALL,接受贝林妥欧单抗治疗患者具有更佳的OS(风险比=0.81)。
奥加伊妥珠单抗(Inotuzumab ozogamicin,INO),为一种人源化抗CD22单克隆抗体,偶联细胞毒素刺孢霉素。在INO-VATE研究中,INO单药对比挽救化疗(FLAG、MA或大剂量阿糖胞苷为基础方案)治疗成人R/R的前体B-ALL的全球Ⅲ期随机研究,INO组总体缓解率(81% vs 29%,P < 0.001)、MRD转阴(78% vs 28%,P < 0.001)、PFS(5个月 vs 1.8 个月,P < 0.001)及 OS(7.7 个月 vs 6.2个月,P=0.004)显著获益。针对初诊老年患者,MD安德森中心先后开展Ⅱ、Ⅲ研究,分别纳入34、52例新诊断 > 60岁ALL患者,采用减低剂量CVAD联合INO治疗,总缓解率为97%、98%,2年OS为70%、66%,显著高于历史对照(2年OS 38%)。在INO-VATE研究中针对Ph+ALL患者,INO单药组与挽救化疗组缓解率虽无显著差异(78.6%vs 44.4%,P=0.08),但INO组显示出良好的CR率。在Ⅰ/Ⅱ期实验中纳入14例R/R Ph+ALL患者(除外T315I突变),中位年龄62岁,采用INO联合普纳替尼治疗,11例(79%)获得缓解,其中73%患者达到流式MRD阴性,55%患者获得CMR,中位OS为8.2个月。
嵌合抗原受体T细胞(CAR-T)是将可识别白血病细胞表面抗原的抗体偶联到T细胞表面,由此形成带有能攻击白血病细胞的嵌合抗原受体的免疫细胞,快速、精准杀伤白血病细胞。目前CAR-T细胞主要有针对B淋巴细胞白血病的CD19 CAR-T和CD22 CAR-T,在R/R急性B淋巴细胞白血病(包括Ph+ALL)取得惊人疗效。大量临床试验数据显示CD19 CAR-T在难治和复发急性B淋巴细胞白血病CR高达90%以上,少数患者可获得持久疗效。
(3)“庇护所”白血病的预防:白血病的庇护所(如中枢神经系统、睾丸、卵巢、眼眶等)是AL治疗必不可少的环节,对ALL尤为重要,老年人急性白血病在这方面与青壮年人急性白血病的预防无大差别。CNSL的预防要贯穿于ALL治疗的整个过程。CNSL的防治措施包括颅脊椎照射、鞘内注射化疗药(如甲氨蝶呤、Ara-C、糖皮质激素)和/或高剂量的全身化疗药(如高剂量甲氨蝶呤、Ara-C)。颅脊椎照射疗效确切,但其不良反应如认知障碍、继发肿瘤、内分泌受损和神经毒性(如白质脑病)限制了其应用。现在多釆用早期强化全身治疗和鞘内注射化疗预防CNSL发生,而颅脊椎照射仅作为CNSL发生时的挽救治疗。对于睾丸白血病患者,即使仅有单侧睾丸白血病也要进行双侧照射和全身化疗。
(4)骨髓移植:由于老年患者不能耐受骨髓移植前的大剂量化疗、放疗的毒性反应和移植后出现的严重并发症所致的极高死亡率。所以老年急性白血病不主张行骨髄移植术。













