心搏骤停(cardiac arrest,CA)指心脏搏动突然停止,失去有效收缩和泵血功能,导致全身严重缺氧而迅速死亡。心搏骤停与呼吸骤停互为因果,伴随发生,因此也称心搏呼吸骤停(cardiopulmonary arrest,CPA)。 心肺复苏(cardiopulmonary resuscitation,CPR)是指采用急救医学手段,恢复已中断的循环及呼吸功能,为急救技术中最关键的抢救措施。
CPR的最终目标不仅是重建呼吸和循环,更重要的是保护脑功能,尽量避免神经系统后遗症,保障生存质量。复苏成功的标准是心肺功能恢复至病前水平,神经系统功能基本正常,无明显后遗症。
1960年6月JAMA杂志首次报道了心脏按压技术,2个月后在马里兰医学协会年度会议上将心外按压和口对口人工呼吸联合起来,称为心肺复苏术,标志着现代CPR技术的诞生。1966年提出标准化CPR。20世纪80年代,美国心脏协会(American Heart Association,AHA)和美国儿科学会(American Academy of Pediatrics,AAP)联合建立了儿童基础生命支持(pediatric basic life support,PBLS)和儿童高级生命支持(pediatric advanced life support,PALS)培训课程,1988年出版了第1版培训教材。2000年,多位国际儿科专家以循证医学为依据,进行大幅度修订后,作为儿童CPR指南推荐给全世界儿科工作者。之后基本上每5年修订一次,并不定时对部分内容进行修订,于2020年发表了最新的指南修订意见。是目前全球普及面最广的儿童复苏指南。
儿童CPA的原因具有年龄特点,新生儿、婴幼儿以先天性疾病、感染等相对多见,幼儿及学龄期儿童意外伤害则明显增多。常见的病因如下:
1.呼吸系统疾病
包括各种原因导致的呼吸衰竭,如先天性气道或肺部发育异常、感染性或吸入性肺炎、急性呼吸窘迫综合征、喉部水肿或支气管哮喘等导致的急性气道梗阻等,是小儿CPA最常见的原因。
2.心血管系统疾病
包括严重的先天性心脏病、心肌炎、各种心肌病及离子通道病等导致的心力衰竭、心源性休克及心律失常等。
3.神经系统及肌肉疾病
中枢神经系统病变如颅内感染、肿瘤等所致脑水肿、颅内高压、脑疝等;外周神经及肌肉疾患,如感染性多发性神经根炎、脊髓性肌萎缩、肌营养不良、皮肌炎等可导致呼吸肌麻痹,引起呼吸衰竭最终导致CPA。
4.消化系统疾病
如各种原因导致的消化道大出血、肠梗阻、肠穿孔、肠破裂、细菌性腹膜炎、急性胰腺炎、肝功能衰竭等均可导致休克或严重电解质和酸碱平衡紊乱,最终引起CPA。
5.泌尿系统疾病
各种急慢性肾脏疾病等可致急、慢性肾衰竭,导致严重水电解质和酸碱平衡紊乱,引起CPA。
6.酸碱平衡紊乱和电解质失调
多种疾病,包括先天代谢性疾病均可导致严重酸碱平衡和电解质紊乱,如高血钾、严重酸中毒、低血钙、低血糖、甲状腺功能减退等。
7.意外伤害及中毒
近年来交通事故或坠落造成的创伤、溺水和药物中毒已成为儿童意外死亡的主要原因。其他如电击、严重过敏反应等也是导致儿童CPA的重要原因。
8.其他
婴儿猝死综合征国外较多见,国内报告较少。迷走神经张力过高虽不是CPA的常见原因,但值得高度注意,如处于严重缺氧状态时,用压舌板检查咽部即有可能致CPA,应尽量避免。手术、治疗操作和麻醉意外也是原因之一。
美国儿童住院患者数据库(kids’inpatient database)的数据显示[1],1997—2012 年,全美儿童院内心搏骤停(in-hospital cardiac arrest,IHCA)的总发病率为0.78/1 000,总病死率为46%。儿童IHCA发病率由1997年的0.57/1 000上升至2012年的1.01/1 000;病死率则呈下降趋势,由1997年的51%降至2012年的40%。院外心搏骤停(out-of-hospital cardiac arrest,OHCA)的流行病学情况尚不十分清楚,美国的儿童非创伤性OHCA发病率约为每年8.04人次/100 000人口,其中约36%经CPR恢复自主循环,但存活率明显低于IHCA,一项泛亚洲地区的研究仅有8.6%[2]。我国有关儿童心肺复苏的研究很少,总体来说,存活出院率低于发达国家水平。
多种病理生理学过程均可导致CPA,最常见的三种发病机制为:①低氧血症(hypoxemia)。最多见,常见于各种原因导致的呼吸衰竭;②心肌缺血(myocardial ischemia)。常见于各种原因引起的休克;③心律失常(arrhythmia)。CPA前常有心室颤动(ventricular fibrillation,VF)或室性心动过速(ventricular tachycardia,VT)。院内CPA的直接原因中,心律失常大约占10%,缺氧和心肌缺血分别占67%和61%(大部分两者兼有);院外CPA同样大部分由缺氧或心肌缺血引起,5%~20%为心律失常所致。
CPA的病理生理过程可分4个阶段:
1.心搏骤停前期(prearrest phase)
指在心跳停止之前的一段时间。儿童CPA多由进行性加重的缺氧或心肌缺血引起,可通过早期识别、治疗呼吸衰竭和休克预防其发展为CPA。
2.无血流灌注期(no-flow phase)
心搏停止至开始CPR前,此期血流完全中断,持续时间越长,复苏成功的可能性越低,复苏后神经系统损害越重。
3.低血流灌注期(low-flow phase)
即CPR开始至自主循环恢复的一段时间,心排血量取决于胸外按压深度和按压频率。成人有效CPR过程中心排血量可达正常的15%~25%,婴儿可达30%~40%。此期高质量CPR是提高存活率、改善神经系统预后的关键。
4.复苏后阶段(post-resuscitation phase)
自主循环恢复(return of spontaneous circulation,ROSC)后,会发生一系列独特、复杂、快速进展的病理生理过程,包括心搏骤停后脑损伤、心肌功能不全、全身多器官缺血再灌注损伤,称心搏骤停后综合征(post-cardiac arrest syndrome,PCAS)或复苏后综合征(post-resuscitation syndrome)。PCAS的病理生理和病情发展具有明显的时间特征,且随病情严重程度、恢复或恶化的速度而异。ROSC后20分钟内,突出的问题是自主循环仍极不稳定;ROSC后20分钟至6~12小时,临床出现PCAS的相关表现,以循环系统抑制、意识障碍、惊厥发作、脑水肿等最为突出,还可有严重内环境紊乱、其他脏器功能障碍等;ROSC后12~72小时,PCAS仍处于进展期,临床症状可进行性加重;ROSC后72小时~7天,PCAS表现在达高峰后逐渐减轻。早期开始康复治疗可减轻存活者的后遗症,改善生存质量。PCAS的病情依心搏停止持续时间、CPR持续时间和CPR质量等而异,轻者存活后无明显后遗症,甚至实现ROSC后无明显PCAS症状;重者存活后可遗留不同程度的神经系统后遗症;最严重者出现脑死亡或严重器官功能障碍导致再次CPA最终死亡。
(1)缺氧、能量代谢障碍与代谢性酸中毒
缺氧是CPA最突出的问题。心搏一旦停止,氧合血的有效循环和组织供氧立即停止,能量供应大幅减少,细胞膜泵功能障碍,离子通道失活,细胞外钾离子急剧升高,细胞内钙超载、钠潴留、水肿和酸中毒等导致细胞功能受损,引起器官功能障碍。严重缺氧及膜泵功能障碍使心肌传导抑制,并可引起心律失常。心肌缺血3~10分钟,即失去复苏可能。脑对缺氧更敏感,心跳停止30秒即出现神经细胞代谢障碍,1~2分钟脑微循环自动调节功能丧失,脑血管床扩张。无氧代谢情况下,脑细胞只能维持4~5分钟即开始死亡。一般常温下心跳呼吸停止4~6分钟,即存在大脑不可逆性损害,即使复苏成功,也会留有神经系统后遗症。即使在高质量CPR情况下,复苏时间延长也会出现脑损伤,导致各种神经系统后遗症,甚至脑死亡。
(2)呼吸性酸中毒
CPA时,CO2以每分钟 3~6mmHg的速度增长。CO2潴留和呼吸性酸中毒抑制窦房结和房室结的兴奋与传导,兴奋心脏抑制中枢,引起心动过缓和心律不齐,抑制心肌收缩,并扩张脑血管。自主循环恢复后,扩张的脑血管使血流量增加,导致脑血流过度灌注,血管内流体静水压增高,同时缺氧与酸中毒使毛细血管通透性增强,促使脑水肿形成。CO2过度增高可造成CO2麻醉,直接抑制呼吸中枢。
(3)缺血再灌注损伤
是指缺血一定时间的组织器官,在重新得到血液灌注后,其功能不仅未能恢复,结构损伤和功能障碍反而加重。这种损伤见于脑、心、肺、肝、肾等脏器。因脑对缺血缺氧最敏感,缺血再灌注损伤(ischemical reperfusion injury)的表现尤为突出。其发生机制尚未完全阐明。近年的研究证明,缺血再灌注损伤涉及广泛的病理生理过程,包括严重缺氧导致内皮细胞损伤引起的血管通透性增加和渗漏;缺血再灌注激发的细胞死亡程序,包括细胞的凋亡、坏死及自吞噬相关的细胞死亡;缺血导致的基因表达的转录控制的改变;循环重新建立后,部分组织不能立即获得血流再灌注等。更为重要的是,缺血再灌注损伤具备自身免疫反应的特点,包括新抗原的天然抗体识别及随后的补体系统激活(自身免疫)。尽管缺血和再灌注通常发生在无菌环境中,但固有免疫和获得性免疫反应的激活,包括模式识别受体的激活和炎症细胞进入病变器官(固有免疫和获得性免疫激活),激发炎症因子释放和炎症反应,导致组织损伤。这一过程与脓毒症有类似之处。
立即现场实施CPR,保证心、脑重要器官的血流灌注及氧供应是成功复苏的关键。不同病因所致CPA,其CPR方法基本一致,开始CPR时无需强调寻找病因。待心搏恢复后,再明确病因,治疗原发病。
复苏全过程可分3个阶段。基础生命支持(basic life support,BLS):是复苏的开始,由最早发现CPA患儿的人立刻开始CPR,通常由1或2人进行。高级生命支持(advanced life support,ALS):是在紧急反应系统启动后,由多人组成的复苏团队共同进行的CPR,在BLS基础上应用辅助器械与特殊技术、药物等,尽快实现自主循环恢复。复苏后稳定(post resuscitation stabilization):实现ROSC后,继续给予严密监测、生命支持、稳定呼吸和循环功能、治疗PCAS、维持内环境稳定等综合治疗措施,目的是保护脑功能,防止继发性器官损害,寻找病因,力争患儿达到最好的存活状态[3-5]。
(一)儿童基础生命支持
发现CPA时,根据现场施救人员的数量,应采取不同的流程以保证尽快开始CPR。单人施救的CPR流程见图1,双人或多人施救的CPR流程见图2[3,4]。

图1 单人施救的CPR流程
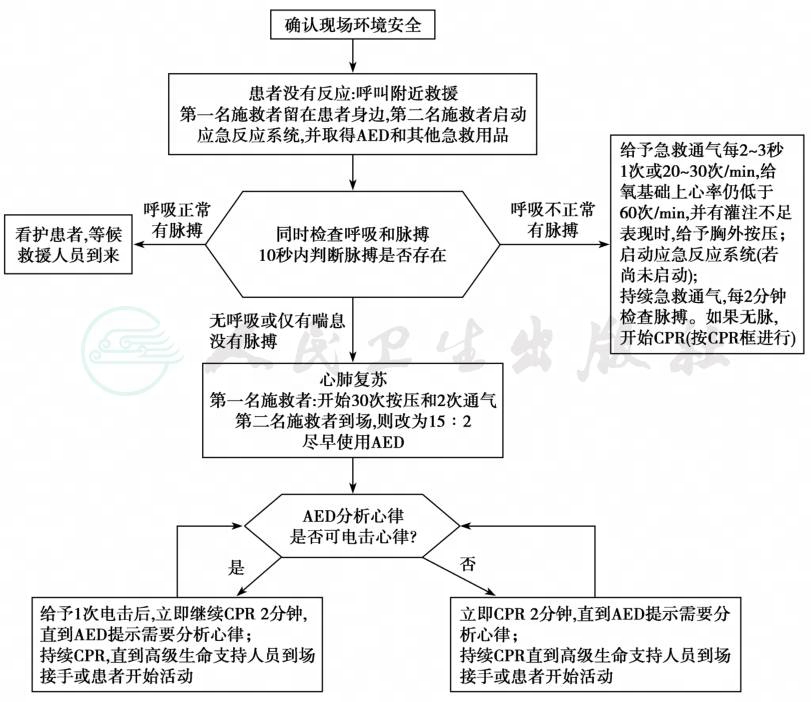
图2 双人或多人施救的CPR流程
1.确认环境安全
遇到CPA或可疑CPA的患儿,必须首先确认环境安全。若患儿处于危险区域,必须首先将其移动到安全区域,搬动外伤患儿需要特别注意保护颈椎和脊柱。
2.检查反应、呼吸和脉搏
发现患儿倒地后,轻拍患儿双肩,并大声说:“喂!你怎么了?”如知道患儿姓名可大声唤其姓名。同时检查患儿是否有肢体活动或语言。对于婴儿,轻拍足底,检查其是否有反应。
如患儿有反应,则快速检查是否存在外伤,是否需要其他医疗帮助。可用手机或离开患儿拨打当地急救电话,随后迅速回到患儿身边,反复评估,等候急救人员到场。对有呼吸窘迫者,使其保持舒适体位。
如患儿无反应,立即现场呼救,然后同时检查呼吸和脉搏,再启动应急反应系统(或请求支援)。AHA 2010版指南已经取消了采用“看、听、感觉”判断自主呼吸的步骤,更新为评估过程中查看患儿有无呼吸动作。在检查呼吸的同时,医疗人员可用5~10秒触摸脉搏(婴儿触摸肱动脉,儿童触摸颈动脉),如10秒内无法确认触摸到脉搏,或脉搏明显缓慢(<60次/min),立即开始胸外按压。若无自主呼吸或呼吸微弱,但大动脉搏动存在且脉率>60次/min,予每分钟20~30次人工呼吸,无需胸外按压。
3.启动紧急反应系统
在医院内复苏或有多人在场时,应立即派人去启动紧急反应系统并获取除颤/监护仪。对无目击者的OHCA,单人复苏时,应首先进行5个循环CPR,再去启动紧急反应系统;对有目击者的OHCA(如体育活动时突然昏迷倒地),应高度怀疑是VF导致,应首先启动紧急反应系统,获得除颤仪,再进行CPR并尽早除颤。
4.心脏按压
是最重要的复苏措施,一般采用胸外按压(chest compression),胸内心脏按压仅用于手术过程中发生的CPA。实施胸外按压时,将患儿仰卧于地面或硬板上,施救者通过向脊柱方向挤压胸骨,使心脏内血液被动排出而维持血液循环。胸外按压的频率为100~120次/min,深度婴儿大约为4cm,儿童大约为5cm,青少年与成人一致,为5~6cm。每次按压后应保证胸廓完全回弹复位。具体方法包括:①双掌按压法。适用于年长儿和成人。施救者双掌重叠,掌根置于患儿双乳头连线以下的胸骨下半部,肘关节伸直,凭借体重、肩臂之力垂直向患儿脊柱方向挤压(图3)。按压时手指不可触及胸壁以免肋骨骨折,放松时手掌不应离开患儿胸骨,以免按压部位变动。②单掌按压法。适用于年幼儿童。除仅用一只手掌按压外,其他同双掌按压。③双指按压法。适用于单人对婴儿实施CPR,施救者一手置于患儿后背起支撑作用,另一手示指和中指置于两乳头连线下方之胸骨上,向患儿脊柱方向按压(图4),效果不及双手环抱法。④双手环抱按压法。是双人或多人对婴儿和新生儿进行CPR时首选的胸外按压方法。施救者双拇指重叠或平放于两乳头连线下方的胸骨上,两手其余四指环抱婴儿胸部,双拇指向背部按压胸骨的同时,用其他手指挤压胸背部(图5)。与双指按压相比,环抱按压法能产生较高的动脉灌注压,按压深度及力度更均匀。

图3 双掌按压法
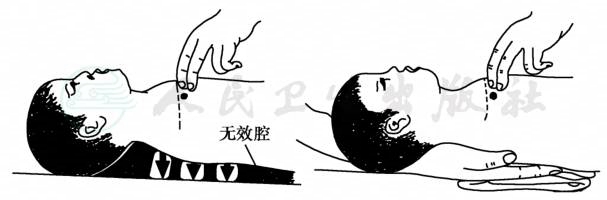
图4 双指法胸外心脏按压

图5 双掌环抱法心脏按压
5.打开气道
呼吸道梗阻是小儿CPA的重要原因,也影响复苏效果,单人CPR按压30次后,双人或多人CPR按压15次后,进行人工呼吸前需打开气道(open airway)。若患儿无头颈部损伤,使用“压额抬颏”法打开气道(图6),颈部过度伸展或过度屈曲都会导致气道阻塞。如怀疑存在头颈部外伤,应使用“上提下颌角”法打开气道(图7),这种方法能尽可能减少移动患儿颈部或头部。若“上提下颌角”法无法有效打开气道,仍使用“压额抬颏”法。亦可放置口咽通气道,使口咽部处于开放状态(图8),打开气道后,首先检查气道内有无异物或分泌物堵塞,若有则予以清除,并保持头轻度后仰,使气道平直,并防止舌后坠堵塞气道。后鼻孔闭锁的新生儿需放置口咽通气道后再转院。
6.人工呼吸
打开并清理气道后给予2次人工正压通气(positive pressure ventilation)。在院外,打开患儿气道后,采用口对口方式,施救者一手捏紧患儿鼻子,一手使患儿的嘴张开,张大嘴完全覆盖患儿口部,平静呼吸后给予通气,每次送气时间1秒钟,同时观察患儿胸部是否抬举。对于婴儿,可张口同时覆盖患儿口、鼻进行通气。若有型号合适的单向阀面罩,将面罩覆盖患儿口鼻,施救者对面罩吹气进行通气。如果人工呼吸时胸廓无抬起,气道开放不恰当导致气道堵塞是最常见的原因,应再次尝试开放气道;若再次开放气道后人工呼吸仍不能使胸廓抬起,应考虑可能有异物堵塞气道,须给予相应处理排除异物。

图6 压额抬颏法
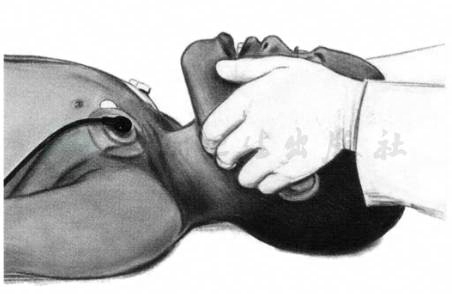
图7 上提下颌角法
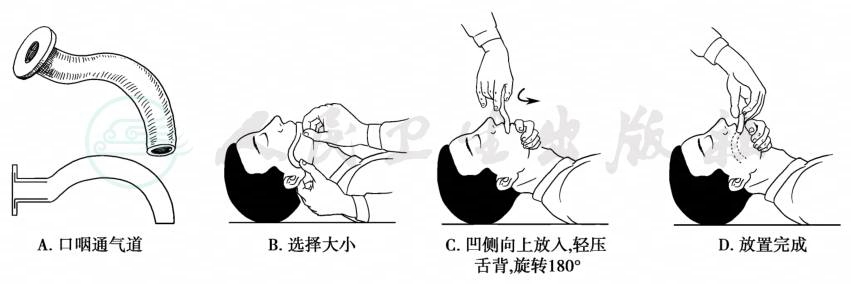
图8 放置口咽通气道
医疗人员在院内进行人工呼吸可使用气囊面罩通气。复苏器构造简单、携带方便,通过挤压呼吸囊进行正压通气(图9A)。插管与非插管患儿皆可使用。非插管患儿首先选择面罩,大小以完全覆盖鼻、口,上不压迫双眼,下不超过下颌为宜。使用E~C钳技术(图9B)扣紧面罩并打开气道,方法为左手拇指与示指呈C状将面罩紧扣于患儿脸部,中指、无名指及小指呈E状置于下颌骨控制头部位置,打开气道,注意不要在下颌软组织上施加过多压力,这样可能阻塞气道。右手挤压球囊给予通气,每次通气时应注意观察胸廓是否抬起。医疗人员充足的情况下,可考虑双人面罩加压通气。气囊面罩人工通气过程中,最好使用100%的氧气。

图9 复苏气囊结构示意图(A)与E-C夹法(B)
7.按压与通气的协调
对儿童而言,理想的按压通气比例尚不清楚。目前推荐:未建立高级气道时,按压通气比单人复苏为30∶2,双人复苏为15∶2;建立高级气道后,按压频率仍为100~120次/min,通气频率为20~30次/min,通气时不再停止按压。若未接受过正规CPR培训或因特殊情况不能进行人工呼吸时,可只进行胸外按压。
8.除颤
对VF或VT导致的CPA,单纯胸外按压和人工通气不能挽救患儿生命,应尽快除颤。除颤每延迟1分钟,复苏成功率降低5%~10%。1岁以下婴儿首选手动除颤器,如无法获得,可考虑使用能量衰减型自动体外除颤器(automated external defibrillator,AED),如两者均无法获得,可使用标准型AED。
9.高质量心肺复苏
高质量CPR的具体要求包括:①同时进行胸外按压和人工呼吸,胸外按压频率100~120次/min;②按压幅度至少达到胸廓前后径的1/3;③每次按压后保证胸廓完全回弹复位;④尽量缩短中止按压的时间;⑤单人复苏时按压通气比例为30∶2,双人复苏时为15∶2,避免过度通气;每2分钟更换按压者,如按压者疲劳可提前更换。
高质量CPR特别强调给予持续有效的心脏按压。一定量的心肌血液灌注是自主循环恢复的前提,适当的冠状动脉和脑灌注是复苏成功的关键。心肌血液灌注取决于血液由主动脉进入冠状动脉的“驱动压”,或称冠状动脉灌注压(coronary perfusion pressure),即舒张期主动脉和右心房间的压力差。在成人,如果CPR期间冠状动脉灌注压低于15mmHg,自主循环恢复的可能性大幅降低。目前尚不清楚儿童CPR期间主动脉压的恰当数值,动物实验数据和成人资料提示:主动脉舒张期(即胸外按压放松时)血压的合理目标是>20~30mmHg。与之相似,主动脉收缩期(即胸外按压时)血压的合理目标为:新生儿>50mmHg,婴儿>60mmHg,儿童>70~80mmHg,青春期>80~90mmHg。
心脏按压是CA期间引起血液流动的唯一动力,按压深度和按压频率决定了CPR时的心排血量。放射影像学研究表明:胸外按压时胸廓压缩很难达到胸廓前后径的1/2,但婴儿胸廓压缩应达4cm,儿童应达5cm,青少年应达5~6cm,心脏才能产生足够的排出量来保证最低的有效灌注。目前尚不能确定胸外按压的适当频率。大样本的动物实验显示,与80次/min相比,按压频率为100次/min时冠状动脉灌注压、心排血量和生存率明显提高。成人临床研究也显示呼气末CO2水平在按压频率为120次/min时较80次/min明显增高。即使短暂的停止心脏按压(例如两次人工呼吸时停止按压4秒),也可使主动脉舒张压和冠状动脉灌注压明显降低,进而导致心肌灌注不足。因此应尽可能地缩短停止心脏按压的时间,每次的停止按压时间<10秒,每个复苏周期中按压时间应占整个复苏周期的80%以上,以保持冠状动脉灌注,促进自主循环恢复。
研究表明,医务人员进行CPR时,约1/2胸外按压幅度太浅;CPR过程中24%~49%的时间未进行按压;按压开始仅1~2分钟后,施救者虽并未感到疲劳,但按压效果已有下降。因此双人在场时,按压2分钟左右即应换人,转换应在5秒钟内完成。
过度通气可使胸膜腔内压增高,静脉回心血量减少,降低心搏输出量,因此应该避免。
(二)儿童高级生命支持
CPR是一个连续的过程,若要达到最理想的复苏效果,重点应注意如下几个方面:①开始BLS时,第一个复苏者立刻开始胸外按压,第二个复苏者到场后,应立刻准备好用气囊面罩人工通气。由于儿童CPA多数由缺氧引起,及时人工通气尤为重要。②保证高质量心肺复苏,这是影响PALS效果的关键。③当两个复苏者分别进行胸外按压和人工通气时,其他复苏者应尽快准备好监护仪、除颤仪,建立血管通路,并准备好预计需使用的药物。图10是CPA时儿童高级生命支持(pediatric advanced life support,PALS)的流程[3,5]。
1.尽快做好监护
尽快连接心电监护并确认心电图表现,若为VF或pVT,则尽早除颤;若为等电位线或PEA,则继续CPR。气管插管后监测呼气末CO2除可帮助快速确认和监测气管插管的位置外,当其突然或持续增加时,提示自主循环恢复,可减少因确认自主循环是否恢复停止心脏按压的时间。若已行有创动脉压监测,自主循环恢复后,则动脉血压监测波形由仅在按压时出现,变为自发的、与脉搏搏动一致的动脉压力波形;中心静脉压则可协助判断血容量和心脏功能,为复苏后稳定治疗提供更多的有用信息。
2.建立高级气道
CPR开始后应尽快气管插管(intubation)或使用喉罩建立声门上高级气道,但不可因建立高级气道长时间停止心脏按压。气管插管前先给予气囊面罩加压通气以使患儿有足够氧储备,插入后立刻验证位置,确认位置恰当后固定插管,开始经气管插管正压通气。
3.建立血管通路
应尽快建立血管通路(vascular access),首选静脉通路(intravenous access,IV),以周围静脉穿刺最常用。静脉穿刺困难时可予骨髓穿刺,建立骨髓通路(intraosseous access,IO)。所有需静脉输入的复苏药物均可经骨髓通路给予。
骨髓通路建立通常选择胫骨。手动操作时通常选择胫骨粗隆内下方2~3cm处为穿刺点。穿刺时进针方向应略向足部倾斜,进针深度为1~2cm。当有落空感、骨髓穿刺针固定后,拔出针芯,用事先抽好3~5ml生理盐水的注射器与骨髓穿刺针连接、抽吸,见到骨髓抽出则证明骨髓穿刺成功。随后推注生理盐水,若推注时阻力小且观察骨髓穿刺针周围无渗出,则可连接输液器输液或给药。有时可能未见骨髓,但推注生理盐水阻力小,骨髓穿刺针周围无渗出,亦说明骨髓穿刺成功。
骨髓输液虽然操作简单,可很快建立血管通路,但其并发症较静脉通路多,发生率随时间延长增高,且可能出现骨髓炎、骨筋膜室综合征等严重并发症。因此,一旦复苏成功,应尽快建立静脉通路。可靠的静脉通路建立后,立刻停止使用骨髓通路并拔除骨髓穿刺针。
4.药物治疗
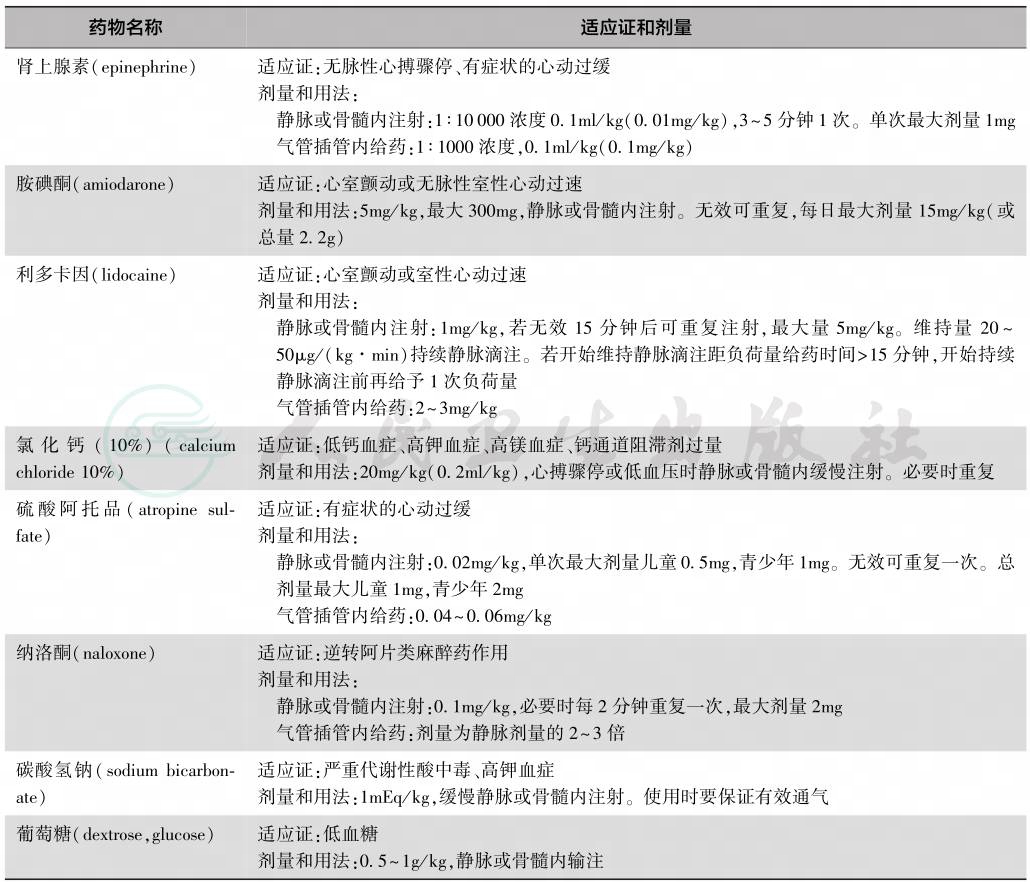
复苏药物最好经血管通路注射或输入。血管通路建立困难、已经气管插管者,可经气管插管给予肾上腺素、利多卡因、阿托品和纳洛酮,其他药物不能经气管插管给予。复苏时常用药物适应证、剂量和给药途径见表1。
(1)氧
氧气(oxygen)在复苏中十分重要,输送到组织中的氧量取决于吸入氧浓度、血氧含量、血红蛋白浓度、心排血量及氧的组织弥散力等。即使是高质量CPR,心搏输出量也仅有正常的25%~30%,只能提供正常需氧量的16%~17%,加之许多其他因素,可导致严重低氧血症。故复苏需用100%氧,而无须顾忌氧中毒。扩张的瞳孔缩小为氧合血液灌注适宜的最早征象,继而皮肤和黏膜方转红润。
(2)肾上腺素
是肾上腺素(epinephrine)受体兴奋剂,为复苏的首选药物。对心脏停搏、通气和氧疗后无反应的症状性心动过缓、非低血容量性低血压疗效确切,还可使心室颤动频率减低,改善电除颤效果。其β1受体兴奋作用可加强心肌收缩力,兴奋窦房结、房室结,加速传导;β2受体兴奋可使周围血管舒张,减轻外周血管阻力;α受体兴奋作用可使周围血管收缩,提高血压特别是舒张压,保证冠脉灌注;由于心、脑血管α受体相对少,因此周围血管的收缩较心、脑血管明显,有利于心、脑供血。肾上腺素的α与β受体兴奋作用与用药剂量关系密切,中小剂量时以兴奋β受体为主、大剂量时α效应更显著。大剂量肾上腺素可增加自主循环恢复率,但不能降低死亡率,且可能与较重的神经系统后遗症有关,因此自2005版以后指南均推荐标准剂量,即经静脉或骨髓内给药,首次及随后剂量均为1∶10 000肾上腺素0.1ml/kg(0.01mg/kg)。若经气管导管内给药,剂量为1∶1 000肾上腺素0.1ml/kg(0.1mg/kg)。 每3~5分钟给药1次。3次用药无效或心复跳后心率又逐渐变慢,可用肾上腺素 0.1~1μg/(kg·min)持续静脉输入。大剂量肾上腺素仅用于β受体阻滞剂过量或中毒时。酸性环境可使肾上腺素灭活,pH值<7.0~7.2时,药物效应减弱。
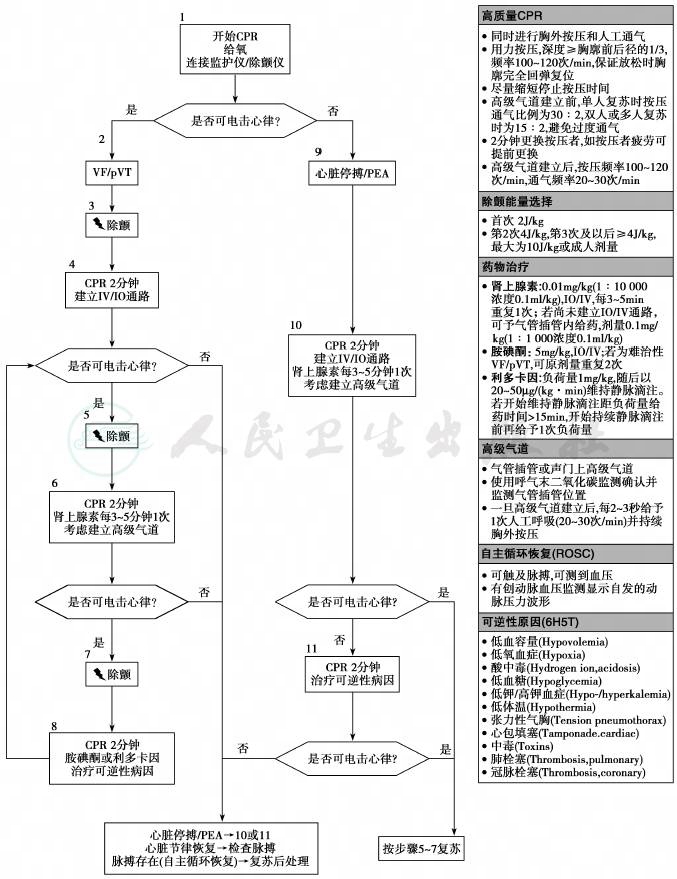
图10 儿童心搏骤停高级生命支持流程
表1 儿童复苏常用药物
(3)碳酸氢钠
CPA时组织缺氧而致的高AG代谢性酸中毒用碳酸氢钠(sodium bicarbonate)往往不易纠正。因此复苏时使用碳酸氢钠要谨慎,以免矫枉过正,引起高钠血症、血渗透压过高、代谢性碱中毒及血CO2升高。其应用指征是:pH值<7.2、严重肺动脉高压、高钾血症、三环类抗抑郁药过量、长时间心脏停跳。剂量为5%碳酸氢钠5ml/kg,稀释成等张液快速静脉输注。此后视血气结果而定。使用碳酸氢钠的同时必须保证有效通气。
(4)阿托品
用于治疗迷走神经张力增高所致心动过缓、二度房室传导阻滞等。小儿心动过缓多因缺氧所致,改善通气更为重要。尚未证实阿托品(atropine)能使停搏的心脏恢复跳动。
(5)胺碘酮
VF、pVT若经 CPR、除颤及给予肾上腺素均无效,可考虑使用胺碘酮(amiodarone)。胺碘酮虽不抑制心肌收缩力,但能减慢房室传导、延长房室结不应期和QT间期、减慢心室内传导(QRS增宽)。因此应避免与其他延长QT间期的药物同时使用。
(6)利多卡因
利多卡因(lidocaine)能抑制心脏自律性和室性异位起搏点,常用于VF或VT。疗效与胺碘酮相当,其特点是半衰期短,起效快,为维持疗效必须持续静脉输入,但若发生不良反应,停药后可很快消失。 首剂负荷量 1mg/kg,随后以 20~50μg/(kg·min)维持静脉滴注。若开始维持静脉滴注距负荷量给药时间>15分钟,开始持续静脉滴注前再给予1次负荷量。
(7)钙剂
已有充分证据显示CPR过程中常规使用氯化钙(calcium chloride)可增加死亡率,使用钙剂的指征仅限于低钙血症、高钾血症、高镁血症和钙通道阻滞剂过量。
5.除颤
除颤(defibrillation)指以电击终止VF或pVT,目的是恢复有序的、可触及脉搏的心电节律和心肌收缩。在心脏导管检查过程中诱发的VF,快速除颤后存活率接近100%。有目击者在场的成人VF在3分钟内接受自动除颤器除颤者长期存活率在70%以上。pVT虽然心电图表现为VT波形,但其心肌收缩呈蠕动状,无有效排血,病理生理与 VF相同,也应立即除颤。除颤前先给予CPR。首次除颤剂量2J/kg。对顽固性VF,应提高除颤剂量,第2次及以后除颤应至少达4J/kg,但最高不超过10J/kg或成人剂量。每次除颤后立刻以胸外按压开始CPR,2分钟后评估心律是否恢复。双相除颤的效果可能优于单相除颤。
操作方法:首先根据患儿年龄和体重选择大小合适的电极板,一般体重10kg以上选用成人用直径8.0cm电极板,10kg以下儿童选用直径4.5cm电极板。若使用AED,打开电源后按照语音提示步骤操作即可。若使用手动调节能量的除颤器,选择好电极板后首先在电极板上均匀涂好导电膏,随后根据患儿体重调节好除颤剂量并按压充电键充电,充电完成后,按照电极板的标示位置,一个置于胸骨右侧锁骨中线第二肋间,另一个置于左腋中线第4肋间,电击前提醒并确认所有复苏者勿接触患儿或与患儿相连的导体,随后双手拇指同时按下放电键除颤。除颤前CPR要持续进行,所有除颤准备做好后再停止按压进行除颤,以尽量缩短停止按压的时间。放电后立刻以胸外按压开始CPR,2分钟后评估心律是否恢复及是否需要再次除颤。若仍为VF或pVT,重复上述步骤再次除颤。
6.终止心肺复苏的指征
对自主循环不能恢复者,目前尚无证据支持何时终止心肺复苏最为恰当。意识和自主呼吸等中枢神经系统功能未恢复的表现不能作为终止复苏的指征;在复苏期间不作脑死亡判断,必须待心血管功能重新恢复后再做判断。只要心脏对各种刺激(包括药物)有反应,CPR至少应持续1小时。
7.体外心肺复苏
近年来有证据表明,对于常规复苏不能恢复自主循环的顽固性CPA,在复苏期间开始体外膜氧合(extracorporeal membrane oxygenation,ECMO),能够维持氧合和循环,增加存活的可能性,称为体外心肺复苏(extracorporeal CPR,ECPR)。 对于可逆性病因导致的顽固性CPA,常规复苏无效时,若具备条件,可以实施ECPR。
(三)复苏后稳定
经CPR自主循环恢复并能维持者,进入复苏后治疗阶段,主要包括:严密监护;维持各种高级生命支持措施,维持有效通气、氧合和循环功能;积极治疗PCAS;维持内环境稳定;避免继发感染;查找病因治疗原发病[5,6]。治疗的目的是提高存活率,减轻后遗症,改善生存质量。复苏后稳定治疗流程见图11。
1.监护
实现ROSC后,应进行密切监护,监护的内容应根据病情选择。基本的监测包括意识状态、体温、尿量、经皮氧饱和度、呼气末二氧化碳水平、心电图、血压、血糖、血乳酸、血气分析、电解质、凝血功能、胸部影像学等。循环状态不稳定者应监测中心静脉压、有创动脉血压、中心静脉血氧饱和度、心脏超声等。神经系统损害明显者应进行脑损伤评估,监测脑电图,并行经颅多普勒超声监测脑血流及颅脑CT或MRI等影像学检查。脑电图监测不仅可发现癫痫性电持续状态,指导抗惊厥治疗,而且可协助判断预后。
2.维持通气和氧合
复苏后继续保持有效通气和维持氧供。过度通气可使心排血量和脑灌注压下降,脑血管收缩,脑血流减少,对神经系统预后弊大于利。除非有脑疝先期症状,不常规使用过度通气。对躁动患儿给予镇静剂(地西泮或咪达唑仑)乃至肌松剂,以保证最佳通气、减少氧耗与气压伤。
复苏后低氧或高氧血症均增加死亡率,但低氧血症更加明显。因此,自主循环恢复后要特别注意吸入氧浓度。在CPR时给予100%氧是合理的。一旦自主循环恢复,应监测血氧饱和度,逐渐调节吸入氧浓度使动脉血氧饱和度维持在≥94%,但<100%。这样既可保证足够氧供,又可防止发生低氧或高氧血症。
复苏后可能存在脑血管的调节异常,动脉血二氧化碳是影响脑血管的重要因素。因此,自主循环恢复后,应尽可能维持正常的动脉血二氧化碳分压,避免过高或过低。
3.稳定循环功能
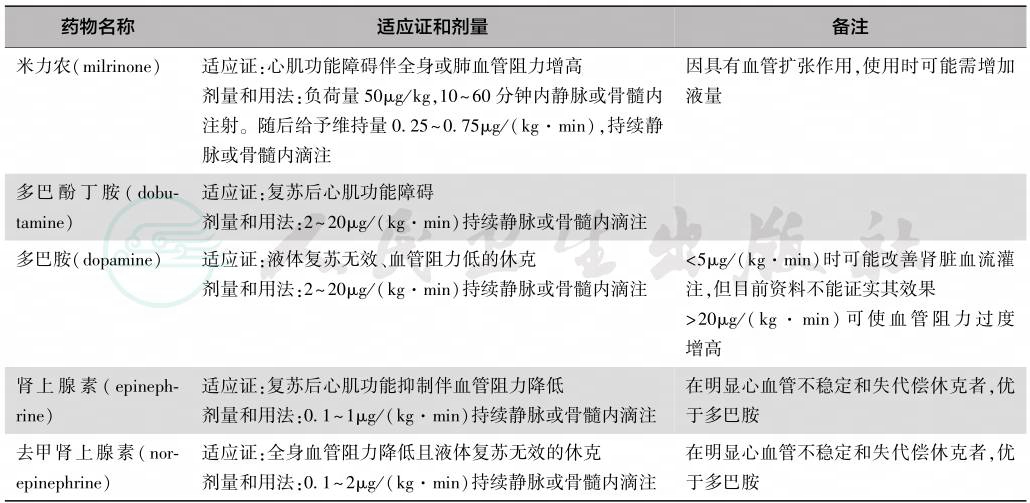
复苏后休克很常见,发生的原因主要为心肌抑制和血管调节功能障碍。一般发生在复苏后数小时内,约8小时以内达到高峰,24小时后开始减轻,通常在48~72小时恢复。积极的血流动力学支持治疗可改善预后。研究表明,复苏后低血压或高血压均与不良预后相关,因此复苏后循环支持的目标是达到同年龄的正常血压。对CPR后确认或怀疑有心血管功能障碍者,应该给予血管活性药物调节心血管功能,常用药物见表2。此外,对复苏后低血压同时有中心静脉压降低等确认或可疑血容量不足者给予液体复苏,有严重心律失常应给予纠正,并维持电解质和内环境稳定。

图11 复苏后稳定治疗流程
表2 复苏后稳定循环常用药物
4.控制体温
治疗性低体温(therapeutic hypothermia)对CPR后对神经系统的保护作用已被证实。2015版PALS指南推荐:对婴儿或儿童OHCA复苏后处于昏迷状态者,应维持5天的正常体温(36~37.5℃),或开始2天的治疗性低体温(32~34℃),随之3天的正常体温;对于婴儿和儿童IHCA复苏后处于昏迷状态者,目前证据尚不足以对采取低温还是正常体温作出推荐意见,但应积极控制体温,在体温达到或超过38℃时积极退热。
5.控制惊厥发作、治疗颅内高压
10%~50%的复苏后脑损伤患儿会发生惊厥发作。部分患儿表现为癫痫性电持续状态,只有脑电图监测才能发现。惊厥发作或癫痫性电持续状态均可使代谢率增高、加重脑损伤和颅内高压,应积极治疗。常用苯二氮䓬类药物、苯巴比妥、左乙拉西坦等。有颅内高压者应给予降颅压治疗。
6.血糖控制
虽然已证实低血糖或高血糖均可增加危重症儿童的病死率,但儿童PCAS血糖的最佳水平尚不清楚。以控制血糖水平在8.3~10.0mmol/L为宜,避免严重高血糖和低血糖。
7.维持肾功能
CPR之后可因肾前原因(血容量不足、肾灌注减少)、肾缺血损害、再灌注损伤等导致急性肾损伤。应针对原因处理,如补充血容量;维持正常血压和循环功能;避免或慎用对肾有毒或通过肾排泄的药物以避免或减轻肾损害。已发生急性肾损伤者则应根据肾损伤程度采取适当限制液量、利尿等措施,必要时可给予持续血液净化治疗,以维持水电解质平衡和内环境稳定。
8.维持水与电解质平衡
复苏患儿均存在水潴留,宜使出入量略呈负平衡状态。最好每日测量体重,保持体重恒定,同时注意纠正酸中毒、低钙、低钾。
9.治疗原发病及防治感染
祛除病因是避免再次发生心搏呼吸骤停的根本方法。应特别注意寻找并尽快治疗可逆性的病因。为方便记忆和查找病因,将引起心停搏和血流动力学改变的潜在可逆因素归结为6H、5T。 6H 指:低血容量(hypovolemia)、缺氧(hypoxia)、酸中毒(acidosis)、高/低血钾(hyper-hypokalemia)、低血糖(hypoglycemia)、低温(hypothermia)。 5T 指:中毒(toxins)、心脏压塞(tamponade cardiac)、张力性气胸(tension pneumothorax)、肺栓塞(pulmonary thrombosis)、冠脉栓塞(coronary thrombosis)。
[1]MARTINEZ PA,TOTAPALLY BR.The epidemiology and outcomes of pediatric in-hospital cardiopulmonary arrest in the United States during 1997 to 2012.Resuscitation,2016,105:177-181.
[2]THAM LP,WAH W,PHILLIPS R,et al.Epidemiology and outcome of paediatric out-of-hospital cardiac arrests:A paediatric sub-study of the Pan-Asian resuscitation outcomes study(PAROS).Resuscitation,2018,125:111-117.
[3]DE CAEN AR,MACONOCHIE IK,AICKIN R,et al. Part 6:Pediatric Basic Life Support and Pediatric Advanced Life Support:2015 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations.Circulation,2015,132(16 Suppl 1):S177-S203.
[4]TOPJIAN AA,RAYMOND TT,ATKINS D,et al.Part 4:pediatric basic and advanced life support:2020 American heart association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care.Circulation,2020,142(16 suppl 2):S469-S523.
[5]MACONOCHIE IK,AICKIN R,HAZINSKI MF,et al. Pediatric life support:2020 international consensus on cardiopulmonary resuscitation and emergency cardiovascular care science with treatment recommendations.Circulation,2020,142(16 suppl 1):S140-S184.
[6]TOPJIAN AA,DE CAEN A,WAINWRIGHT MS,et al.Pediatric Post-Cardiac Arrest Care:A Scientific Statement From the American Heart Association.Circulation,2019,140(6):e194-233.













