英文名称 :infantile hemangioma
婴儿血管瘤(infantile hemangioma,IH)又称婴儿血管内皮瘤,旧称草莓状血管瘤,是毛细血管内皮细胞及支持细胞良性增生所致。
IH的发病受到多种因素影响,目前认为与血管发生失衡、细胞因子调节通路突变、基因发生错义突变、免疫学以及缺氧等外源性因素有关。
(1)血管瘤的发生与增生
1)血管瘤细胞的来源:IH发展中涉及的血管增生有两种形式,一种是由祖细胞和干细胞发育而来的新生血管(也称血管新生);另一种是从成熟的血管发出新血管(血管发生)。
2)IH并非来源于胚胎滋养层细胞:如上所述,曾经认为血管瘤细胞与人胎盘内皮细胞相同的免疫组化表型说明,血管瘤细胞可能是胚胎起源或向胎盘微血管细胞分化。Bree等为了证实IH是否是来源于胎盘滋养层细胞,选取出生5天至2岁患儿的12个组织样本进行选择性滋养层细胞标记免疫组织化学分析(包括人胎盘催乳素,胎盘碱性磷酸酶及角蛋白7,8,17)结果均为阴性。故认为IH并非来源于胚胎滋养层细胞,目前已不再认为血管瘤来源于胎盘内皮细胞栓塞。
3)血管生成与抑制失衡:Folkman提出IH发生是血管生成失调或血管生成和抑制因子间的失衡。许多研究发现,在增生期IH中,血管内皮细胞生长因子(VEGF)、碱性成纤维细胞生长因子(bFGF)、TIE2、IGF-2的表达均上调。同时血清学也检测到VEGF、bFGF、雌二醇-17β显著升高,这些都促进IH的快速增生。
4)细胞因子调节通路突变:研究证实VEGF信号转导的重要性。在正常内皮细胞中,β1整合蛋白可形成肿瘤内皮细胞标志物8(tumor endothelial marker 8,TEM8)和 VEGF 受体2(VEGF receptors-2,VEGFR-2),通过激活活化 T 细胞核因子(nuclear factor of active T cells,NFAT),促使 VEGFR-1 的表达增加。VEGFR-1更易与VEGF结合,却结合后几乎不传导信号。而VEGFR-2与VEGF结合可强烈刺激内皮细胞的增生。另一研究也发现VEGF和bFGF通路的异常上调可引起IH的增生。
(2)血管瘤的消退
1)细胞成分改变:在IH消退过程中,肥大细胞数量最多。肥大细胞的作用,既可促进血管生成又可抑制血管生成。肥大细胞在IH各期发挥了主要作用,但目前对其在消退期中的作用较为肯定。在激素治疗后,肥大细胞数量增加4倍,此时肥大细胞生成凋亡相关蛋白clusterin/apolipopotein J以及其他因子,IFN-α、IFN-β、IFN-γ和TGF-β等。
2)细胞因子的表达改变与凋亡:细胞凋亡是正常组织存在的细胞程序性死亡。IH消退过程中凋亡较增生期和消退后期增加5倍。而且1/3的凋亡细胞是内皮细胞。在这一自发消退过程中,cyt b基因转录增强,促进凋亡。同时,增生期IH局部应用激素后,也发现线粒体cyt b基因表达上调,导致增生期IH加速消退。
金属蛋白酶-1组织抑制因子为血管生成抑制因子,在血管瘤消退期表达升高;凋亡抑制因子在增生期上调,而凋亡促进因子在消退期升高,对婴儿血管瘤消退发挥作用。
(3)遗传因素:多种遗传因素与血管瘤的发生、发展有关。血管瘤内皮细胞是细胞的一种克隆性扩增,细胞内编码与血管生长或其调节途径有关的一个或几个基因发生了体细胞突变。有文献报道,如血管瘤组织中基因发生错义突变,这些基因编码VEGF信号通路以及其他影响血管发育的信号通路中的蛋白质。此外,在部分IH患儿中发现编码TEM8和VEGFR2的基因存在错义突变,突变导致整合蛋白-NFAT信号通路抑制,VEGFR1表达下降,NFAT活性降低。此外,还有发现,部分家族性婴儿血管瘤与5q染色体变异相关。
(4)免疫学:免疫细胞功能不完善,细胞凋亡与增殖失衡,血管内皮细胞增殖;IH内聚集CD8+细胞毒性T淋巴细胞,可能通过释放细胞因子促进血管内皮细胞的增殖。增生期高水平的吲哚胺-2-3-双加氧酶(imdoleamine 2.3-dioxygenase,IDO),色氨酸降解增加,抑制T细胞功能,使IH逃脱免疫监视。
随着患儿免疫系统功能完善,在消退期IDO活性下降,细胞毒性T淋巴细胞(CTL)、Th1细胞、NK细胞、树突状细胞增多,产生FasL增多,FasL-Fas结合产生凋亡信号,激活半胱氨酰天冬氨酸特异性蛋白酶-3(caspase-3),酶切聚ADP核糖聚合酶(PARP),使DNA碎片化,导致血管瘤细胞凋亡,最终瘤体消退。
(5)缺氧和其他外源性因素:母体黄体酮使用、早产、多胎、妊娠高血压、先兆子痫及妊娠糖尿病均为IHs的高风险因素,研究进一步证实宫内缺氧环境可诱发血管瘤发生。先兆子痫、妊娠高血压疾病和妊娠糖尿病均可导致宫内缺氧环境,缺氧促进血管瘤生长因子(如VEGF)的分泌。婴儿血管瘤的发生与消退机制示意图见图1。
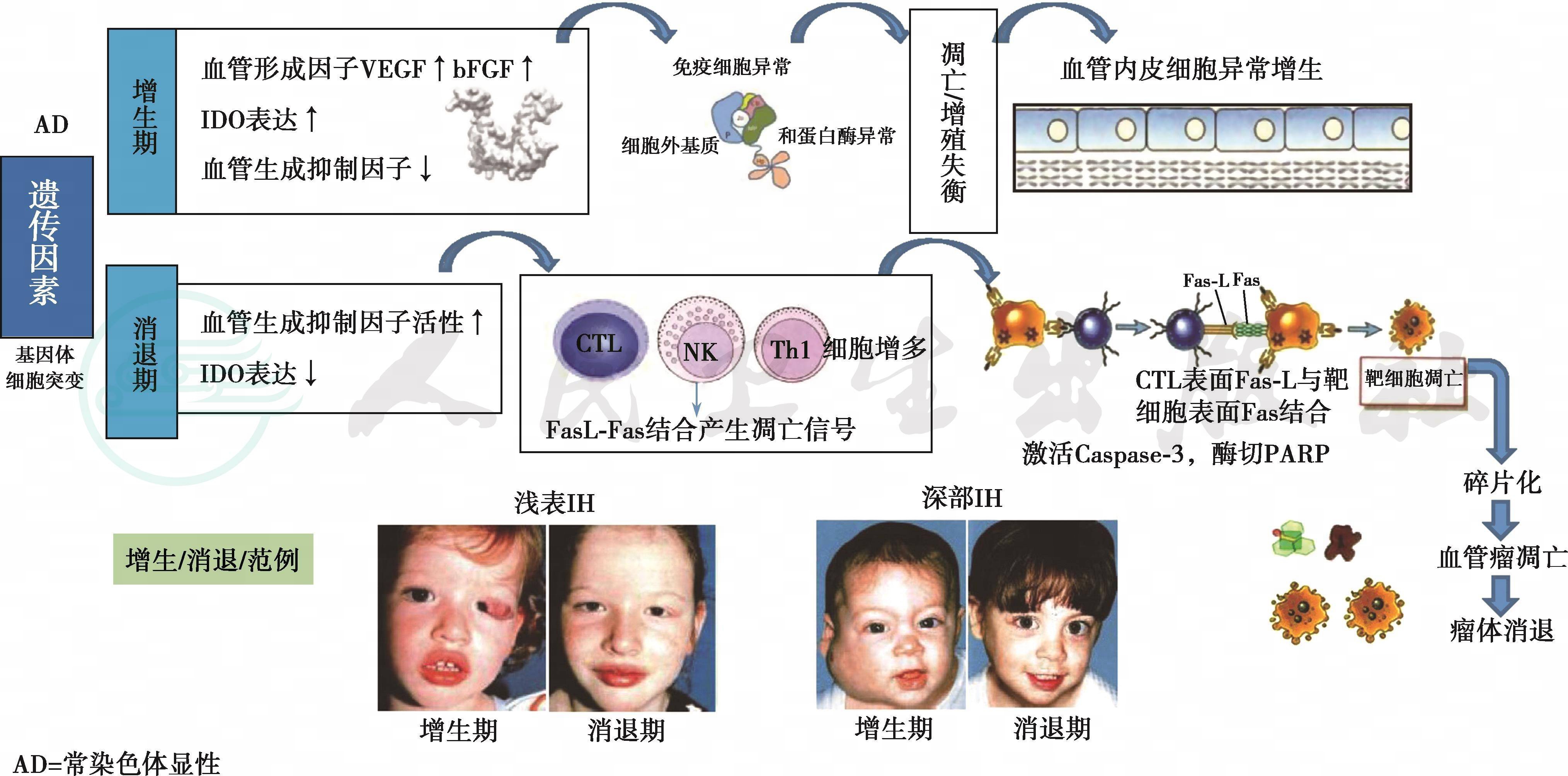
图1婴儿血管瘤的发生与消退机制示意图
引自:现代皮肤科学.第1版.ISBN:978-7-117-31724-5.主编:
血管瘤发病率为2.5%~12%,新生儿期发病率为1.1%~2.6%,婴幼儿期发病率最高10%~12%。血管瘤可发生在全身各部位,好发于头颈部。血管瘤发病率存在明显的性别差异,女多于男,比例约为5︰1~2︰1,低出生体重儿及有血管瘤家族史的婴幼儿是血管瘤发病的危险因素,女性发病率高。出生体重小于1000g的超低出生体重早产儿发病率可高达22.9%,15%~30%患儿为多发性。
血管瘤的病理特征是具有增殖期和内皮细胞的增生。增生的血管瘤在组织学上通常表现为大量的内皮细胞分裂增生、肥大细胞浸润及基底膜层的增厚,几乎没有明显的血管管腔。消退期血管瘤内部都有不同程度的肥大细胞浸润,血管周围开始出现逐渐明显的纤维组织和脂肪组织沉积,伴有血管管腔数量减少并融合成膨大的管腔。目前国际血管异常研究协会(International Society for the Study of Vascular Anomalies,ISSVA)所采纳分类标准目前已被临床医师广泛认同,见表1。
表1国际血管异常研究协会血管瘤分类(ISSVA,1996)

婴儿血管瘤的病理生理见(表2)。
表2婴儿血管瘤的病理生理

注:VEGF=血管内皮生长因子;
引自:现代皮肤科学.第1版.ISBN:978-7-117-31724-5.主编:
1.血常规
一般大致正常,如出现血小板降低,则应考虑Kasabach-Merritt综合征。
2.组织病理
主要表现为大量的血管内皮细胞增生,形成团块状。
(1)治疗原则
1)正确诊断和分型:由于婴儿血管瘤(可消退型、不消退型)的预后不同,故治疗时机和方法也不同。对于许多患儿而言,不干预是最好的手段,因为自行消退在美观方面的效果最好。多数皮损(80%)愈后不留痕迹;少数残余萎缩、色素减退、毛细血管扩张和瘢痕。仅1/4的婴儿血管瘤有治疗指征,包括溃疡(5%)、阻塞重要结构如眼、耳、喉头(20%),并且<1%的患者有生命危险。
2)不干预原则受到动摇:随着泼尼松、普萘洛尔、伊曲康唑以及外用β受体阻滞剂等治疗方法的成熟,选择干预或不干预时应权衡利弊,以最好的结果和预后来确定。
(2)治疗时机与方法:包括药物、激光和手术,以药物治疗为主,抑制内皮细胞增生,促进瘤体消退。原则上,高危病例应尽快治疗,首选普萘洛尔,如有禁忌则系统使用糖皮质激素;中危病例也应尽快治疗,早期外用β受体阻滞剂或联用脉冲染料激光,如控制欠佳则采取高危病例的方案;低危病例可观察或外用药;消退期或消退后的损害采用手术整复,最佳年龄3~4岁,此时自发消退已经结束。高危病例特征:①面部、会阴和腰骶部节段型损害(>5cm);②面部厚度达真皮或皮下或明显隆起的非节段型大面积损害;③早期有白色色素减退;④面中部损害;⑤眼、鼻和口周损害。中危病例特征:①面部两侧、头皮、手、足部损害;②颈、腋或会阴等皱褶部位;③躯干四肢节段型损害(>5cm)。低危病例特征:躯干、四肢的不明显损害。
(3)局部治疗
1)外用药物:包括β受体阻滞剂和5%咪喹莫特软膏,适用于浅表型婴儿血管瘤。
①β受体阻滞剂包括0.5%噻吗洛尔滴眼液、0.2%溴莫尼定+0.5%噻吗洛尔复方滴眼溶液、0.1%噻吗洛尔凝胶、普萘洛尔纳米水溶胶。瘤体外涂,2~4次/d,用3~6个月或至瘤体颜色完全消失,用药2~3个月时疗效最明显。1%普萘洛尔软膏可用于较表浅的婴儿血管瘤,59%的患者明显消退,26%无明显进展,15%无效;噻吗洛尔凝胶的作用强度较普萘洛尔高8倍;0.5%噻吗洛尔滴眼液治疗本病,特别是表浅型安全有效;噻吗洛尔疗效优于卡替洛尔,但由于卡替洛尔有内在拟交感活性,故治疗早产儿婴儿时,相对更安全。②5%咪喹莫特软膏疗效与0.5%噻吗洛尔相当。它通过调节体内多种细胞因子及基质金属蛋白酶而抑制血管形成和瘤体增生。睡前外涂,8小时后以温和肥皂水洗去,隔日1次,疗程为4个月。主要副作用有红斑、糜烂、水肿,甚至瘢痕形成。
2)局部注射治疗:①糖皮质激素诱导内皮细胞凋亡和抑制其增殖,使间质纤维化,纤维隔增厚,毛细血管腔最后完全闭塞。新生儿血管瘤剂量为醋酸泼尼松龙15~20mg/次,瘤体中心和边缘分点注射,每处0.2ml,注射后压迫数分钟;5~7天重复一次,一般3次即可治愈,适用于直径<1cm的头顶、面颊、唇及大阴唇血管瘤。醋酸缩丙酮曲安西龙20~50mg/次+倍他米松磷酸钠5.26mg/次,直接注入瘤体间质,应注意回抽无血后再缓慢多方向推药,间隔6~8周可重复注射,一般注射3~4次。②抗肿瘤药用于口服或局部注射糖皮质激素疗效不佳者。瘤体内注射平阳霉素用于体积较小的局限性表浅型婴儿血管瘤,或糖皮质激素疗效不佳的肥厚型病变,用注射用水配制成1mg/ml注射液,自瘤体内注射药物,直至瘤体呈苍白色为止,每次用量不超过8mg,病变较大者可重复注射。也可注射博来霉素。
3)激光治疗:有585/595nm脉冲染料激光、532nm倍频Nd:YAG(掺钕钇铝石榴石)激光(KTP激光)、长脉冲1064nm Nd:YAG激光等。常用于治疗早期、浅表、扁平的损害,以及消退期遗留的红斑和毛细血管扩张。血管瘤深度<4mm时,推荐使用脉冲染科激光或KTP激光,>4mm时,首选长脉冲Nd:YAG激光。
4)选择性动脉插管注射:参见海绵状血管瘤。
(4)系统治疗
1)糖皮质激素:糖皮质激素可抑制间充质细胞由休止期转入增殖期,引起血管收缩、血栓形成和血管闭塞,诱导内皮细胞凋亡和抑制其增殖,对浅表型(草莓状)和深部婴儿血管瘤皆有疗效。目前国内比较认同的方案是口服泼尼松3~5mg/kg(总量≤50mg),隔日晨起顿服,共8周,在第9周减量1/2,第10周服10mg/次,第11周服5mg/次,第12周停服,上述为一个疗程。必要时可间隔4~6周重复第二或第三个疗程。通常在用药数天至数周内即有明显效果,约1/3的血管瘤明显皱缩,1/3停止生长而无明显皱缩,1/3无反应。
2)普萘洛尔:普萘洛尔为β受体阻滞剂,用于治疗各种心律失常、心绞痛、高血压,它对血管瘤的疗效由法国医生Leatue-Labreze等在2008年发现,作用机制可能为:引起血管收缩,使瘤体颜色变暗,质地变软;抑制增生期的碱性成纤维细胞生长因子(bFGF)和血管内皮细胞生长因子上调,促进血管瘤的消退;促进增生的内皮细胞凋亡。普萘洛尔对增殖期和稳定期的婴儿血管瘤均有良好而迅速的疗效,即使是巨大、复杂、伴溃疡或对糖皮质激素抵抗的血管瘤。
推荐剂量为1.5~2mg/(kg·d),分2次服用,以0.5mg/kg起始,如无精神萎靡、呼吸困难、烦躁、肢端湿冷等反应,12h后再服0.5mg/kg,如仍无异常,次日加量至1.5mg/(kg·d),第3天加量至 2.0mg/(kg·d),并维持治疗。多数婴儿对 2~3mg/(kg·d)剂量耐受良好,但出于安全,对首次接受治疗的患儿,应在给药6h内密切监测血压、心率和心电图,如无异常,可回家治疗,对1周龄的患儿应避免使用普萘洛尔。通常在用药后1~3天起效,疗程为1~1.5年,位于眼、口、鼻周的瘤体消退缓慢,部分患儿需服药>2年。需逐步减量,一般需历时2~3周,切忌突然停药导致反弹。停药后出现复发或反弹可再次使用。
国内李丽、马琳等研究(n=235)显示多数患儿服药24~48小时即起效,半年瘤体明显缩小、颜色变浅,部分患儿仅遗留毛细血管扩张。停药半年内复发率约为28%(66例),其中15例为严重复发,复发的危险因素包括服药剂量为1.5mg/(kg·d)、首次服药年龄>8周、疗程≤0.5年和停药年龄<1岁。普萘洛尔剂量越大,复发率越低;服药较晚者瘤体已较大,疗效降低。疗程过短或停药年龄过小的患儿,复发风险亦升高,如无严重不良反应,停药年龄应>15个月。消退的颜色在停药后可再次出现,可能由于药物缩血管作用消失所致的血管扩张,如果在4岁时还存在毛细血管扩张,可行脉冲染料激光治疗,如瘤体再次增大或颜色明显加深,需再次服药。
3)阿替洛尔:为选择性β1受体阻滞剂。国内王琦等报道阿替洛尔治疗本病的疗效与普萘洛尔相仿,但不良反应更少。治疗方案为第1周服用0.5mg/(kg·d),第2~24周服用1mg/(kg·d),1次/d。每次随访时监测血糖、心电图和血压等指标。治疗24周后,75.6%消退满意。不良反应有睡眠障碍、烦躁、细支气管炎合并气道高反应性、呕吐、腹泻、便秘、食欲减退等。
4)伊曲康唑:国内冉玉平等发现三唑类抗真菌药伊曲康唑对婴儿血管瘤有效,受到国际同行的关注。体内外研究发现伊曲康唑可抑制血管发生和肿瘤生长,对血管瘤细胞生长的抑制作用较普萘洛尔强10倍。伊曲康唑有可能作为婴儿血管瘤治疗的新选择。推荐剂量为5mg/(kg·d),疗程2~22周(平均8.8周),治疗第1个月血管瘤颜色变浅、生长速度放缓,第3个月时所有患儿皮损均明显改善,有效率约71%。
5)干扰素:Ezekowitz等采用干扰素治疗糖皮质激素抵抗的新生儿血管瘤(n=20),有效率高达90%。作用机制可能为非特异性抑制内皮细胞增殖和血管发生,调节血管生成相关基因表达,抑制内皮细胞增殖和促进凋亡。剂量为每天皮下注射100~300万IU/m2,持续2~4.5个月。但干扰素α-2a有神经毒性,可引起瘫痪或痉挛,故后期多改用干扰素α-2b,尽管如此仍有许多副作用,故仅限于其它治疗无效、危及生命的病变。主要适应证包括作为系统性糖皮质激素治疗无效的重症婴幼儿血管瘤二线药物,或作为Kasabach-Merritt综合征的一线治疗。
6)新开拓的药物:有人使用醋丁洛尔(8mg/kg,2次/d)治愈1例声门下血管瘤,安全性好,无复发或严重支气管挛缩。其他药物还包括他克莫司、吡美莫司、血管内皮生长因子拮抗剂贝伐单抗、他莫昔芬和沙利度胺。
(5)手术治疗:对于生长迅速、面积大和较肥厚的血管瘤,或影响重要器官功能时可采取手术切除。增生期手术指征包括:①影响视力发育;②阻塞呼吸道;③头皮或窄蒂损害;④出血;⑤保守治疗无效的溃疡。消退期/消退后期手术指征包括:①保守治疗无效的皮肤松弛、瘢痕、纤维脂肪组织残留;②预期术后功能和外观效果理想。













