儿童肿瘤(childhood cancer)是指发生在儿童期的良性和恶性肿瘤。多数儿童恶性实体瘤起源于神经外胚层、中胚层间叶组织、生殖细胞或胚胎残余组织,主要有中枢神经系统肿瘤、神经母细胞瘤、间叶组织来源的各种肉瘤、胚胎性肿瘤、生殖细胞恶性肿瘤等。首都医科大学附属北京儿童医院1955—1995年40年中收治的小儿肿瘤资料显示,良性肿瘤8 337例,恶性肿瘤2 705例。良性肿瘤中,以软组织肿瘤居首,占45.28%,其次为胚胎残余组织肿瘤,占19.73%,第三位为神经组织来源的肿瘤,占14.56%。上皮来源的肿瘤占极少数。软组织肿瘤依次为血管瘤、淋巴管瘤、纤维瘤和脂肪瘤,以淋巴网状内皮系统肿瘤居首位(图1);而成人以上皮源性肿瘤为主,常侵犯肺、乳腺、胃肠道、肝脏和头颈部等。在儿童尤其是婴儿期的肿瘤,无论是良性或恶性,有自行消退的可能性。如毛细血管瘤大部分可自行消退;婴儿期的神经母细胞瘤部分也有自行消退或转化为良性神经节细胞瘤的病例。儿童肿瘤的主要致病因素与遗传有关,常伴发多种先天性畸形和常呈双侧或多发性发病;染色体异常较为常见。
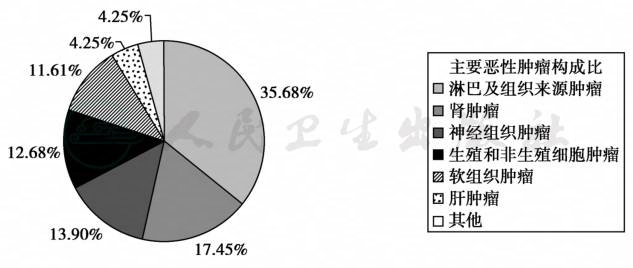
图1 小儿主要恶性肿瘤的构成比例
儿童肿瘤主要致病因素与遗传有关。有很多肿瘤,如神经母细胞瘤、肾母细胞瘤、肝母细胞瘤和视网膜母细胞瘤等,常伴发多种先天性畸形或常呈双侧或多发性发病,染色体异常较为常见,且多集中分布在若干条染色体上,如第11对染色体,主要表现为缺失、重复、移位、倒位等。这些肿瘤的发生可为单基因所致。但更多肿瘤的发生受内外环境多种因素调节。
1.参与肿瘤发生的基因
主要有两种:原癌基因(proto-oncogene)和抑癌基因(tumor suppressor genes)。原癌基因是细胞内与细胞增殖相关的基因,其表达产物对细胞的生理功能极其重要,负责调节细胞周期、控制细胞生长和分裂的进程,是维持机体正常生命活动所必须的。当原癌基因的结构或调控区发生变异,基因产物增多或活性增强时,使细胞过度增殖,从而形成肿瘤。原癌基因根据其作用机制分类(表1)。
表1 儿童肿瘤相关的原癌基因激活
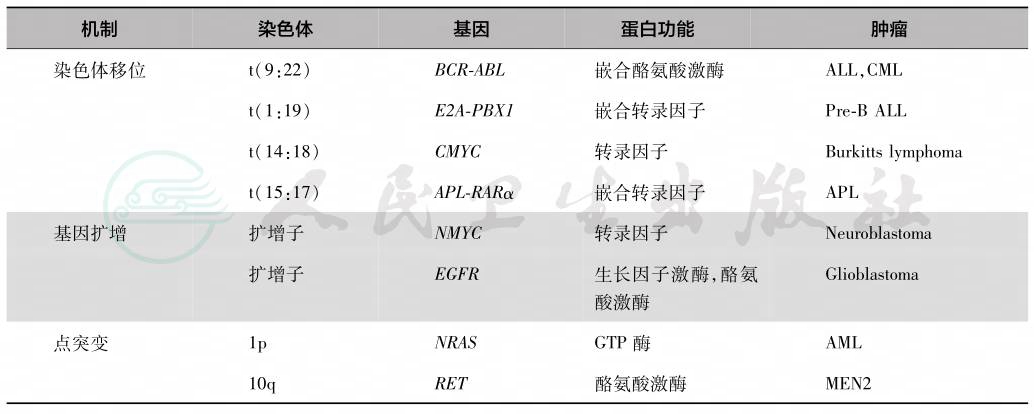
注:ALL:acute lymphocytic leukemia,急性淋巴细胞白血病;CML:chronic myelocytic leukemia,慢性髓细胞白血病;APL:acute promyelocytic leukemia,急性早幼粒细胞白血病;AML:acute myelocytic leukemia,急性髓细胞性白血病;Burkitts lymphoma:伯基特淋巴瘤;Neuroblastoma:神经母细胞瘤;Glioblastoma:神经胶质瘤;MEN 2:multiple endocrine neoplasia,type 2,多发性内分泌瘤病2型。
抑癌基因是正常细胞中存在的基因。对细胞的发育、生长和分化的调节起重要作用,抑制细胞增殖,促进细胞分化和抑制细胞迁移,起负调控作用,其产物主要包括转录调节因子,如视网膜母细胞瘤基因(Rb)、p53等。Rb基因是人类发现的第1个肿瘤抑制基因,定位于13q14。大多数视网膜母细胞瘤以及多种其他恶性肿瘤中Rb蛋白表达缺失或降低。Rb蛋白通过抑制多种与细胞周期进程有关的基因的转录活性,从而抑制细胞周期的进程,Rb基因与细胞凋亡有关。
2.与肿瘤相关的综合征
小儿患某些疾病时,并发肿瘤的频数增高,如有些先天性畸形患儿较易并发肿瘤。单侧肢体肥大的患儿易发生肾母细胞瘤;小儿有毛细血管扩张性共济失调综合征或着色性干皮病时,合成脱氧核糖核酸障碍,对放射线易感性增加,前者易并发淋巴瘤和白血病。免疫缺陷患儿发生白血病、淋巴瘤的频数增加。13号染色体失去长臂时,易并发视网膜母细胞瘤。又如慢性粒细胞白血病患者的细胞有“Ph1”染色体。因此,小儿患恶性肿瘤时,应详询家族中有无肿瘤的历史,并检查有无先天畸形及免疫缺陷等异常情况。
3.其他因素
成人60%~90%的肿瘤都与环境中的致癌因素有关,故多见上皮性肿瘤,如胃肠道癌、肺癌、膀胱癌。而小儿肿瘤与外环境有关的,目前只有在伯基特(Burkitt)淋巴瘤患儿的恶性淋巴细胞及血清中可找到Epstein Barr病毒;恶性肿瘤放疗时发生第二个恶性肿瘤的概率增加。此外,曾有用合成雄性类固醇(anabolic androgenic steroids)治疗再生障碍性贫血时并发肝细胞癌的报道。
近年来,儿童癌症的基因组图谱方面取得了显著的进展。基因组研究结果为靶向药物治疗提供了方向,包括:NPM-ALK融合基因与间变性大细胞淋巴瘤的关系、ALK点突变与神经母细胞瘤相关、与儿童胶质瘤亚群相关的BRAF基因改变、与急性淋巴细胞白血病(ALL)患者ABL家族基因易位激活的研究。基因组学的发现对于在组织学中确定具有独特生物学特征和临床特征有重要意义,以髓母细胞瘤的WNT亚型为例,由于其良好的疗效,临床试验中单独研究如何降低治疗强度,以保持良好的疗效,同时降低远期慢性病的发病率。
研究显示,儿童癌症的突变并非随机发生,而是与疾病类别相关。如横纹肌样肿瘤中SMARCB1的丢失、幕上室管膜瘤中RELA移位的存在、不同儿童肉瘤中特异性融合蛋白的存在等。结构变异对许多儿童癌症起着重要作用。易位导致癌基因融合或癌基因过度表达,尤其是对于白血病和肉瘤。将全基因组和外显子组测序应用于儿童癌症队列,有助于理解生殖系突变作为儿童癌症的病因。致病性生殖系突变明显与患者的癌症有关,例如,在Li-Fraumeni综合征的TP53突变。生殖系突变的频率因肿瘤类型而异,如神经母细胞瘤较低,骨肉瘤较高,且许多已鉴定的种系突变符合已知的易感综合征(如胸膜肺母细胞瘤DICER1,横纹肌样瘤和小细胞卵巢癌 SMARCB1和SMARCA4,肾上腺皮质癌和Li-Fraumeni综合征TP53,视网膜母细胞瘤RB1等)。
《2015年中国恶性肿瘤流行情况分析》显示:全国2015年新发恶性肿瘤病例约392.9万例,全国恶性肿瘤发病率为285.83/10万(男性305.47/10万,女性265.21/10万)。全国2015年恶性肿瘤死亡病例约233.8万,死亡率为170.05/10万(男性210.10/10万,女性 128.00/10万),累积死亡率(0~74岁)为11.94%。城市地区死亡率为172.61/10万,农村地区死亡率为166.79/10万。但我国儿童肿瘤的发病情况缺乏全国性统计。上海市肿瘤研究所报告2002—2004年上海全市共新诊断儿童恶性肿瘤447例,粗发病率为 112.5/100万,标化发病率为 120.3/100万。男、女性儿童恶性肿瘤发病率接近,分别为118.2/100万和122.6/100万。不同年龄组发病率不同,0~4岁组发病率最高,达148.7/100万。白血病是最常见的儿童恶性肿瘤,约占全部病例的1/3(30.9%),主要为淋巴细胞白血病(66.7%)。中枢神经系统肿瘤为第二位常见的肿瘤(21.9%),其次为淋巴瘤(9.6%)。不同性别和不同年龄别发病率不同,且瘤别分布也不同,提示儿童恶性肿瘤病因的复杂性。而据北京市肿瘤防治研究所、北京市肿瘤防治研究办公室提供的资料,1988年0~14岁小儿恶性肿瘤在北京城区的发病率男性为 85/10万,女性为 69/10万,合计为 77/10万,1990年男性为 65/10万、女性为 26/10万,合计46/10万,两个年份中均为男性发病率显著高于女性。1993年北京0~14岁小儿恶性肿瘤死亡率为31/10万。
儿童肿瘤发病与年龄密切相关,多见于出生后5年内,根据国内5所儿科医院1 805例恶性肿瘤的统计显示,1 176例(65.2%)诊断时年龄小于5岁。小婴儿以神经母细胞瘤为多,1岁以后以肾母细胞瘤和肉瘤为主,但骨肿瘤及卵巢肿瘤多见于青春期前后。颅内肿瘤在婴幼儿发病率较低。首都医科大学附属北京儿童医院2 705例小儿恶性肿瘤的统计资料显示,儿童恶性肿瘤中,以造血和网状内皮系统肿瘤最常见(35.68%),其中非霍奇金淋巴瘤和霍奇金淋巴瘤最多见,占全部肿瘤的19.26%。白血病为最常见的恶性肿瘤,但多数通过血液学检查即可诊断,病理活检诊断的只是一小部分(表2)。
表2 首都医科大学附属北京儿童医院2 705例小儿恶性肿瘤的构成比
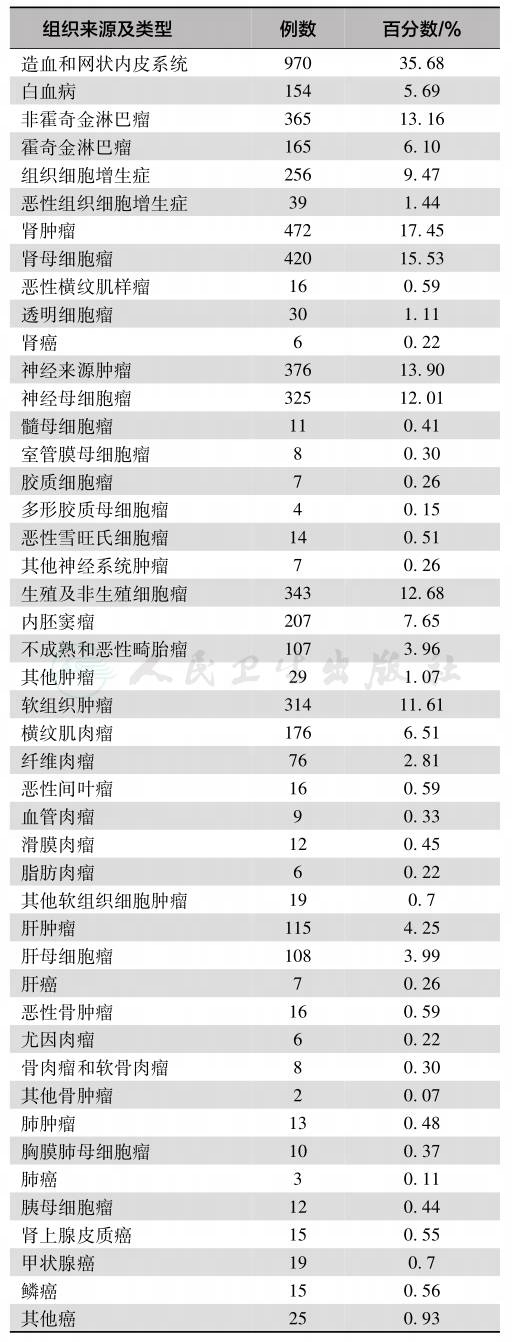
引自:北京儿童医院1955—1995经病理科检查证实诊断的病例统计(李佩娟.小儿肿瘤病理学.北京出版社,2001)。
(一)儿童恶性实体肿瘤的病理学特点
儿童恶性实体瘤的组织学形态重叠,多种肿瘤表现为缺乏明确组织分化证据的低分化或未分化小细胞肿瘤,主要有尤因肉瘤/原始神经外胚叶瘤PNET、腺泡状横纹肌肉瘤、某些胚胎性横纹肌肉瘤、促纤维增生性小圆细胞肿瘤等,淋巴造血系统恶性肿瘤(淋巴瘤、白血病)和神经母细胞瘤通常也表现为小圆细胞肿瘤。同样,多种儿童常见的肿瘤表现为梭形细胞肿瘤,包括滑膜肉瘤、先天性婴儿型纤维肉瘤、成人普通型纤维肉瘤、恶性外周神经鞘 膜 瘤 (malignantperipheralnerve sheath tumor,MPNST)、未分化梭形细胞肉瘤等。某些梭形细胞肿瘤也可能出现部分圆形细胞形态,如低分化滑膜肉瘤、黏液样脂肪肉瘤。某些圆形细胞肉瘤也可有梭形细胞结构,如尤因肉瘤,使肿瘤分型更加困难。而准确诊断和分型决定了患者正确入组、治疗和预后评估。
儿童很多肿瘤与胚胎期残余幼稚组织有关,称为各种母细胞瘤,随着生长发育可能有成熟变化趋势。包括肝母细胞瘤、肾母细胞瘤、肺母细胞瘤、视网膜母细胞瘤、神经母细胞瘤、髓母细胞瘤、骨母细胞瘤、软骨母细胞瘤等,可以是良性、中间性或恶性。除了病理组织学检查,临床信息对于正确的病理诊断有重要参考价值,如患者年龄和病变部位。根据患者年龄有不同诊断思路。小圆细胞肿瘤如果发生在1岁以内,以神经母细胞瘤多见。位于肢体末端或浅筋膜表浅部位肿瘤以良性多见,躯干、胸腹腔等中心部位肿瘤以恶性多见。来自儿童肾脏的肿瘤以肾母细胞瘤和横纹肌样瘤可能性较大。特别是在穿刺或少量活检样本标本较少的情况下,病变部位对正确诊断具有重要意义。
儿童肿瘤类型多样,不乏病理特点和发病部位不典型的肿瘤。儿童实体瘤的完整病理诊断应该包括如下信息:肿瘤类型、具体分型(亚型)、分子标记。肿瘤类型和具体分型对治疗方案选择及预后评估尤为重要。
(二)活体组织检查方法
1.切取活检
是指从病变处切取适量组织进行病理切片检查,适用病变较大、部位较深或尚未破溃的肿瘤。
2.钳取活检
适用于体表或腔道黏膜之表浅肿瘤或溃疡性肿瘤。
3.切除活检
适用于原发瘤较小或病变较浅,容易将整个病灶切除,既达到活检目的,也是治疗措施之一。
4.穿刺活检
优点为操作简单,可取较深部的组织。缺点为不能直视,有可能引起出血或转移,也可能使肿瘤沿穿刺针道播散。并且,取出的组织小,易被挤压。细针穿刺取出的组织较难保留组织结构,适用于细胞学检查。粗针穿刺取出组织稍多,能用于常规切片、免疫组化染色和分子检测等。最好在病灶内多点穿刺活检。
(三)儿童恶性实体肿瘤病理学检查方法
儿童恶性实体瘤临床病理诊断通常需要特殊染色、免疫组化、电镜、分子检测等多种方法的辅助才能确诊。
1.组织固定
常规组织学检查最常用的组织固定液是中性缓冲的甲醛溶液(甲醛终浓度4%),固定石蜡包埋组织可适用于常规组织学检查、免疫组织化学染色、FISH染色、DNA提取PCR检测等。少数分析方法需要留取未经固定的新鲜组织冻存,比如核型分析、流式细胞分析、蛋白质免疫印迹、比较基因组杂交、转录组学分析等。
2.免疫组织化学染色
甲醛溶液固定会使氨基酸残基形成醛基,多肽链在醛基的作用下发生交联,抗原决定簇可能被封闭,因此需要进行抗原修复。可采用热修复、蛋白酶消化等不同的抗原修复方法将抗原决定簇暴露。多数免疫组化抗体并不具有绝对特异性,并且受到染色技术、组织制备过程、抗体特异性、抗体来源、肿瘤异质性表达等多种因素影响,可能存在非特异着色、交叉反应、假阳性/假阴性等情况,需要根据所用抗体进行正确评判,包括有无着色、着色强度、阳性细胞类型、亚细胞定位:胞膜、胞质、胞核、核周、高尔基器、胞膜/胞质、胞质/胞核。应当设置阴性对照和阳性对照保证染色结果的可靠性。
3.儿童实体肿瘤的分子病理学检测
近些年关于肉瘤的分子遗传学研究取得极大进展,发现多种染色体易位/转位、与细胞生长分化密切相关的癌基因扩增、抑癌基因突变、DNA甲基化、染色体印迹、DNA错配修复基因缺陷、端粒酶活性等。这些遗传学改变与肿瘤发病机制密切相关,如NTRK3基因易位对婴儿型纤维肉瘤的诊断。FOXO1基因易位仅见于腺泡状横纹肌肉瘤,不存在于胚胎性横纹肌肉瘤。有些改变与肿瘤预后及治疗相关,例如神经母细胞瘤中N-MYC基因扩增。
4.临床病理诊断中常用的分子病理学检测方法
(1)染色体荧光原位杂交技术(FISH)
目前成为很多病理科的常用技术。尤因肉瘤常用EWSR1基因的分离探针,分离探针可以观察所标记基因是否发生断裂,但无法显示断裂之后发生易位的伙伴基因。FISH方法也可以通过计数荧光信号的数量反映标记基因扩增、获得/丢失情况。
(2)聚合酶链反应(PCR)
主要用于单个位点基因突变检测和易位或伴已知的融合基因检测。近年以PCR反应为基础的高通量基因测序技术可以同时对成百上千个基因序列同时进行扩增测序。
(3)单核苷酸多态性(SNP)
单核苷酸多态性(single nucleotide polymorphisms,SNP)是单个核苷酸变异引起的DNA序列多态性,成为第三代遗传标记。SNP在人群中的变异频率大于1%。发生在基因编码区或调控区的SNP与个体表型差异、疾病易感性和药物敏感性等有密切关系。对肿瘤组织进行全基因组范围的SNP芯片基因型分析可以反映基因丢失、获得全貌,类似于高通量的核型分析或比较基因组杂交方法,可用于疾病研究、疾病诊断和临床预后风险评估。
1.血液学和血清学常规检查
包括血常规、尿、粪便常规、电解质、肝肾功能、血清钙磷和尿酸水平。
2.胸腹水、脑脊液及其他体液的细胞学检查
脑脊液检查为白血病、淋巴瘤和中枢肿瘤治疗前的常规检查,是确定有无中枢神经系统受累最好的诊断方法。有胸腔或腹腔积液时,也应进行胸腹水的检查以明确肿瘤的性质。
肿瘤生物因子(特殊标记物)检查:主要应用免疫化学方法。目前主要有临床价值的是甲胎蛋白(alpha fetoprotein,AFP)。它开始产生于6周胎龄,至12周时达最高峰,出生后1周迅速下降,用一般免疫学方法已不能测出,一般在生后2个月降到成人水平(<25ng/ml)。原发性肝细胞癌患儿约80%AFP阳性。睾丸和卵巢的恶性畸胎瘤约半数AFP阳性。而卵黄囊瘤则多伴AFP增高,经治疗后原已下降的AFP又复增高时,说明有肿瘤复发或转移。其他还包括血清乳酸脱氢酶(lactate dehydrogenase,LDH),是一种非特异肿瘤标志物,对预后有判断价值。神经元特异性烯醇化酶(neurone specific enolase,NSE),也是神经母细胞瘤的重要标志物之一,但特异性不高。另外,小儿常见的交感神经源类肿瘤如神经母细胞瘤,可有儿茶酚胺增高,可查尿内最终代谢产物,最常见的是香草杏仁酸(vanillylmandelic acid,VMA)增高,少数病例高香草酸(homovanillic acid,HVA)增高,或两者均增高。VMA可协助诊断神经母细胞瘤,并用以监测对治疗的反应。
3.骨髓常规和病理检查
骨髓常规是诊断白血病的主要依据。神经母细胞瘤在骨髓腔的瘤细胞浸润常出现在骨质有可见的X线影像变化之前。故也为诊断实体瘤骨髓转移的重要手段,但由于肿瘤转移呈区域性,故容易漏诊。最好选择瘤灶就近的部位进行(如腹腔瘤灶选择髂后)。骨髓病理检查可以弥补骨髓常规检查的不足,进一步确定是否存在骨髓侵犯,包括形态学和免疫组化(图2,表4)。
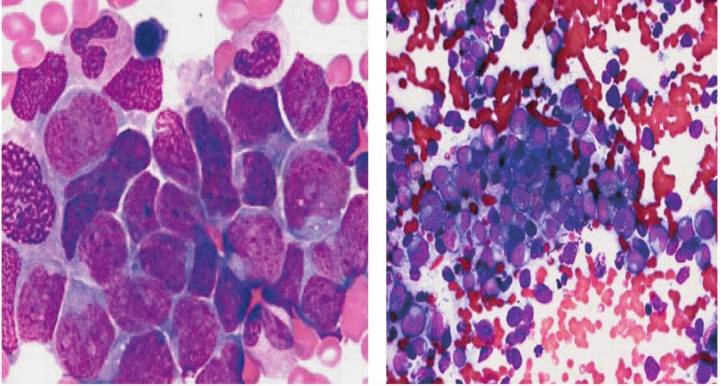
图2 神经母细胞瘤骨髓侵犯,骨髓常规涂片可见菊花团样肿瘤细胞
表4 常用的儿童恶性肿瘤检查方法以评估原发肿瘤及潜在的转移肿瘤
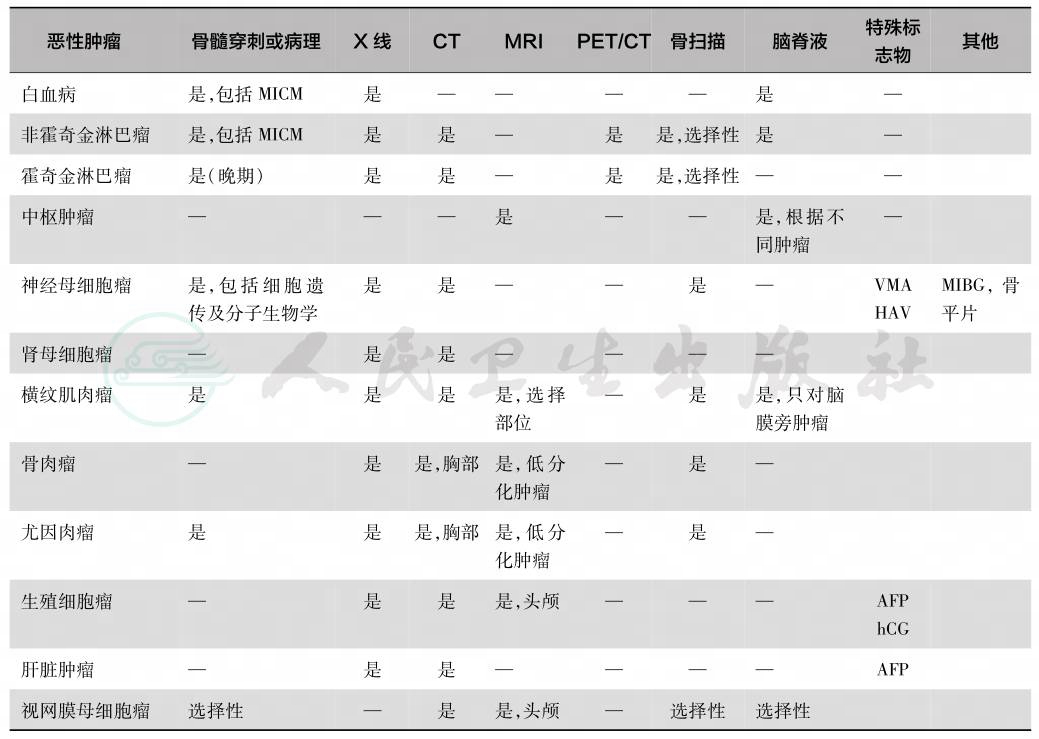
注:MICM:morphology immunophenotype cytogenetics molecular biology,即形态学-免疫学-细胞遗传学-分子生物学;hCG:human chorionic gonadotropin,人绒毛膜促性腺激素;AFP:alpha fetoprotein,甲胎蛋白:VMA,vanillylmandelic acid,香草杏仁酸。
国际公认的儿童肿瘤标准治疗策略为“保护器官、切除肿瘤、配合化疗”。良性肿瘤及瘤样病变以手术治疗为主,而恶性肿瘤则采取手术、放射治疗及化学治疗的综合措施,临床需要肿瘤内、外科、放疗科以及影像、病理等多学科联合诊治。
(一)多学科联合诊治模式(multimodal,multisciplinary myapproach)
是指多个儿童肿瘤治疗专业参与诊断、治疗和管理。包括主要治疗和辅助治疗(图6)。化疗、手术、放疗和生物治疗是最重要的治疗方法。通常单一治疗效果差,至少有两种手段联合应用。儿童白血病通常以化疗为主,少部分患者接受颅脑放疗,以预防中枢神经系统白血病(central nervous system leukemia,CNSL)。
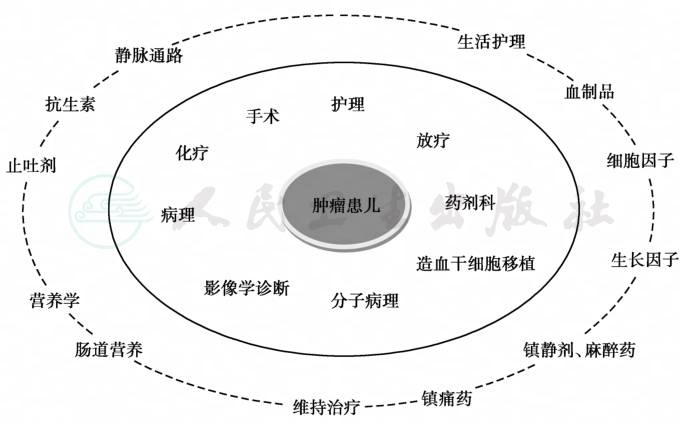
图6 儿童肿瘤的多学科诊治和管理模式图
儿童非霍奇金淋巴瘤(non-Hodgkin lymphoma)伴有中枢神经系统受累者,在化疗的同时也需放射治疗。放疗和手术治疗是大多数儿童实体瘤包括霍奇金淋巴瘤局部治疗的重要手段。为提高儿童肿瘤的治愈率,临床需要肿瘤内科管理下的,包括外科、放疗科、移植科以及影像、病理等多学科的参与,进行规范化的诊治。
生物免疫治疗已经成为一些儿童肿瘤的重要手段。如视黄酸(retinoic acid)治疗急性早幼粒细胞白血病(acute promyelocytic leukemia),单克隆抗体(monoclonal antibody)用于神经母细胞瘤和一些类型的非霍奇金淋巴瘤的治疗,伊马替尼(imatinib mesylate)治疗费城染色体阳性的慢性粒细胞白血病(chronic myelogenous Philadelphia chromosome-positive leukemia),以及 MIBG 治疗神经母细胞瘤。
儿童处于生长发育期,可能出现化疗药物及放疗对机体器官的损伤,造成生长发育障碍及远期的脏器功能不良,因此,儿童肿瘤在整个治疗过程中应长期随访。目前越来越多的儿童肿瘤患者可以采用输液泵、口服化疗药物、强化疗后尽早出院在门诊给予支持治疗和家庭护理等。只要有可能,儿童在整个门诊治疗过程中,可以像正常儿童一样在家和学校生活。如果有些患儿为了治疗的需要,在诊断和治疗的第1年无法上学,尽可能保留学籍,帮助和鼓励他们完成学业。
(二)手术治疗
手术切除治疗小儿肿瘤,不受年龄限制。经过准备的小儿只要保证手术时循环血量充足,一般对手术耐受良好。对易继发感染的淋巴管瘤,有恶性变可能的畸胎瘤以及肿块生长过大易产生压迫腔道或增加手术操作困难等良性肿瘤,均应尽早手术切除。而对早期局限性恶性肿瘤,则应视为紧急手术。相反,对于体积小,生长慢,不造成任何症状的良性肿瘤,可以定期检查,不必急于手术。
一般说来,患儿年龄越大,手术越安全。小儿肿瘤在手术完全切除的基础上(Ⅰ期或Ⅱ期)加用连续全身化疗效果最好。对于巨大、侵犯周围组织器官或大血管而不能一次性手术切除干净的肿瘤(如Ⅲ期),应暂不手术,给予2~3个月的术前化疗。术前化疗可使肿瘤的体积减小、血供障碍、包膜增厚,还可使肿瘤与正常组织界限变得清楚,降低肿瘤破裂转移的概率,有利于手术完整切除。
为保障肿瘤患儿、患儿监护人或近亲属、授权委托人合法权益,主管医护人员应向患儿监护人或近亲属、授权委托人说明病情及治疗方式、特殊治疗及处置并获得其同意,说明内容应有记录。开展试验性临床医疗应严格遵守国家法律、法规及部门规章制度,有审核管理程序并征得患儿监护人或近亲属、授权委托人的书面同意。保护患儿的隐私权,尊重民族习惯和宗教信仰。
(三)放射治疗
放疗一直是小儿实体肿瘤综合治疗的常用手段之一。放疗也存在明确的近期和远期不良反应,并可影响长期生存者的生活质量,尤其影响骨骼生长、性腺功能和智力发育等,使其在儿科的应用一直受到限制和争议。因此,只有在明确放疗能改善其预后或利大于弊的条件下才能采用。
放疗可单独用于治疗颅内肿瘤,表浅血管瘤等,也可作为手术的辅助治疗,如对于肾母细胞瘤、神经母细胞瘤、横纹肌肉瘤等,一般用于术后治疗。对于巨大肿瘤,与化疗并用,使肿瘤缩小,可增加手术切除的可能性。放疗与化疗并用治疗恶性淋巴瘤及一些转移瘤,也可提高疗效。对1岁以下小儿的恶性肿瘤,放疗剂量较难控制,应谨慎使用。
在临床上,小儿对放疗的耐受量相对较大,但实际上由于控制部位及深度和范围都有困难,因此,放疗对小儿的损害却比成人严重,特别是远期影响。近年来,由于应用高能放射线如钴-60(Co60)、β线后,骨吸收量少,可减少骨骼的发育障碍。虽然小儿全身反应如食欲缺乏、恶心、呕吐较成人轻,但照射过程中,需注意照顾小儿饮食,每周应测体重。照射野广泛则易产生骨髓抑制现象,故在治疗过程中,每周需查血象1~2次。
(四)化疗
对化疗敏感的肿瘤,除白血病外,尚有恶性淋巴瘤、神经母细胞瘤、肾母细胞瘤、横纹肌肉瘤、胚胎性癌、肝母细胞瘤、恶性畸胎瘤、未分化癌、视网膜母细胞瘤及脑的髓母细胞瘤和松果体恶性肿瘤等。未确诊为恶性肿瘤的不宜应用化疗;凡有手术指征的,也不应单纯用化学治疗。
1.化疗原则
个体化化疗:同一种肿瘤有不同的病理形态或免疫、细胞遗传学亚型,化疗敏感性不同。诊断时处于不同的疾病阶段,需接受不同强度的治疗。联合用药:3~5种药物联合化疗不仅能够提高完全缓解率和获得长期缓解,还可以克服副作用和单一化疗药物的耐药性。
2.常见化疗药物分类
常用于小儿的抗癌化学治疗药物及其作用机制(表5)。
(1)烷化剂类
1)环磷酰胺(cyclophosphamide,CTX):本品静脉注射300~1 000mg/m2。可用于治疗各种恶性实体瘤、淋巴瘤及白血病,也是横纹肌肉瘤、肾母细胞瘤和神经母细胞瘤的一线化疗药物。
表5 儿童常用化疗药物
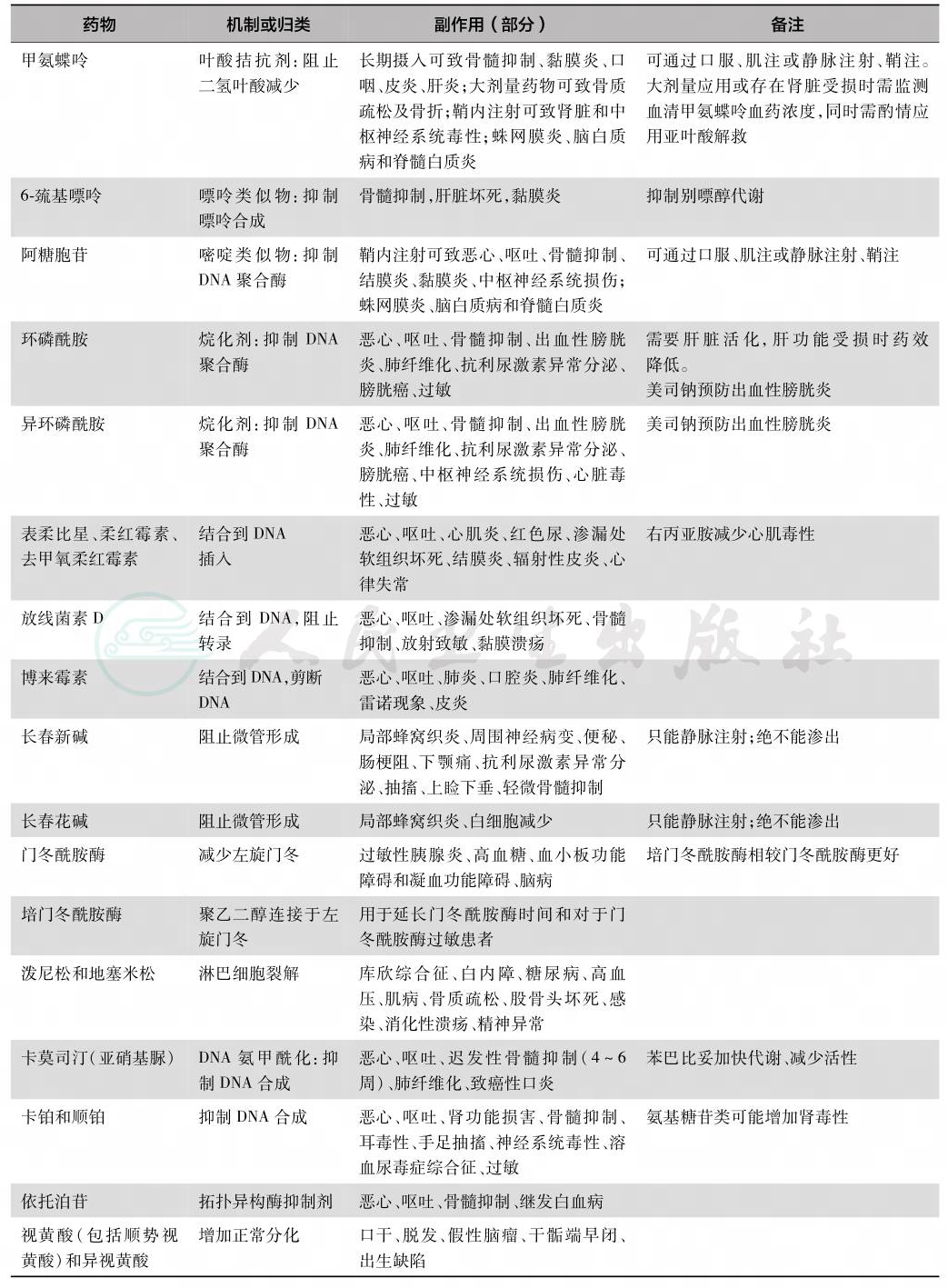
2)异环磷酰胺(ifosfamide,IFO)为CTX的同分异构体,静脉注射800~3 000mg/m2可用于治疗急性淋巴细胞白血病、非霍奇金淋巴瘤、霍奇金淋巴瘤、软组织肿瘤、尤因肉瘤。
(2)抗生素类
1)放线菌素D(dactinomycin D)
静脉注射12μg/(kg·d),或 15μg/(kg·d)。用于治疗肾母细胞瘤、各种肉瘤。
2)多柔比星(adriamycin,doxorubicin)
静脉注射每3~4周40~50mg/m2,由静脉1次注入或分为2~3天注入,累积量不可超360mg/m2(大于18岁者,累积剂量最大可达550mg/m2)。用于急性白血病、淋巴瘤、肾母细胞瘤、神经母细胞瘤、骨肉瘤、卵巢或甲状腺瘤、尤因肉瘤、横纹肌肉瘤和其他软组织肉瘤。如总剂量超过最大累积剂量,较易发生心肌损害(坏死),甚至可致死。心脏功能不全者忌用多柔比星。对曾因肺转移瘤接受胸部放疗的患儿可促使心脏损害的发生。
3)博来霉素(bleomycin)
非霍奇金淋巴瘤、霍奇金淋巴瘤、恶性生殖细胞瘤。
(3)植物碱类
1)长春新碱(vincristine)
静脉注射,每周 1次,1.5~2mg/m2,连续6~10周,然后根据各种肿瘤的治疗方案每隔1~2周1次。每次极量是2mg。用于急性白血病、淋巴瘤、横纹肌肉瘤、肾母细胞瘤、神经母细胞瘤、尤因肉瘤、视网膜母细胞瘤、肝母细胞瘤、骨肉瘤和中枢肿瘤等。
2)长春花碱
非霍奇金淋巴瘤、霍奇金淋巴瘤等。
(4)抗代谢药物
1)甲氨蝶呤(methotrexate,MTX)
口服或肌注每次15~20mg/m2,每周1~2次,患中枢神经系统白血病时,做蛛网膜下腔注射12~15mg/m2,每周1次。用于淋巴细胞白血病、中枢神经系统白血病、淋巴瘤、中枢肿瘤。
2)5-氟尿嘧啶(5-fluorouracil,5-FU)
静脉注射 12~15mg/(kg·d),连用5天。用于肝癌和肝母细胞瘤。
3)丙卡巴肼(procarbazine)
用于缓解诱导,开始时口服25~50mg/(m2·d),以后渐增至 100mg/(m2·d),服 7天停7天为一疗程。目前只用于霍奇金淋巴瘤。
4)6-巯嘌呤(6-mercaptopurine,6-MP)
口服 50~60mg/(m2·d)。用于急性淋巴细胞白血病,是急性白血病维持治疗的首选药物。
5)阿糖胞苷(cytarabine,cytosine arabinoside)
静脉注射或肌注100mg/(m2·d),每周注射5天。用于急性淋巴细胞白血病、急性髓细胞白血病、非霍奇金淋巴瘤、霍奇金淋巴瘤。也可用于中枢神经系统白血病做蛛网膜下腔注射,每次 30~50mg/m2。
(5)激素类
1)泼尼松(prednisone,PRED)
口服 40~60mg/(m2·d),分 2~3 次。
2)地塞米松(dexamethasone,Dex)
6~10mg/(m2·d),每日分2~3次,口服或静脉给予。用于白血病、淋巴瘤、转移瘤所致骨痛和中枢神经系肿瘤,可增进食欲,但亦可致钠潴留和高血压及骨质疏松。因此,口服激素2周以上者,需同时服用钙剂和维生素D。
(6)其他
1)左旋门冬酰胺酶(L-Asparaginase,L-Asp)或培门冬酰胺酶(pegaspargase,PEG)
用于急性淋巴细胞白血病的治疗。
2)卡铂和顺铂
骨肉瘤、神经母细胞瘤、中枢神经系统肿瘤、生殖细胞瘤等实体肿瘤。
3)依托泊苷
急性淋巴细胞白血病、非霍奇金淋巴瘤、生殖细胞瘤。
4)视黄酸(包括顺势视黄酸)和异视黄酸
急性早幼粒白血病、神经母细胞瘤。
常见肿瘤急症主要为肿瘤压迫、肿瘤破裂和肿瘤溶解所致的电解质功能紊乱、弥散性血管内凝血(DIC)等(表7)。
表7 肿瘤的急症
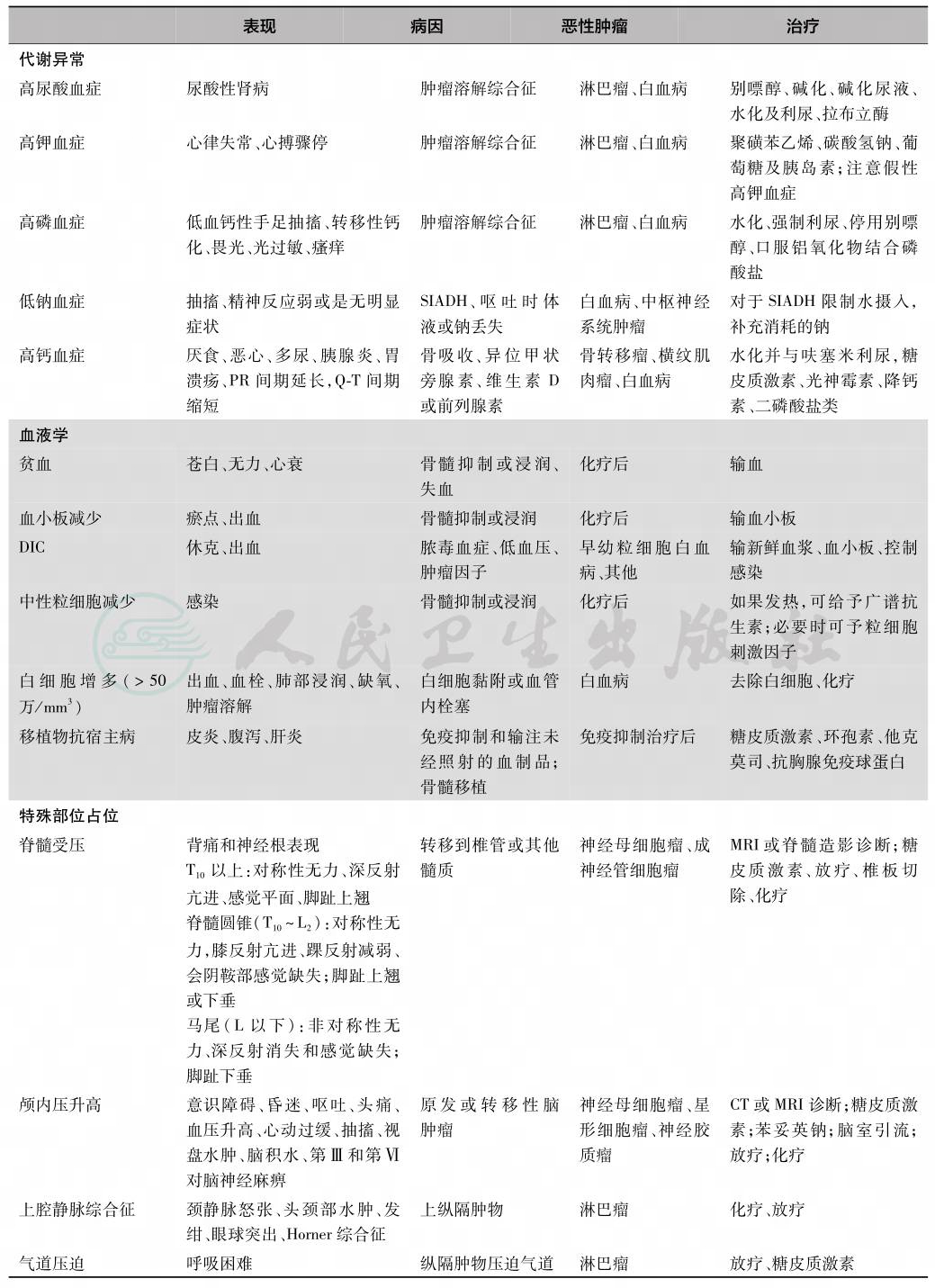
1.呼吸道梗阻
原因是气道受压和纵隔侵犯,治疗措施为变换体位,保持通气;必要时气管插管,机械通气;应用小剂量化疗减积、局部放疗等。
2.肿瘤溶解综合征
强化疗作用下,尤其是第一疗程,大量肿瘤细胞溶解坏死,引起高尿酸血症,高磷酸血症的低钙血症,尿酸结晶堵塞肾小管导致急性肾功能衰竭。治疗原则是水化、碱化尿液,利尿,别嘌醇口服。
3.急腹症
很多实体瘤原发于腹腔内,以消化道症状和急腹症表现为主,常出现上下消化道出血,机械性肠梗阻,粘连性梗阻,胃肠道继发感染,套叠或肠穿孔。治疗措施为对症和外科急诊手术。
4.肿瘤破裂
儿童实体肿瘤,如肝母细胞瘤、神经母细胞瘤伴有巨大肿瘤,侵犯局部血管,可发生肿瘤破裂,临床表现为贫血加重,腹痛等。治疗措施为严格保静,避免有创操作,对症止血,输注血制品等。













