英文名称 :adolescent idiopathic scliosis
特发性脊柱侧凸(idiopathic scoliosis,IS)是骨骼肌肉系统疾病最常见的脊柱畸形。早期无特殊临床症状,随着畸形进展,侧凸会引起身体外观改变,继而导致功能障碍等,可影响患者自尊心,降低生存质量与幸福感。当侧凸进展到一定角度,成人期健康风险显著增加。因此,需要在生长发育时期实施早期干预以预防侧凸进展。早期规范的康复治疗可以有效控制脊柱侧凸的进展,改善姿势不对称与外观畸形,避免手术治疗,降低致残率。
目前关于AIS病因学存在许多假说,包括遗传、骨骼发育异常、内分泌及代谢系统异常、中枢神经系统异常以及结缔组织异常等。近年来对AIS的病因研究取得了不少进展,有些假说获得支持,也有部分假说被认为可能是继发现象。
1.遗传因素
关于AIS的遗传模式,早期有研究认为AIS可能是常染色体显性遗传或X连锁遗传,亦有学者认为是多基因遗传,并且在X染色体上有某个易感位点。目前对AIS发病的相关基因定位采用的方法包括连锁分析和关联分析。
2.骨骼系统发育异常
(1)生长发育及软骨内成骨异常:AIS发生于青春期,且其畸形加重与脊柱生长明确相关,提示生长发育在AIS的发生发展中有重要价值。Guo用 MRI测量比较正常和AIS患者椎体的高度,在矢状面上发现AIS患者的椎体明显高于正常对照,因此认为AIS患者的软骨内成骨较快。邱勇在对AIS和先天性脊柱侧凸(congenital scoliosis,CS)椎体生长板的组织计量学研究后亦发现前者的增殖活性较后者高,支持AIS患者的软骨内成骨活跃。
表1 脊柱侧凸的病因学分类

(本表参考:Newton PO,Wenger DR.Idiopathic Scoliosis.In:Morrissy RT,Weinstein SL,eds.Lovell and Winter’s Pediatric Orthopaedics(6th Edition). Philadephia:Lippincott Williams & Wilkins;2006:694-762.
(2)骨密度(bone mineral density,BMD)降低:除了AIS的人体测量学之外,大量研究发现AIS患者存在全身性的骨量减低,且这种状况一直从青春期持续到成年期。近年来,郑振耀和邱勇等在AIS与骨量减低相关性的研究中做了大量工作。Cheng等发现68%的AIS组患者存在显著BMD降低,且这种低BMD与AIS的弯曲程度及弯曲类型无关。吴洁等运用DEXA法检测了中国大陆101名AIS患者的BMD,并与同龄对照组青少年相比,也得出类似的结论。此外,朱锋等通过microCT观察AIS患者骨小梁的超微结构,在三维空间揭示了AIS患者存在髂骨的微结构异常:骨容积比减小、骨小梁变细和骨小梁间距离增大。该研究在证实AIS患者存在低BMD的同时,进一步深化了对AIS患者三维空间骨小梁微结构的认识。
3.内分泌及代谢调节系统异常
(1)瘦素(Leptin):在青春期前后这个特定的生长发育时期,瘦素对女孩的生长发育起着至关重要的作用。邱勇课题组的研究结果表明AIS女性患者外周血瘦素生物利用度明显低于同龄健康女孩,这一结果提示,降低的外周血瘦素生物利用度可能是联系降低的体质量和降低的骨量之间关系的重要因素,可能在AIS患者发生发展中起重要作用。Burwell等提出AIS发病机制可能与瘦素-下丘脑-交感神经系统(sympathetic nervous system,SNS)功能紊乱密切相关,并认为AIS女孩下丘脑可能存在功能异常,下丘脑瘦素受体对瘦素敏感性增高,循环瘦素通过下丘脑反射性增加SNS活性,调节相应的神经内分泌机制,导致青春期AIS患者生长速度加快,全身骨量减少、体重及低BMI。
(2)褪黑素(Melatonin):Machida等最早报道切除雏鸡松果体可以在动物身上建立脊柱侧凸模型,其后许多学者成功重复该实验,并发现该方法还可以在大西洋鲑鱼及切除双前肢的站立鼠上建立脊柱侧凸。其他方式导致的褪黑素降低亦可建立脊柱侧凸动物模型,且在三维结构上与AIS的结构有很大的相似之处,提示松果体分泌的褪黑素降低是建立动物脊柱侧凸模型的关键。Moreau等对AIS患者的成骨细胞中的褪黑素信号通路进行研究后发现其信号通路存在异常。许多细胞水平的研究均表明褪黑素可以抑制破骨细胞的作用,并且可以促进成骨细胞的作用。
(3)钙调蛋白(Calmodulin,CaM):Yarom等发现AIS患者椎旁肌细胞内钙离子浓度上升并伴有肌球蛋白的变性。这些异常可能是由于CaM控制的钙离子内稳态失衡所致。尽管早期研究显示,CaM含量与侧凸严重程度相关,但Lowe等随访研究发现,CaM含量与侧凸进展相关,进展型侧凸的血小板CaM含量明显增加,而当侧凸稳定后即使Cobb角较大,其CaM含量仍与正常对照组无明显差异,不支持CaM与AIS的发病有关。
4.中枢神经系统功能异常
对AIS的神经传导功能进行检查,发现有11.6%~27.6%的患者存在异常,提示AIS患者的中枢神经系统功能可能存在异常。Chu等发现AIS患者的脊髓长度与前柱高度比明显小于正常对照;该作者还发现随着比值降低,其顶椎横断面上的脊髓由椭圆形向圆形改变并向凹侧偏移,并且小脑扁桃体的位置下降而圆锥位置无明显变化,但这些变化与AIS的神经传导功能无明显的相关性,提示脊髓的这些变化可能不是导致AIS患者神经传导功能改变的原因。
5.结缔组织异常
近年来国内多位学者对AIS侧凸顶椎或端椎凹、凸侧的椎间盘进行了比较。朱锋等发现AIS患者椎间盘凹侧Ⅰ、Ⅱ型胶原mRNA的表达均低于凸侧,且较CS患者相应部位低,这一结果表明AIS患者椎间盘存在着基质合成代谢的异常,不能产生足够的正常Ⅰ、Ⅱ型胶原来维持椎间盘的生物力学功能,使得脊柱在正常的应力或轻微的非正常负荷下出现畸形。该课题组还发现胸椎侧凸顶椎椎间盘凹侧纤维环的Ⅱ型胶原明显低于腰椎侧凸顶椎相应部位,与正常分布不符。
虽然对AIS病因学的研究已经持续了100多年,但直到今天AIS的病因仍然不明。AIS只是一个临床诊断,可能存在多种病因,上述任一假说都可能是一部分AIS的发病原因。目前大多数学者的观点倾向于AIS的发病是多因素综合作用的结果。
特发性脊柱侧凸占脊柱侧凸发病总数的80%。国外特发性脊柱侧凸患病率约为2%~3%,我国患病率约为1.02%~5.14%。
特发性脊柱侧凸可发生在儿童青少年任一时期,最常见于快速生长发育时期,如生后1个月、6~24个月龄、5~8岁、11~14岁是身高发育高峰期,也是生长发育成熟的关键时期,因此脊柱发生弯曲最常发生在青春期初期。不同年龄、不同性别、不同纬度,特发性脊柱侧凸患病率不相同:①10~13岁时,脊柱侧凸患病率最高;②不同角度存在性别差异,Cobb角10°~20°时,男女患病率比例为 1∶1.3;Cobb 角 20°~30°增加至 1∶5.4,Cobb 角 >30°高达 1∶7;③北纬30°、初潮年龄较晚的女性更易发生脊柱侧凸;④青少年时期,女性患者较男性更容易发生进展;⑤特发性脊柱侧凸有家族聚集性,X染色体上可能存在家族脊柱侧凸表达基因,尤其对双胞胎家庭和单个多基因家族的影响更大:一级亲属患病率为11%,二级亲属患病率为2.4%,三级亲属患病率为1.4%。单卵双胞胎和异卵双胞胎的共患率分别为73%和36%。
特发性脊柱侧凸临床分型多样,可根据发病年龄、侧弯部位、严重程度等分型。临床上不同治疗方案有不同的分型,如Ponseti分型主要是用于保守治疗分型和术前分型,King分型、Lenke分型、PUMC(协和分型)为手术治疗常用分型,Rigo分型为色努支具制作专用分型。
(一)按发病年龄分型
根据侧凸发病年龄分型,可分为婴儿型、儿童型、青少年型、成人型特发性脊柱侧凸:①婴儿型特发性脊柱侧凸,发病年龄在2岁11个月龄以下,多见于男性,以胸段和胸腰段为主,常见于左侧弯,绝大部分患者在出生后6个月内进展,双胸弯易进展并发展为严重畸形,常常伴发先天性畸形,如扁头畸形、蝙蝠耳畸形、先天性斜颈以及进行性髋关节发育不良等;②儿童型,发病年龄在3岁~9岁11个月龄,多见女性,男女比例为1∶2~1∶4,多见右侧胸弯和双主弯,70%患者可进展为严重畸形,损害肺功能;③青少年型,发病年龄10岁~17岁11个月龄,多见女性,自然史相对较好;④成人型,发病年龄18岁以上,通常由青少年型特发性脊柱侧凸患者在成年期进一步发展,以及脊柱逐渐退变(磨损和撕裂)在成年期以后出现的脊柱侧凸畸形。
(二)按侧弯部位分型
根据侧弯部位分型,可分为主胸弯、主腰弯、胸腰弯、胸腰双弯、颈胸弯特发性脊柱侧凸:①主胸弯型,端椎通常位于T6~T11,顶椎位于T8/T9,常见右侧凸;②主腰弯型,端椎通常位于T11~L3,顶椎位于L1/L2,常见左侧凸;③胸腰弯型,端椎通常位于T6/T7~L1/L2,顶椎位于T11/T12,常见右侧凸;④胸腰双弯,端椎通常位于T6/T7~T10(胸部)、T11~L4/T5(腰部),顶椎位于T8/T9(胸部)、L4(腰部),常见胸右侧凸、腰左侧凸;⑤颈胸型,端椎通常位于C7/T1~T4/T5,顶椎位于T3,常见左侧凸。
(三)按严重程度分型
根据侧凸严重程度分型,可分为轻度、中度、重度、极重度特发性脊柱侧凸:①轻度,Cobb 角11°~20°;②中度,Cobb 角21°~35°;③中-重度,Cobb角36°~40°;④重度,Cobb角41°~50°;⑤重 -极重度,Cobb 角 51°~55°;⑥极重度,Cobb 角 56°以上。
1.脊椎
伴随脊柱侧凸可发生一系列的脊柱解剖学改变(图1):顶椎椎体楔形变伴旋转、凹侧椎弓根变短变窄、椎管变形、终板早期退变钙化,严重的AIS或AIS进入成年期后,在顶椎区可发生关节突的退变,尤其以凹侧为甚。一般认为这是发生脊柱侧凸后的继发性改变。

图1 脊柱侧凸顶椎出现明显的楔形变伴旋转
2.椎间盘
椎间盘以形态学改变为主,即凹侧椎间隙窄,凸侧椎间隙宽。进入成年期后,椎间盘即可逐渐出现退变,特别是脊柱侧凸的下交界区或双弯型脊柱侧凸的两个弯曲交界区。而顶椎区由于关节突退变增生甚至融合,使顶椎区椎间盘受力减少,因而椎间盘退变反而较轻。
3.椎旁肌
AIS凹凸侧椎旁肌不同,凸侧椎旁肌较薄,肌纤维较松散,而凹侧椎旁肌较厚,肌肉挛缩而紧张。
4.肋骨及胸廓的改变
胸廓畸形为脊柱侧凸伴随的常见畸形,发生原理是由于脊柱旋转和脊柱侧凸导致凸侧肋骨变形,相互分开、向后突出,而凹侧肋骨相互拥挤在一起、水平走向,并向前突出。总体造成胸廓旋转变形侧移,形成剃刀背畸形和前胸壁畸形(图2)。

图2 特发性胸椎侧凸,弧度均匀,CT三维重建示无脊椎形成障碍及分节不良,无肋骨发育畸形;凸侧肋骨相互分开、向后突出,而凹侧肋骨相互拥挤在一起、并向前突出,造成胸廓旋转变形及侧移,形成剃刀背畸形和前胸壁畸形。(A、B)
5.心肺功能影响
胸弯型AIS的侧凸畸形可造成不同程度的胸廓畸形和胸腔容积下降,一般只有轻度的限制性通气功能障碍,不至严重影响心肺功能。少数严重进展的AIS(胸弯>100°)或前凸型脊柱侧凸可严重影响肺的膨胀运动,甚至在局部发生肺不张,用力肺活量(forced vital capacity)通常下降到预期值的70%~80%,可严重影响患者生活质量。患者早期有可能死于肺心病(cor pulmonale)。文献报道严重侧弯患者的死亡率是一般人群的2倍,吸烟则增加肺心病相关的死亡风险。
1.非手术治疗
一般认为不是所有的脊柱侧凸都会进展,也不是所有的脊柱侧凸都需治疗;但当患者已发育成熟,其脊柱侧凸不一定都停止进展。对于围青春期的AIS患儿,早期对其进行干预治疗,有可能较好地改善患者的脊柱畸形。大部分患儿需要观察随访及适当的非手术治疗,但仍有部分脊柱侧凸需行手术治疗。脊柱侧凸的治疗目的在于:矫正畸形;获得稳定;维持或重建平衡。治疗方法包括观察、非手术治疗和手术治疗。
具体治疗原则如下:
(1)侧凸Cobb角<25°:应严格观察,如每年进展>5°并且Cobb角>25°,应行支具治疗;如Cobb角为20°,但伴脊椎Ⅱ度旋转,也应支具治疗。
(2)Cobb角在25°~40°的脊柱侧凸:应行支具治疗,如每年进展>5°且>40°可采取手术治疗。
(3)Cobb角40°~50°:由于侧凸>40°,进展的概率较大,因此如果患者发育未成熟,应建议其手术治疗。对于发育成熟的患者,如果随访发现侧凸有明显进展,且>50°,也应手术治疗。
(4)Cobb角>50°:手术治疗。
非手术治疗的目的是控制侧凸,使侧凸不会进一步进展,改善外观,避免因侧凸加重而接受手术治疗。目前对于AIS 的非手术治疗包括锻炼、脊柱按摩、表面电刺激及支具治疗。经过漫长的实践和研究发现,对于早期发现的轻中度AIS,支具治疗是唯一可单独使用而有效的非手术疗法。国际脊柱侧凸研究学会(Scoliosis Research Society,SRS)对AIS支具治疗的纳入标准进行了统一,具体适应证如下:年龄≥10 岁;Risser 征0~2 级;原发弯Cobb角20°~40°,并且之前未接受任何治疗;对于女性患者,月经未至或月经已至但不满1年。总体来说骨骼未成熟的柔韧性较好的轻中度特发性脊柱侧凸患儿宜行支具治疗,结构性侧凸超过40°时,不宜支具治疗。在国内支具治疗的适应证一般适当放宽,Risser征3级的未成熟患儿也可行支具治疗。对于合并胸前凸的脊柱侧凸,接受支具治疗能加重脊柱前凸畸形,使胸腔前后径进一步减小,因而不宜行支具治疗。
目前临床应用较广泛的支具包括Milwaukee支具(Cervical-Thoraco-Lumbar-Sacral Orthosis,CTLSO)和Boston支具(Thoraco-Lumbar-Sacral Orthosis,TLSO)(图11)。Milwaukee支具由轻型的塑料加三条金属片连接,上方形成颈圈,顶住枕后及下颌;下方为紧贴骨盆的塑料壳,侧方有带,能提供横向加力。一般用于顶椎在胸七以上的胸段侧凸。该支具在纵轴方向的牵引力一半以上由枕后产生,仰卧时更明显。一般认为该支具能防止侧凸加重,改善患儿的外观。Boston支具(腋下型支具)是一种上方在腋下,下方贴附于骨盆之上的一种带状支具。侧方的加压带能根据患儿的特点,进行收紧扣实,提供侧方加压力,使脊柱变直,适用于顶椎位于第七胸椎以下的脊柱侧凸。40°以下弹性较好的腰段或胸腰段侧凸,Boston支具效果最佳(图12)。其他支具还包括Charleston夜间支具和Spincor等。Charleston夜间支具对侧凸有较大的矫正力,但戴上此支具病人不能行走,所以只能夜间佩戴。Spincor则由附于骨盆的塑料外壳,棉制外套,固定带和可调节带组成,构成一个能动的矫形带,从而提供动态矫正脊柱侧凸的过程。该支具穿戴隐蔽,不影响形象,较易为患儿接受。近期结果显示对30度以内成熟儿疗效较好,远期效果还需要更长期的随访研究。

图11 患者佩戴Milwaukee支具正位及侧位观(A,B);患者佩戴Boston支具正位及侧位观(C,D)

图12 女,初诊年龄7.88岁,初诊Cobb角TL31°,先行Boston后改为Milwaukee支具治疗,图②-⑧分别为7.88岁、8.46岁、9.44岁、9.95岁、10.45岁、11.05岁、11.62岁及12.18岁时的随访X线片;末次随访12.7岁,月经初潮后2.5年,Risser4级,末次随访Cobb角TL15°,支具治疗成功

图12(续)
2.手术治疗
随着脊柱三维矫形理论的提出与推广,各种新型内固定器械的出现,脊柱侧凸手术成功率大大提高。但脊柱侧凸矫形手术的目的不是最大限度Cobb角的矫正,而是使脊柱获得最大可能的平衡,要使原来不平衡的脊柱建立新的平衡,同时不能破坏平衡和制造新的不平衡。因此AIS合理的、个体化的手术策略的制订需要解决以下几个问题:评估可矫正度;如何选择手术入路;术中监测;临床分型和融合策略。
(1)评估可矫正度:脊柱侧凸的可矫正度是影响手术方法和矫形疗效的重要因素,但提高侧凸的矫正率并非治疗的最终目的,在达到侧凸有限矫正的同时,保持躯干的力学平衡显得更为重要。特发性脊柱侧凸的可矫正度主要受限于脊柱侧凸类型、畸形程度和脊柱柔韧性,但同时还与矫正方法和手术医师对手术技术掌握的熟练程度有关。一般轻中度单弯患者,采用全节段椎弓根螺钉内固定进行三维矫正,其矫正率可达到70%~80%甚至更高;而脊柱柔韧性较差的重度脊柱侧凸患者,即使采用多棒分节段三维矫形或前后路分期矫形治疗或全脊椎截骨技术,矫正率也很难超过60%。另外年龄越大病程越长的患者,脊髓对牵拉刺激的耐受性越差,神经损伤的风险增加,限制了畸形的矫正度。对于翻修手术的患者,既往的内固定和植骨融合使畸形更僵硬,脊柱及其周围组织的解剖结构紊乱不清,二次手术时矫正更困难,且神经、血管损伤概率增加。
术前的心肺功能状态也可影响脊柱侧凸的可矫正度。中重度脊柱侧凸均有不同程度的限制性通气功能下降,表现为呼吸效率和肺活量下降,心肺储备功能较差,对麻醉和手术创伤打击的耐受性明显降低,直接影响脊柱侧凸的矫正效果。术前针对性心肺功能锻炼,如跑步、爬楼梯、吹气球等,能提高心肺的储备能力,增加对手术创伤的耐受性,可直接降低并发症的发生率、间接提高脊柱畸形的矫正度。
(2)手术入路:根据手术入路,脊柱侧凸的矫形手术分为:前路矫形,后路矫形和前后路联合或分期矫形。
1)后路脊柱矫形融合术:后路手术是最常用的脊柱侧凸矫形手术,现已成为脊柱侧凸矫形手术的金标准。理论上各种需要手术治疗的脊柱侧凸都可以通过后路三维节段性内固定进行矫形。传统的观念认为对于胸段柔软的Cobb角小于90°的脊柱侧凸可行单纯后路矫形内固定,而对于角度大于90°的病人则根据畸形僵硬程度、肺功能等决定是否先行前路松解。后路多节段V形截骨术的广泛使用,可使得单次后路矫正率增加。近年来,随着胸椎椎弓根螺钉技术的广泛使用,使得通过从后方达到三柱固定成为可能;而双棒去旋转、直接椎体旋转等当代后路矫形技术的开发应用,大幅提高了对顶椎区旋转畸形的矫正能力。有学者提出对于Cobb角100°以内的胸椎侧凸可通过单纯后路椎弓根螺钉矫形内固定达到较满意的矫形效果。对于脊柱矫形后仍残留明显剃刀背畸形的病例,可在后路同一切口内显露凸起的肋骨床,进行凸侧胸廓成形术。如凹侧胸廓向腹侧塌陷严重,可通过凹侧胸廓抬高成形术增大胸腔容积。后路手术具有容易暴露,有多种内植物可供选择等优点,但也存在融合节段长,椎体去旋转效果差及邻近节段退变等问题。
2)前路脊柱矫形融合术:理论上固定范围在T4-L5之间的柔软性较好,度数小于90°的脊柱侧凸都可以使用前路矫形,但考虑到胸段前路内固定的难度和较高的并发症,目前脊柱前路矫形手术主要用于侧屈X线片显示腰椎能良好去旋转和水平化的腰椎侧凸和胸腰椎侧凸。具体适应证如下:①青少年非僵硬型侧凸;②中度的胸腰椎和腰椎的侧凸(Cobb角<90°);③主弯在侧屈位上被动矫正达50%以上,上方次发弯具有良好的代偿功能;④具有柔韧的良好代偿能力的胸椎侧凸;⑤在侧屈位片上可减少至20°甚至更少;⑥矢状面上没有异常的后凸或前凸存在。手术切口可根据需要融合的部位进行选择,包括:开胸(单开胸、双开胸),胸腹联合切口和腹膜外斜切口等。邱勇等所研发的保护膈肌的小切口在减小创伤、保护膈肌,缩短手术时间的同时,获得了良好的矫正效果,是一种比较适合中国国情的手术入路选择(图3-12-2-13)。胸腔镜辅助的前路矫形术用胸壁锁孔替代长的手术切口,减小了对肩关节和呼吸功能的影响,瘢痕小,恢复快,但学习曲线较陡。前路手术的优点在于短节段融合;同时矫形力可直接作用于侧方移位和旋转的椎体,拥有力学优势。缺点在于技术要求高,暴露困难(上下终椎区处理不彻底),麻醉需双腔管插管、单肺通气等。随着后路三柱固定系统的出现和三维矫正技术的应用,前路手术的局限性和手术本身对胸腹腔脏器的影响等,使其适应证逐渐减少。
3)前后路联合手术或分期手术:前后路联合手术的适应证为僵硬的脊柱侧凸,尤其是90°以上,脊柱柔韧性小于20%,被动矫形差或残留角度大于40°的脊柱侧凸,可以先行前路脊柱松解,一期或二期后路三维技术矫正脊柱侧凸加植骨融合。对术前有神经系统症状的患者,为降低手术矫正过程中可能造成的神经系统症状加重,也可采用颅盆环牵引矫正。通过颅盆环牵引对脊柱施加缓慢矫正力,利用脊柱的蠕变特性,能有效提高侧凸的矫正率。另外,由于颅盆环牵引速度缓慢,提高了脊髓对牵拉的耐受性,即使治疗中出现神经损伤症状,通过及时调整外固定架,也可使症状得到缓解。对于年龄较大或凹侧早期融合的严重病人,可以一期后路脊柱松解,同时完成置钉,然后卧床大重量牵引2-3周,二期再行后路矫形手术。这样的分期手术既可在较安全的情况下提高矫形的效果,又避免开胸松解手术使得原本较差的肺功能进一步加重。
Risser征小于1,仍具有较多生长潜能的患者为避免后路内固定后出现曲轴现象,可先行一期前路骨骺阻滞再行二期后路内固定术。部分患者可先行单纯后路内固定术,术后严密随访,如有曲轴现象的迹象,则再行前路骨骺阻滞术。对于胸腰椎后凸畸形明显,躯干塌陷,脊柱支撑作用已丧失的患者在一期后路矫形术后需行二期前路凹侧支撑融合术。
(3)术中脊髓神经电生理检查:在脊柱矫形过程中有潜在的神经并发症,因此需要好的监测方法尽早的发现神经损害,并辅助手术医生及时采取干预措施避免或减轻术后神经损害。目前常用的监测手段包括:
1)唤醒试验反应运动功能的特异性较高,结果阳性,则说明总体运动功能完整。但由于临床中一般只是手术结束前行唤醒试验,故它不能及时发现术中损害。
2)踝阵挛试验主要反映是由s1神经控制的脊髓牵张反射,但可重复性差,不能单独作为一种监测方法进行脊髓监测。
3)体感诱发电位(somatosensory evoked potentials,SEP)测定是通过特定的神经电生理仪器,采用脉冲电刺激周围混合神经的感觉支,在近端周围神经、脊髓表面或头皮皮层感觉区记录生物电活动波形的方法。术中SEP监测主要观测指标为潜伏期和波幅。为了及时发现异常的SEP改变,基准值和警戒标准十分重要。现在一致认为,波幅下降超过50%和或潜伏期延长超过10%是警戒标准。SEP改变持续10min以上提示有神经损害的危险。SEP可重复性较好,可连续监测,远离手术野,对手术影响小,安全性高,因此可操作性好,现已广泛应用于临床(图14,图15)。尽管如此,在手术过程中,只靠单一的体感诱发电位,不能达到对脊髓整体功能状态的监测,不能保证患者术后的运动功能正常。特别是在脊髓前动脉综合征中体感诱发电位的假阴性率更高。同时美国脊髓研究协会在33000名脊髓手术病例的回顾调查中发现,28%的神经并发症并不能被体感诱发电位检测出来。因此,必须借助运动诱发电位来监测脊髓的运动功能状态。


图13 女,15岁,特发性胸腰椎脊柱侧凸lenke 5c,术前胸腰弯Cobb角53°(A);行前路保护膈肌小切口胸腰椎脊柱侧弯CDH矫形术+前路钛网支撑融合术,术后1年冠状面矫形满意(B);术后两年随访冠状面矫形满意(C);分段手术切口较传统切口明显减小(D)
4)运动诱发电位(motor—evoked potentials,MEP)是指应用电或磁刺激皮层运动区或脊髓产生兴奋,通过下行传导径路,使脊髓前角细胞或周围神经运动纤维去极化,在相应肌肉或神经表面记录到的生物电活动。近30年来,MEP的价值和高效性在术中监护中已越来越受到重视。常用的刺激方法有经颅电刺激和经脊髓刺激。经头颅刺激运动诱发电位是通过刺激头皮运动区代表区,在手术操作节段以下的肌肉记录的电位;经脊髓刺激运动诱发电位是通过在硬膜外或硬膜下直接刺激脊髓,在手术操作节段以下的肌肉记录的电位(图16)。
图14 正常SEP波形:上面是经正中神经刺激引出的波形,下面是经胫后神经刺激引出的波形

MEP根据记录的部位不同可分肌源性MEP和神经源性MEP。肌源性MEP和神经源性MEP记录各有优缺点。肌源性MEP优点是波幅大和潜伏期可靠,缺点是波幅和形态变异性较大。肌源性MEP监测警戒标准争议较大,现在大部分学者倾向于接受“全或无”的警戒标准。肌源性MEP监测过程中因肌肉收缩会影响手术操作,使得监测次数减少,也就降低了发现神经损害的敏感性。而神经源性MEP在波幅、潜伏期及波形上变异性较小,监测警戒标准的制订相对容易,一般认为潜伏期延长10%和波幅下降80%为警戒标准。MEP的预警标准现下主要有四种:①“全“或“无”标准,②波幅标准,③阈值标准,④波形标准。应用最广泛的是“全“或“无”标准。基于这项标准,只有当MEP全部消失才预示术后的运动障碍。图17为一名术中患者典型阳性表现。但正是由于这一标准,可能术中一些小的神经损伤不能在术中及时发现而导致术后的运动障碍。波幅标准是由Langeloo提出的,至少6次有1次的波幅降低80%视为阳性变化。他通过142例病人的研究发现,此标准的灵敏性是100%,特异性是91%。总的来说MEP监测的可重复性比SEP差,但MEP将是一种非常有前景的术中脊髓监测手段,它与SEP等其他监测技术的联合应用将会大大降低脊柱手术的神经并发症。
(4)临床分型和融合策略:脊柱侧凸分型系统的建立对AIS的术前评估及手术策略制订具有非常重要的临床指导意义。迄今为止临床应用较广泛的分型系统包括Lenke分型和PUMC分型。
Lenke分型
Lenke分型近年来已成为国际上通用的关于特发性脊柱侧凸的标准分型方法。该分型以脊柱冠状面、矢状面二维因素为基础提出,是一个三步分型系统,可重复用于AIS的准确分型。其优点在于是可分析每个弯,可有效地进行术前计划。Lenke分型的第一步是根据冠状面结构性弯的位置进行分型,共分为6型(表2);第二步再根据腰弯顶椎与骶骨正中线(center sacral vertical line,CSVL)的位置关系制订的腰弯修正型;最后再增加胸椎矢状面修正型。

图15 手术中异常SEP波形
16Y(#9307),男,先天性脊柱侧凸,矫形过程中出现(3)右侧波幅降低超过50%,接着出现(2)潜伏期延长超过10%,进而出现(1)右侧波形消失
图16 正常的MEP波形,从左到右依次是左、右手大小鱼际肌、左右下肢腓肠肌的波形

图17 典型的MEP阳性表现

14岁(#9475),男,先天性脊柱侧凸,行胸12半椎体切除。M1、M2及M3是置钉时的波形,示基本无变化;M4、M5示在矫形时,突然出现右侧拇展肌MEP波形消失。M6、M7及M8示减压后,MEP又重新恢复
Lenke分型步骤:
1)确认脊柱侧凸类型:局部侧凸包括上胸弯,主胸弯和胸腰弯/腰弯。主弯指Cobb角最大的侧凸,通常为主胸弯或胸腰弯/腰弯。若上胸弯Cobb角最大时(这种情况极少见)仍默认主胸弯是主弯。主弯通常被认为是结构性弯。在1-3型,主弯为主胸弯,而在5型和6型,胸腰弯/腰弯则是主弯。在Lenke4型中(三主弯),主胸弯或胸腰弯/腰弯都可以是主弯,根据何者Cobb角最大而定。若主胸弯和胸腰弯/腰弯度数相同,则认为主胸弯是主弯。
次弯(除主弯以外的侧弯)可以是结构性弯或非结构性弯。在站立位前后位X线片上Cobb角≥25°,且在Bending像上冠状面Cobb角≥25°,则认为此弯为结构性弯。若局部矢状面后凸≥20°,此次弯也被认为是结构性弯:换言之,即使上胸弯在冠状面上不符合结构性弯的标准,但如果T2-T5局部后凸≥20°,则此弯也被认为是结构性弯;同样,即使主胸弯和胸腰弯/腰弯在冠状面上不符合结构性弯的标准,但如果T10-L2局部后凸≥20°,那么此弯也是结构性弯。在确定完每个弯是结构性弯或非结构性弯之后,Lenke分型1-6型即可得到确认(图18,图19)。特发性脊柱侧凸Lenke分型标准(参考:Lenke LG,et al. J Bone Joint Surg Am,2001)
2)腰椎修正型(A~C):根据脊柱前后位片上骶骨中垂线(center sacral vertical line,CSVL)与腰椎的位置关系,将腰椎侧凸进一步分为A、B、C 三型。若CSVL在腰弯顶椎双侧椎弓根之间穿过,腰椎修正型为A;若CSVL位于腰弯顶椎凹侧椎弓根内侧缘与椎体或椎间盘外缘之间,腰椎修正型为B;若CSVL位于腰弯顶椎椎体或椎弓根外缘之外,腰椎修正型则为C。当难以区分腰椎修正型是A还是B,或是B还是C时均认为腰椎修正型为B(图20,图21,图22)。
3)胸椎矢状面修正型(-,N,+):胸椎矢状面修正型通过测量T5~T12矢状面Cobb角确定。“-”型指T5~12后凸角<10°;N型指T5-T12后凸角在10°~40°之间;“+”型指T5-T12后凸角>40°(图23)。
图18 特发性脊柱侧凸Lenke分型示意

4)融合区域的正确选择:融合节段的正确选择,目的在于既矫正侧凸使脊柱处于平衡代偿状态,又尽可能多地保留活动节段。融合范围太短可导致术后失代偿(Adding on叠加现象),融合节段太长则使脊柱的活动不必要地受限。融合术后脊柱的平衡不是由融合的节段而是由未融合的能活动的节段来保持。一般地,通过评估动态的左右侧曲位(Bending)脊柱X线片了解侧凸节段柔韧性及失平衡程度,可粗略决定脊柱融合的范围。一般而言,所有结构性主弯和结构性代偿弯都应融合,矢状面上所有异常的节段应包括在融合范围之内。一个侧凸弧中可能仅部分是结构性的,可通过Bending位X线片来判断;融合端椎应该在各个方向都能活动,最重要的是远端融合椎,也就是说远端融合椎的远端椎间隙在Bending相中应能自由闭合,远端融合椎终板在凹侧弯曲相中小于15°,旋转不能超过20%,Bending相的轴状面中应达到中立位。尽管如此,脊柱融合节段的选择是个非常复杂的问题,有许多因素决定,一些共同的原则包括:①侧凸构成节段或受到减压的节段必须融合;②内固定避免终止于T8-9水平;③在年幼AIS患者需要在L4/5或L5、S1之间取舍时,应选择上位脊椎为下端固定椎;④所有矢状面上的畸形节段必须包括在融合区内,特别是胸腰段交界区后凸畸形;⑤融合固定的上下端在矢状面和冠状面上都不能终止于侧凸的顶椎区。

图19 Lenke分型1-6型示意图
A. 女(#3899),16岁,主胸弯68°,上胸弯(19°)和远端腰弯(35°)在Bending相上均小于25°,均为非结构性弯,为Lenke1型;B. 女(#4174),13岁,主胸弯65°,上胸弯60°为结构性次弯,远端腰弯21°为非结构性弯,为Lenke2型;C. 女(#4099),11岁,主胸弯Cobb角(100°)为结构性主弯,腰弯Cobb角(68°)是结构性次弯;上胸弯(32°)在Bending相上Cobb小于25°,为非结构性弯,故为Lenke3型;D. 女(#3776),14岁,三弯均为结构性弯,主胸弯为主弯(100°),为Lenke4型;E. 女(#3129),15岁,胸腰弯(42°)为结构性主弯,为Lenke5型;F. 女(#3751),15岁,胸腰弯(63°)大于主胸弯(50°)超过5°,故胸腰弯为结构性主弯,主胸弯为结构性次弯,为Lenke6型

图20 腰椎修正A型。CSVL位于L3双侧椎弓根之间(#3899-772)

图21 腰椎修正B型。CSVL位于L2,L3凹侧椎弓根之内侧缘与椎体外缘之间

图22 腰椎修正C型。CSVL位于L3凹侧椎体外缘之外
脊柱侧凸分型系统的建立对AIS的术前评估及手术策略制订具有非常重要的临床指导意义。King首先将分型和融合范围的选择结合起来,但King分型仅对特发性胸椎侧凸进行分型,并不包括双主弯、三主弯、胸腰弯及腰弯等,且对KingⅡ型侧凸的治疗目前存在较大的争议,按King分型原则进行手术术后常发生躯干失平衡,已被公认是一种不完整的分型方法。Lenke分型作为国际上临床使用最广泛的标准分型系统,侧凸类型较全面、对结构性侧凸的定义明确,且同时考虑到了冠状面和矢状面上的畸形,因而对侧凸融合节段的选择有重要指导意义。其中腰弯修正型对选择性融合与否有一定参考意义,而胸椎矢状面修正型-、N或+的手术指导意义在于恢复矢状面胸椎正常后凸形态。
总之,正确的融合区选择既要获得侧凸的矫正,达到有效融合,又要尽量减少不必要的脊柱活动度的丧失,从而减少失代偿(叠加现象,躯干倾斜,假关节等)的发生。另外在目前翻修手术仍难被患者理解的国情下,是否进行选择性融合须十分慎重。

图23 胸椎矢状面修正型由左至右依次为:-,T5~12后凸角<10°(A);N,T5~12后凸角10°~40°之间(B);+,T5-T12后凸角>40°(C)
● Lenke1A型(图24、25)。
● Lenke1B型(图26)。
● Lenke1C型(图27)。
● Lenke2A型(图28)。
● Lenke3C型(图29)。
● Lenke 5C型(图30)。

图24 女,18岁,AIS Lenke1AN型(A、B);行前路选择性融合术后3年冠状面和矢状面矫形满意(C、D)
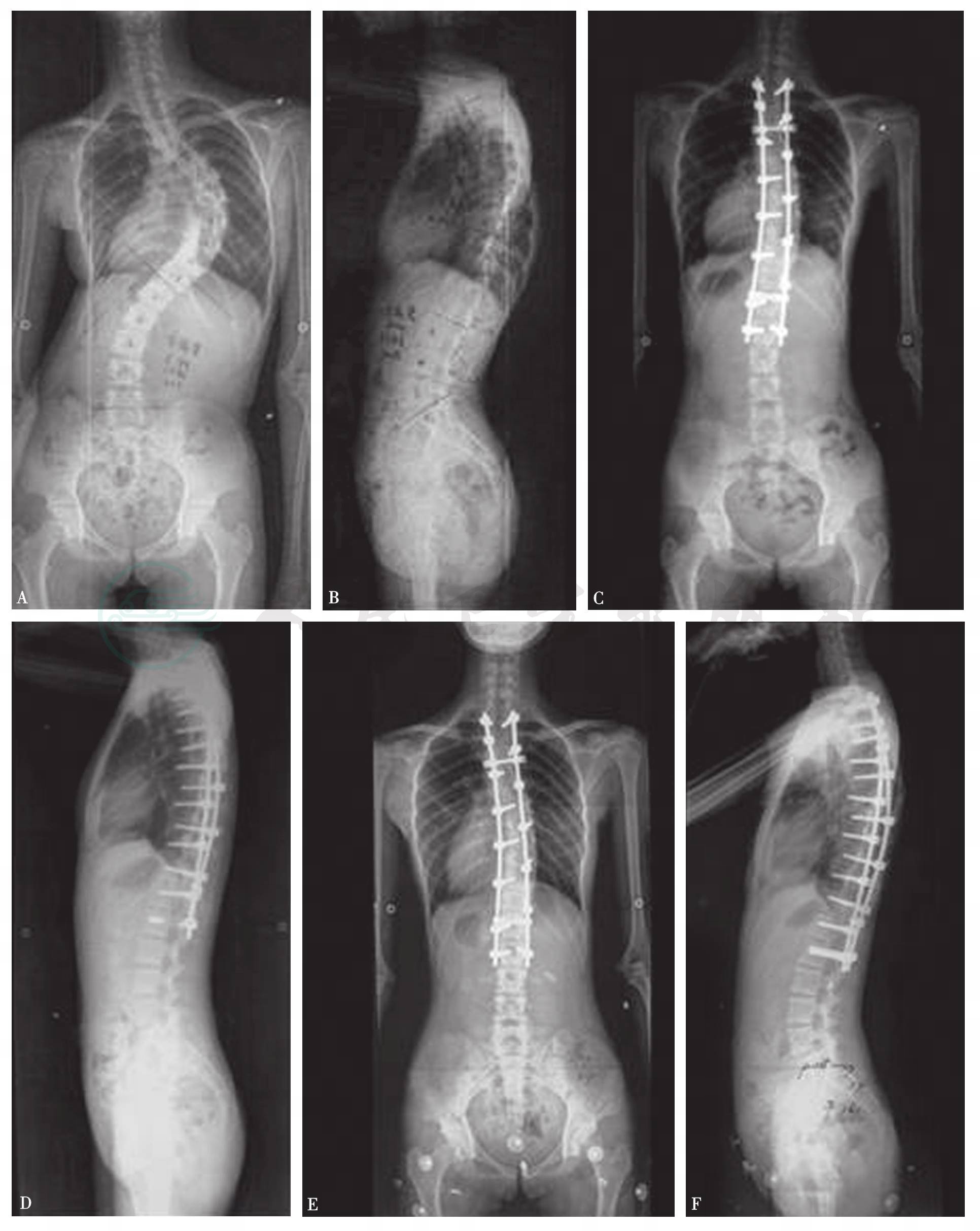
图25 女,14岁,AIS Lenke1AN型(A、B);术前Cobb角86°,行后路选择性融合术,术后矫形效果良好,Cobb纠正到25°(C,D),术后1年冠状面和矢状面矫形满意(E、F)

图26 女,13岁,AIS Lenke1B-型(A、B);术前Cobb角71°,行后路选择性融合术术后即刻矫形效果良好Cobb纠正到25°(C、D),术后2年冠状面和矢状面矫形满意(E、F)

图27 女,15岁,AIS Lenke1C-型(A、B);行后路选择性融合术后2年冠状面和矢状面矫形满意(C、D)

图28 女,14岁,AIS Lenke2AN型(A、B);行后路选择性融合术后18月冠状面和矢状面矫形满意(C、D)

图29 女,12岁,AIS Lenke 3CN型(A、B);行后路矫形融合术后2年冠状面和矢状面矫形满意(C、D)

图30 女,14岁,AIS Lenke5CN型(A、B)。行前路选择性融合术后8月冠状面和矢状面矫形满意(C、D)













