英文名称 :lumbar spondylolisthesis
脊柱滑脱(spondylolisthesis)是由Killian在1854年首先提出,这个词源自于希腊语“spondylo”(椎体)和“listhesis”(滑移),其定义为“由于椎弓根峡部断裂或延长,上位椎体相对于下位椎体向前或向后的滑移,滑移部分包括椎体及其椎弓根、横突和上关节突”。
病因较为复杂,可以确定的两个重要原因是创伤性因素和先天性因素,前者更为常见。
1.创伤性因素
创伤性因素可以分为急性创伤和慢性劳损。腰椎峡部可因急性外伤,尤其是后伸性外伤产生急性骨折,多见于竞技运动员或强体力劳动的搬运工。体操运动员、蝶泳运动员、举重运动员、划艇运动员、潜水员、摔跤手和网球运动员常需进行过度腰椎运动,可导致疲劳性骨折。
2.先天性因素
先天性因素所导致的脊柱滑脱约占总体的14%~21%。Fredrickson等的椎体滑脱的标志性文献中,报道6岁儿童L5脊柱滑脱的发生率为4.4%,成人增加到5.8%。
3.退变性因素
由于椎间盘和小关节突的退变,导致椎间不稳、前纵韧带松弛,下腰椎应力增加,从而逐渐发生滑脱。由于其峡部仍保持完整,故又称为假性滑脱。常见于50岁以上患者,女性的发病率高于男性,多见于L4,其次是L5椎体。一份200人规模的病例调查指出,平均滑脱距离为14%。
4.病理性因素
病理性因素可分为全身性因素和局部性因素,病变累及椎弓、峡部、上下关节突,使椎体后方结构稳定性丧失。全身性因素包括可累及脊柱的Paget病、骨质疏松和成骨不全等;局部性因素包括梅毒、结核、肿瘤等,可导致峡部病理性骨折及脊柱滑脱。
5.医源性因素
医源性脊柱滑脱最早由White 于1976报道,发生于椎板切除术后。椎间盘摘除或椎管减压的手术均有可能导致医源性脊柱滑脱,原因主要是术中切除椎板和关节突过多,术中未行脊柱融合或术后脊柱融合失败所致。Fox等发现行后路减压但未能有效融合的病例中,脊柱滑脱的发生率可达31%。脊柱后路融合术后也可出现峡部裂,通常于术后5年发生,且多数病例发生于融合完成前。
腰椎滑脱(lumbar spondylolisthesis)的发病率因地区而异,并有明显的种族倾向,非洲人发病率约为2.8%,北欧人的发病率为6.4%,爱斯基摩人的发病率约为26%~50%,我国的发病率约为4.7%~5%。我国的发病年龄以20~50岁为主,约占85%,男性多于女性。最常见的滑脱部位是L4~L5及L5~S1,近90%的滑脱发生于L5~S1节段。
(一)腰椎滑脱的分类
1983年,Wiltse、Newman和Macnab根据发病学和局部解剖学,对脊柱滑脱进行了分类(表1,图1)。
1.发育不良性(先天性)脊柱滑脱
发育不良性腰椎滑脱根据关节突关节面的方向分为三种亚型。
Ⅰ-A亚型——表现为L5、S1水平位而非冠状位的关节突发育不良,S1上位终板圆滑,可有L5或S1或二者均累及的隐性脊柱裂。典型影像学特征:从前后位X线投影来看,L5椎体前移、倾斜,导致椎体轴向出现“拿破仑帽”征(图2A);侧位片上看,通常可见L5高度前移,椎体后方成楔形,S1上位终板圆滑(图2B),峡部被拉长,可保持完整或出现断裂(图2B),经常也可发现隐性脊柱裂。峡部情况可通过矢状面CT三维重建予以明确,也可通过MRI检查,后者对腰椎退行性改变和疑似腰骶椎间盘突出的检查也有效(图3A)。根据滑脱程度不同,可在L5~S1椎间孔处出现L5神经根明显压迫,也可在L4椎弓与骶骨后上方区域之间出现马尾神经压迫。
表1 Wiltse-Newman-Macnab分类

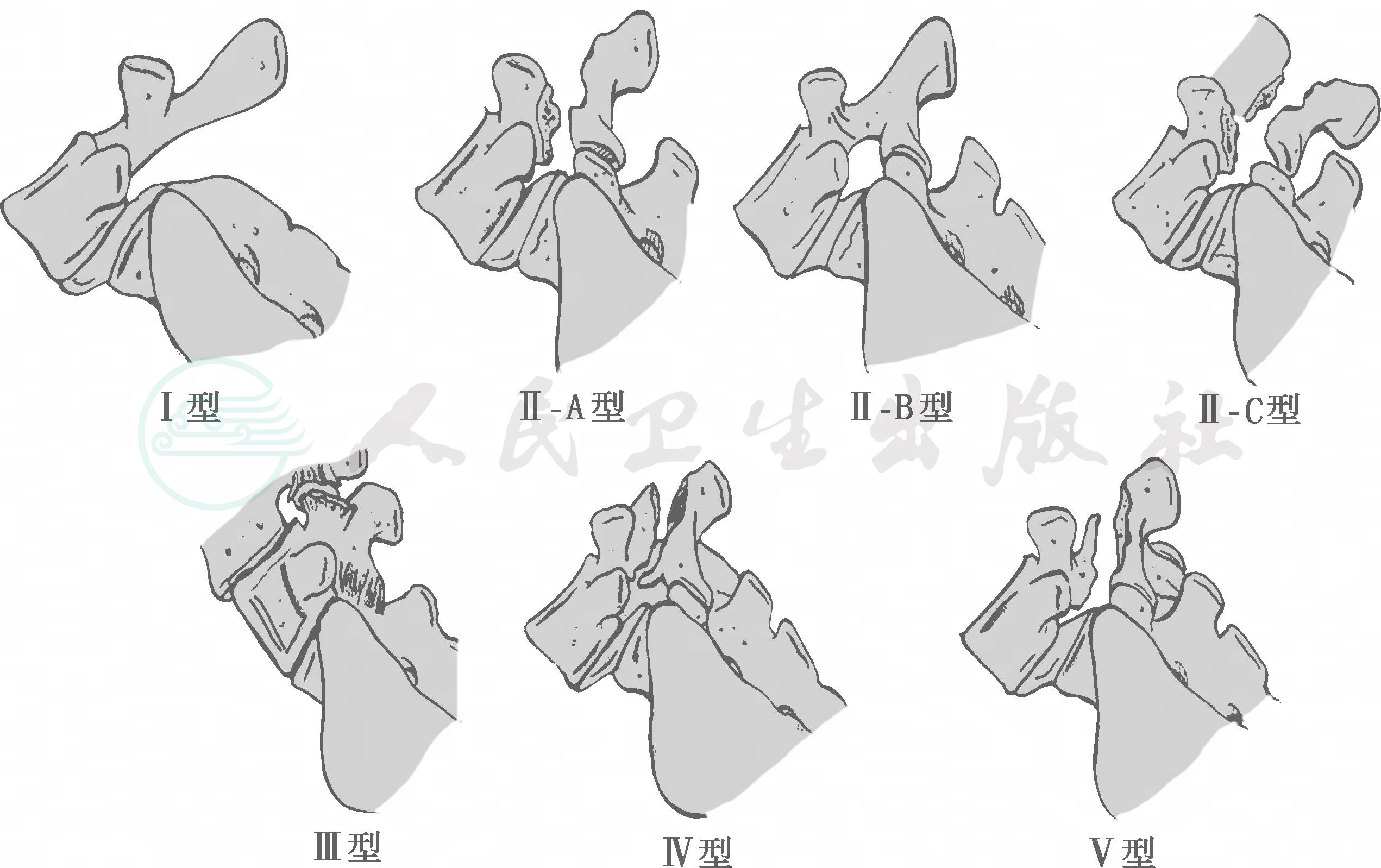
图1 腰椎滑脱的Wiltse-Newman-Macnab分型
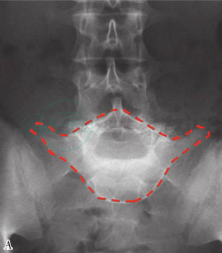
A
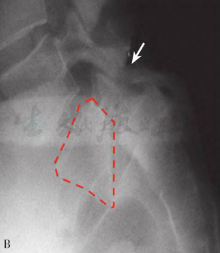
B
图2 Ⅰ-A型脊柱滑脱
正位片(左)示“拿破仑帽”征。侧位片(右)示滑脱程度约为70%,L5后方呈梯形,S1上位终板圆滑,箭头所示为L5峡部缺损
早期临床表现以腘绳肌腱紧张比较常见。由于这种亚型存在先天性脊柱失稳,治疗上需要进行脊柱融合。
Ⅰ-B亚型——表现为矢状位的关节突关节面不对称,椎弓多为完整,多见于成年患者。典型影像学特征:关节突关节的发育不全和出现旋转,导致关节面的矢状位不对称(图3B),该类型滑脱的特有表现有助于与退变性滑脱进行鉴别。临床表现以腘绳肌腱紧张、下肢放散痛及马尾神经功能障碍较为常见。由于此类型滑脱的骨环结构是完整的,因此即使轻度滑脱也可能出现神经压迫症状。这种亚型存在神经功能障碍,治疗上需要进行减压和脊柱融合。
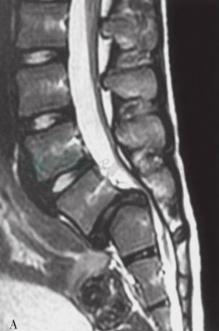
A
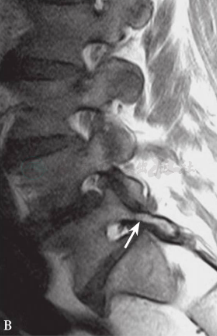
B
图3
A图为Ⅰ-A型脊柱滑脱。正中矢状位MRI示:腰5骶1椎间盘退变,在L5椎弓与骶骨后上方之间出现马尾神经的严重压迫。B图为Ⅰ-B型成年患者脊柱滑脱。旁矢状位MRI:S1关节突关节发育不全,L5峡部拉长(白色箭头所示)
Ⅰ-C亚型——腰骶关节的先天畸形引起的腰椎滑脱。Ⅰ-C亚型可合并好发于胸腰段的先天性脊柱侧凸,还包括其他各种腰椎椎弓发育不良,如先天性关节突缺如等(图4)。
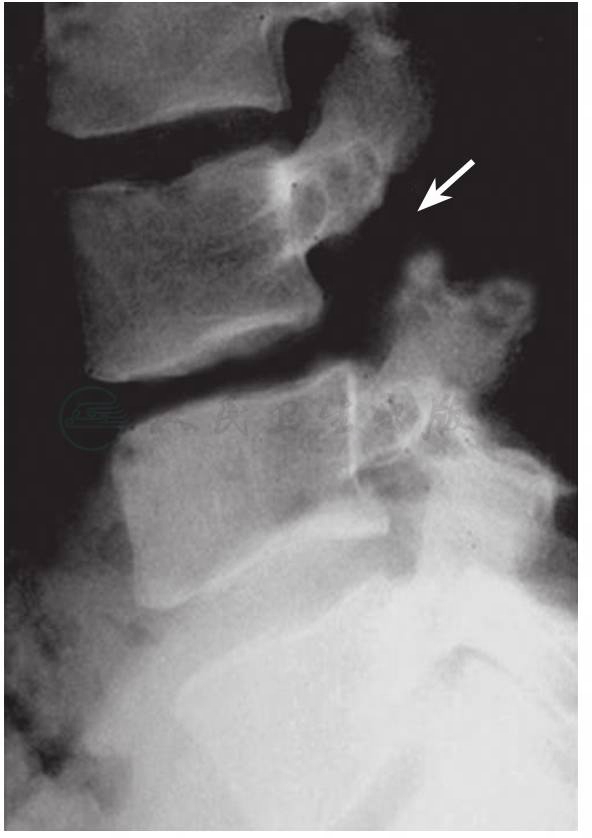
图4 Ⅰ-C型脊柱滑脱
侧位X线示:L3下关节突先天缺如,L3/4 Ⅰ度滑脱
2.峡部裂性脊柱滑脱
Wiltse认为峡部疲劳性骨折是峡部裂性脊柱滑脱的基础病变,并得到了很多研究的支持,据此Wiltse率先分为3个亚型。
(1)Ⅱ-A亚型
此类峡部缺损并非出生时就有,而是由于先天发育不良致峡部骨质强度不佳,或长期劳损,或二者兼具,逐渐引起的。此为50岁以下腰椎滑脱患者最常见的原因,矢状位及冠状位CT三维重建有助于进一步明确峡部缺损情况(图5)。
(2)Ⅱ-B亚型
峡部被拉长,其实质为应力性骨折。长期反复劳损不断导致细微骨折,骨折愈合的同时,峡部逐渐被拉长,从而无法抵抗椎体向前滑动。此类型较为少见。
(3)Ⅱ-C亚型
急性损伤导致脊柱复杂骨折,同时伴有峡部骨折。单纯的峡部急性损伤极其罕见。
根据文献报道,以下结论与脊柱滑脱发病机制有关:
(1)遗传倾向。
(2)敏感或高危人群由于环境和职业因素造成的峡部疲劳性骨折。
(3)轻微创伤和持续性相关疲劳性损伤可加剧峡部疲劳性骨折的发生。
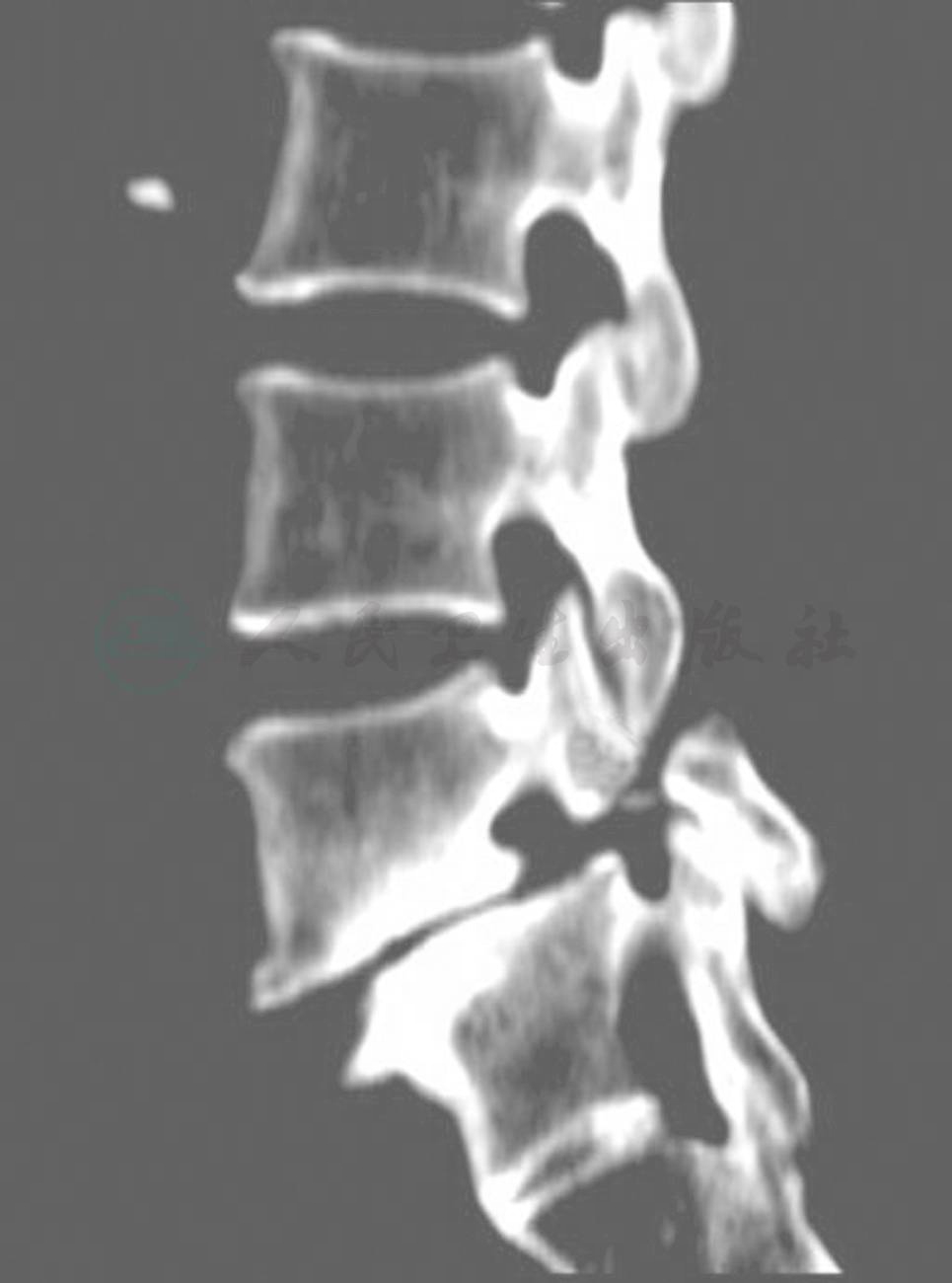
图5 Ⅱ-A峡部裂性脊柱滑脱
箭头所示为L5双侧峡部断裂
(4)峡部断裂可引起脊柱不稳和不同程度的脊柱滑脱。
(5)女性患者更易出现比较严重的滑脱,常常需要进行稳定性手术治疗,以减轻症状。只有不到20%的脊柱滑脱患者会出现临床症状。
3.退变性脊柱滑脱
此类型在50岁以上腰椎滑脱患者中最多见。滑脱的原因是关节面与椎间盘的退变,椎弓保持完整。此类患者多为下腰椎矢状位关节面先天变异,导致关节面在传递身体重力时,力线前移,继而引起椎间盘过早退变。滑脱程度通常为轻度。由于椎弓是完整的,即使轻微滑脱也可导致马尾神经受压,最常累及L4/5节段(发病率比其他节段高6~9倍),女性发病率比男性高4倍,非洲裔人种发病率比高加索人种高3倍,若有L5骶骨化,发病率可增加4倍。可有多种骨关节炎改变:滑膜炎、软骨退化、骨赘、关节突骨折、骨软骨游离体和关节囊松弛。
4.创伤性脊柱滑脱
文献报道椎弓峡部的急性骨折是非常少见的,通常继发于严重创伤,除峡部外,还可致椎弓其他部位如椎弓根或关节面的骨折或脱位,即刻或数月后逐渐出现滑脱(图6)。创伤型脊柱滑脱中一般比较常见双侧椎弓根骨折,重度创伤时合并脊柱后方结构的脱位。Wiltse曾报道在新兵训练营中的全副装备急行军可导致峡部骨折,这种骨折往往会自愈,但在骨折部位常出现“fluffy callus”现象。Wiltse还列举了一些造成创伤型脊柱滑脱的情况,如后摔、腰背部打击,并在影像学上可发现峡部骨折。通过CT三维重建可以明确创伤性脊柱滑脱合并骨折的情况。MRI可以显示相关软组织损伤情况,包括椎间盘破裂、后纵韧带完整性。
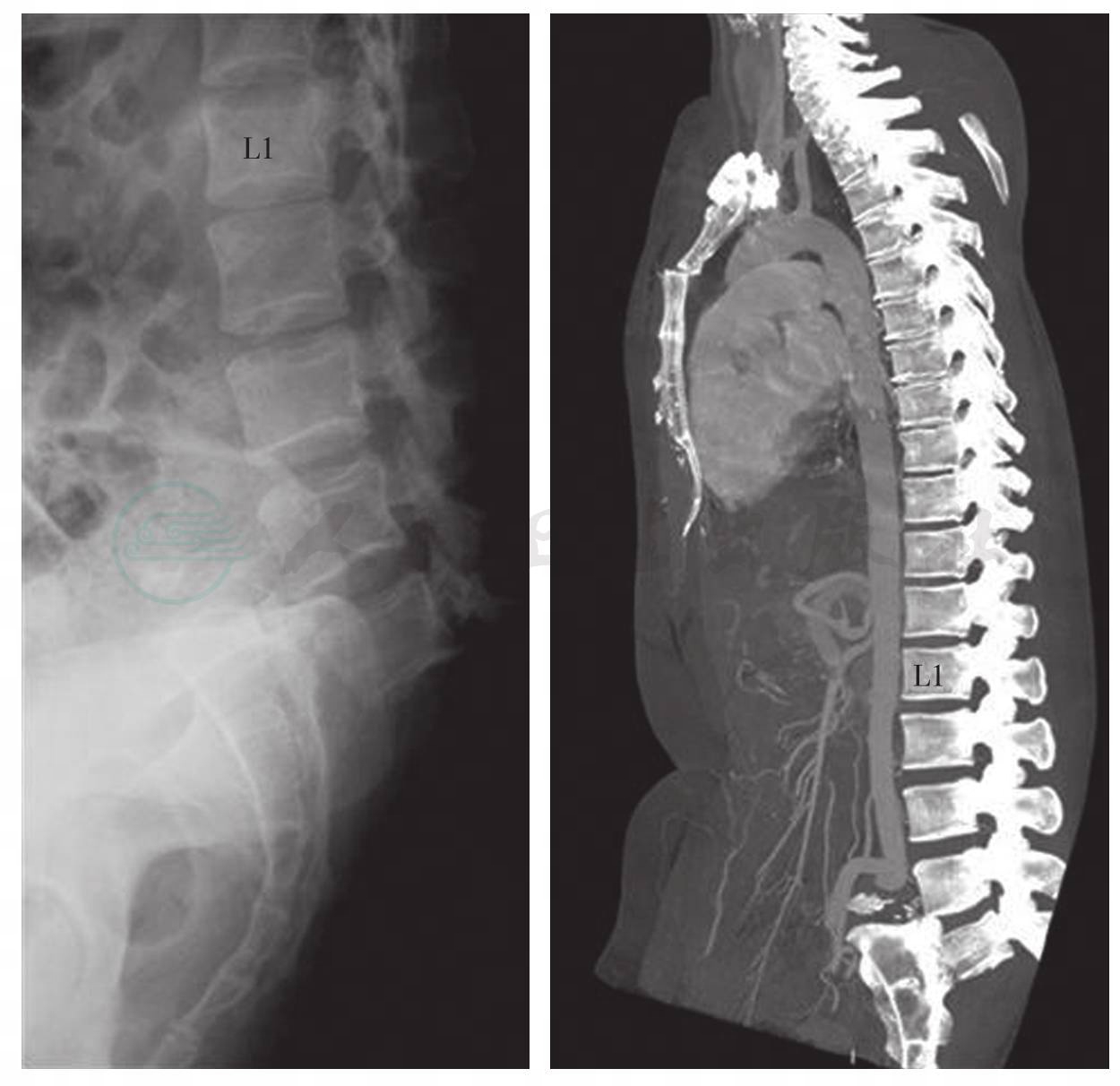
图6 Ⅳ型腰椎滑脱
X线(左)显示L5椎体向后方移位,完全滑至骶骨后方;三维CT示(右):L5椎体完全脱位伴L5椎体及骶骨骨折,骶前血管严重屈曲成角
5.病理性脊柱滑脱
累及椎弓、峡部、上、下关节突的全身性和局部性的病理性因素可使椎体后结构稳定性丧失,导致滑脱出现,如Paget病、成骨不全、梅毒、结核、肿瘤等。
6.医源性脊柱滑脱
椎间盘摘除或椎管减压的手术均有可能导致医源性脊柱滑脱,原因主要是术中切除椎板和关节突过多,术中未行脊柱融合或术后脊柱融合失败所致。
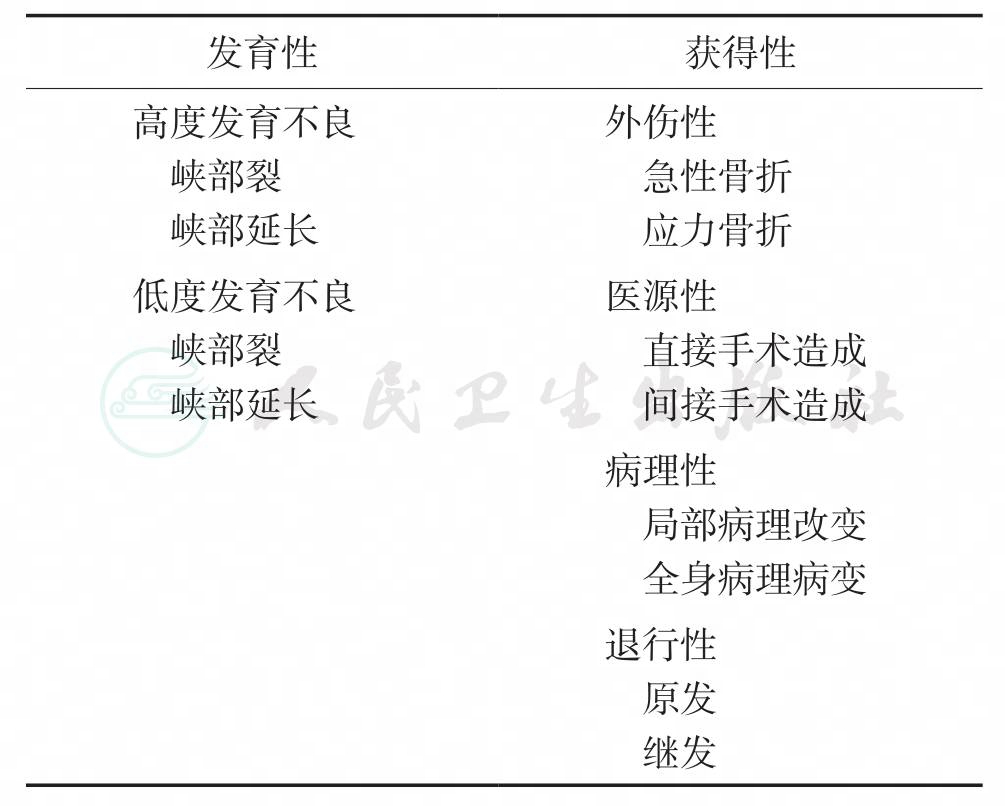
1994年,Marchetti和Bartolozzi认为,Wiltse等人的分类很难预测滑脱的进展程度,关键是不能对滑脱进行准确的分型,不利于手术效果的评价。因此,他们将腰椎滑脱分为发育性和获得性两大类(表2)。该分类没有将峡部性腰椎滑脱放在最重要的位置,而是强调了发育和形成不良对峡部不连的影响。在分析脊柱滑脱的病因时,外科医师必须首先确认是发育性还是获得性滑脱。如果是发育性的滑脱,还必须通过评价后侧骨钩的发育程度,从而确定是高度还是低度发育不良。脊柱滑脱的进展到何种程度是由发育不良的部位及程度、脊柱生物力学特性和椎间盘完整性所预先决定的。这就是Marchetti和Bartolozzi分类意义所在。
下腰椎的异常可表现为多种形式,这些异常与拍摄X线片的时间、患者的年龄以及该异常的生物力学状况有关。腰椎前凸的角度和矢状位重力线的位置对腰椎滑脱的发生、程度和进展影响很大,重力线越靠前,脊椎滑脱进展的可能性越大。存在滑脱节段的椎间盘质量同样十分重要,这需要MRI检查进行判断。
表2 Marchetti-Bartolozzi分类
不稳定的滑脱指征包括:
(1)局部明显后凸,滑脱角超过25°。
(2)腰5椎体梯形变:当L5椎体后缘的高度小于椎体前缘高度的75%时,梯形变或楔形变的L5椎体可被看做是滑脱加重的单独的危险因素。Bosworth发现,有轻度楔形变者,滑脱9.5%;前后椎体高度差为25%者,滑脱23%。
(3)骶骨终板变圆:骶骨终板的前缘消失或变圆的患者,滑脱倾向于进一步发展,原因可能在于变圆的骶椎终板对L5椎体支撑不足。(图7)相反,如果骶骨前方已经形成很大的骨赘,滑脱进展的可能性较小。
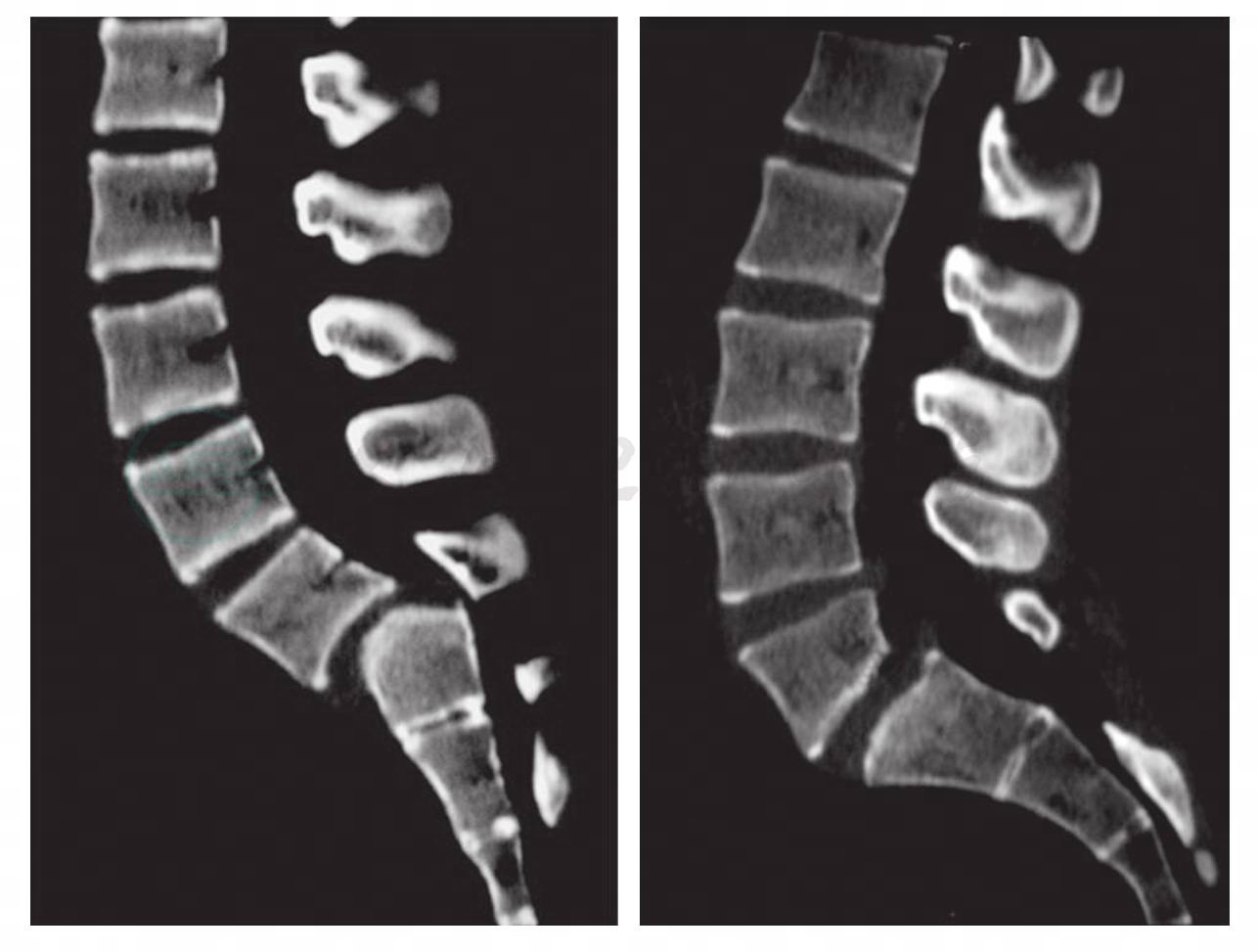
图7 不稳定的腰椎滑脱
二维CT示:骶骨终板呈圆弧形,与之对应的L5下终板也呈弧形,椎体梯形变(左图);腰骶过度前凸,S1终板倾斜明显,L5椎体呈梯形(右图)
(4)L2~S2过度前凸(超过50°):腰椎的过度前屈使腰骶椎终板倾斜度增加(图7),使垂直方向的剪切力增加,从而使滑脱进一步加重。
(5)峡部延长或分离。这种分类的意义在于,形成不良的程度越高,越是不稳定,滑脱进展可能性越大,因此越需要更加积极的外科干预。
大多数儿童和青少年的脊柱滑脱类型是发育性的,这些患儿出生后就存在形成不良的骨钩结构。患儿开始行走后,多种生物力学机制可造成峡部的应力增加,导致峡部发生延长或骨折,同时受累节段的椎间盘可较早发生退变,进一步加重滑脱的进展。如果这种不稳定的情况能够尽早发现,早期的干预措施可避免脊柱滑脱的进行性加重,从而避免未来进行更长节段固定及危险性更高的脊柱手术。
什么是骨钩?骨钩是由钩和钩扣组成的复合体,以L5~S1为例:钩是由L5椎弓根、关节突间的峡部及L5下关节突的前部组成,而钩扣为S1关节突(图8)。钩和钩扣是维持腰骶椎后方结构稳定的关键结构,峡部裂或椎弓崩裂相当于骨钩结构断裂,骨钩复合体丧失功能,导致L5椎体沿骶骨斜坡向前滑移。骨钩的概念由DeWald于1997年提出。
(二)腰椎滑脱的分度
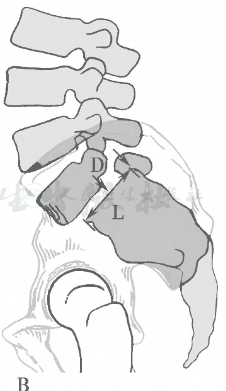
目前最为常用的腰椎滑脱分度方法有两种:一种称为Myerding法,即将下位椎体上表面前后径(AP)四等分,根据上位椎体后缘向前滑脱的距离与AP径之比,相应分为Ⅰ、Ⅱ、Ⅲ、Ⅳ度(图9A),滑脱少于50%定为低度腰椎滑脱,大于50%定为高度;另一种称为Taillard法,即根据上位椎体滑脱距离所占下位椎体上表面前后径的百分比进行分类(图9B)。若整个L5椎体滑脱至S1前方,称为完全滑脱(Ⅴ度)。Taillard法以其较好的精确性和可重复性在临床获得广泛认可。尽管如此,滑脱距离的测量和程度的判定仍需谨慎为之。有研究表明,对于程度为15%滑脱的测量,不同测量者之间以及同一测量者前后测量之间均存在明显误差,若伴有脊柱旋转,测量误差就会更大。因此,只有对于程度超过20%的滑脱进行的测量相对可靠。
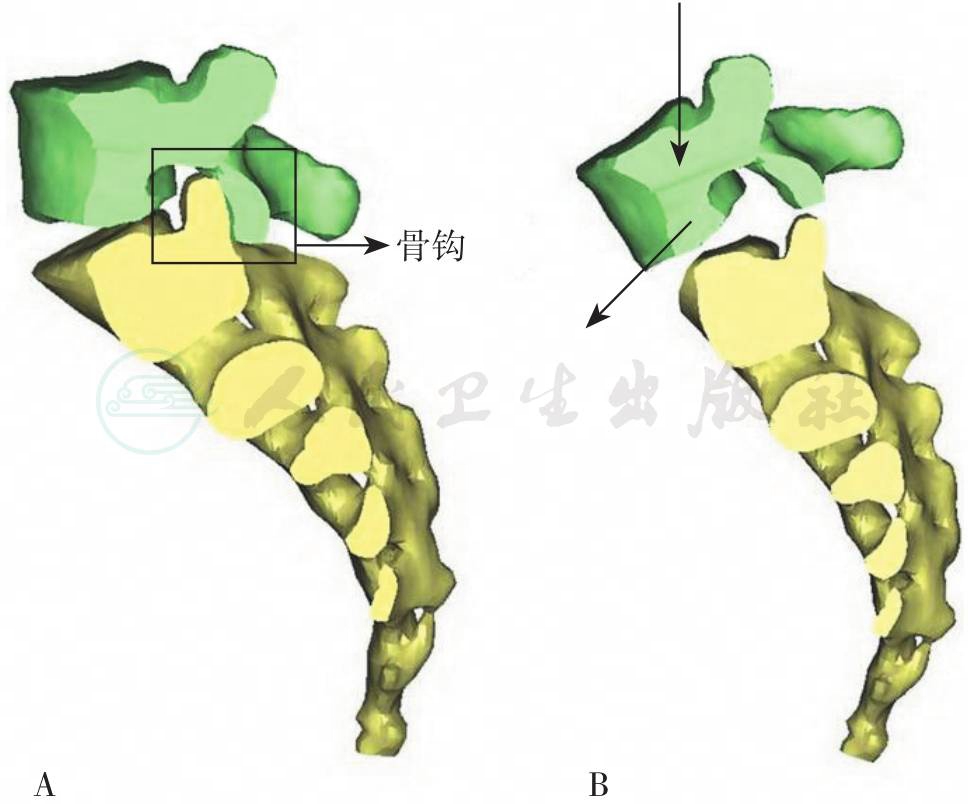
图8
一个正常的腰骶椎骨钩的结构(左图),包括发育良好的L5椎弓根、峡部、下关节突,S1椎弓根和关节突,正常关节突关节间隙及正常L5S1椎间盘的高度。其中钩为:L5椎弓根、峡部及下关节突;钩扣为S1关节突。骨钩可以对抗脊柱沿骶骨上端的终板斜面向前滑脱的趋势。正常骨钩和发育不良骨钩间的区别(右图):后者在上方脊柱传导下来的应力作用下不能对抗脊柱向前滑移
A
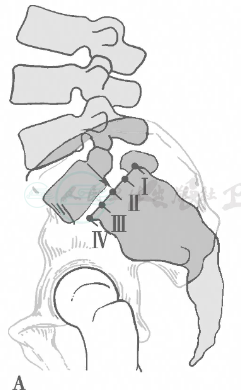
B
图9 腰椎滑脱的分度方法
A图为Myerding法,滑脱程度为Ⅲ度。B图为Taillard法,滑脱程度= D/L×100%
对于高度腰椎滑脱,还有一些特殊的影像学测量指标。 骨盆投射角(PI)是描述骶骨在骨盆内的位置的影像学指标。骨盆投射角定义为通过骶骨终板中点垂直于骶骨终板的直线与从骶骨终板到股骨头轴连线的角度(图10)。 骶骨倾斜角(SS)定义为骶骨终板与水平线之间的角度,而骨盆倾角(PT)是骶骨终板中点和股骨头轴心的连线与垂线之间的角度。骨盆投射角是骶骨倾斜角与骨盆倾角之和。因此,骨盆投射角增大,意味着骶骨倾斜角与骨盆倾角都增加。虽然PT和SS取决于盆腔的倾斜度(例如,姿势:坐位和站立),PI是衡量骨盆形态的指标,每一个人是恒定的,无论患者或坐或站。骨盆投射角在儿童期比较稳定,青少年时增加,一旦骨骼发育成熟就稳定了。较高的骨盆投射角意味着更大的腰椎前凸和更高的腰骶交界处部的剪力,如果不固定骨盆可能会增加假关节的可能性。骨盆投射角没有被证明能够预测脊柱滑脱的进展,但骨盆投射角确实随着腰椎滑脱Meyerding等级的增加而增加。
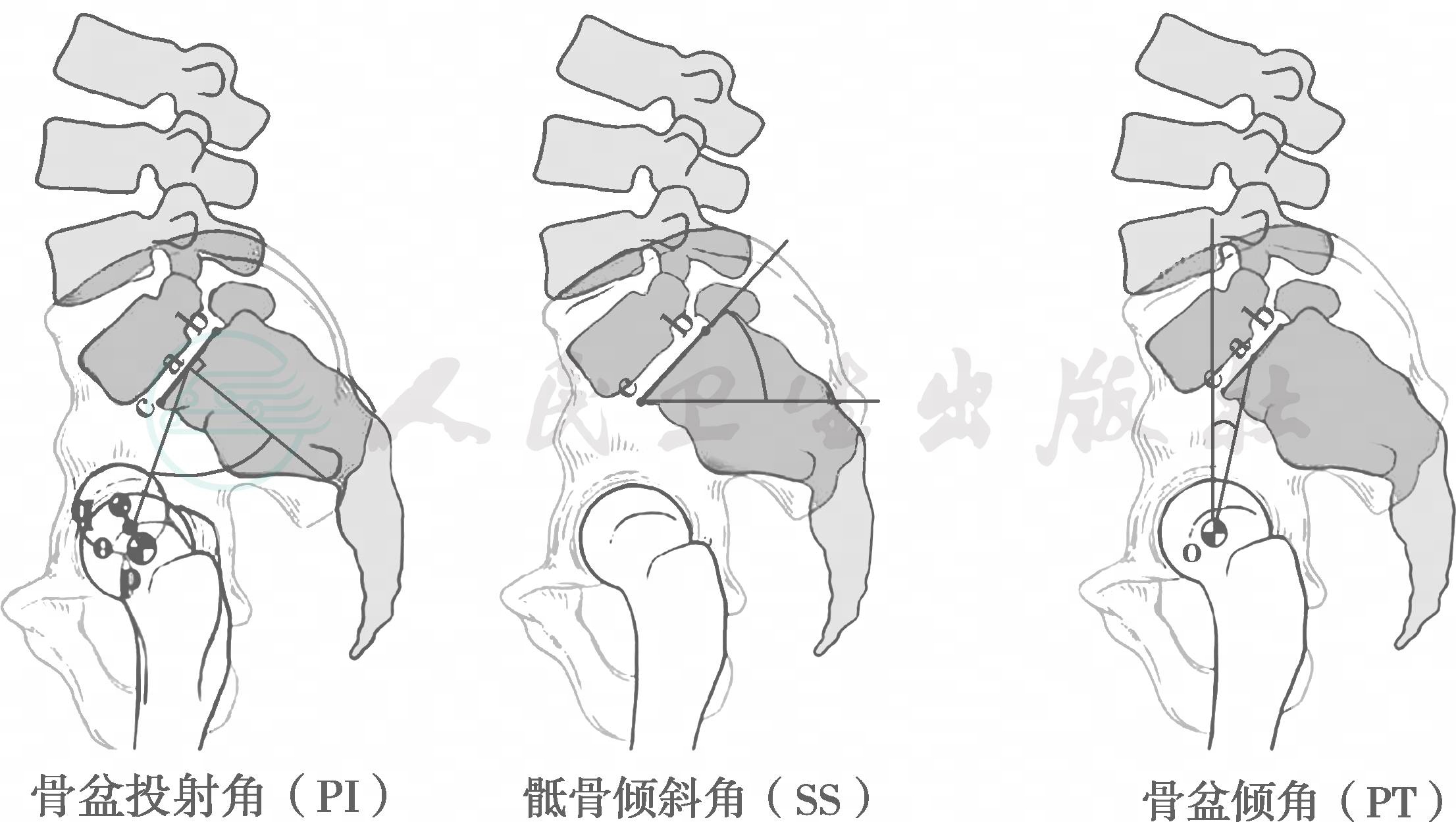
图10 骨盆投射角(左)、骶骨倾斜角(中)以及骨盆倾角(右)的测量方法
峡部裂性腰椎滑脱的病理特征主要是腰椎解剖结构破坏刺激或挤压神经,引起不同的临床症状。根据病变部位不同,产生腰痛、下肢痛、下肢麻木甚至大小便功能障碍等症状。鉴于椎弓峡部裂性腰椎滑脱是临床上最常见的类型,因此本文将做重点讨论。
1.腰椎峡部裂的病理
椎弓峡部裂被认为是椎体滑脱的前期病变,主要发生在上下关节突间的峡部。峡部裂引起下腰痛或下肢放散痛的病理基础主要包括三方面:
(1)峡部裂处局部纤维瘢痕增生或骨痂形成压迫神经根。
(2)峡部裂处的异常活动使峡部疲劳骨折难以愈合。骨折处新生纤维软骨,骨痂样组织中可带有神经末梢,峡部的异常活动可以刺激该部的神经末梢引起腰痛。同时,峡部的神经末梢,在椎管外面系脊神经后支的内侧支,在椎管的内侧为窦椎神经的分支,二者均可通过脊神经前支出现向臀部或股后部之反应痛。
(3)峡部裂加速椎间盘退变,可导致纤维环破裂并失去稳定性,腰部韧带关节囊及腰背肌劳损,产生腰痛或下肢放散痛。
2.腰椎滑脱的病理改变
腰椎滑脱导致腰痛的原因比峡部裂更为复杂,可包括以下三方面:
(1)腰骶部软组织及关节的劳损:腰椎滑脱可导致前纵韧带、后纵韧带、椎间盘以及关节突关节的力学负荷加重,易于疲劳。同时,腰椎滑脱导致腰椎生理前凸增加,腰骶部后方肌肉韧带结构的代偿增强,易于发生劳损,导致下腰痛的出现。
(2)骨性结构改变:生理前凸增加时,下腰椎的关节突关节负重增加,由不负重关节成为负重关节,且下腰椎棘突可以撞击或挤压棘间韧带,甚至创伤性关节炎,导致下腰痛的出现。
(3)滑脱部位的脊神经根或马尾神经受压:滑脱可造成椎管矢状径相对狭小,压迫硬脊膜及马尾神经,以下位椎体的后上缘“台阶”状突起处较为明显(图11)。滑脱严重者可直接造成神经根牵拉,引起神经症状,但症状与滑脱程度并不成正比。
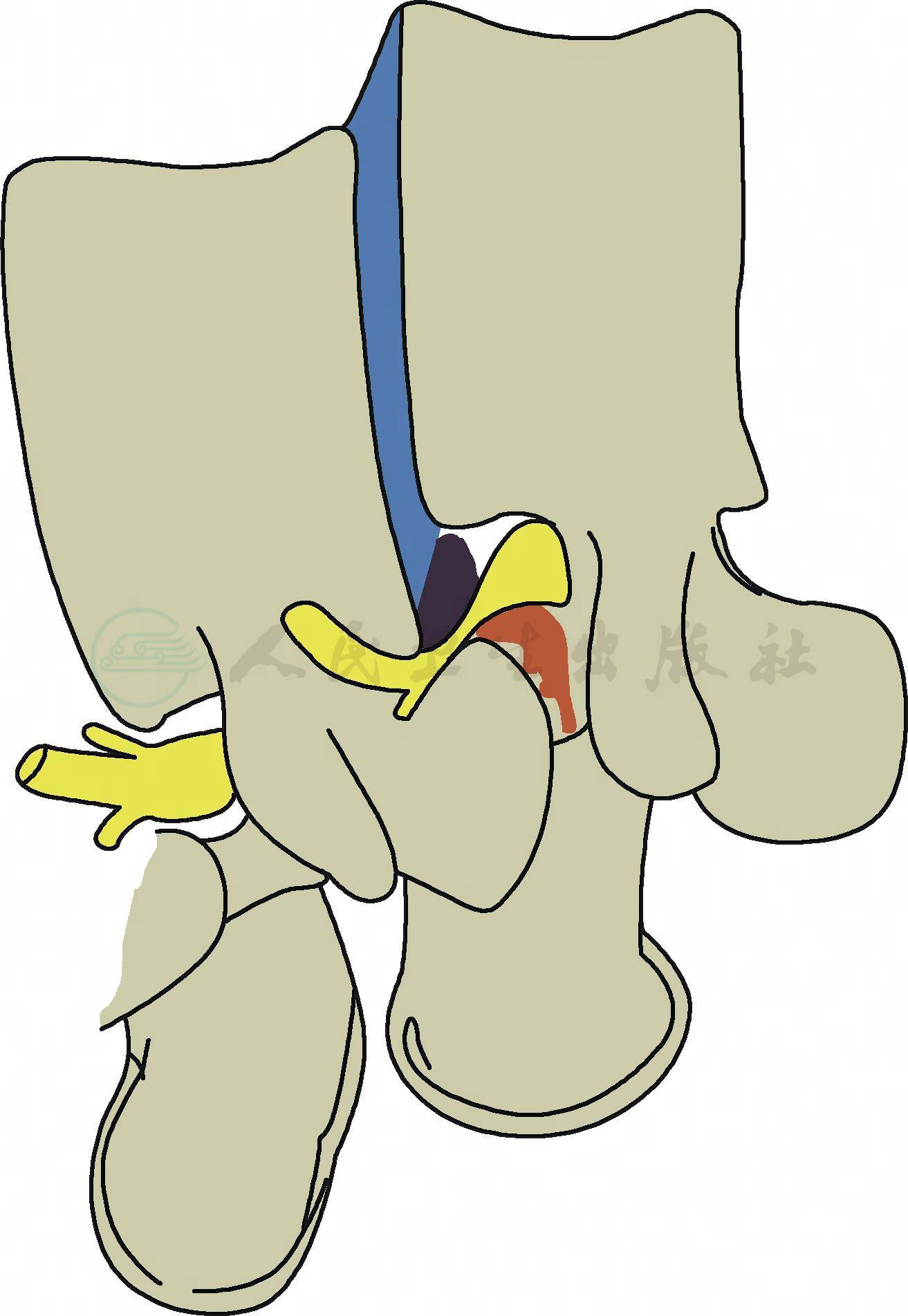
图11 腰椎滑脱示意图
滑脱节段神经根可受到峡部增生骨痂(红色)以及下位椎体后上缘及间盘(蓝色)的压迫,导致神经根性症状出现
以L5椎体向前滑脱为例,滑脱椎间隙是L5S1,向前滑移的骨性结构包括L5椎体、横突、椎弓根、上关节突及上位脊柱(L4)的所有结构,维持原位的结构包括L5椎板、下关节突及棘突与下位脊柱(S1)相连。可能受到压迫或刺激的神经根是:①L5神经根。由椎弓峡部裂处纤维瘢痕组织及骨痂样组织增生,造成L5神经根管或椎间孔狭窄,压迫刺激L5神经根;②S1神经根。腰椎滑脱及椎间盘退变突出及椎管狭窄可压迫S1神经根;③马尾神经。重度腰椎滑脱造成椎管错位,导致椎管狭窄,直接牵拉或压迫马尾神经。
解剖结构对腰椎滑脱的发病机制具有重要意义。腰椎存在正常的生理性前凸,当姿势改变或负重时可导致轴向负荷分配比例的改变。此时关节突关节承受大约总负荷的1/3,其余2/3由椎间盘承受。腰椎关节突关节面是倾斜的,在上腰椎关节面近似矢状位,而下腰椎则近似冠状位,限制了脊柱的轴向和矢状旋转。腰椎前屈时下腰椎关节突关节抵抗来自前方的剪切力,尤其是腰骶部更加明显。在L5~S1节段,强大的髂腰韧带显著限制了腰椎的前屈和侧屈运动,应力主要集中于上位腰椎节段即L4~L5运动节段,这也是L4~L5更容易出现腰椎滑脱的原因。发生峡部裂时,棘突、椎板和下关节突作为一个活动单位,受棘上韧带及背伸肌的牵拉,使该峡部发生头尾端的异常活动。背伸肌肌肉收缩,前弯腰时拉紧棘突,后伸腰时挤嵌棘突,引起此上下关节突之间的头尾侧异常活动。
Newman等人于20世纪60年代对引起腰椎滑脱的各种发病因素进行了研究,研究结果所形成的很多观点一直沿用至今。直立行走时,腰骶部对下腰椎椎体可产生持续的向下、向前的牵引力,这种分离趋势产生的负荷被椎间关节、椎弓根、椎板等骨性结构分担。这些骨性结构的解剖学特性也是Wiltse分类法的基础:椎间关节突关节、椎弓根、椎板或其他骨性结构不全可导致腰椎滑脱。
(一)X线片表现
X线表现对于腰椎滑脱的诊断及治疗方案的制订十分重要。所有腰椎滑脱患者均应常规拍摄站立位的正侧位、双斜位及动力位X线片。
1.正位片
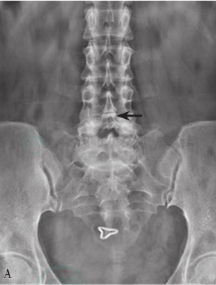
峡部裂性腰椎滑脱患者可在椎弓根阴影下方发现骨质密度减低的斜行或水平裂隙,多为双侧,宽度约1~2mm。明显滑脱的患者,滑脱的椎体因与下位椎体重叠而显示高度减小,椎体倾斜、下缘模糊不清、密度较高。滑脱节段棘突与上位椎体棘突撞击摩擦,形成“假关节”,密度明显增高(图12A)。
2.侧位片
侧位片可显示腰椎滑脱,并能测量滑脱分度。部分患者还能显示出上下关节突间的骨折裂隙。裂隙于椎弓根后下方,在上关节突与下关节突之间,自后上斜向前下,边缘常有硬化征象。单侧峡部裂患者的骨折裂隙显示不清楚,两侧较明显(图12B)。
3.双斜位片
可清晰显示峡部病变。在椎弓崩裂时,峡部可出现一带状裂隙,称为苏格兰(Scotty)狗颈断裂征或长颈犬(Greyhound)征(图12C、图12D)。L5峡部裂,其前下方常位于骶骨关节突顶点上数毫米,偶尔可位于顶点的稍前方。斜位片中影像学解剖对应关系见图13。
4.动力位
X线片:可判断滑移的活动性,对评估有无腰椎不稳价值较高(图14)。腰椎不稳的X线诊断标准包括:动力位X线片椎体之间向前或向后位移>3mm或终板角度变化>15°;正位片上侧方移位>3mm;相邻终板角度>5°。
(二)CT及三维CT扫描
1.腰椎滑脱CT扫描的特征性表现为
(1)椎体双边征:椎体后缘与下位椎体后缘出现在同一层面上,两条弧带状平行于椎管前(图15A)。
(2)双椎管征:骨性椎管前后径增大,横径相对缩小,椎管近于“葫芦状”改变(图15B)。
(3)峡部裂隙:峡部裂隙在CT诊断中应当注意与关节突关节面区别:关节突位于椎间盘水平,小关节突的骨性关节面光滑、平行,关节间隙宽窄一致,宽约2~3mm;峡部裂位于椎弓根下缘层面,表面粗糙,裂隙3~8mm,锯齿状或不规则形,其走行与水平方向夹角较小(图15C)。
此外,由于腰椎滑脱患者多合并退行性改变,因此还存在以下表现:
(4)关节突病变:关节突的骨皮质局限性增厚、变形,严重时呈小丘状或不规则状的高密度骨性突起的骨赘,如蘑菇帽状“包绕”下关节突。关节面明显呈矢状位,关节面粗糙、边缘硬白,关节面下囊性变;关节间隙呈非均匀或均匀变窄,甚至消失,关节紊乱、脱位,关节腔内出现真空现象。
(5)椎间盘变性改变:滑脱节段可同时存在椎间盘突出、钙化等。
(6)椎体病变:椎体边缘唇棘样骨质增生、骨质疏松、许氏结节形成等。
(7)周围韧带病变:前纵韧带、后纵韧带、黄韧带的钙化、肥厚。
(8)椎管、椎间孔及侧隐窝变窄。
2.三维CT重建
A
B
C
D
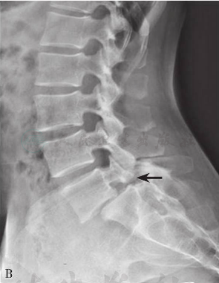
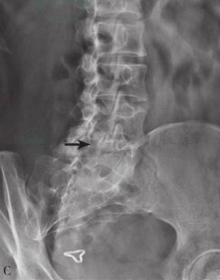
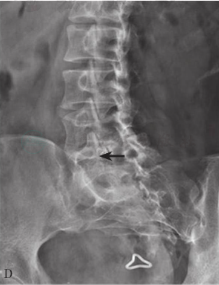
图12
腰椎正位X线片(A图)可见滑脱的椎体高度减小,骶骨平面可见“拿破仑帽”征,黑色箭头所示为L5棘突与L4棘突之间撞击形成的“假关节”。腰椎侧位X线片(B图)可见L5椎体向前滑脱Ⅱ度,黑色箭头所示为椎弓根峡部断裂。腰椎左右斜位片可见(C和D图),L5峡部断裂(黑色箭头所示)
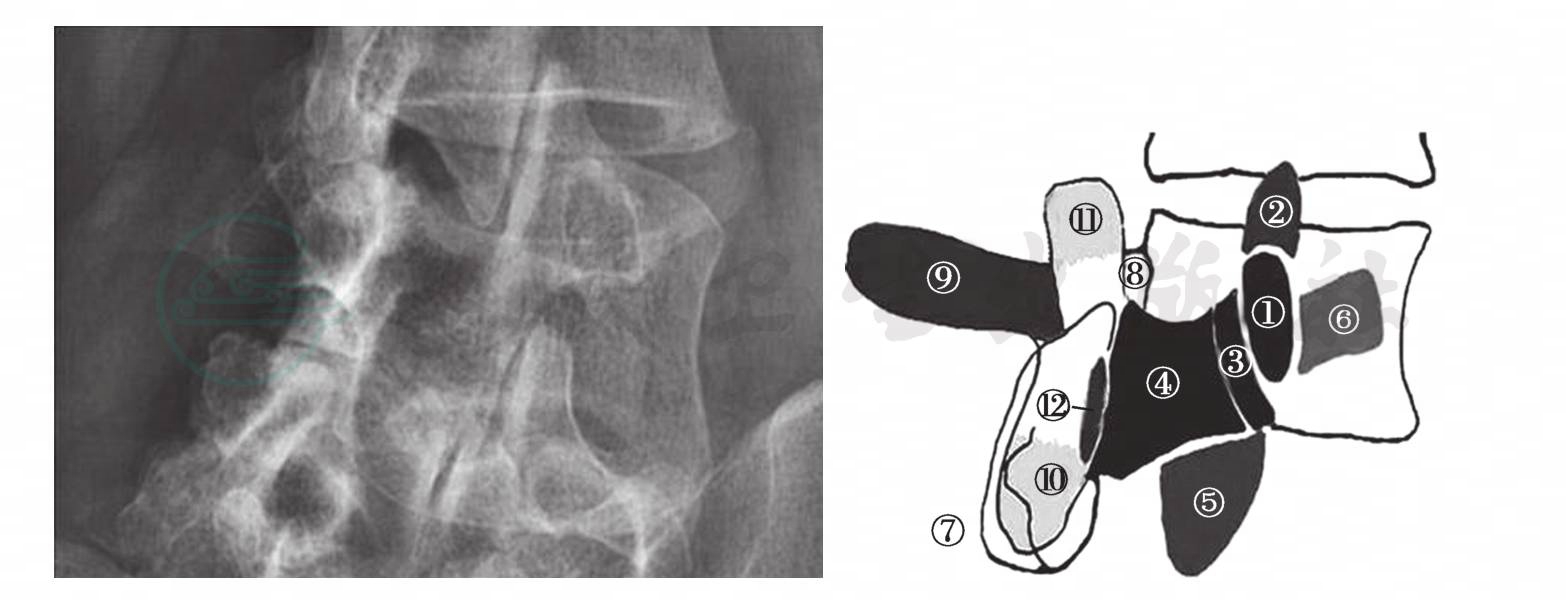
图13
左图为正常腰椎斜位X线片,关节突及椎板呈“小狗”形状。右图为示意图,标识影像学部位所代表的解剖结构:1.椎弓根(右侧);2.上关节突(右侧);3.峡部(右侧);4.椎板(右侧);5.下关节突(右侧);6.横突(右侧);7.棘突;8.椎板间隙;9.横突(左侧);10.下关节突(左侧);11.上关节突(左侧);12.椎板(左侧)
三维重建对椎体滑脱程度的测量较X线片更精确,对椎弓峡部裂的检出率可达100%,尤其对合并腰椎侧弯或旋转者较常规CT扫描显示更为准确,还可以明确椎间孔的变化(图16),便于临床制订完善的手术方案。
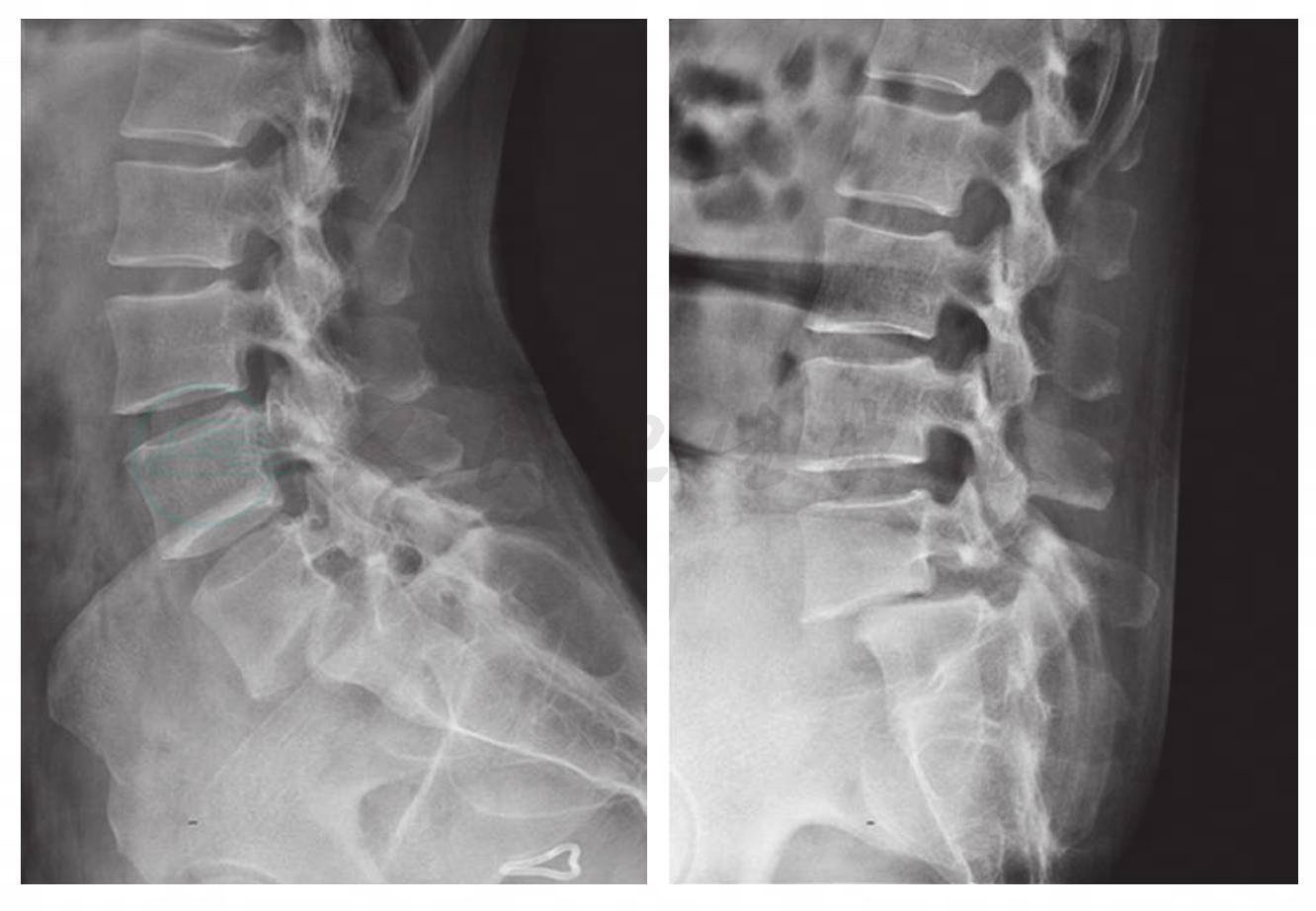
图14 腰椎滑脱动力位X线片
图中可见,腰椎屈伸活动过程中滑脱程度无明显改变
A
B
C
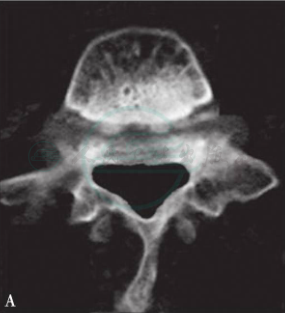
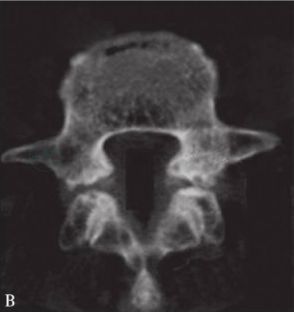
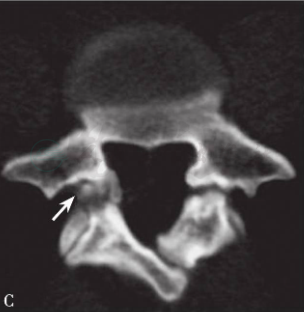
图15 腰椎滑脱节段的水平面CT图像
A图显示为同一层面中椎体呈现“双边征”。B图显示为椎管矢状径延长,椎管呈“葫芦状”。C图显示为峡部骨折,白色箭头所示为增生的骨痂,左侧峡部裂处呈“锯齿状”,走行方向接近水平
三维CT表现可归纳为两个方面:
(1)腰椎峡部裂:关节突间骨性缺损,边缘不整伴骨质增生(图17)。
(2)腰椎滑脱:同层面椎管前后径延长,椎间孔形态改变,椎间孔高度降低,前后方宽度增加。椎间盘假性膨出征和夹心征。假性椎间盘膨出有明显方向性,呈前后方向,一般不向侧方突出。
(三)磁共振检查
腰椎滑脱患者行MRI检查主要有两个作用:①MRI可以显示毗邻节段椎间盘退变情况,明确腰背部疼痛是否与毗邻节段椎间盘退变有关,从而确定融合节段;②对于表现为腰部神经根症状的患者,MRI有助于明确神经根受压的部位和原因,从而制订减压的方案。
对于峡部裂型腰椎滑脱,由于椎间孔高度下降以及椎间盘突出的联合作用,神经根受压多位于椎间孔处及峡部裂前下方。偶尔也可见滑脱合并椎间盘突出引起神经根压迫(图18)。对于峡部裂型腰椎滑脱,中央椎管扩大,因此通过正中矢状位MRI判断椎管前后径是否增加,有助于精确鉴别峡部裂性滑脱与退变性滑脱。
磁共振T2加权像可显示椎间盘的含水情况及终板的水肿情况。在成人峡部裂性腰椎滑脱中,椎间盘的退变多发于峡部骨折的节段。而正常成人椎间盘的典型影像是T2加权像上呈现为白色,并在中央有低信号的细小裂隙影,椎间盘非对称性变薄提示椎间盘有脱水和退变。
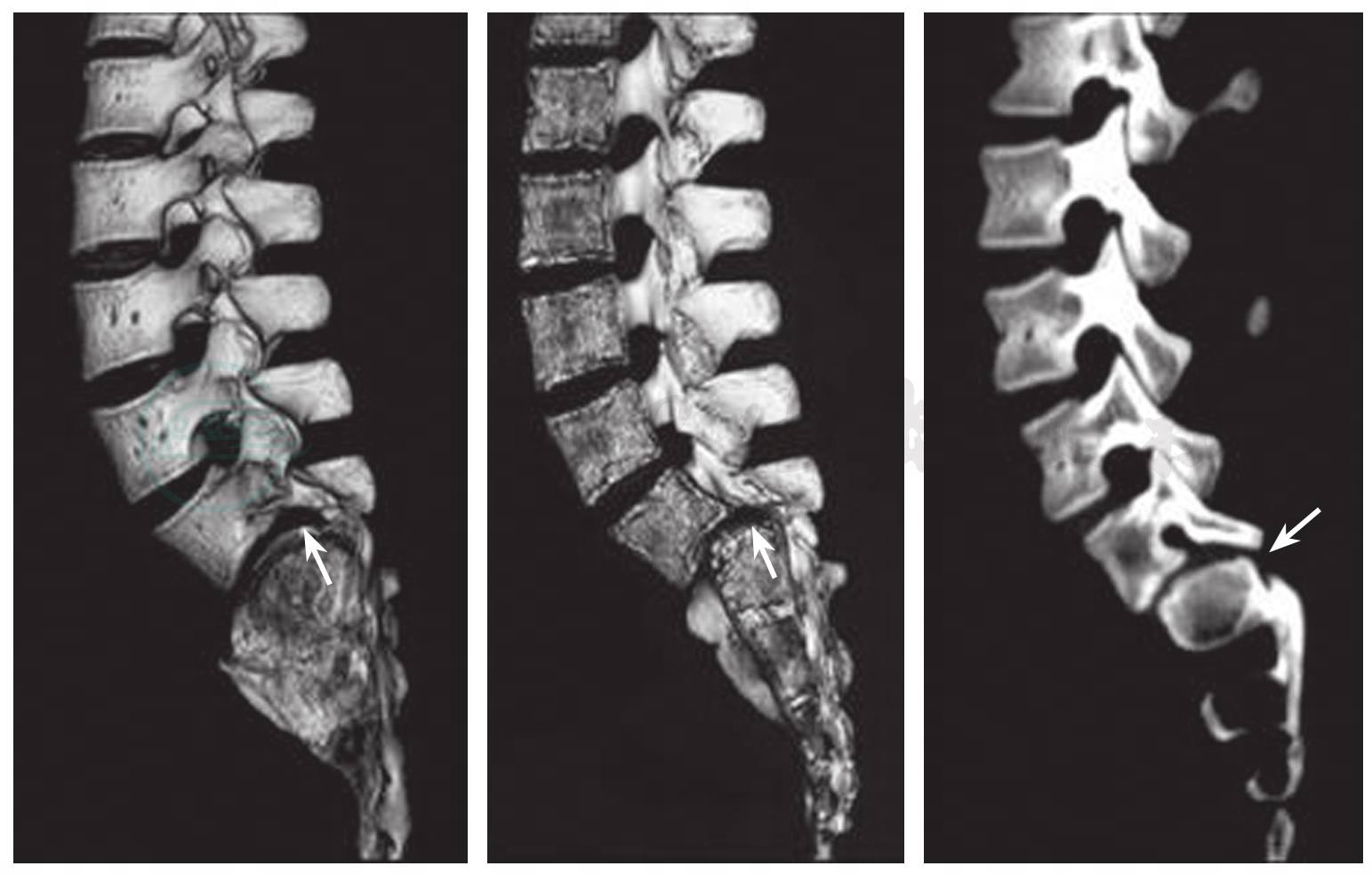
图16
L5S1滑脱的三维CT图像,可见L5椎间孔高度显著降低,L5S1关节突发育异常(白色箭头所示)
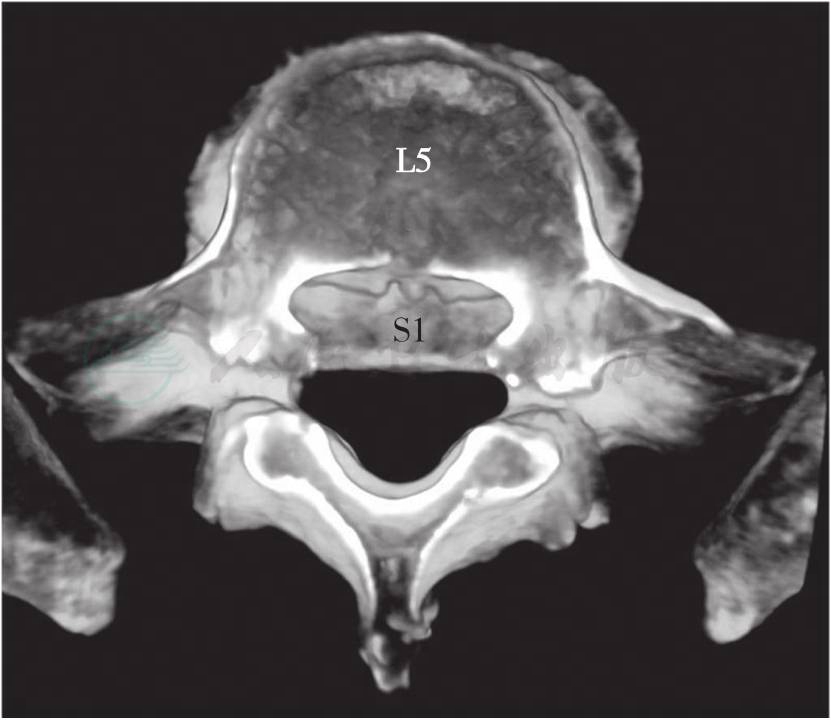
图17
L5S1滑脱的三维CT图像,可见L5双侧峡部断裂
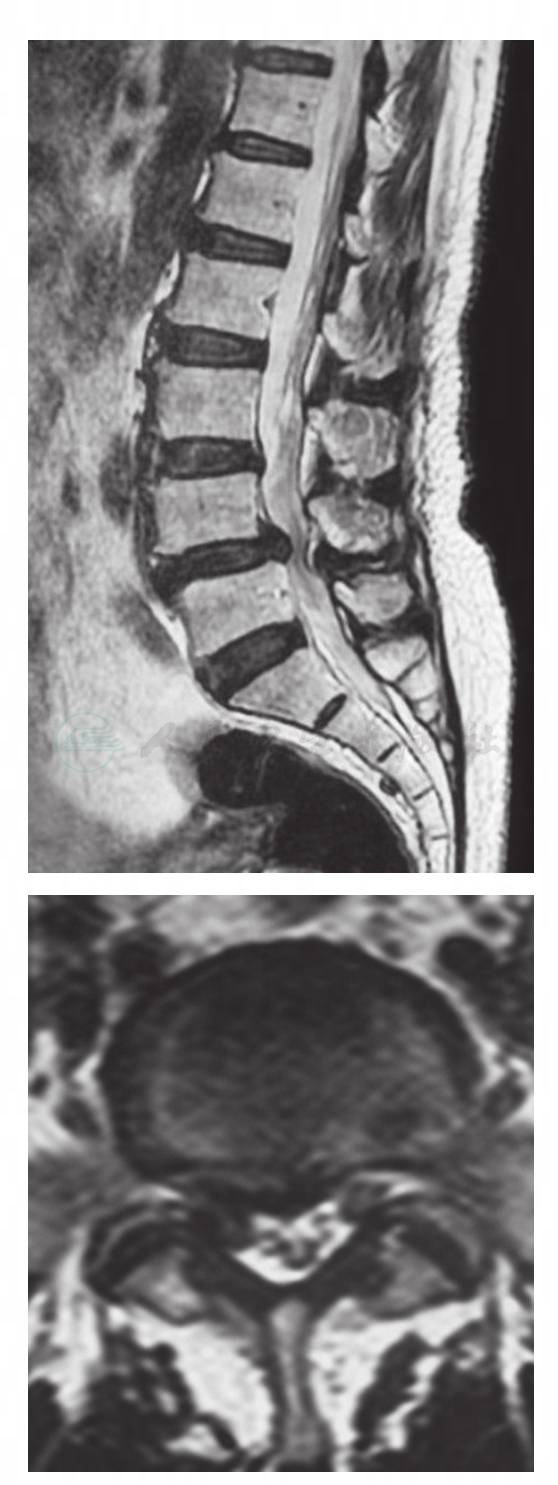
图18 腰椎滑脱伴椎间盘突出
矢状位MRI示:L4~5滑脱伴椎间盘突出。轴位MRI示:L4~5椎间盘中央偏右侧突出,压迫右侧L5神经根
(四)同位素骨扫描
同位素骨扫描有助于确诊年轻患者的急性峡部骨折及隐性峡部骨折,尤其是对于X线片中无明显峡部骨折的运动员患者。采用锝元素的同位素骨扫描还有助于成人轴性腰痛的鉴别诊断,如骶髂关节炎导致关节面硬化而出现牵涉痛,其症状与峡部裂及小关节突病变的疼痛症状相似。此外,小关节突关节炎、急性骨折、即将出现的峡部骨折、肿瘤、感染和代谢性骨病,均可通过骨扫描进行诊断。
尽管同位素骨扫描对于腰椎滑脱的诊断并不是必须的,但这一检查有助于排除其他可能导致相似症状的疾病。
(五)椎管造影
椎管造影是一种有创检查,目前已经很少应用于腰椎滑脱的诊断。
临床上有相当一部分腰椎滑脱患者终生无腰痛症状,无需治疗。 Wiltse等认为,绝大多数有低度腰椎滑脱(Ⅰ、Ⅱ度)但无明显临床症状的成人患者可采取非手术治疗。2010年Denard报道的大样本、多中心、流行病学研究结果显示,与正常男性相比,腰椎滑脱患者的严重腰背痛及其引起活动受限的发生率并未显著增加,获得性腰椎滑脱患者的慢性腰痛的程度及类型与正常人无实质性差异,但是腰椎滑脱患者出现根性疼痛、感觉异常及下肢无力的百分率明显增高。
一、非手术治疗
并非所有存在腰痛的腰椎滑脱都需要手术,多数患者对非手术治疗有效。对有腰痛症状的腰椎滑脱患者,首先应明确其疼痛的部位及性质,判断其疼痛是否与滑脱有关,因为与滑脱部位相邻椎间盘的变性、小关节病变或软组织损伤等都可导致腰痛。因此,应针对腰痛原因进行对症治疗或试验性治疗,如制动、理疗、关节突封闭、硬膜外激素注射等。但是,非手术治疗不能改变解剖和自然病程。它的目的是减轻疼痛,防止疼痛反复发作,恢复功能以及改善患者的生活质量。
(一)适应证
1.单纯峡部裂患者,无明显滑脱。
2.青少年L4椎体轻度滑脱,无L5骶化。
3.轻度腰椎滑脱患者,无神经症状。
4.年龄大、体质差患者,无法耐受手术。
多数的轻度峡部裂性腰椎滑脱患者并无症状,即使存在症状如根性痛、下腰痛,或两者兼有,采取非手术治疗仍然能够获得良好的效果,很少需要手术。
(二)治疗方法
儿童及青少年轻度滑脱若无症状只需密切观察。对于Ⅱ度滑脱的患者,建议避免进行对抗性运动以及需要腰椎过伸的运动,如体操等。采用改变运动方式、物理治疗和支具保护等非手术治疗措施后,大多数患者的症状会改善。非甾体抗炎药以及慎重使用的麻醉剂、肌肉松弛剂能够控制疼痛。局部的物理治疗包括加强腹部力量、提高躯干稳定性和拉伸腘绳肌和髋部屈肌。同时需要强调身体姿势以及正确提拉重物技巧的重要性。非手术治疗计划也应当包括有氧运动。对于接受物理治疗症状无明显改善的患者,有人认为可以尝试采取硬膜外类固醇激素注射、选择性神经阻滞和小关节注射。表3中为目前常用的非手术治疗方法。非手术治疗6个月以上无效的患者应考虑手术治疗。
表3 腰椎滑脱的非手术治疗方法

二、手术治疗
经过充分非手术治疗仍存在顽固性下腰痛,伴有或不伴有下肢症状以及下肢根性症状是外科手术治疗的指征。滑脱进展的风险取决于多种因素,滑脱的类型不同、程度不同会导致患者滑脱进展的风险也不相同。青少年先天性腰椎滑脱的进展速度取决于局部解剖缺陷程度、腰椎滑脱节段以及腰椎滑脱的严重程度。
(一)适应证
1.双侧峡部裂并有明显腰痛患者。
2.青少年患者
滑脱大于Ⅱ度,合并或不合并临床症状。
3.成人患者
滑脱Ⅰ~Ⅱ度,非手术治疗不能缓解疼痛症状。
4.腰椎滑脱大于Ⅲ度。
5.腰椎滑脱伴发腰椎间盘突出或腰椎管狭窄,合并神经症状。
(二)手术的关键问题
1.神经减压
神经彻底减压是确保手术疗效的关键环节,是解除临床症状的主要手段。轻度腰椎滑脱是否需要进行神经根减压尚存争议。对于重度滑脱多数作者主张进行神经减压。减压范围应当包括黄韧带、椎间盘、增生的关节突、侧隐窝,尤其要注意去除峡部裂处增生的纤维组织及骨痂,解除神经压迫。减压除了可以解除硬脊膜和神经根的压迫外,还有利于滑脱复位。但由于减压后破坏腰椎后柱结构,削弱脊柱稳定性,故应同时进行脊柱融合术。
2.复位及内固定
目前国内外大部分学者认为原则上应尽量争取复位及内固定;如不能完全复位,部分复位亦可。文献报道,采用脊柱原位融合术治疗各种程度的腰椎滑脱能够获得较满意的临床结果。
但是,由于原位融合无法纠正脊柱畸形,在未使用内置物情况下,会存在如下缺点:①假关节形成;②活动节段丢失;③滑脱进行性加重;④神经功能缺失;⑤残存畸形。鉴于以上原因,大多数医师并不能接受原位融合,而倾向于进行复位内固定手术。随着脊柱器械的发展,对严重滑脱者复位已不是难题。
复位内固定的优势在于:
(1)预防畸形进展:良好的滑脱复位能够纠正滑脱角,改善腰骶部力学异常,重新获得新的躯干平衡,消除滑脱进展的力学因素。同时,腰骶部负重力线的改善也能够减少作用于脊柱内置物上的前屈载荷,增加脊柱内置物的稳定性,提高脊柱融合率。
(2)减轻术后疼痛:有效的内固定可以消除脊柱屈曲的不稳定,从而减轻了脊柱融合术后早期行走而产生的腰背痛。
(3)有利神经减压:在对神经进行彻底减压时,使用内固定可不必担心会由此造成脊柱的不稳定或进一步滑脱的可能。
(4)促进植骨融合:滑脱复位可重建躯干在骶骨上的中心轴线,通过恢复腰骶间隙的轴向负荷,显著降低植骨块的前移趋势,提高融合率。
(5)减少融合节段:采用复位及脊柱内置物矫正腰椎滑脱畸形时,能够使融合仅局限于滑脱的节段,而不必要融合更多的节段。但是,目前对于融合节段的选择仍然存在争议,通常认为重度的L5S1滑脱,融合应包括L4与骶骨。
(6)恢复腰骶力线:纠正腰椎滑脱能够恢复身体正常的力线和形态。重建躯干力线及高度能够改善椎旁肌和腹肌的长度与张力关系,缓解肌肉疲劳。
(7)改善体型步态:腰椎滑脱的复位能够改善患者的外形:纠正臀部后翘能够改善腰臀部轮廓、消除蹒跚步态和胸廓突出;躯干高度的恢复消除了腹部皮褶、重建了身体比例及增加了患者身高,有利于患者获得良好的心态。
3.植骨融合
获得滑脱节段牢固的脊柱融合是手术的最终目的。随着对腰椎滑脱认识的不断深入和手术技术、器械的不断进步,出现了不同的融合方法及术式。融合术可分为前路融合、后路融合及前后联合手术;按植骨融合部位分为峡部修补、椎板植骨融合、椎体间融合、侧后方植骨融合术。不同的融合方式,有着不同的手术适应证,也有不同的优缺点,临床医师应谨慎根据患者个体情况及自身的手术熟悉程度进行选择。
三、常用手术方法
腰椎滑脱的手术方式非常多,但无非是神经减压、复位固定和脊柱融合。数十年来,大量的学者报道了不同术式治疗腰椎滑脱的临床结果,但由于缺乏严格的随机对照研究,因此并未形成“金标准”式的手术方式。选择手术时,应考虑患者的主诉、既往史、体格检查和影像学表现等因素。解除患者症状、完成滑脱节段的骨融合,是手术治疗的最终目的。
(一)峡部裂修复术
1.直接修复术
直接修复峡部可以保存腰椎的活动度,恢复其正常的解剖结构。1968年,Kimura最早提出峡部裂修复手术,去除峡部纤维增生组织,直接植骨,以达到峡部裂骨融合的目的。
2.单枚螺钉固定技术
1970年,Buck改进固定方法,暴露椎弓峡部后采用一枚拉力螺钉横穿峡部裂并植骨,获得83%~94%的愈合率。此后,有学者采用椎弓根螺钉和棘突钢丝对这项技术进行改良(图19)。
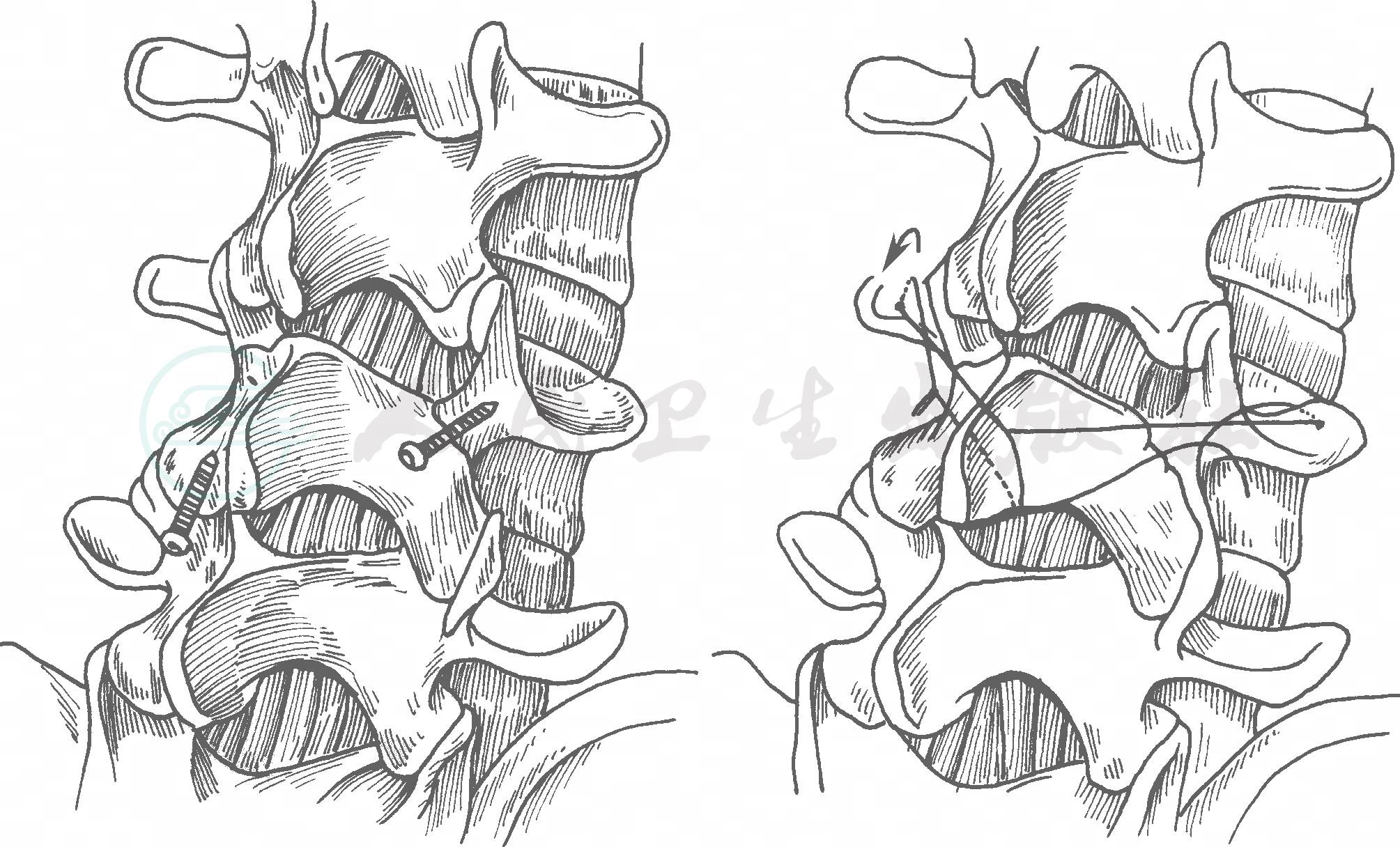
图19 拉力螺钉固定法和棘突钢丝固定法示意图
3.椎弓根螺钉联合椎板钩技术
这是目前最常用的峡部裂修复技术(图20)。
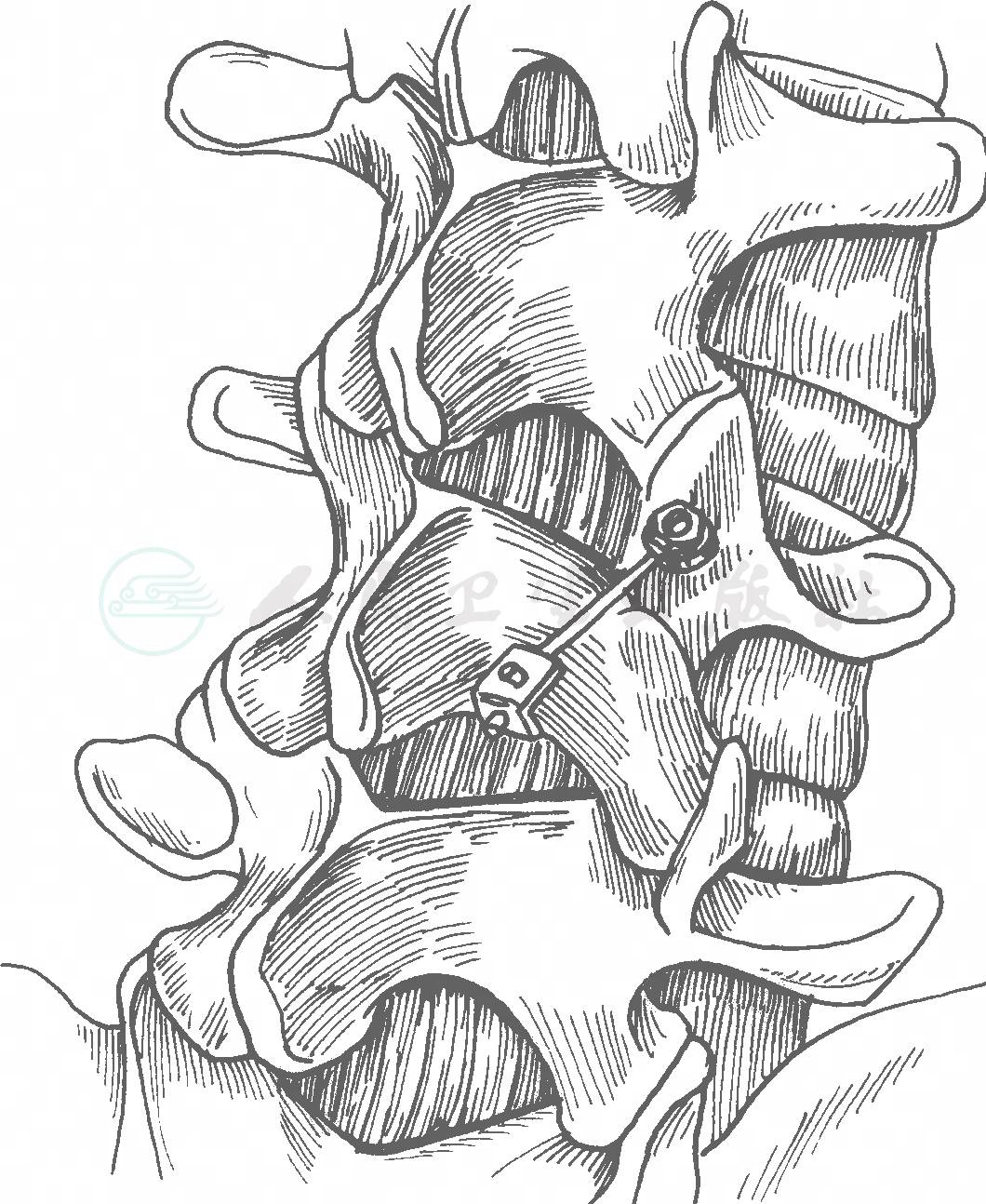
图20 椎弓根螺钉联合椎板钩技术示意图
手术适应证:单纯峡部裂或峡部裂合并轻度滑脱,无神经根症状;磁共振显示椎间盘信号正常的青少年患者。
手术禁忌证:成人患者以及磁共振显示椎间盘退变的患者。
手术要点:清理峡部裂处纤维骨痂,采用自体骨或人工骨在峡部裂处植骨,椎弓根螺钉及椎板钩对上下关节突两端进行加压,缩小峡部裂间隙,促进峡部裂愈合。
手术注意事项:
(1)由于不做椎体间融合,因此在显露过程中要避免损伤关节突关节囊。
(2)进行峡部裂修复时需要特别注意椎间盘及小关节突的质量。退变性椎间盘疾病本身存在脊柱不稳及异常活动,会导致早期小关节突退变、骨赘形成及异常活动。因此,如果存在明显椎间盘退变,不能采用峡部直接修复术。
(3)部分轻度的L5S1峡部裂患者可合并隐性脊柱裂,对这些先天性缺损或后部结构缺损进行直接修复,可能十分困难,需特别注意。
(4)术后腰骶部支具保护,时间为3~6个月,定期X线及CT扫描随访,观察峡部裂的愈合情况。
(二)后路神经减压、滑脱复位内固定、植骨融合术
1.神经减压
神经彻底减压是确保手术疗效的关键环节。应根据具体的病理情况,采用开窗、半椎板切除或全椎板切除,对神经进行减压。
2.复位内固定
(1)后路椎弓根螺钉复位技术:对于腰椎滑脱,目前最常用的复位技术是椎弓根螺钉复位技术。通过在滑脱椎体上置入提拉复位螺钉,对滑脱节段进行撑开、提拉,达到复位的目的。
以L5S1滑脱为例,椎弓根螺钉复位技术包括4个步骤:①在L5、S1椎体上置入椎弓根螺钉,必要时在L4椎体上也置入螺钉;②切除退变的L5S1椎间盘;③安装预弯的固定棒,行L5S1间隙撑开,行椎体间融合;④逐渐锁紧L5提拉螺钉螺帽,使滑脱椎体逐渐复位;⑤L5S1节段间进行加压,行后路植骨融合。
典型病例一(图21)
典型病例二(图22)
A
B
C
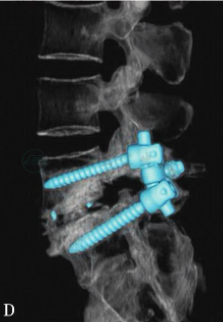
D
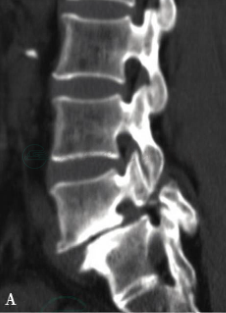
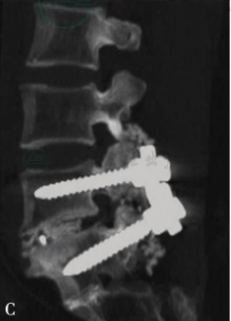
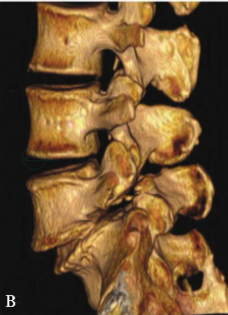
图21 57岁,女性,主诉下肢神经源性跛行和下腰痛
三维CT重建显示L5椎体双侧峡部裂,Ⅱ度滑脱(A,B)。行L5至骶骨椎板切除减压、滑脱复位、椎体间及后外侧植骨融合、椎弓根螺钉固定术。术后三维CT重建显示双侧L5及S1椎弓根螺钉位置良好(C,D),滑脱复位效果明显,术后患者跛行及下腰痛症状改善
(2)后路撬拔复位技术:重度腰椎滑脱常伴有不同程度的椎体倾斜和脊柱高度的丢失,因此单纯依靠后路钉棒系统进行复位较为困难。为了获得必要的高度和腰椎前凸,临床医师采用了许多复位方法,如骨折牵引床复位、临时撑开棒等。Schollner发明了后路撬拔复位技术,Steffee 在20世纪80年代末将此方法进行推广。
以L5S1滑脱为例,后路撬拔复位技术有5个步骤:①切除L5椎板和L5S1椎间盘,如复位困难,可考虑脊柱短缩,切除骶骨穹隆;②用一个放置于L5S1椎间隙的杠杆(Cobb剥离器)将L5撬起以达到撑开目的;③通过固定棒或钢板和提拉螺钉将滑脱复位;④后路行椎体间融合(PLIF)以获得前方稳定,并行后外侧髂骨融合;⑤椎弓根钉固定。
典型病例三(图23)
(3)膨胀螺钉技术:腰椎滑脱患者主要为中老年患者,其中多数合并有骨质疏松。骨密度对椎弓根螺钉固定的稳定性具有重要影响,力学实验证实,椎弓根螺钉的拔出强度、扭矩与BMD之间存在着明显的正相关。因此,对骨质疏松椎体进行滑脱复位,螺钉松动的风险更高。
提高骨质疏松椎体上螺钉固定强度的方法,除了使用更粗更长的螺钉以外,还可以通过改善手术操作的细节,如:
1)上移螺钉进钉点:将进钉点向椎体的头侧移动,使螺钉沿椎弓根上缘走行,使螺钉螺纹切入更多的椎弓根皮质骨和椎体上终板下优良的松质骨。
2)增加螺钉内倾角度:增加螺钉内倾角度可以延长钉尖与椎体前缘皮质的距离,从而增加相应螺钉的长度,提高螺钉固定强度。同时,连接固定棒及横连后,内倾角度大的内置物框架结构稳定性显著高于采用平行植入的框架结构。
3)避免螺钉平行植入:与增加内倾角的力学原理类似,非平行置钉也能够提高螺钉稳定性。最理想的螺钉位置是螺钉在位于椎弓根及椎体内的前提下,上位螺钉适当向上倾斜靠近椎体上位椎板、下位螺钉适当向下倾斜靠近椎体下位椎板,这更符合力学平行四边形法则,并可减少螺钉承受的弯折剪力。
A
B
C
D
E
F
G
H
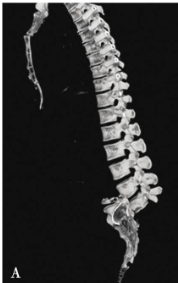
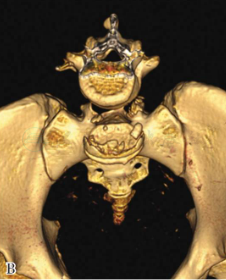
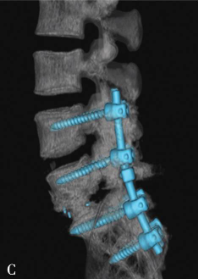
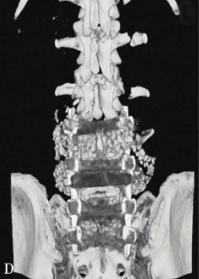
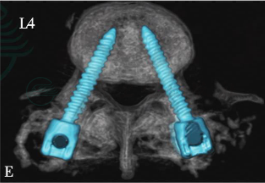
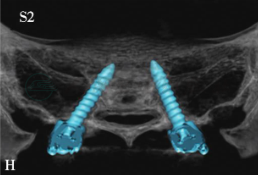
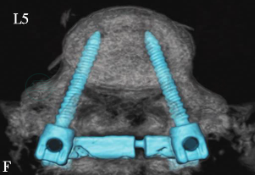
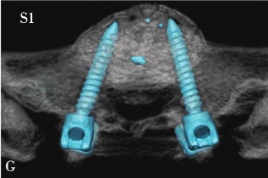
图22 35岁,女性患者,外伤后下腰部疼痛,大小便功能障碍
三维CT重建显示L5椎体完全脱位伴L5椎体及骶骨骨折(A,B)。行L4至S2后路椎板切除减压、后外侧植骨融合、椎弓根螺钉固定术。术后三维CT重建显示完全脱位的L5椎体复位良好 (C,D),双侧L4、L5、S1及S2椎弓根螺钉位置良好(E-H),术后患者下腰痛症状明显缓解,大小便功能改善
A
B
C
D
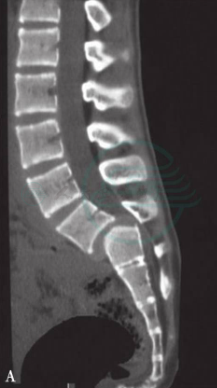
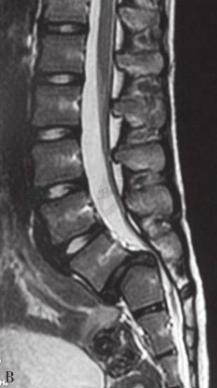
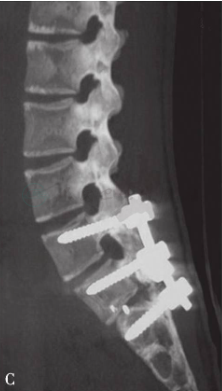
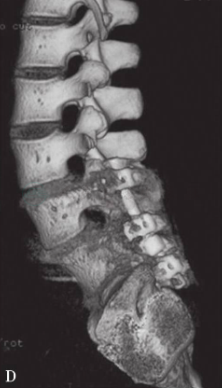
图23 14岁,女性患者,持续性腰痛2年
三维CT(A图)及MR(B图)显示L5S1Ⅲ度滑脱。采用后路撬拨技术进行滑脱复位、椎体间及后外侧植骨融合、椎弓根螺钉固定术。术后三维CT(C,D图)显示腰椎滑脱完全复位
4)避免攻丝及重复置钉:攻丝植入的螺钉的拔出力较非攻丝螺钉的有显著降低,因此,对于骨质疏松椎体,尽量避免攻丝。重复置钉是导致螺钉松动的重要原因之一。改变进钉点、修正钉道方向等手术操作均会严重破坏钉道周围骨质完整性,导致螺钉的松动失败。即使在不改变钉道方向的情况下,取出原有螺钉后重新植入也将明显降低螺钉的抗拔出力下降。
但是,对于骨质疏松较为严重的患者,单纯使用上述方法提高螺钉稳定性的效果有限,则需要使用特殊结构的椎弓根螺钉——膨胀式椎弓根螺钉。
膨胀式椎弓根螺钉能够在不增加椎弓根处螺钉直径的基础上,使椎体内部分螺钉直径增加,达到提高把持力的目的。
典型病例四(图24)
A
B
C
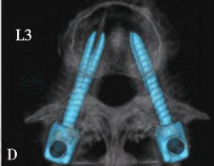
D
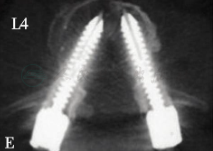
E
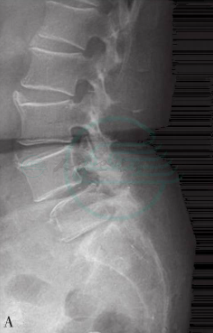
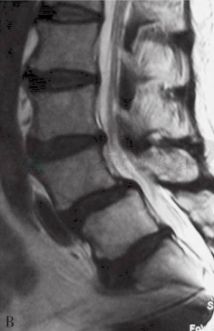
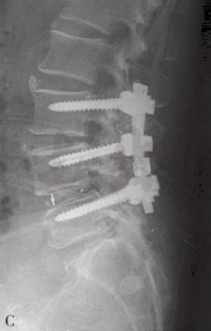
图24
60岁,女性,入院诊断为:术前X线(A)及MR(B)显示:L3~4椎间盘突出、L4~5腰椎滑脱。双能X线吸收骨密度测量结果表明,患者合并骨质疏松症。患者行L3~4、L4~5至S2后路椎板切除减压、后外侧植骨融合、膨胀式椎弓根螺钉固定术。术后X线及三维CT重建显示腰椎滑脱完全复位(C),膨胀螺钉在体内完全膨胀,位置良好(D、E)
3.植骨融合术
目前,植骨融合术包括椎体间融合术及后外侧融合术。椎体间融合术包括后路腰椎间融合术、经椎间孔椎体间融合术、腰椎极外侧椎体间融合、前路椎体间融合以及轴向腰椎椎间融合术。后外侧融合术:参见椎板及横突间融合技术章节。
(1)后路腰椎间融合术(PLIF):手术要点:显露脊椎并植入椎弓根钉;切除融合节段黄韧带上下各1/2椎板,并向两侧切除小关节内侧1/2部分;显露硬膜囊、椎间盘及神经根,行椎间盘切除术;植入椎体间融合器并进行加压固定。如果是一侧神经症状,可行单侧椎板间扩大开窗,行后路PLIF(图25)。
优点:PLIF可以通过一个手术切口,同时完成椎间融合术和椎管减压术。通过后外侧植骨和后路内固定系统,PLIF可以获得腰椎的三柱融合。
缺点:术中需要将神经根和硬膜牵拉过中线,可能造成神经根损伤。
(2)经椎间孔椎体间融合术(TLIF):考虑到PLIF对神经根及硬膜牵拉过多,容易造成神经损伤,Harms等提出了经椎间孔入路的腰椎椎体间融合术(图26)。
手术要点:显露脊椎并植入椎弓根钉;切除融合节段的少量椎板及所需减压侧的下关节突和上关节突上部;显露椎间隙的外侧1/3硬膜囊和走行的神经根,行椎间盘切除术;植入椎体间融合器及植骨,同时椎体间加压固定。
优点:减少过度牵拉神经根,损伤硬膜的风险;能够经后方一侧入路即可完成椎间融合,保留了前纵韧带和大部分后纵韧带的完整性;避免了椎板切除和对椎管的干扰,防止术后管内瘢痕组织形成。为了进一步减少对椎旁肌肉的剥离损伤,Wiltse提出采用旁正中入路进行椎管加压及椎体间融合术。(图27)
缺点:破坏一侧的关节突关节
(3)前路腰椎椎间融合术(ALIF):
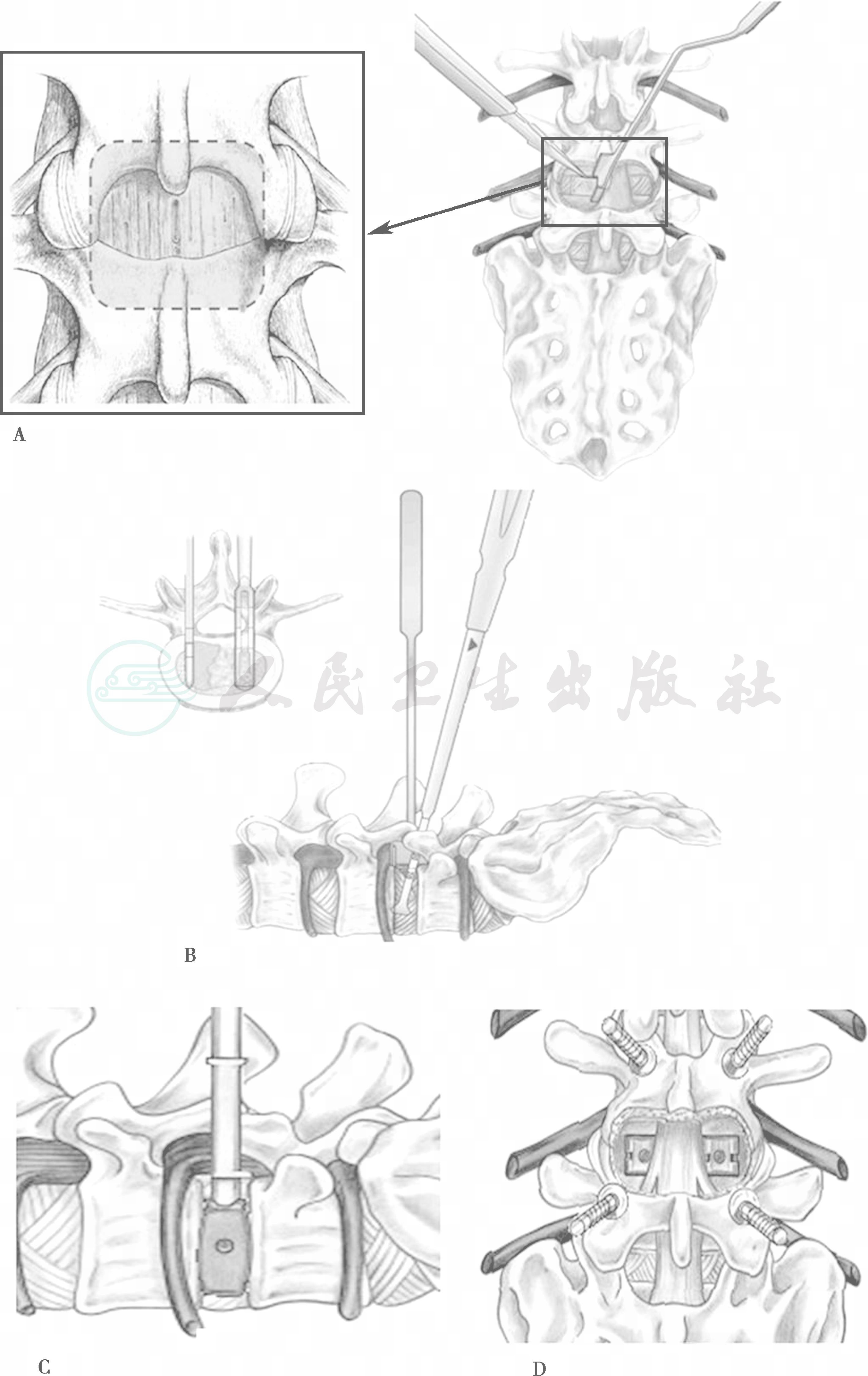
图25
A. PLIF手术的减压范围;B.刮刀处理终板;C.放入椎体间融合器;D.完成椎管减压及椎体间融合

图26
A.显露椎板,置入脊柱螺钉;B和C对减压间隙进行适度撑开;D.切除一侧关节突行椎管减压;E.刮除椎间盘;F.刮刀处理上下终板;G和H分别放入椎体间融合器
与PLIF比较,ALIF更加适用于医源性腰椎后凸、PLIF术后失败及后路减压术后不稳等。ALIF手术入路包括:经腹膜途径,经腹膜外途径以及腹腔镜下前路融合。目前,腹腔镜经腹膜途径融合L5/S1已成为一种常用方式(图28)。
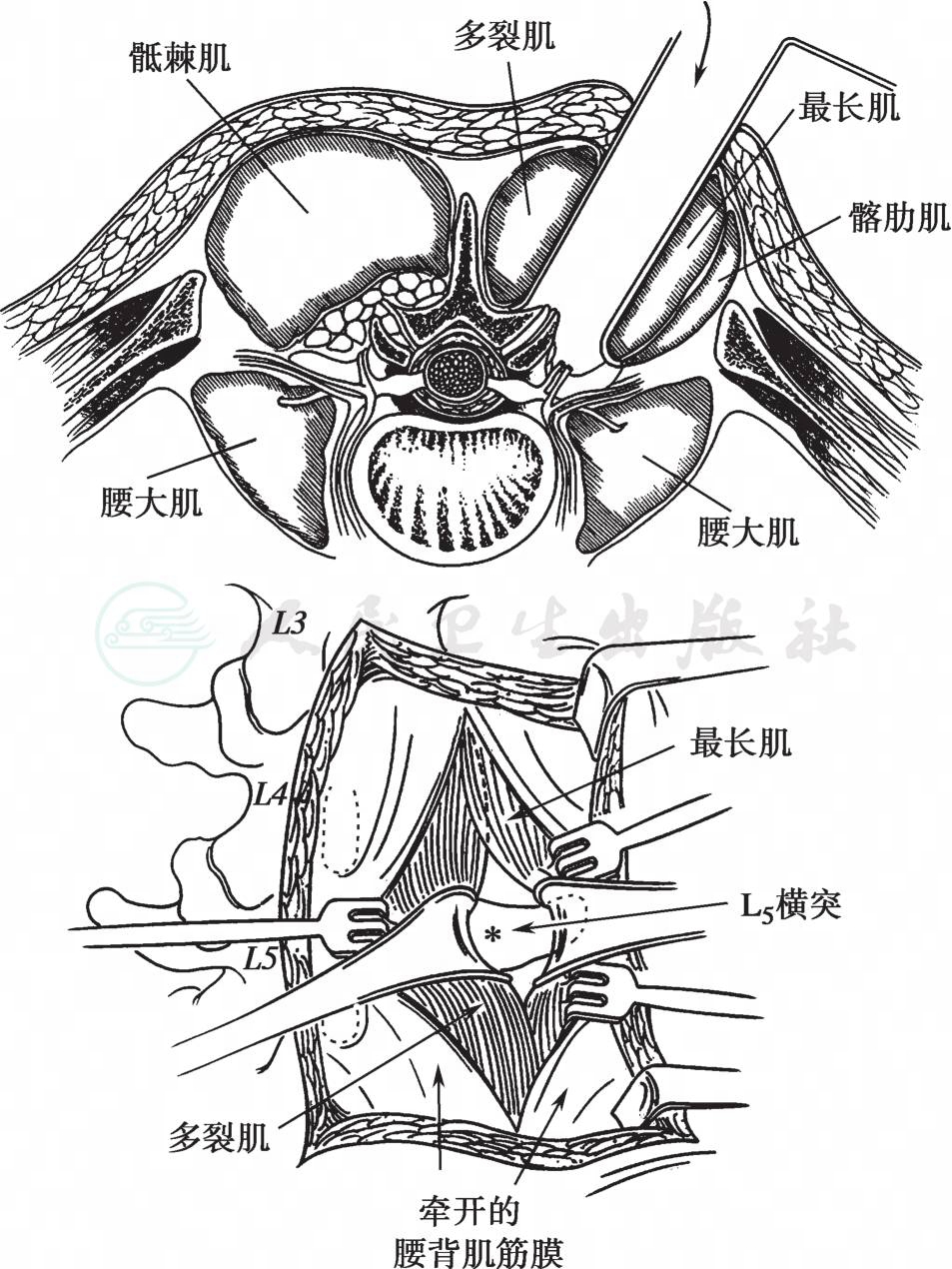
图27 Wiltse入路的解剖示意图
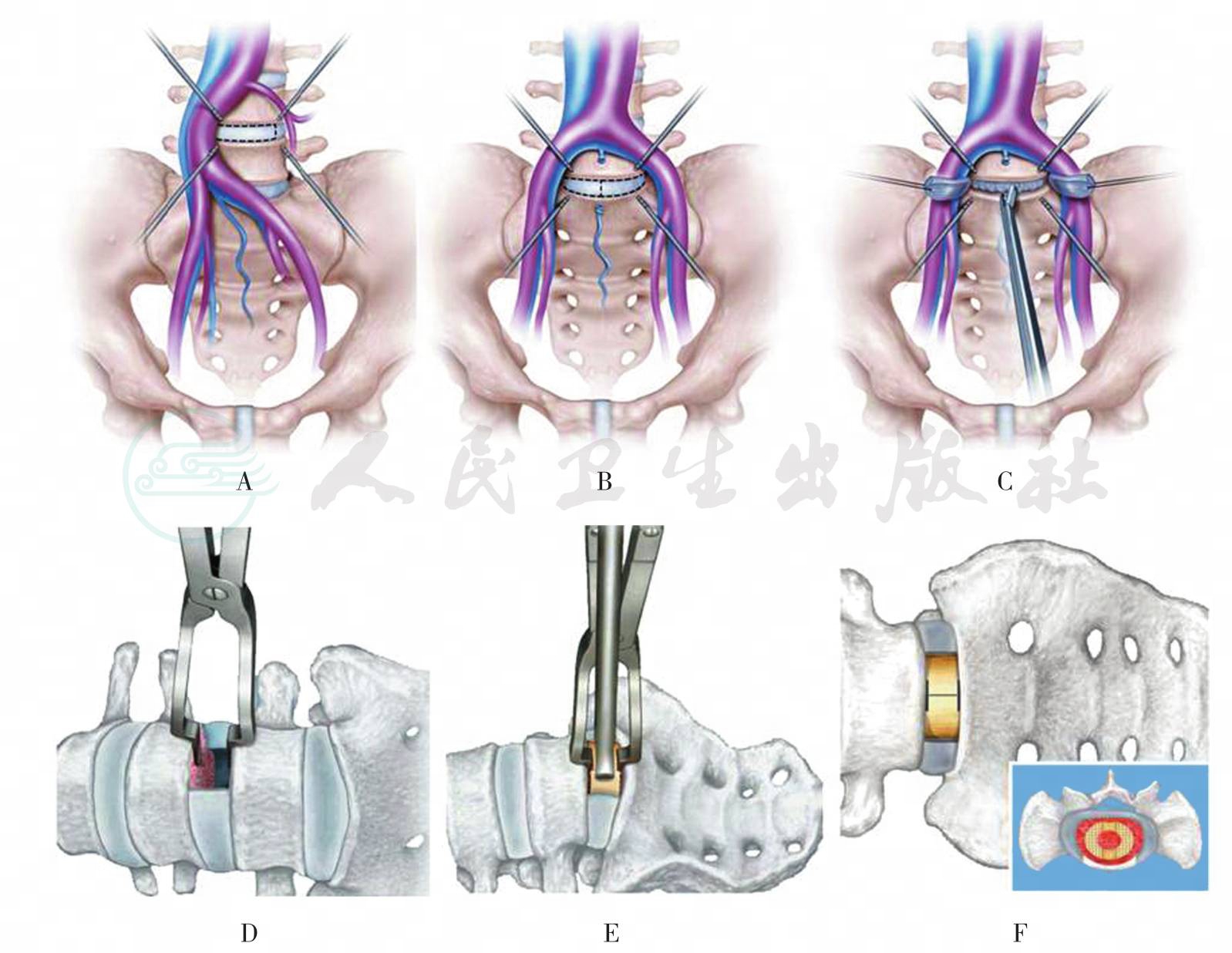
图28
A和B从前路显露L4/5或L5S1椎间盘;C.切除椎间盘及上下终板;D.模具测量椎间隙高度;E.置入椎体间融合器;F.完成前路椎体间减压术,根据需要置入前路钢板
手术要点:通过腹膜或腹膜外入路,显露腰椎椎间盘。分离保护腰骶前血管及神经丛,切除椎间盘,并行腰椎前路椎体间融合。
优点:能更有效地撑开和恢复椎间隙高度;手术视野清楚,切除椎间盘更彻底;无须牵拉硬膜和神经根,避免神经损伤;保持腰椎后部结构完整,最大限度的避免了手术造成的脊柱失稳。
缺点:可引起腹膜后器官、重要血管的损伤,对男性患者可能损伤上腹下丛神经,导致逆行射精。
(4)腰椎极外侧椎体间融合(XLIF):最早在2003年由Neilwright首次报道,是经外侧穿过腹膜后间隙和腰大肌到达腰椎的一种新的微创腰椎椎间融合技术(图29)。
手术要点:在后正中线患椎棘突与腋中线的水平线中点开口,腰肌前1/3或中间分离,并在脊髓电生理监测系统指导下分离血管、肌肉并显露并切除椎间盘;植入椎体间融合器行脊柱融合。
优点:手术创伤小,肌肉软组织剥离少;椎间盘显露充分,操作安全;不经腹膜腔、不需要分离大血管和神经丛,显著减少并发症的发生率。
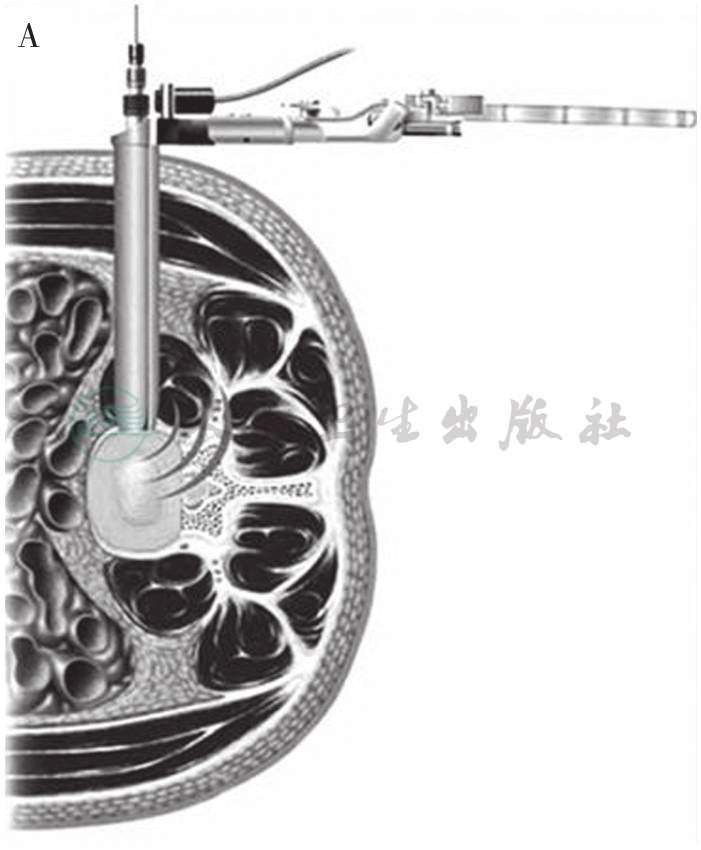
A
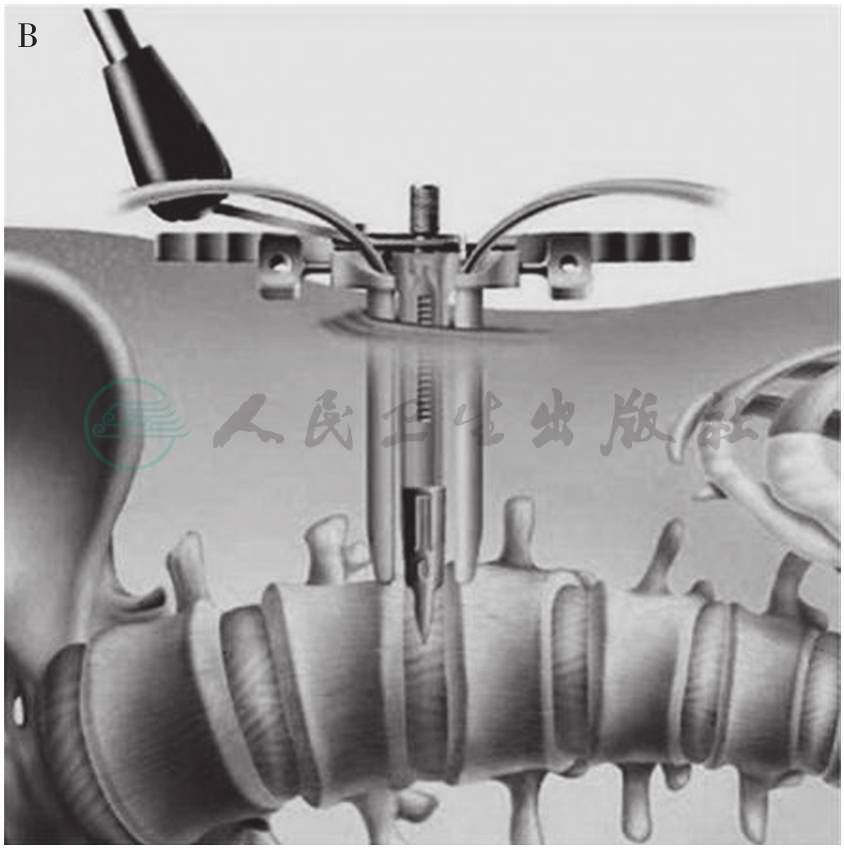
B
图29 XLIF的手术示意图
A.脊髓电生理监测系统监护下将工作套管插入到椎间盘侧方;B.腰椎取侧弯位,在工作通道内切除腰椎间盘,完成椎体间减压
缺点:切口受到第12肋下缘和髂嵴上缘的限制,显露L1-L2和L5-S1困难;分离腰大肌可能损伤腰丛神经,导致腰肌麻痹。
(5)轴向腰椎椎间融合术(AxiaLIF):2004年Andrew Cragg等人首次提出通过骶骨前间隙行L5S1间融合的崭新术式(图30)。
手术要点:通过特制的器械,经皮到达S1椎体前下方,再穿过S1椎体到达L5~S1椎间盘,最终到达L5椎体,然后形成一个工作通道,在这个工作通道中,完成椎间盘部分切除、植骨、撑开、椎间融合。
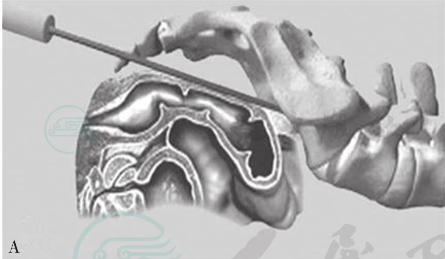
A
B
C
D
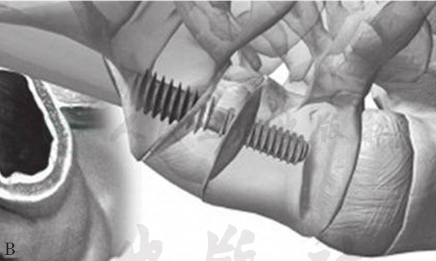
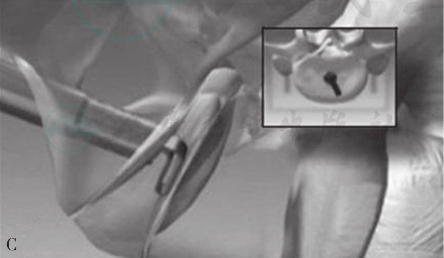
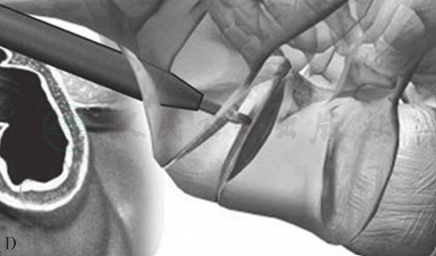
图30
A.透视下将探针引导至骶1椎体下方;B.通过特殊器械在骶骨上打孔,建立减压工作通道;C.切除L5S1椎间盘;D.将特制融合器钻入L5S1椎体内,完成椎体间融合
优点:切口小,操作简单,操作过程中不会产生失活组织和解剖死腔,感染的风险较小;无须牵拉硬膜和神经根,避免神经损伤;保持腰椎后部结构完整,最大限度地避免了手术造成的脊柱失稳;椎间隙的撑开高度可以任意选择;轴向融合的生物力学强度优于椎体间融合,有利于脊柱融合稳定。
缺点:伴有椎间盘突出时,不能同时处理;有损伤直肠、骶前血管神经的潜在风险;融合的远期效果有待进一步验证。
(三)腰5椎体切除术
L5椎体滑脱中最严重的类型脊柱前移,表现为L5整个椎体向前滑移至S1终板之下。由于复位困难及较高的神经损伤发生率,目前对于此类腰椎滑脱,主要采用L5椎体切除手术进行治疗,目的是恢复脊柱在矢状面的平衡,避免因复位时牵拉马尾神经和神经根引起的损伤。该手术在不改变脊柱高度的情况下,能够提供术者一个良好的神经根和马尾的显露环境,使其在手术中得到保护,同时切除所有影响复位的组织结构,以便恢复脊柱的矢状序列。
手术适应证:L5整个椎体向前滑移至S1终板之下的Ⅴ型腰椎滑脱。
手术要点:取腹横切口,保护L5椎体周围的血管,确认两侧的L4/L5和L5/S1椎间孔及L5神经根,行L4/L5和L5/S1椎间盘切除,经椎弓根基底部将L5椎体切除。取后正中入路显露L5椎弓根及横突,置入L4和S1两侧椎弓根螺钉。松解并切除L5椎后结构、椎弓根和横突。通过钉棒系统复位L4椎体,将L5椎体松质骨植于脊柱侧后方以及L4和S1椎体之间。
手术并发症:L5椎体切除术的并发症较为常见,大约有30%的患者会出现神经根损伤症状,但约半数患者的症状最终会缓解。最常见的神经根功能障碍为足下垂,植骨不融合的发生率为10%~15%。前路手术并发症包括:肠梗阻、便秘、髂静脉血栓及男性性功能障碍。而后路手术并发症发生率较低。
(四)后外侧原位融合术
有学者认为,后外侧原位融合术也是治疗小儿和成年重度腰椎滑脱的一种术式,但是由于椎弓根螺钉复位技术能够提供良好的脊柱滑脱复位效果,因此,该术式的使用明显减少。长期随访发现重度滑脱患者行原位融合术后功能逐渐好转,临床症状也有所缓解。对于重度滑脱的病例,不管是否行前柱融合术,都应融合至L4节段,形成更加垂直的融合,提高生物力学强度。重度滑脱的病例中,推荐使用内置物。对于严重滑脱或不稳定的病例,可考虑使用髂骨螺钉固定,以降低S1螺钉松动脱出的风险。
手术适应证:青少年或成人的重度腰椎滑脱
手术要点:对滑脱节段行椎板切除,对双侧L5和S1神经根进行减压。在L5和S1置入椎弓根螺钉,必要时可增加双侧髂骨翼钉。轻度牵引L5~S1节段,行骶骨成形术以缩短骶骨并减轻L5神经根的牵拉。切除L5~S1椎间盘,置入椎间融合器。预弯固定棒,屈曲骶骨以适应L5节段。
(五)经骶骨腰椎原位融合术
对重度滑脱病例,由于L5到S1间的骨性接触过小而导致经后路的椎间融合很难形成。此外,在没有进行局部复位的情况下,由于L5的位置相对于S1较深,使得将椎弓根螺钉置入L5非常困难。Bohlman和Cook在1982年首先提出经腰骶椎的后路方法,当严重的滑脱阻碍正常的椎间融合时,使用腓骨移植物放置于L5S1的椎间盘间,促进原位融合(不行复位)(图31)。如果脊髓造影显示骶骨对硬膜形成压迫时,他们采用L4到S1椎板切除术,然后行骶骨穹隆截骨术进行后路减压。随访发现所有11例患者(10例成年人)都获得骨性融合。Hanson等人将此技术用于14例患者,其中13人腓骨移植愈合效果好并形成了骨性融合。1994年Abdu报道“经椎弓根椎体间内固定”治疗腰椎滑脱的方法。他采用两枚骶骨螺钉从S1椎弓根进入,向上、内、前方穿过骶岬,L5S1椎间盘,进入L5椎体内,不穿透其前缘,具有“矢状面斜钉效应”,进行滑脱复位固定及后外侧植骨术,取得良好效果(图32)。
手术适应证:青少年或成人的重度腰椎滑脱。
手术要点:显露L3-S2椎板、椎间关节突、横突及S1后孔。以S1后孔上缘中点为进针点,进针方向为冠状面内倾10°,矢状面自S1斜向L5椎体,即向上、内、前方钻入,令骶骨螺钉斜行经S1椎弓根、L5S1椎间盘深入L5椎体内,不宜穿透L5椎体前缘。在L4两侧椎弓根椎弓根螺钉。根据神经受压情况,常规方法行L4或L5神经减压,行后外侧融合。
四、术后康复
腰椎滑脱手术的疗效不仅取决于手术操作,同时也取决于术后康复训练的质量。腰椎滑脱患者的术后康复训练应当循序渐进,包括:
1. 术后3~5天行直腿抬高训练,锻炼股四头肌,预防下肢静脉血栓形成。
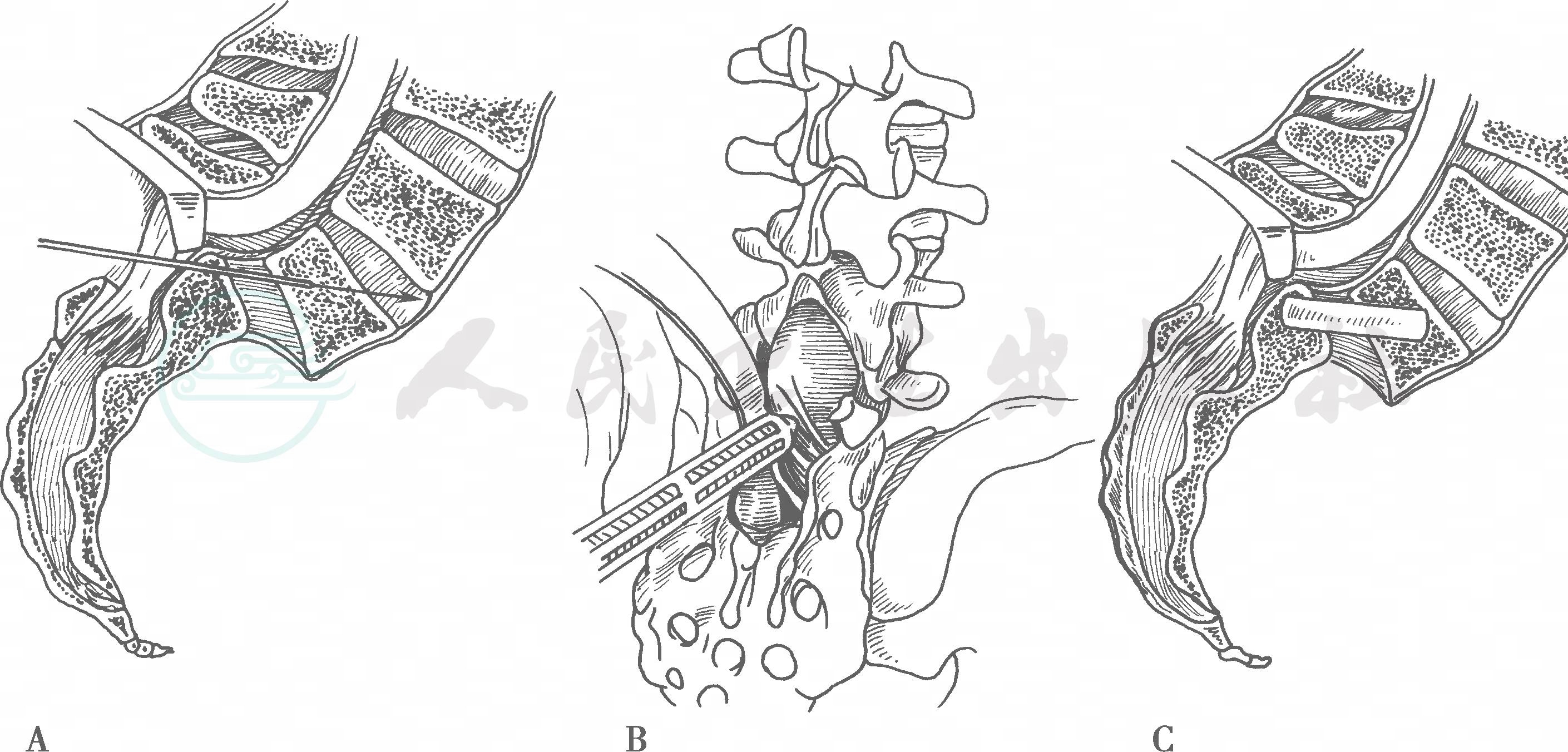
图31
A.完成椎板切除减压后,将硬膜牵开,透视下将导针由骶骨后方穿至L5椎体内;B.在套筒保护下,沿导针方向在骶骨及L5椎体上钻孔,大小与腓骨移植物相当;C.将腓骨沿骨洞穿入至椎体内,完成原位融合
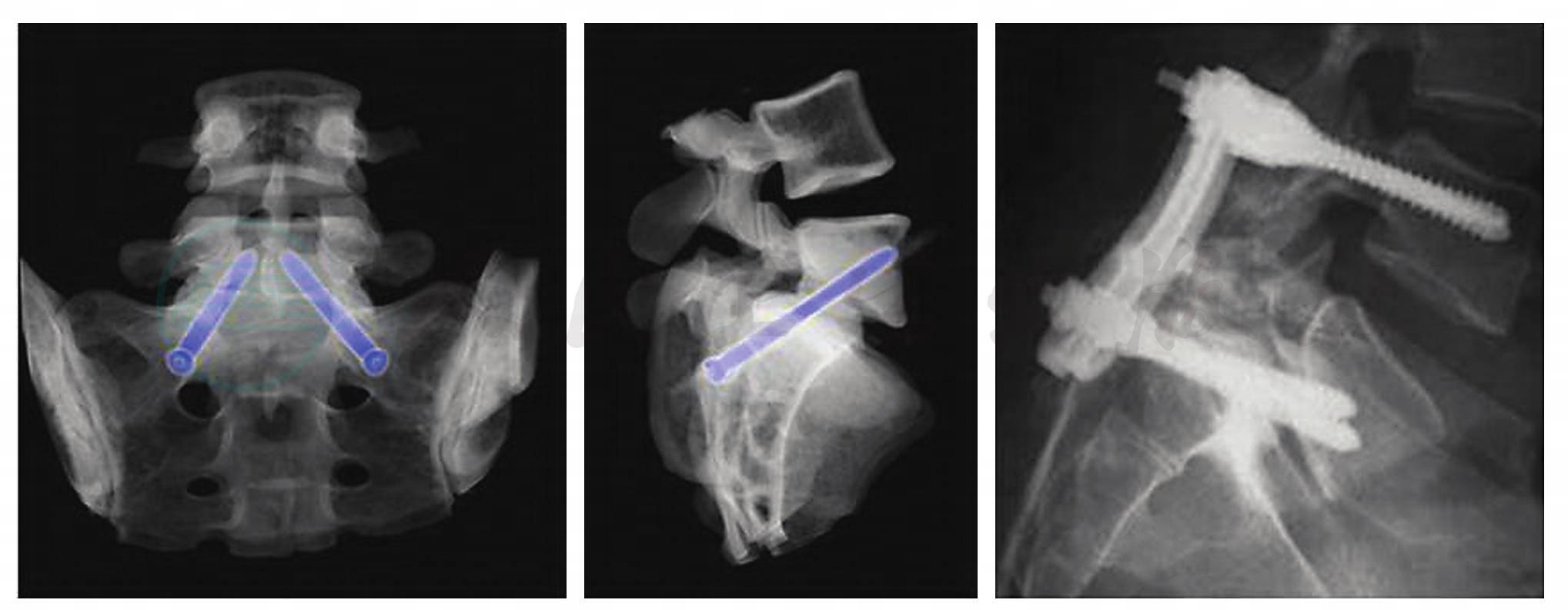
图32 采用“经椎弓根椎体间内固定”技术进行原位固定融合的三维CT重建图(左)及术后X线图
2.术后1周开始行拱桥式背伸肌锻炼,包括三点支撑或五点支撑抬腰锻炼。
3.术后2周可在胸腰骶支具保护下逐步下床活动,活动范围及强度应循序渐进。
4.术后3个月内在支具保护下活动,期间避免腰椎屈曲及扭转类活动。
5.3个月后去除支具,恢复日常活动,避免弯腰及剧烈运动,继续加强背肌功能锻炼。
腰椎滑脱患者术后的上下床动作与日常生活不同,应遵循一定动作流程,以减轻腰部肌肉负荷,促进患者康复。患者下床活动时,动作过程为:
1.在床上佩戴好支具,由仰卧位变换为腹卧位,并移至床边。
2.双下肢先后离开床面,双脚踏实地面。
3.双手以“俯卧撑”姿势支撑躯干,使躯干及腰部离开床面。
4.在他人帮助下缓慢扶起,使患者腰部用力最小。
5.起床过程中,注意患者有无体位性低血压症状,防止晕厥。
6.上床动作与起床动作相反。













