早在1893年,Bizzozero在哺乳类动物胃内发现螺旋形微生物。1906年,Krientz报道,从溃疡性胃癌患儿的表面坏死物和胃内容物中发现了人胃螺旋体(human gastric spirochete)。1982年,澳大利亚学者Warren和Marshall报道,在人胃黏膜活检组织中发现并在厌氧环境下培养出幽门螺杆菌(Helicobacter pylori,Hp)(图1),并认为与慢性胃炎和消化性溃疡病关系密切。随后世界各国对此进行了多方面的研究,并被医学界认为Hp的发现是医学史上的重要发现之一。
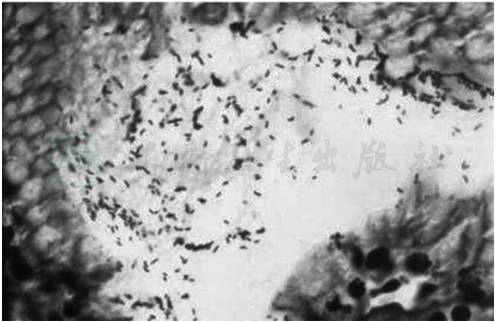
图1 幽门螺杆菌W-S染色
在光镜下,Hp呈轻度S形弯曲,为革兰氏阴性菌,长约3μm,宽0.5μm。菌体周围有类似荚膜的不易着色的淡染区。大多数菌体一端有2~6根长3~5μm的鞭毛。当生存环境发生改变时,Hp的体形会发生变异而呈现球形、长丝形等,但均为革兰氏阴性菌,细胞空泡毒素(vacuolating cytotoxin,VacA)和细胞毒素相关蛋白(cytotoxin associated protein,CagA)也都存在,还能被特异性的Hp抗体所识别。
Hp是一种微需氧菌,所以培养时应有5%微氧环境,最适温度为37℃,pH值在5.5~8.5为适宜的生长条件。Hp的生化特性是具有尿素酶的高度活性。
1.感染率
自从Hp被确认为与慢性胃炎和消化性溃疡有密切关系后,世界上许多国家对Hp的流行病学进行了大量研究工作。世界胃肠病学组织(WGOOMGE)报告显示,儿童Hp的感染率为10%~80%,10岁前超过50%的儿童被感染。儿童时期为幽门螺杆菌感染剧增期:以每年3%~8%速度递增,至10岁约40%~60%人受到感染。最新的研究显示全世界Hp感染率为44.3%,其中发展中国家感染率为50.8%,发达国家为34.7%,成人的感染率为48.6%,儿童感染率为32.6%。中国的一项多中心研究(北京、广州和成都)显示在0~18岁无症状儿童中Hp的感染率为6.8%[8]。感染率随着年龄增加而增加,新生儿期感染率为0.6%,而16~18岁时感染率达13.5%。上海地区的研究显示7~18岁在校学生中Hp感染率为36.3%,小学组、初中组和高中组的感染率分别为27.4%、33.6%和45.1%。
2.Hp的感染途径
至今不明,比较多的研究证明,Hp是从人到人进行传播的,主要根据是在流行病学调查中发现Hp阳性的儿童,家庭成员的Hp感染率明显高于Hp阴性儿童组。多伦多的一项研究发现,74%的父母和82%的兄弟、姐妹同胞有Hp IgG血清抗体阳性。国内也有类似的报道。家庭内成员间的传播方式可能为共用餐具、牙具,母亲咀嚼食物后喂养小儿,以及粪-口途径。有学者从Hp阳性者的粪便中培养出了幽门螺杆菌。
3.Hp感染的高危因素
社会经济环境因素对Hp感染率的影响是主要的,已知的危险因素包括:人口拥挤、卫生状况差、不洁净的食用水、居住条件拥挤、多人同睡一张床、缺乏对母亲喂养知识的教育和辅导、水源污染、家庭成员中有感染者。另有一些因素可增加Hp感染的危险性,包括家庭中有Hp感染者、母亲以咀嚼过食物喂小孩、家长受教育程度低等。
自从Warren和Marshall提出Hp与慢性胃炎和消化性溃疡有密切关系之后,人们对Hp的致病机制,从Hp的生物特性,到人体对Hp感染后出现的免疫反应,做了大量研究工作,但至今对这一问题仍不完全清楚。根据目前研究的结果,也是被多数学者所认可的有以下几个方面:
1.Hp的鞭毛动力
Hp依靠鞭毛动力穿过黏液层,到达胃肠黏膜表面。
2.尿素酶
1989年,Langenberg发现Hp能产生大量尿素酶,该酶具有很高的酶活性,可以通过免疫途径损害胃黏膜上皮,同时尿素酶水解尿素产生的氨能阻止H+从胃腺排入胃腔,并能使H+反渗,结果导致胃酸降低,氨还能引起离体胃上皮细胞功能和形态改变。也有报道认为,在其他动物的胃内也有尿素酶阳性的螺杆菌存在,但是无胃内炎症发生,因此,不支持尿素酶作为主要的致病因素。
3.Hp的毒力
Hp感染的人群中10%~20%可能发展为消化性溃疡,仅1%~2%发展为胃癌,部分带菌者而不发病。这可能有两种原因,即Hp毒力的强弱;与人体防御能力有关。Hp产生的毒力因子有细胞空泡毒素(vacuolating cytotoxin,VacA)和细胞毒素相关蛋白(cytotoxin associated protein,CagA)。VacA是能使细胞产生空泡变性的蛋白,可能通过改变离子通透性导致细胞空泡形成,进而损伤胃黏膜形成糜烂或溃疡。CagA基因是基因组中存在cagPAI(cag致病岛)的标志。cagPAI包含30~40个基因,目前认为由功能性cagPAI编码蛋白形成的跨膜蛋白复合物具有ATP酶和NTP酶活性及构成细菌Ⅳ型分泌系统的相关功能,通过转运相关毒素而参与Hp诱导的上皮细胞内酪氨酸磷酸化、细胞骨架重排、活化核转录因子NF-κB、诱导促炎因子的表达等,发挥其致病作用。
4.抑制胃酸分泌
Hp菌株与胃酸分泌的相互作用不同也许与致病性有关。一些Hp菌株能够抑制胃的酶活性,在体外显示了明显的抑制壁细胞分泌功能。
5.其他致病因子
Hp产生的氧化酶、过氧化氢、脂肪酶,能抵制机体巨噬细胞和中性粒细胞的氧化杀伤作用。磷脂酶、蛋白酶能溶解黏液蛋白,破坏黏液层。
1.Hp与慢性胃炎的关系
在成人已有了大量报道,2012年中国慢性胃炎共识意见中也指出80%~95%的慢性活动性胃炎患者胃黏膜中有Hp感染。幽门螺杆菌患儿内镜下可见黏膜呈颗粒样改变(图2),结节型胃炎中Hp的感染率接近100%。
2.Hp与消化性溃疡的关系
成人消化性溃疡中,胃溃疡Hp检出率为70%~80%,十二指肠球溃疡则高达80%~100%。儿童十二指肠球部溃疡中Hp检出率为62.5%~76.6%。Hp与消化性溃疡的关系虽未做出过人体模型,但根据以往单用酸抑制剂治疗十二指肠球溃疡,一年以后的复发率为80%,根除Hp以后复发率下降到3%,这足以证明它们之间的密切关系。
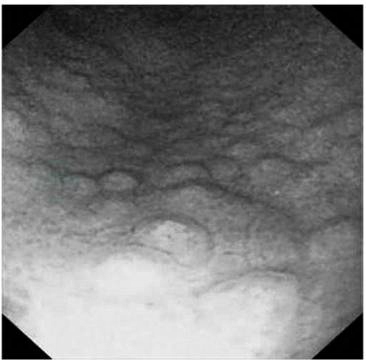
图2 幽门螺杆菌感染的黏膜改变
检测方法包括侵入性和非侵入性两类。侵入性方法依赖胃镜检查及胃黏膜组织活检,包括快速尿素酶试验(rapid urease test,RUT)、胃黏膜组织切片染色和胃黏膜Hp培养、核酸检测等。非侵入性检测方法包括尿素呼气试验(urea breath test,UBT)、粪便Hp抗原检测(Helicobacter pylori stool antigen,HpSA,or stool antigen test,SAT)和血清Hp抗体检测等。除了血清抗体检查,其他检查前均需停质子泵抑制剂(proton pump inhibitor,PPI)2 周、抗生素和铋剂4周。
1.快速尿素酶试验
敏感性75%~100%,特异性84%~100%,其操作简便、费用低、省时,但检测结果易受试剂pH值、取材部位、组织大小、细菌量及分布、观察时间、环境温度和胃炎严重程度等因素影响,故存在结果假阴性的情况。同时取2块组织进行检测(胃窦和胃体各1块)可以提高检测敏感性。
2.组织学检测
敏感性66%~100%,特异性94%~100%,检测Hp的同时,可对胃黏膜病变进行诊断(HE染色),是唯一能确诊Hp感染同时判断其损伤程度的方法,但Hp在胃内呈灶性分布,其检出率易受取材部位及大小、细菌数量及一些疾病,如消化道出血、胃黏膜萎缩等的影响。
3.Hp培养
敏感性55%~96%,特异性100%,是诊断Hp现症感染的“金标准”,培养可进行药敏试验和细菌学研究。但复杂、耗时,需一定实验室条件,标本转送培养需专门的转送液并保持低温。
4.尿素呼气试验
Hp是人体胃内唯一能产生大量尿素酶的细菌。口服用核素标记的尿素,在胃内被Hp产生的尿素酶分解,生成氨和CO2,CO2被吸收进入体循环,转运至肺,由呼气中排出,因此检测呼气中CO2的核素碳即可间接诊断Hp。呼吸试验试剂有13C和14C两种。13C尿素是一种稳定的、无放射性的核素,儿童和孕妇均可使用。敏感性75%~100%,特异性77.5%~100%,可反映全胃Hp感染状况,不会出现因细菌灶性分布而造成的假阴性结果。可用于诊断Hp现症感染,还可用于治疗后的复查。
5.粪便抗原检测
敏感性96.6%~98%,特异性94.7%~100%,检查时不需要口服任何试剂,是唯一一项诊断准确性不受患儿年龄影响的无创性检测方法。该方法的准确性可与尿素呼气试验相当。可用于Hp治疗前诊断和治疗后复查。
6.血清抗体检测
敏感性50%~100%,特异性70%~98%,未经根除Hp的患儿,其血清IgG抗体水平在相当长的时间内保持不变,但经药物根除Hp感染后,抗体水平则逐渐下降,一般于Hp消失后3个月血清IgG水平方见明显下降,但不易达到阴性。由于Hp抗体水平下降缓慢,故Hp血清抗体IgG检查,不能作为判断根除Hp和现感染的依据,多用于流行病学调查。小婴儿血清Hp抗体还有特殊意义,新生儿抗体阳性率在某种程度上反映了母亲抗体的阳性率,且在1岁以内母传抗体的滴度有一个自然下降的过程。否则应考虑为生后Hp感染所致。
7.分子生物学检测
可用于检测粪便或胃黏膜组织等标本。其中聚合酶链反应(polymerase chain reaction,PCR)应用较为广泛。目前主要用作分子生物学及分子流行病学研究,尤其适用于菌株的DNA分型、耐药基因突变的检测。
近十多年,世界上许多国家的学者对Hp的治疗进行了大量的研究,但至今尚未找到一个理想的治疗方案,究其原因是与Hp的耐药性和定居的环境有关。Hp定居于胃黏液的下层、黏膜的表面,许多药物难以穿透黏液层达到有效的治疗浓度。此外,大多数抗生素在胃的酸性环境中其活性明显降低。
1.抗Hp治疗的几个概念
(1)根除(eradication)Hp感染:
是指抗Hp药物治疗一个疗程后,停药4周,再经活组织形态学和/或尿素酶依赖性试验,检测Hp转变成阴性。临床上与其相关的消化性溃疡、慢性胃炎的症状和病理变化明显改善,且不复发。
(2)清除(clearance)Hp感染:
是指抗Hp治疗结束时,检查Hp阴性。这种结果很不可信,此时可能由于Hp在药物作用下发生了形态改变,尿素酶活性被抑制,或其定居部位迁移,从而使形态学和尿素酶依赖性检查出现假阴性,停药后Hp感染可能会很快复发。
(3)再感染(reinfection)Hp:
是指Hp被根除后,又被相同或不同菌株感染,称为再感染。根据成年人的资料,一般再感染率不超过15%。6个月内再现者认为是复发。6个月后再现者认为是再感染。如何区分复发与再感染的界限,尚需做深入的研究。
2.根除适应证
消化性溃疡、胃MALT淋巴瘤必须根治,以下情况可考虑根治:①慢性胃炎;②胃癌家族史;③不明原因的难治性缺铁性贫血;④计划长期服用非甾体消炎药(包括低剂量阿司匹林);⑤监护人、年长儿强烈要求治疗。
3.根除治疗药物
Hp的药物及用药方法根据体内、外大量研究结果表明,单独使用任何一种药物,根除治疗效果都不理想。联合两种以上药物可以提高其疗效,但副作用和费用也随之增高。比较理想的药物治疗方案应是以疗效高、副作用小、价格适中、耐药性低为原则,目前国内外常用的药物有以下几种:
(1)铋剂:
长期以来人们用铋剂治疗消化性溃疡,近来的研究发现铋剂具有杀灭幽门螺杆菌的作用,其机制比较复杂。铋剂可以形成复合物覆盖在细菌表面,破坏细胞壁;抑制Hp所产生的蛋白酶、尿激酶和磷脂酶,影响Hp的生长环境;抑制细菌ATP酶的合成;抑制Hp黏附细胞膜。药用铋剂化合物,包括硝酸铋、次水杨酸铋和次枸橼酸铋,常用的铋剂为枸橼酸铋钾,剂量(大于6岁),6~8mg/(kg·d),分2~3次(餐前口服)。20世纪70年代欧洲长时间、高剂量使用铋剂,发生了铋剂相关性脑病,因此部分国家铋剂被禁用。目前临床上使用的铋剂是不易溶解的无机盐,全身吸收少(<1%),且用于治疗Hp的铋剂剂量小,不会导致神经中毒。一项纳入4 763名患者的荟萃分析结果显示,铋剂使用7~56天,剂量400~2 100mg/d,没有人发生严重不良反应如死亡和神经毒性。
(2)质子泵抑制剂(proton pump inhibitor,PPI):
奥美拉唑,0.6~1.0mg/(kg·d),分2次(餐前口服)。PPI具有抗Hp的作用,但其机制尚不明,在体内的主要作用可能还是通过降低胃内酸度,增强抗生素的活性和改变Hp在胃内生存环境有关。
(3)抗生素:
儿童中常用的抗Hp的抗生素有:阿莫西林50mg/(kg·d),分2次(最大剂量1g,b.i.d.),其作用于细菌的糖苷酶,使细胞壁的合成受到抑制;甲硝唑20mg/(kg·d),分2次(最大剂量0.5g,b.i.d.);替硝唑20mg/(kg·d),分2次,其抑制细菌脱氧核糖核酸的合成,从而干扰细菌的生长、繁殖,最终导致细菌死亡;克拉霉素15~20mg/(kg·d),分2次(最大剂量0.5,b.i.d.),其抑制细菌蛋白质合成,影响细菌的流出泵功能,使细菌不能很快驱除进入人体的药物,使药物离开组织与细胞非常缓慢。
4.治疗方案
提高Hp首次根除成功率,可以减少抗生素继发性耐药,减少后续的医疗费用。儿童中用于Hp补救治疗的药物有限,因此对于儿童提高首次根除成功率更为重要。标准三联疗法曾经在世界范围内广泛使用,该治疗方案包括质子泵抑制剂(proton pump inhibitor,PPI)和2种抗生素(阿莫西林和克拉霉素,如果青霉素过敏,可用甲硝唑代替阿莫西林)。这种治疗方案在20世纪90年代根除率可以达到90%以上,且使用方便,因此1996年起多个指南都推荐标准三联疗法作为Hp的一线治疗方案。近年来随着抗生素耐药率的升高,全球多数研究均显示该治疗方案的根除率低于80%。多个共识均建议该方案只适合用于克拉霉素耐药率低于15%的地区或者在治疗前,药物敏感试验提示克拉霉素敏感。
近年来出现了一些新的治疗方案,主要包括含铋的四联疗法和不含铋的四联疗法(序贯治疗、伴同治疗和杂合治疗)。经典的含铋四联方案指:PPI+铋剂+甲硝唑+四环素。多项研究显示即使存在克拉霉素和甲硝唑耐药,含铋四联治疗的根除率仍可大于90%。因此Maastricht V共识建议该治疗方案可以作为一线治疗方案[10],当无法获得四环素时,可以用阿莫西林代替。序贯疗法指:前5天使用PPI+阿莫西林,后5天使用PPI+克拉霉素+甲硝唑或替硝唑。该治疗方案最早在意大利广泛使用,当时根除率可以达到95%。之后多项儿童中的研究均显示序贯疗法根除率明显优于标准三联治疗。但欧洲儿童中的一个多中心研究显示,当克拉霉素耐药率为14.4%,甲硝唑耐药率为15.3%时,10天序贯疗法的根除率只有80.4%,当存在克拉霉素或甲硝唑耐药时,其根除率下降至72.6%。台湾的一项研究将疗程延长至14天,结果显示14天序贯疗法的根除率可以达到90.7%。伴同疗法指:PPI+阿莫西林+克拉霉素+甲硝唑。当克拉霉素耐药率为15%,甲硝唑耐药率为25%~30%时,伴同疗法的根除率可以达到91.7%。
复旦大学附属儿科医院比较14天标准三联、序贯治疗、含铋四联疗法和伴同疗法在Hp感染儿童中的根除率,结果显示4种治疗方案的根除率分别为74.1%、69.5%、89.8%和84.6%。含铋的四联疗法根除率明显高于标准三联治疗。4种治疗方案的不良反应发生率分别为12.1%、6.8%、15.3%和15.4%。所有的不良反应均为轻度,停药后自行缓解。四组之间不良反应发生率无显著差别。该研究提示含铋的四联治疗根除率接近90%,安全且患儿可以耐受。该治疗方案有望成为中国儿童Hp治疗的一线根除方案[11]。
5.根除H.pylori的个体化治疗
“个体化治疗”是针对Hp根除治疗失败的患儿,分析其失败原因和提出处理方法。具体建议如下:
(1)了解患儿以前治疗时用药的依从性,判断治疗失败的原因。
(2)有条件者根据药敏试验结果选择有效抗生素,无条件者用分子检测方法(如原位免疫荧光杂交)检测克拉霉素的耐药性。
(3)无条件行药敏试验,再次治疗时应尽量避免重复使用初次治疗时的抗生素或加用铋剂,对青霉素过敏的患儿可供选择的药物有限,能否选用氟喹诺酮类等药物,需根据儿童的年龄来考虑使用。
(4)延长治疗时间或加大药物剂量(建议不超过药物说明书用量)。
(5)抑酸剂在根除治疗中起重要作用,但PPI代谢的CYP2C19基因多态性会影响根除效果。因此,可选择作用稳定、疗效高、受CYP2 C19基因多态性影响较小的PPI,如埃索美拉唑,可提高根除率;或提高奥美拉唑剂量,增加口服次数。
(6)对多次治疗失败者,可考虑停药3月或半年,使细菌恢复一定的负荷量,以便提高下一次治疗时Hp的根除率。
(7)根除治疗失败,但症状缓解者,可暂缓再次根除治疗。
6.疗效评估
应在根除治疗结束后至少4周后进行,即使患儿症状消失也建议复查,首选尿素呼气试验。符合下述三项之一者可判断为Hp根除:①尿素呼气试验阴性;②粪便抗原检测阴性;③基于胃窦、胃体两个部位取材的快速尿素酶试验均阴性。













