补体是天然免疫的重要组成部分,同时作为天然免疫和获得性免疫的桥梁。补体与免疫系统的很多分支相互作用,不但保护机体免于感染,对机体保持免疫稳态起重要作用。补体系统缺陷导致广泛的临床表现形式,包括反复细菌感染、遗传性血管神经性水肿(hereditary angioedema,HAE)、风湿性异常、白细胞黏附分子缺陷-1型(leucocyte adhesion deficiency type 1,LAD-Ⅰ)和溶血尿毒综合征。通常聚集为2个临床分类:反复荚膜菌感染伴或不伴风湿性异常和反复耐瑟菌感染。风湿性异常包括系统性红斑狼疮(SLE)、SLE样疾病、皮肌炎、过敏性紫癜、膜增殖性肾小球肾炎、血管炎等。C1抑制物缺陷导致HAE,CR3缺陷导致LAD-Ⅰ,CD59缺陷导致阵发性睡眠性血红蛋白尿(paroxysmal nocturnal hemoglobinuria,PNH)。
补体最初被描述为能溶解抗体致敏的细菌和红细胞的物质。补体的不同功能均需要通过2个不同的通路来达到C3的活化或固定。经典通路通常利用抗体作为识别分子。一旦获得性免疫防护被活化,特异性抗体结合到微生物,形成C1q的结合位点,导致有效的经典途径的活化。凝集素通路由甘露聚糖结合凝集素(MBL)始动,它通过结合MBL相关的丝氨酸蛋白酶(mannan-binding lectin-associated serine protease,MASP)形成复合体,裂解C4和C2形成凝集素通路C3转化酶(C4b2a)。凝集素通路也可被纤维凝胶蛋白(ficolin)活化。替代途径是抗体非依赖的,依赖于天然C3进行最小的自动的水解。水解的C3与因子B结合。与水解的C3结合的因子B,被因子D裂解为Ba和Bb。水解的C3Bb,可持续低水平地将C3裂解为 C3b。若C3b结合于适当的表面,则因子B与之相关,由因子D裂解为C3bBb,是一种强力有效的C3转化酶。在替代通路,备解素(properdin)稳定C3b与Bb的复合体,延长酶的半衰期。备解素见于伴有降低唾液酸内容物的活化的病原表面,而不见于富含唾液酸的宿主细胞膜。抑制性因子H抑制C3bBb的形成和降解C3bBb。因子Ⅰ灭活C3b。不同的通路均汇集于C3成分,通常结局是C3b在靶表面丛集性沉积。C3b上的不稳定硫酯组可共价稳定结合于相邻病原细胞表面或改变的宿主细胞膜暴露的氨基或羟基组,该过程放大C3的缓慢水解,也促进后续靶病原表面或改变的自身结构上的补体活化。替代途径也被经典或凝集素通路产生的C3b活化和放大。C3b可作为吞噬细胞的调理素,也始动最后的常见通路。当C3b与C3转化酶结合,C5被裂解。C5具有一个不稳定的细胞膜结合位点,与C6结合后形成稳定的复合物。活性C5b67可与脂膜结合。结合的C8可插入细胞膜。C9的加入使脂质双层穿透导致细胞的渗透性溶解。
总的溶血补体分析(CH50)检测患儿的血清溶解兔抗羊抗体包被的绵羊红细胞的能力。一个CH50值为200意味着一份血清稀释1∶200倍能溶解50%兔抗羊抗体包被的绵羊红细胞。AH50试验利用兔或豚鼠红细胞,特异性活化替代通路,用EGTA螯合钙离子阻断经典和凝集素通路。溶血的替代通路分析不能检测properdin缺陷。
部分C4A、C4B、C2或联合的C4A/C2缺陷,CH50、C3和C4可在正常范围内。若患儿持续低C4或C4低-正常水平,C4的同种异型分析是最简便的方法来检测部分C4A或C4B缺陷。1~5个拷贝的长(21kb)或短(14.6kb)C4基因位于6p上MHC的中间区域。至今,2~7个拷贝C4基因经常存在于正常个体的二倍体基因组中。通过实时PCR分析可准确检测C4A和C4B基因的拷贝数变异。
CH50为零或极低,AH50正常,提示C1q、C1r、C1s、C2或C4缺陷。AH50为零或极低,CH50正常,提示因子B或D(极少见),或备解素缺陷。AH50和CH50均为零或极低,提示C3、C5、C6、C7、C8或C9缺陷。晚期成分低,尤其C3、AH50和CH50低,提示因子H或I缺失。携带者的CH50分析通常是正常的。补体缺陷诊断思路流程图见图1,诊断方法组合分析见表1。

图1 补体缺陷诊断思路流程图
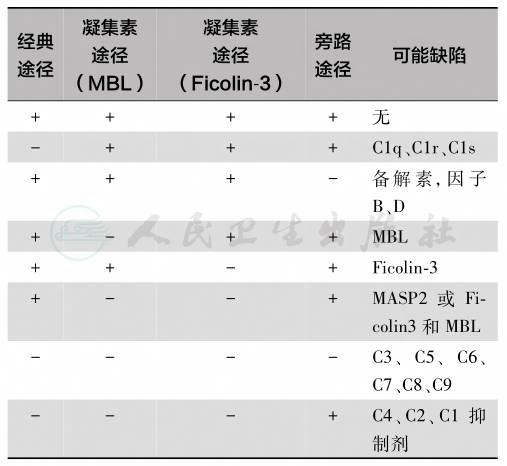
表1 补体缺陷诊断方法组合分析
建议用结合四价(A、C、Y、W-135)脑膜炎球菌疫苗预防接种所有补体缺陷患儿,但不能提供完全的保护。近端补体缺陷使C3d产生减少者,需2个月后重复接种该疫苗。C3形成缺陷者需接种13价结合和23价非结合肺炎双球菌疫苗。接种后需监测抗体滴度以确保出现保护作用。旁路途径或C5~C9缺陷者是脑膜炎球菌感染的高危人群,可预防或按需应用抗生素(利福平、头孢曲松,>18岁时可用环丙沙星)。
C1-INH应用于上呼吸道水肿,痛性腹部痉挛,口咽部手术时的预防应用和其他方法治疗无效的频繁发作者。MBL建议应用于MBL缺陷同时合并其他免疫缺陷而易于出现严重感染者。新鲜冰冻血浆可提供C2,也是目前C1q或C3缺陷者的唯一治疗方法。新鲜冰冻血浆置换可清除自身抗体和补充缺陷的补体成分,可用于因子H缺陷者和不典型溶血尿毒综合征者,建议每周2次应用。













