英文名称 :White matter injury in premature infants
脑白质损伤是早产儿特有的脑损伤形式之一,包括脑室旁白质软化(PVL)和弥散性脑白质损伤。前者指特征性分布在脑室旁局灶性坏死,继而发展成囊腔,有人称为“囊性PVL”。后者指更广泛的脑白质和灰质损伤,常无囊腔形成,也被称为弥散性“非囊性PVL”。早产儿脑白质损伤可遗留神经系统后遗症,最常见的是脑瘫、视力障碍和认知缺陷。
对PVL的描述起始于100 多年前,Parrot首先发现了脑室旁脑白质损伤,后Banker和Larroche正式将其命名为“脑室旁白质软化”,并研究了病理改变过程,以及其与临床疾病间的关系。
脑白质损伤主要发生在小胎龄的VLBW儿,发生率在不同的地区报告不同,特别是不同的诊断手段使发生率有别。神经病理检查证据显示,死亡的VLBW儿PVL发生率为25%~75%,抢救6天以上死亡者发生率高达60%以上,而早期死亡者发生率仅7%。颅脑超声对VLBW儿PVL检出率为5%~15%,MRI检出率高于B超。
1.缺血
所有造成脑血流减少的疾病都可能与早产儿脑白质损伤有关[4]。
(1)产前、产时因素
母亲妊娠高血压疾病,胎盘、脐带异常,胎-胎输血,产前出血,宫内窘迫等。
(2)新生儿因素
窒息、休克、低血压、低氧血症、低碳酸血症等。
2.感染
许多研究结果已显示,感染是早产儿脑白质损伤的重要原因,是感染后炎症性细胞因子介入了白质损伤过程,各类细胞因子损伤了少突胶质细胞前体,白质中反应性星形胶质细胞和小胶质细胞数量增加。如母亲绒毛膜羊膜炎、胎膜早破、产道细菌、脐带炎、新生儿败血症、细菌性脑膜炎、重症肺炎、NEC等,均增加了脑白质损伤的机会。有一项研究对94例早产儿的羊水做了检查,其中23例最终发展为 PVL,在这些早产儿的羊水中,TNF-α、IL-1β、IL-6明显升高,后期8例发生脑瘫。
3.其他
一些研究提出遗传因素与白质损伤有关联,母亲、胎儿基因组的特殊性,增加了对PVL的易感。如有些早产儿在编码IL-6的部位存在基因型改变,增加了IL-6的产生,PVL、IVH和出血性梗死的危险性增高。
脑白质损伤主要发生于胎龄小于32周的早产儿和极低出生体重儿。美国胎龄小于32周出生的婴儿约占全部活产儿的2%,极低出生体重儿约占全部活产儿的1%。这些人群中,通过超声检查发现的脑室周围白质软化发病率是5%~15%,通过MRI检查发现的弥散性脑白质软化的发病率甚至高达50%,对夭折的极低出生体重儿行神经病理检查,25%~75%的患儿有脑白质软化。
根据受损白质所处的位置,脑白质损伤分为脑室周围白质损伤及弥散性脑白质损伤。严重者发生白质软化,根据白质软化灶的多少分为单灶性及多灶性白质软化。
1.脑室周围白质损伤
是传统概念中最经典的早产儿脑白质损伤的类型,主要发生在长穿通支动脉的终末供血区,损伤集中分布于脑室周围,是最严重的脑白质损伤结局,也有人称为“囊性脑室旁白质软化”。病灶一般位于侧脑室周围白质,如前角和体部周围白质,即半卵圆区(大脑前动脉和中动脉的终末供血区),以及侧脑室三角区和枕角周围白质(大脑中动脉和后动脉的终末供血区)。白质区有一个或多个局灶性坏死灶,最终形成囊腔,多见于23~32周的早产儿。
2.弥散性脑白质损伤
是另一种类型的脑白质损伤,也是脑白质损伤最常见的类型。白质损伤比较广泛、弥漫,脑室周围白质和皮质下白质均受累。病变范围较大,可以在侧脑室附近,也可以从侧脑室附近弥散至皮层下,对于胎龄小于32周的早产儿患儿不形成软化灶,而是表现为整体性的白质容积减少。
在缺血后6~12小时,显微镜下可见神经元的凝固坏死,轴突水肿。继早期神经轴突水肿之后,是构成轴突髓鞘的少突胶质细胞不同程度坏死,丢失,于是轴突发生断裂,软化灶形成。脑室旁白质软化主要发生在长穿支动脉的终末供血部位,即侧脑室前角和中央部的周围白质和侧脑室后角三角区周围白质及侧脑室下角的周围白质。因软化灶主要分布于侧脑室的周围,早产儿脑室旁白质软化(PVL)由此冠名。软化灶大小不等,形态不规则,可以单灶形式存在,也可多灶形成密集的小囊腔。脑室旁白质软化发生后,即有小胶质细胞填充病变部位。弥散性白质损伤,从病变早期即伴有小胶质细胞、星形胶质细胞及少突胶质细胞的增生,较少发生液化,而是脑白质整体容积的缩小,脑室扩大。病变更广泛时累及灰质。
早产儿脑白质损伤发生的基础是脑发育过程中的血管和细胞特点,对缺血、感染后炎症性损伤有很高的易感性。
1.血管发育特点
早产儿脑血管发育不完全。从大脑前、中、后动脉发出的长穿支在妊娠24~28周出现,延伸到脑室的边缘,保证脑室周围深部白质的供血,早期在脑室周围形成血管化减少的区带。妊娠32~40周,是短穿支发育最活跃的时期,满足皮层下白质的血液供应。长穿支与短穿支间的吻合支在妊娠32周后才开始逐渐形成(图1)。由此可知,早产儿生后的一段时间内,供应白质血液的小血管在组织解剖结构上并未完全发育成熟,在功能上脑血管自主调节能力差,维持“压力被动性血流”的特点,在缺氧、低血压、低碳酸血症等疾病状态下,脑血流、脑灌注减少,脑白质容易发生缺血性损伤。
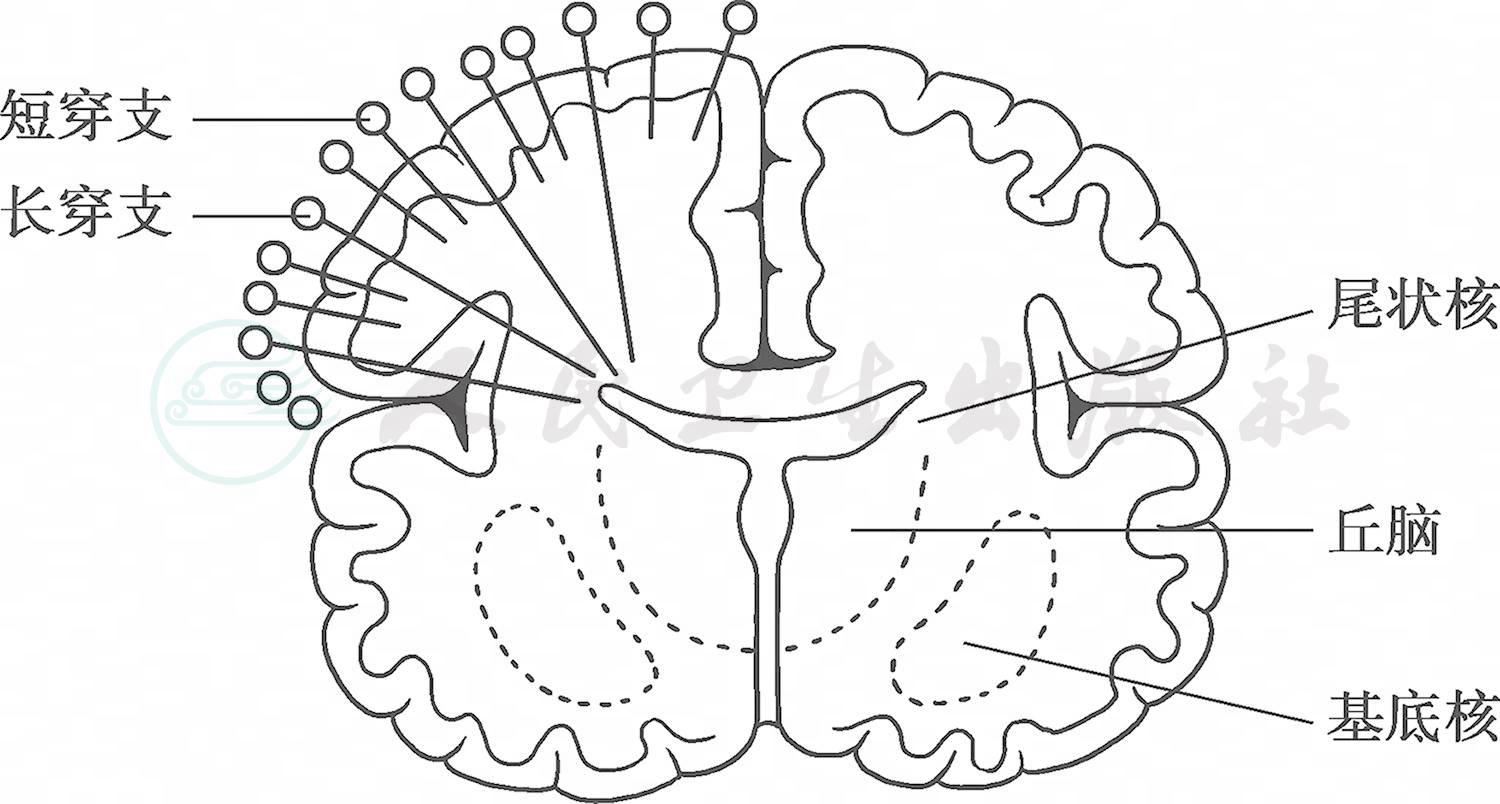
图1脑白质的血液供应
引自:实用新生儿学.第5版.ISBN:978-7-117-27403-6.主编:
2.细胞发育特点
PVL主要发生在脑室旁的深部白质,局部的坏死与此处的少突胶质细胞(oligodendrocytes,OL)有关,少突胶质细胞是神经纤维轴突上髓鞘的重要成分。早产儿脑发育过程中,少突胶质细胞未成熟,仅处于分化中的少突细胞前体(preoligodendrocytes,preOLs)阶段。很多实验已证实,少突胶质细胞前体对兴奋性谷氨酸介导的细胞死亡、氧化应激损伤、缺血性损伤、炎症性细胞因子损伤较成熟的细胞更为敏感。少突胶质细胞前体的损伤、坏死,成为神经轴突损伤的组织基础。
1.超声
颅脑超声的优势是无创、便捷,可床边多次检查。
(1)脑白质损伤的超声影像特点
1)早期
损伤部位回声增强,冠状面扫描可见异常回声分布于侧脑室角的外部和侧脑室旁。在旁矢状面扫描,分布于脑室上方和侧脑室后角三角区附近。
2)PVL形成期
3~4周后软化灶逐渐出现,在上述部位,部分异常回声转化为多个无回声小囊腔,有些可融合成较大囊腔。
3)后期
1~3个月后,一些小囊在影像上消失,脑室增宽(图2)。
(2)检查时间
对胎龄≤32周,出生体重≤1500g的早产儿,应常规行颅脑超声筛查。对有高危因素的大胎龄早产儿可酌情检查。
1)筛查
生后 7~14 天。
2)复查
①对筛查有异常者最好每周复查一次。3~4周时观察PVL发生和脑室增宽情况。婴儿期酌情复查,注意脑白质减少程度,包括脑室增宽,脑裂、脑外间隙增宽;②对筛查无异常的早产儿,建议在出院前或矫正胎龄40周时复查一次。
(3)超声的局限性
对直径<2mm的软化灶诊断敏感性较低,由于扇形扫描存在盲区和分辨率的限制,对弥散性白质损伤的诊断不及MRI。
2.MRI
MRI的分辨率高于超声,尤其是不断进展的检查序列有利于对早产儿脑白质损伤的诊断,可在病变早期精确描述病变位置,损伤范围和病变类型(图3)。
(1)白质损伤不同时间的影像特点
1)早期
常规的T1WI可显示脑室旁低信号损伤,T2WI则显示高信号,较前者更为敏感。
弥散加权核磁成像(DWI)反映组织中水分子运动,当白质损伤时,由于细胞壁泵功能失调,水分子由细胞外向细胞内移动,因此,减少了组织中水分子的正常弥散,图像为高信号,代表弥散数值的扩散系数(diffusion coefficient,ADC)值减低,这种直观的过程和敏感的定量数值,与尸解后神经组织学研究结果相一致,显示了病变区域少突胶质细胞内水肿状态,不但可先于超声和MRI T2WI发现脑室旁白质损伤,也便于发现弥散性脑白质损伤,对非囊腔性白质损伤的诊断具有高敏感性。
磁共振波谱成像(MRS)也已被用于脑白质损伤的诊断,进一步增补了传统的磁共振在急性脑损伤时的检查内容,提供神经损伤的直接的证据,如乳酸聚集,N-甲基-天冬氨酸(NAA)水平减少,NAA与胆碱比值增加等。
2)后期
T1WI和T2WI均可显示PVL形成,以及损伤后期脑室增宽。脑室增宽是脑白质丢失的结果,伴胶质细胞增生,形成瘢痕,皮层减少,在MRI T1WI显示清晰,脑室宽而壁不规则,信号增强,同时皮层脑沟异常加深,与脑室接近,胼胝体变薄。显示了脑室旁和更广泛的灰白质损伤的结局,是遗留后遗症小儿脑内组织解剖基础[5]。
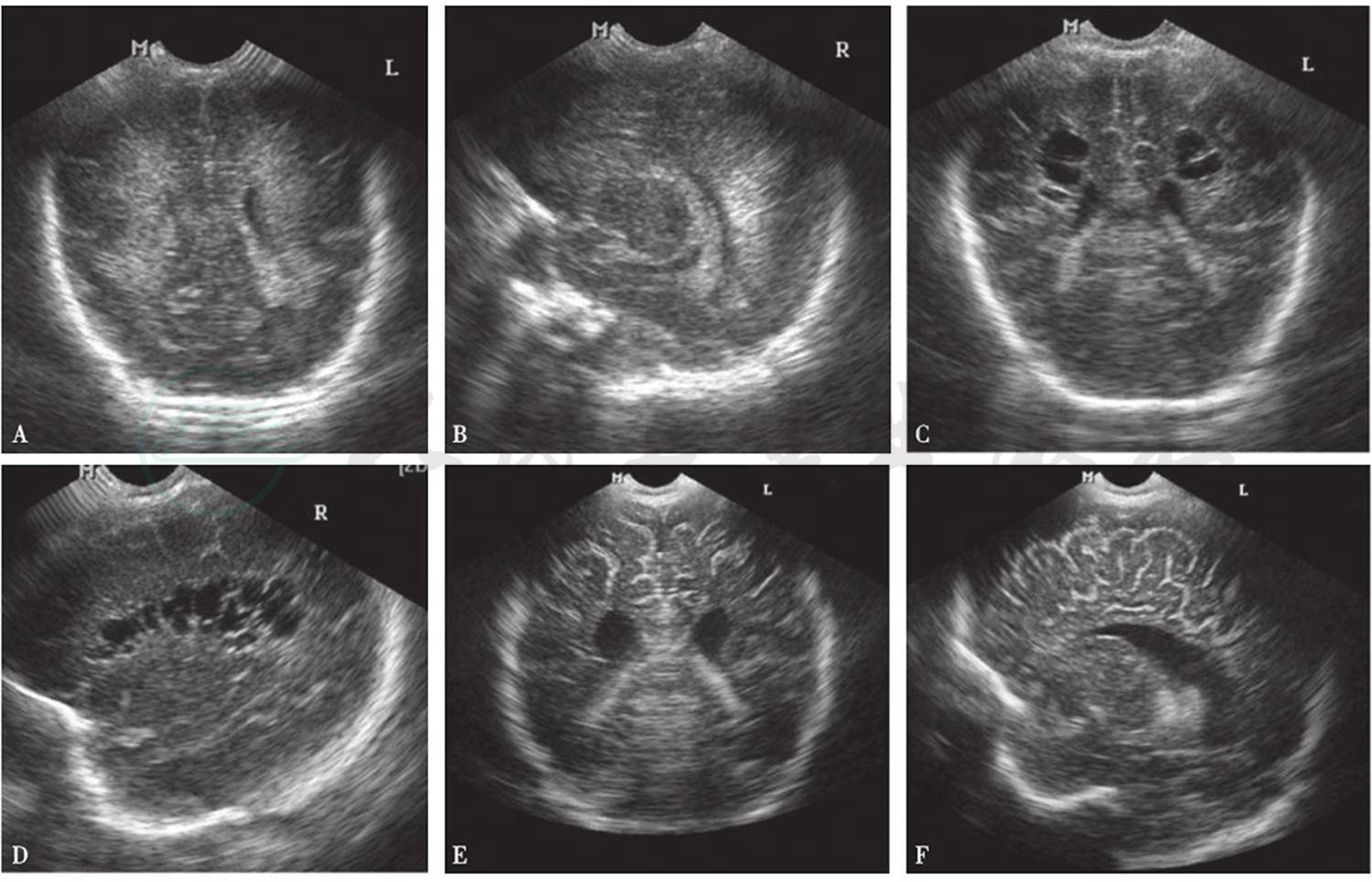
图2脑白质损伤的超声影像
A、B.损伤早期,脑室旁白质回声增强;C、D. PVL形成期;E、F.损伤后期,侧脑室增宽
引自:实用新生儿学.第5版.ISBN:978-7-117-27403-6.主编:
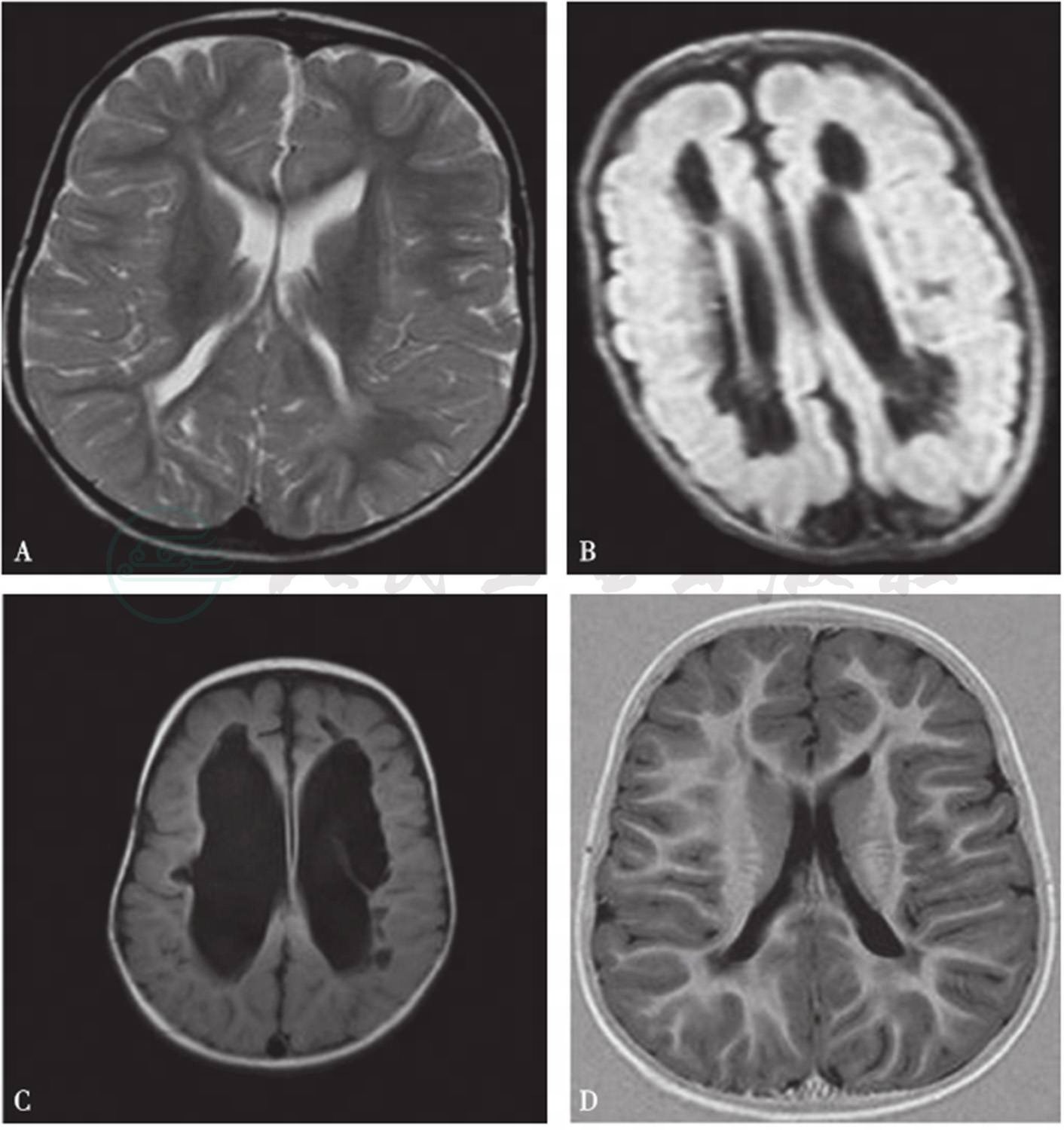
图3脑白质损伤的MRI影像
A.脑室旁T2高信号;B,C.脑室旁软化灶,不同程度脑室增宽;D.脑室变形,脑沟加深,脑白质不规则丢失
引自:实用新生儿学.第5版.ISBN:978-7-117-27403-6.主编:
对于白质损伤后的发育异常,弥散张量成像(DTI)技术具有独特优势。通过水分子在三维空间中弥散轨迹的定量分析、成像,显示脑白质纤维束的走行、方向、排列密度等。DTI是白质束成像的方法,皮质脊髓束异常可先于脑瘫临床症状出现之前,对脑白质损伤后运动障碍的诊治是有益的。
(2)MRI的不足
检查所需时间较长,要求严格,抢救中的危重早产儿难以搬动完成检查,不便于反复检查,故对考虑弥散性白质损伤的早产儿,或后期存在神经发育异常的小儿,可选择性进行MRI检查,而不作为筛查手段。
3.CT
现很少将CT用作早产儿脑白质损伤的常规筛查、诊断手段,原因是存在一定量的放射性,针对早产儿脑白质损伤能够发现的异常敏感性不及MRI和超声。损伤后期,对年龄长些的婴幼儿,针对脑室增宽、脑白质丢失改变,必要时可适当选用CT检查。
早产儿脑白质损伤一旦发生,无特殊有效的治疗方法,故应从发病机制的角度,尽可能减轻损伤,并注重对早产儿的后期综合管理和干预治疗。
1.减轻损伤
强调维持脑灌注,可采取的方法是尽力避免、减少有可能引发脑血灌注减少、损害脑血管自主调节功能的疾病,如休克、低血压、血气异常(低氧血症、低碳酸血症)等。
对于一些实验性神经保护剂,目前均无临床应用的循证医学依据。
2.综合管理
小胎龄早产儿住院期间适时行影像学筛查与检查,发现脑白质损伤。这些小儿出院后定期随访,及时发现运动、视觉、认知等方面存在的发育障碍,予以物理康复和其他专业化、个体化的必要治疗。但研究已显示,在未出现运动异常时,提前予以各类治疗与对照组是无差别的。
产科水平的提高及孕产妇保健的广泛开展是减少围生期窒息,预防母/胎感染、早产发生的最为重要措施。治疗母亲合并症,防治母子间感染的传播,尽量延长孕周,减少小胎龄早产。
提高NICU救治水平,出生时规范复苏,转运过程中适宜温度管理及呼吸管理,维持稳定的血压,特别重要的是维持脑灌注压,保证适宜和稳定的脑血流及氧合,避免低碳酸血症,积极控制感染。合理的肠内肠外营养,避免和减少宫外发育迟滞。生后常规影像筛查、检查,早期及时发现脑白质损伤。
定期随访:体格发育;神经发育随访中及时发现神经异常症状体征,如运动障碍、惊厥、认知障碍、癫痫等;注意有无视听障碍;及时发现行为心理异常。
后期发育中存在问题的儿童,需要多学科间的联系与协作,包括物理康复科、神经内科、神经外科、眼耳鼻喉科、保健科、精神科等。建议建立早产儿神经重症监护团队(多学科),进行个体化干预。













