英文名称 :bronchopulmonary dysplasia
中文别名 :慢性肺疾病
支气管肺发育不良(bronchopulmonary dysplasia,BPD)是指生后不久发生呼吸困难,需要无创通气或机械通气,在纠正胎龄36周仍依赖氧疗,并有肺功能异常。近年来,由于早产儿存活率显著提高,BPD发生率也呈增加趋势,在胎龄<32周早产儿,BPD发生率达20%~30%,胎龄<28周早产儿,BPD发生率达50%~60%,重症BPD病死率比较高,BPD已成为NICU最棘手的问题之一。
40多年来,BPD的概念一直存在不同观点。1967年Northway首次报道的病例名称为支气管肺发育不良,属于“经典型”或“老型”BPD,主要发生在胎龄>32周早产儿,日龄>28天仍依赖氧疗,肺部病变比较严重。后来,经典型BPD越来越少见,新型BPD更为常见,新型BPD主要发生在胎龄<32周早产儿,到纠正胎龄36周仍依赖氧疗,曾称为慢性肺疾病(chronic lung disease,CLD)。2000年和2018年,美国国立儿童健康与人类发育研究所(National Institute of Child Health and Human Development,NICHD)BPD 研讨会决定,仍使用 BPD 名称,而不再使用CLD名称。
BPD病因非常复杂,是多种因素综合作用所致,研究显示,BPD的发生主要与以下危险因素相关。
1.早产和低出生体重
绝大多数BPD发生在早产儿,早产儿是BPD发病的根本内在原因,胎龄越小、出生体重越低,BPD发生率越高。目前,BPD主要发生在胎龄<32周早产儿,在胎龄<28周、出生体重<1 000g早产儿中发生率更高。
2.易感性和遗传倾向
研究显示,有些早产儿更容易发生BPD,起病早,病情重,可能具有一定的易感性和遗传倾向。近几年对遗传在早产儿BPD发生中的作用进行了许多研究。
3.吸氧
早产儿肺发育未成熟,对氧非常敏感,研究证实早产儿暴露于高浓度或长时间氧疗与肺损伤密切相关,氧疗浓度越高、时间越长,BPD发生率越高。
4.机械通气
BPD与机械通气密切相关,许多证据显示,机械通气参数越高、时间越长,BPD发生率越高,机械通气是BPD的重要病因。
5.感染
研究显示宫内感染是BPD的重要危险因素,绒毛膜羊膜炎与BPD密切相关,宫内解脲脲原体感染容易累及肺,发生BPD,生后第一天解脲脲原体培养阳性的患儿气道炎症反应增加,解脲脲原体在气道持续定植与BPD的危险性增加有关。宫内巨细胞病毒感染会导致全身多脏器损伤,肺是重要受累脏器,使肺发育障碍,生后继续发生肺损伤,最终发生BPD。生后感染:早产儿长时间气管插管和机械通气容易合并反复肺部感染,是导致BPD的重要危险因素。生后发生败血症者也增加BPD的危险性。同时肺部反复感染不容易撤离机械通气,延长机械通气时间,进一步加重肺损伤,导致恶性循环。
6.心肺血流动力学变化
动脉导管开放(PDA)和室间隔缺损(VSD)也是BPD危险因素,PDA和VSD发生左向右分流,导致肺充血水肿,肺血管损伤增生,肺动脉高压、右心室负荷加重,加重肺部炎症反应。同时,PDA和VSD分流量较大者撤离机械通气更加困难,致使长时间依赖氧疗和机械通气。许多研究显示,早产儿左向右分流量越大、持续时间越长,BPD发生率越高,病情越严重。
7.其他因素
此外,还有许多危险因素与早产儿BPD有关。如营养不良、小于胎龄儿(SGA)、肾上腺功能不全等。
BPD主要发病机制是肺部长时间炎症反应。在早产儿肺发育未成熟的基础上,发生高氧肺损伤、容量伤、气压伤、感染等,导致瀑布式的继发性炎症反应,大量炎症细胞浸润,释放大量炎症介质,进一步导致肺损伤,最终发生BPD。整个过程非常复杂,是多种危险因素综合作用的结果,有许多环节尚未清楚。
1.早产儿肺发育未成熟
BPD主要发生在早产儿,与早产儿肺结构及生理特点密切相关。早产儿肺泡毛细血管通透性较足月儿高,容易发生渗出,渗出液富含血浆蛋白,称为“高蛋白性肺水肿”,中性粒细胞也随之渗出。新型BPD与肺发育未成熟的关系更为密切,新型BPD主要发生在超早产儿,由于肺的解剖结构和肺功能极不成熟,出生时肺发育刚完成管道形成,容易受到氧和压力损伤等因素干扰,肺泡发育进程受阻,肺泡发育不良和肺泡数目减少。
2.氧损伤
早产儿对氧非常敏感,极易发生氧损伤,对极低出生体重儿,即使吸室内空气也有可能发生氧损伤,因为与宫内低氧环境比较,吸空气氧的浓度仍过高。吸氧可直接损伤肺泡上皮细胞、毛细血管内皮细胞,使肺泡毛细血管通透性增高,加重肺泡渗出,吸高浓度氧可使肺泡气体交换膜增厚,气体交换变得困难,需要更高浓度的氧,形成恶性循环。
3.容量伤和气压伤
机械通气时过高的潮气量和气道压力可直接损伤气道和肺泡上皮细胞,破坏肺的结构,发生肺泡融合和肺气肿,加重肺泡渗出。未成熟肺过度膨胀可导致毛细血管内皮细胞、上皮细胞和基底膜产生严重裂缝,导致严重的机械性损伤。同时机械通气促发严重的肺部炎症反应和促炎症因子的释放,导致进一步的肺损伤。
4.感染导致肺损伤
感染是导致肺损伤的重要因素,包括宫内感染和出生后感染,发生绒毛膜羊膜炎者羊水中的炎症因子进入胎儿肺,发生肺部炎症反应及肺损伤,出生后肺部炎症反应及肺损伤继续发展。生后早期反复肺部感染可促发肺部炎症反应,发生感染性炎症,加重肺损伤,促使BPD发生发展。
5.继发性炎症反应
大量研究显示,继发性炎症反应导致肺损伤是发生BPD的关键环节,上述各种因素所致的肺损伤都可导致瀑布式继发性炎症反应,释放大量炎症介质。炎症介质具有广泛的生物活性,如引起炎症介质的再释放、细胞趋化作用、毛细血管通透性增加、肺血管收缩,进一步导致肺损伤。
6.肺纤维化
炎症介质能刺激成纤维细胞增殖、分泌纤维蛋白,炎症反应后肺发生修复反应时,向纤维化方向发展,最终形成肺纤维化。
BPD肺病理变化非常广泛,几乎累及各级支气管和肺泡。较大的支气管黏液腺大量增生,广泛或局灶性的支气管软化。小气道发生广泛的黏膜上皮细胞增生,平滑肌增生,管壁增厚,管腔狭窄。各级支气管可见广泛的炎症反应,炎症细胞浸润、水肿,气道上皮细胞坏死、脱落。间质细胞增生、纤维化。肺泡数量减少,肺泡总面积减少,发生肺气肿。肺毛细血管内皮细胞增生、通透性增高。
经典型BPD肺部病变非常严重,支气管结构变形和增生,代偿性肺气肿,肺纤维化非常明显(见彩图1)。新型BPD以肺泡发育进程受阻为主,肺泡发育不良,数目减少,体积增大,肺泡结构简单化,肺微血管发育不良,形态异常,肺和气道损伤或纤维化较轻。
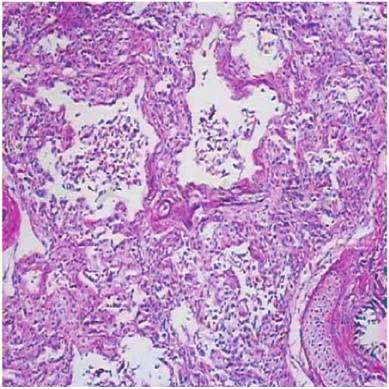
图1 新生儿支气管肺发育不良肺病理变化(肺纤维化)
1.影像学检查
1967年,放射科医师Northway首次描述BPD时主要根据肺部X线表现,国际上多采用Northway的分期法,将BPD肺部X线改变分为4期(表1)。Weinstein采用记分法将BPD肺部X线改变分为6级(表2)。这些是经典型BPD的肺部病变,现在比较少见。而新型BPD的肺部X线表现比较轻,表现为肺纹理增粗,肺气肿,肺纤维化不明显。
表1 BPD肺部X线表现的Northway分期法

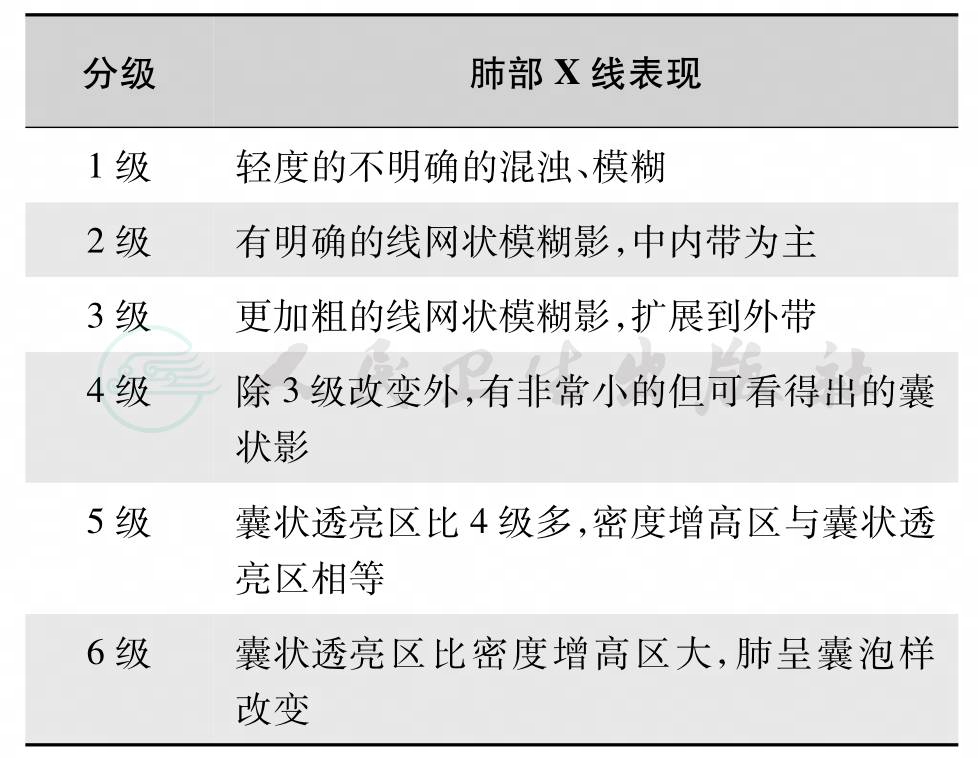
表2 BPD肺部X线表现的Weinstein分级法
此外,肺部超声检查,可观察肺部病变动态变化。对少数特殊病例可进行肺部CT和MRI检查。
2.肺功能检查
BPD患儿肺容量下降,肺顺应性较差,气道阻力明显增高。
目前BPD尚无特别有效的治疗方法,以预防为主,尽可能减少BPD的发生或减轻BPD的严重程度。对已发生BPD者应积极采取综合治疗措施。
1.呼吸支持
早期使用无创呼吸支持,如早产儿刚出生时发生呼吸困难,应尽可能先使用无创呼吸支持,如CPAP、NIPPV或无创高频等,尽可能降低吸入氧浓度,密切监护血氧饱和度,使血氧饱和度保持在90%~95%。
对必须使用机械通气的早产儿,应尽可能降低呼吸机参数,缩短机械通气时间,使用咖啡因等,尽早撤离机械通气。撤离呼吸机后再改用无创通气,然后逐渐撤离无创通气,直至撤离氧疗。
2.积极防治感染
BPD常合并肺部感染,多为耐药菌感染,分泌物多,致使不容易撤离氧疗和机械通气。应采取严格措施预防早产儿感染,对发生肺部感染者,积极控制感染至关重要,只有将肺部感染控制住,才能撤离氧疗或机械通气。经常做痰培养,有针对性使用抗生素,同时积极进行肺部物理治疗,清除气道分泌物。
3.糖皮质激素的应用
激素具有抗炎、降低肺毛细血管通透性等作用,对BPD有一定的治疗作用。但激素不良反应较多,抑制生后早期神经系统发育,增加脑瘫发生率,应谨慎掌握激素的疗效与不良反应的利弊平衡。2012年美国儿科学会建议采用Dart方案,对中重度BPD在生后2周仍依赖机械通气者,使用地塞米松,0.15mg/kg,q.d.×3 天;0.10mg/kg,q.d.×3 天;0.05mg/kg,q.d.×2 天;0.02mg/kg,q.d.×2 天,一个疗程剂量共0.89mg/kg。也可以局部使用激素,减少全身不良反应。
4.营养支持
BPD是消耗性疾病,加强营养支持非常重要,良好的营养状态可增强抗病能力和机体恢复能力。
5.适当限制液体量和使用利尿剂
BPD患儿常有肺水肿、肺间质肿胀,应适当限制液体入量,一般每天110~130ml/kg。早产儿生后早期限制液体量比较困难,可使用利尿剂,减轻肺水肿,改善肺功能,但利尿剂易引起电解质紊乱,应小剂量口服。
6.其他治疗
近年来BPD常合并肺动脉高压,可采用吸入一氧化氮(iNO)或西地那非治疗。













