胎儿水肿(hydrops fetalis,HF)是严重的临床状态,指胎儿存在至少两处体腔异常的液体聚集。HF表现为腹腔积液、胸腔积液、心包积液或皮肤水肿(图1)。它的临床表现还包括羊水过多或胎盘水肿。Potter首先将非免疫性胎儿水肿(nonimmune hydrops fetalis,NIHF)和免疫性水肿区分开(Potter 1943)。
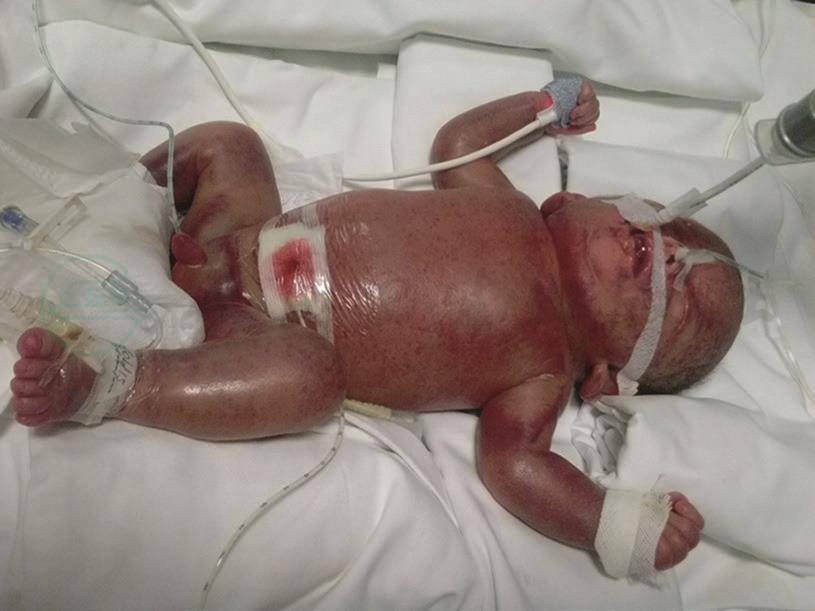
图1非免疫性水肿早产儿
引自:新生儿学:理论与实践(第2版)(上、中、下卷).第2版.ISBN:978-7-117-34390-9.主编:
• 胎儿水肿是一种严重的临床状态,指胎儿存在至少两处体腔异常的液体聚集
• 非免疫性水肿占胎儿水肿的90%
• 胎儿水肿基本机制是组织间液的产生和淋巴回流的不平衡
• 胎儿水肿的主要病因是血液疾病,心血管疾病和感染性疾病,遗传异常,肿瘤和特发性疾病
• 胎儿水肿的管理对胎儿医学和新生儿专家来说是极大的挑战,胎儿水肿的死亡率仍旧较高
• 胎儿水肿是危重的临床状态,诊断即使稍有延迟,都可能耽误及时进行干预措施,甚至危及生命
尽管我们已经知道免疫性水肿的病因,但是在出生前后进一步研究NIHF,提高我们对其病因的认识。大型的临床病例研究和系统综述报道产前将近 60% 的 NIHF 能找到病因(Santo et al. 2011),加上新生儿期进一步检查,85%的NIHF能发现病因(Bellini et al. 2009)。HF 是各种病因造成的非特异性的终末状态。它的病因可以分为6大类:血液疾病、心血管疾病、感染疾病、遗传异常、肿瘤和特发性。表1总结HF的病因。
表1胎儿水肿的病因

续表

引自:新生儿学:理论与实践(第2版)(上、中、下卷).第2版.ISBN:978-7-117-34390-9.主编:
过去Rh溶血症等血液疾病是胎儿和新生儿免疫性水肿的主要病因。目前HF中90%是非免疫性水肿,活产儿的患病率 1/3 800~1/1 500(Santolaya et al. 1992;Warsof 1986)。HF 在东南亚较为常见,泰国非免疫性水肿的主要病因为同种α地中海贫血或者 Bart水肿,发病率为 1/1 500~1/500(Suwanrath-Kengpol et al. 2005;Abrams et al. 2007)。虽然到目前为止HF的产前诊断超声技术大大提高,但是HF的围生期死亡率仍然很高。
HF的基本机制是组织间液的产生和淋巴回流的不平衡。胎儿体内液体的聚集来源于(a)心衰、(b)贫血、(c)淋巴受阻和(d)血浆渗透压减低。胎儿对组织间液积聚较为敏感,因为它有更大的毛细血管通透性、组织间质间室顺应性高,以及由于淋巴回流受损而导致的静脉压力升高(Abrams et al. 2007;Apkon 1995)。临床和动物实验显示中心静脉压升高,对HF 的形成有重要的作用(Shinbane et al. 1997)。中心静脉压升高提高毛细血管静水压和降低淋巴回流,造成水肿和积液(Moise et al. 1992)。白蛋白是维持胶体渗透压的主要血浆蛋白,它在肝脏合成受损,导致毛细血管通透性增加(Abrams et al. 2007;Apkon 1995)。低蛋白血症在 HF 中常见,但是临床和动物的研究发现,低蛋白血症不是触发HF 的主要原因(Pasman et al. 2006)。
HF管理对胎儿医学和新生儿专家都是极大的挑战。HF患儿情况危急,诊断稍有延迟,可能就阻止患儿接受干预措施,甚至危及患儿的生命(Desilets et al. 2013)。
合并有HF的孕妇,如果产前无刺激胎心监护(nonstress test,NST)和胎儿生物物理特征(biophysical profile,BPP)异常,应该收治在三级医院(表3)。住院后继续确定HF的病因。34周后可以分娩。羊水穿刺显示胎儿肺部成熟,或者胎儿病情恶化,都是提早分娩的指征。如果有产科适应证或母亲因为镜像综合征出现病情变差,也需要及时分娩(Van Selm et al. 1991;Norton et al. 2015)。
表3住院保守治疗
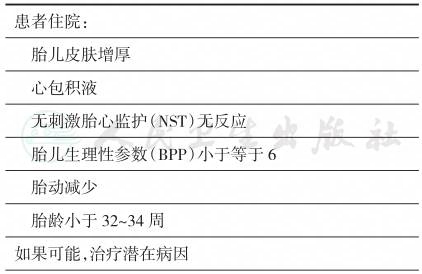
续表

引自:新生儿学:理论与实践(第2版)(上、中、下卷).第2版.ISBN:978-7-117-34390-9.主编:
HF死亡率高,准确诊断后才可以开始正确的治疗。父母双方都需要参与,因为HF的相关异常是严重的,甚至是致死的。此外侵入性的胎儿检查和选择性的早产存有异议。所以需要妇产科医生,胎儿医学和新生儿专家团队会诊,选择最佳的分娩时机,团队中还需要包括儿外科医生,心血管医生和心血管外科医生。文献中对HF的治疗有不同的方法,但是没有设计合理的临床试验给临床医生提供足够循证医学的依据。HF可能会自行消失。但是治理主要集中在矫正潜在的病理生理学问题,包括胎儿输血来纠正贫血(无论何种病因),药物治疗心律失常,纠正或降低体腔占位性因素,缓解心脏静脉回流或淋巴回流,或者采用措施停止胎儿的血液流失(无论何种病因)(Watson and Campbell 1986;Muller-Hansen et al. 1998;Jones 1995)。
严重贫血胎儿的标准治疗是胎儿腹腔输注红细胞。它是风险较低的治疗方法,但是目前仍缺乏随机对照临床研究的确切证据。这个方法已经成功治疗严重的同种免疫妊娠,纠正贫血。特例是妊娠已经接近临产,分娩的风险才比宫内输血的风险要低(Norton et al. 2015)。其他报道过的输血途径包括经皮脐静脉、肝内脐静脉输血、脐动脉和心内输血。其他的方法目标是母亲、胎儿和新生儿。母亲的治疗包括血浆置换及给予异丙嗪和糖皮质激素。胎儿治疗包括部分交换输血、胎儿静脉输注IgG、血小板输注和给予粒细胞集落刺激因子。α地中海贫血的治疗包括新生儿干细胞移植(Carr et al. 1995)。但是新的治疗技术比较胎儿腹腔输血有更高的风险性,所以需要谨慎使用。
高度血管化的肿瘤和急性、大量的胎胎输血是危及生命的疾病,可能需要高风险性治疗。在治疗胎儿骶尾部肿瘤、高度血管化的腹部、胸部或胎盘肿瘤,因为存在大量的动静脉分流,所以可以采用减瘤手术、止血手术、光凝和射频消融手术来治疗。
双胎输血综合征的治疗,至今仍是未解决问题。输血治疗供血者,未显示有益的证据;受血者很少采用减容量或结合输血和减容量方法,或不能矫正已经恶化的病理生理改变。此外,双胞胎中受影响胎儿的胎死腹中后,先前正常存活的胎儿会出现水肿(Mahone et al. 1993)。
胎儿心律失常的治疗,包括不采取措施、药物治疗和立即分娩。因为胎儿心律失常引起的NIHF,需要给母亲抗心律失常药物治疗,除非患儿的胎龄接近足月或者母亲产科并发症,不能应用心律失常药物。另一方面,如果胎儿合并缓慢型心律失常导致胎儿水肿,宫内治疗大多处于研究状态,在研究机构外,尚不推荐(Norton et al. 2015)。
如果胎儿已经成熟,最简单的方式是分娩受累患儿,出生后治疗心律失常。常用的药物包括地高辛、呋塞米、氟卡奈德、维拉帕米、胺碘酮、丙洛尔、普鲁卡因胺、奎尼丁、腺苷、索他洛尔、特布他林、皮质类固醇、免疫球蛋白等。联合用药也很常见。但是药物的选择还是经验性的和任意的,仍需要进一步的临床研究证据支持(Strasburger et al. 1986;Simpson and Sharland 1998)。
占位性肿块的治疗取决于肿块的性质和治疗中心的常规。如果不能立即分娩患儿,可以做减瘤手术或切除手术。胸腔积液、心包积液和腹水可以进行单次穿刺或多次引流。也有报道胎儿手术矫正潜在畸形。成功或失败的案例均有报告。没有证据证明其中一种方法好于另一种方法(Wesolowski and Piazza 2008)。
胎儿水肿的出生后管理对新生儿医生也是挑战。分娩后的治疗取决于患儿的原发疾病。新生儿复苏需要熟练的团队(新生儿医生、护士、呼吸治疗师、放射和超声技师)以及恰当的复苏设备(McMahan and Donovan 1995;American Heart Association 2006)。在新生儿复苏室可能需要立即的胸腔穿刺,心包穿刺或腹腔穿刺治疗,保证患儿的正常的呼吸循环功能。脐动静脉置管监测和治疗动脉血压、血气分析异常、静脉压、红细胞比容和代谢异常。与母亲交叉配血的红细胞悬液或全血可用来部分换血,矫正新生儿严重的贫血,甚至是因为非免疫性因素引起的胎儿水肿。肺表面活性物质和机械通气治疗肺表面活性物质的缺乏和肺发育不全,这些症状可能与水肿相关。新生儿输液量需要应用估计的体重(干重)(例如采用胎龄的第50百分位的体重)并且限制液体(如40~60ml/kg/d)直到水肿消退。血管活性药物的支持(如多巴胺)提高患儿的心输出量(Mascaretti et al. 2003;Teixeira et al. 2008)。
如果胎儿或新生儿死亡,NIHF的患儿必须行进一步检查。遗传咨询、临床照片和胎儿X线片用来评估患儿可能的畸形或骨骼发育不全。尸体解剖强烈推荐。其他治疗包括保存胎儿的血液、组织、DNA和羊水组织。胎盘检查(显微镜和组织学)主要集中在发现肿瘤、胎儿贫血、感染和代谢性疾病(Desilets et al. 2013)。

引自:新生儿学:理论与实践(第2版)(上、中、下卷).第2版.ISBN:978-7-117-34390-9.主编:

引自:新生儿学:理论与实践(第2版)(上、中、下卷).第2版.ISBN:978-7-117-34390-9.主编:

引自:新生儿学:理论与实践(第2版)(上、中、下卷).第2版.ISBN:978-7-117-34390-9.主编:

引自:新生儿学:理论与实践(第2版)(上、中、下卷).第2版.ISBN:978-7-117-34390-9.主编:













