英文名称 :acoustic neurinoma
中文别名 :前庭神经鞘瘤;听神经瘤
前庭神经瘤主要起源于前庭神经的鞘膜,来源于前庭神经纤维本身的神经纤维瘤型则相当罕见。前庭神经瘤是颅内神经鞘瘤中最多见者,占颅内神经鞘瘤的90%以上,占颅内肿瘤的8%~11%,占脑桥小脑角肿瘤的75%~95%。流行病学估计发生率为1/10万或1.3/10万。随着影像学(特别是MRI)检查的普及,无症状的前庭神经瘤可能会增加。成年人多见,平均发病年龄为37.2岁,发病年龄高峰为30~49岁,占总数60%;15岁以下和65岁以上罕见,女性略多于男性。华山医院近10年资料为;平均年龄47.6±12.2岁,发病高峰年龄为40~60岁,占总数57.2%;20岁以下及80岁以上占1.1%,男女比例为0.8∶1,女性略多发。前庭神经瘤大多数位于一侧,基本平均分布于左、右两侧,少数为双侧。绝大多数前庭神经瘤发生于听神经的前庭神经支,故近来也称之为前庭神经鞘瘤(vestibular schwannoma),而少数不到10%的发生于耳蜗神经支的神经瘤则命名为耳蜗神经瘤。
第一例听神经瘤(前庭神经瘤)是Sandiforte(1777)在尸体解剖中发现。以后有先描述了其临床表现,后在患者死亡解剖证实的案例(Lasource,1810;Bell,1830)。多数认为Annandalet(1895)成功完成世界上第一例前庭神经瘤手术,患者为一名年轻的妊娠妇女,右侧听力丧失,术后存活并成功分娩。在随后的几十年中,前庭神经瘤的手术死亡率达80%以上。20世纪初期Cushing通过改良外科手术技术,将听神经瘤的术后死亡率由50%降低到11%;Dandy进一步努力,不仅降低手术死亡率,而且提高肿瘤全切率,以减少肿瘤复发。到20世纪60年代,随着手术显微镜的使用和显微外科技术的发展,死亡率显著降低,House(1964)报道手术死亡率已降为5.4%;同时神经外科医师们开始致力于手术入路的改进,面神经、听神经在解剖和功能上的保留,以及手术并发症的减少。目前前庭神经瘤平均手术死亡率为0%~1%,总体面神经功能保留率在50%~70%;瘤体直径在2cm以下的小型前庭神经瘤的面神经功能保留率在80%~90%,听力保留率达30%左右。部分小型前庭神经瘤(直径小于2cm)和大型前庭神经瘤术后残留者已可使用γ刀和射波刀治疗,在肿瘤控制和神经功能保留等方面获得满意疗效。
从解剖角度看,听神经包括前庭神经和耳蜗神经,与面神经共同走行于内听道中。听神经颅内部分长17~19mm,从脑干到内听道口无神经鞘膜,仅为神经胶质细胞和软脑膜被复,至内听道口穿过软脑膜后,由神经膜细胞被覆,故其多发生在内听道内的前庭神经鞘膜,并逐渐向颅内扩展(图1)。绝大多数前庭神经瘤发生于听神经的前庭神经支,最新研究表明,肿瘤最常见起源于下前庭神经,然后是上前庭神经。而少数不到10%的发生于耳蜗神经支的神经瘤则命名为耳蜗神经瘤。
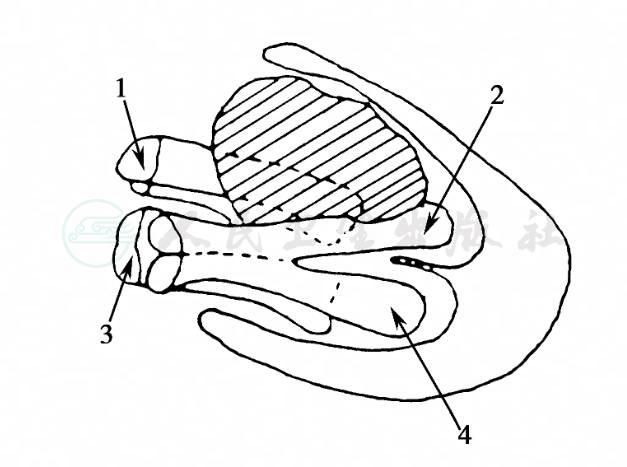
图1 内听道口发生的前庭神经鞘瘤
1.面神经;2.上前庭神经;3.耳蜗神经;4.下前庭神经
在组织学上前庭神经瘤可以为神经鞘瘤,也可以是神经纤维瘤,以前者为主。其组织学形态在镜下可分4种:①Antoni A型细胞为主;②Antoni B型细胞为主;③上述两种细胞混合的肿瘤;④神经纤维瘤型。大多数听神经瘤以Antoni A型为主,囊性肿瘤以Antoni B型为主,MRI上不均匀一致的大肿瘤多为Antoni A和Antoni B混合型或Antoni B型。可见大量的泡沫细胞,与肿瘤呈浅黄色有关;肿瘤内偶见砂粒体,极少数可有钙化。前听神经瘤绝大多数为良性,WHO(2007年)肿瘤分类中归为Ⅰ类,迄今未见恶性变的报道。虽然周围神经的神经纤维瘤可以恶变,但在中枢神经系统的神经纤维瘤基本保持良性。
多发性的颅内神经鞘瘤主要为神经纤维瘤(neurofibroma),多伴有颅内其他肿瘤如脑膜瘤、胶质瘤等和其他多种先天畸形,组成神经纤维瘤病。载瘤神经梭形扩大,肿瘤组织长于神经鞘膜内,将神经纤维分隔,这是在遗传因子的影响下神经鞘膜细胞广泛瘤变的结果,属常染色体显性遗传。在组织学上由不规则排列的双极细胞组成,附有尖细的突起,其间质主要由排列成波浪状的胶原纤维组成,常伴有玻璃样变和黏液样变。而常见的如双侧听神经瘤则属神经纤维瘤,为神经纤维瘤病Ⅱ型,是一种常染色体显性遗传的系统性疾病。
从巨体标本来看,前庭神经瘤是一具有完整包膜的良性肿瘤,表面光滑,有时可呈结节状。肿瘤大多从内听道内开始生长,逐渐突入颅腔,将脑桥池的蛛网膜推向内侧,故肿瘤表面均覆盖有一层增厚的蛛网膜,并包含有脑脊液,外观像一个蛛网膜囊肿;肿瘤小者局限在内听道内,直径仅数毫米,可仅有内听道扩大,随着肿瘤的不断增大,大者可占据整个一侧颅后窝,可向上经小脑幕长入幕上,下方可达枕骨大孔,内侧可越过脑桥的腹侧达对侧。相邻的脑神经、小脑和脑干等结构可遭受不同程度的推移,面神经、三叉神经可被压向前方或前上方,向下延伸至颈静脉孔可累及舌咽神经、迷走神经及副神经,向内可压迫脑干、小脑和第四脑室。肿瘤的实质部分外观色灰黄至灰红色,质地大多较脆,有时也可因瘤组织的退行性变或脂肪性变而偏软、偏韧、呈淡黄色;瘤内常有大小不等、多房性的囊变,内含淡黄色囊液,部分肿瘤可几乎全部囊变。肿瘤一般与脑干、小脑有明显的蛛网膜边界,但肿瘤较大时与小脑半球相邻面黏着较紧,一般不侵犯小脑实质,脑干面多光滑。面神经位置多在肿瘤的前下方,紧贴在肿瘤的包膜外伴同进入内听道内,粘连较紧,肉眼分离困难,仅在肿瘤较小和囊变时易分离,但内听道口脑膜与肿瘤黏着较紧,该处仍是保留面神经的难点。
肿瘤的血供主要来自小脑前下动脉,该动脉从基底动脉的下1/3处的侧面发出,分支进入肿瘤包膜,从基底动脉发出的脑桥动脉、小脑上动脉、小脑后下动脉、内听动脉及小脑表面的动脉等也可有分支供应肿瘤,肿瘤血供可从中等至丰富。其静脉回流主要通过岩静脉汇入岩上窦。
主要的检查项目如下。
实验室检查:
1.听力试验
主要用于区分传导性或感音(神经)性耳聋。从耳科角度看,传导性耳聋为中耳病变,感音性耳聋为耳蜗或第Ⅷ脑神经病变,而前庭神经瘤则被认为是耳蜗后的病变,在肿瘤局限于内听道内时,该类检查具有早期诊断价值。
最简单的听力试验是音叉试验,传导性耳聋为气导<骨导,即气导骨导比较试验(Rinne)为阴性,而感音性耳聋为气导>骨导,即Rinne试验为阳性;两侧骨导比较试验(Weber),传导性耳聋音偏向患侧,感音性耳聋偏向健侧。音叉试验只是大致了解耳聋的情况,在两耳听力相差太大时,骨导可传至健侧而产生假象,可用电测听机进行严格的检查。
(1)纯音听力检查:
前庭神经瘤主要表现为高频纯音听力丧失的感音性耳聋。但不能鉴别耳蜗病变及耳蜗后病变。
(2)语言辨别率测定:
测定语音辨别率对判断听力障碍的性质具有较大参考价值,传导性耳聋的辨别率不变,曲线在横坐标上右移,感音性耳聋有语音辨别率的下降,曲线形态有明显不同。前庭神经瘤均有语音辨别率的下降,甚至可低达0%~30%。
(3)复聪试验:
也称为双耳交替音响平衡试验(ABLB)。指在感音性耳聋中,如耳蜗病变,增加纯音的强度时,患耳响度的增加速度大于正常,因此测定双耳对某一音频判断为等响度时所需增加的分贝数,患耳必定少于健耳,为复聪阳性。复聪试验可用于鉴别耳蜗器官疾病和耳蜗后病变,耳蜗病变如Meniere病、耳蜗型耳硬化、迷路炎等均为复聪阳性,而前庭神经瘤或听神经损伤均为复聪阴性。
(4)强度辨别阈试验(DL):
有复聪现象的患耳对声强的微小变化敏感,故可用该试验进一步明确有无复聪现象。
短增量敏感指数试验(SISI):同样可明确有无复聪现象,辨别耳蜗病变或耳蜗后病变,前庭神经瘤其指数常在20%以下。
(5)阈音衰减试验(MTDT):
正常耳及传导性耳聋没有阈音衰减,耳蜗病变衰减程度较轻,而耳蜗后病变阈音衰减明显,其对前庭神经瘤的诊断率据报道为70%~80%。
(6)Békésy听力计试验:
是一种特殊的能自动记录的听力计,可发生100~10 000Hz缓慢增频的连续音和各种频率的间断音,根据两者之间的关系分为四型,3、4型多见于耳蜗后病变,在前庭神经瘤中常见。
(7)镫骨肌声反射试验:
可用来区别耳蜗病变和耳蜗后病变。镫骨肌反射弧见,耳蜗病变其反射仍在正常范围,而耳蜗后病变则反射减弱或消失。其在纯音检查较正常的患者中诊断率可高达90%。
2.前庭功能试验
(1)冷热水(变温)试验:
可发现患侧的前庭功能消失或减退,是诊断前庭神经瘤的常用方法。但由于前庭核发出的纤维经脑桥交叉至对侧时位于浅部,易受较大桥小脑肿瘤压迫,故可有10%健侧的前庭功能受损。
(2)前庭神经直流电刺激试验:
该试验可鉴别迷路病变与前庭神经病变,用于早期诊断鉴别前庭神经瘤和耳蜗病变。直流电刺激前庭系统时可引起平衡失调及眼球震颤,眼球震颤的快相总是指向阴极一侧,迷路病变该反应存在,而前庭神经病变则完全消失。
3.脑干听觉诱发电位(BAEP)
用短声反复刺激双耳,从头皮电极可记录到一组由连续的7个波形组成的电位活动。在前庭神经瘤中最具特征性的BAEP表现是患侧Ⅰ~Ⅴ波的波间潜伏期延长和两耳Ⅴ波的潜伏期差异的扩大,据此可明确区别耳蜗病变和耳蜗后病变,并可发现直径小于1cm、普通CT难以显示的小型前庭神经瘤。同时,BAEP也可用于术中听力保护的监护手段。
4.面神经功能试验
由于面神经、听神经同位于内听道内,较小的前庭神经瘤即可影响面神经的功能,故测试面神经功能有助于前庭神经瘤的早期诊断。
(1)味觉定量试验和流泪试验:
患侧的味觉减弱和流泪减少均有助于前庭神经瘤的早期诊断。
(2)眼轮匝肌反射试验:
用单次电脉冲刺激三叉神经的眶上支或面神经的颧颞支可引起同侧眼轮匝肌的收缩反应,分别称为三叉神经面肌反射和面神经面肌反射。早反应限于刺激侧的眼轮匝肌,迟反应见于双侧眼轮匝肌,早反应潜伏期延长或消失,迟反应潜伏期明显不对称、延长或消失等现象,均可见于前庭神经瘤,但只有肿瘤影响三叉神经及面神经时才出现,故对听神经瘤的早期诊断价值不大。
5.听觉脑干反应(auditory brainstem response,ABR)
测定是较灵敏的听觉检查,对于听神经瘤的诊断尤为重要。ABR可以详细记录听觉刺激引起的耳蜗神经和听路的神经活动,灵敏度71%~98%,特异度74%~90%。在微小听神经瘤患者,ABR的灵敏度明显降低。ABR可用于听神经瘤的早期诊断。也可用于术前评估听力保留可能性。
6.影像学检查
随着影像技术的不断提高,尤其是CT及MRI的普及应用,对出现类似临床症状的患者,如能考虑前庭神经瘤的可能而早期检查,则早期诊断亦不困难且简便易行。下列各项影像学方法是较常用的。
(1)X线片:
31.6%~81.5%的病例可见内听道的扩大和岩骨嵴的破坏,可用标准前后位、30°前后位(towne位)、45°前后位(stenvor位)及颏顶位(颅底位)来显示内听道。两侧内听道宽度可有1~2mm的差异,超出则有诊断意义。岩锥薄分层摄片:可获得内听道全长的图像,并可对双侧内听道宽度进行对比,相差超过2mm以上时具有诊断价值,同时可了解内听道前后壁的骨质破坏情况。
(2)CT扫描:
前庭神经瘤在CT普通扫描常表现为均匀的等密度或低密度占位病灶,少数为略高密度,肿瘤内钙化极罕见,不仔细分辨常易遗漏,但在中等以上的听神经瘤可依据第四脑室移位、环池翼增宽等间接征象来判断桥小脑角的占位情况,再行增强CT或MRI明确病灶(图2)。静脉注射造影剂增强后,肿瘤表现为桥小脑角的高密度区,呈均匀或不均匀强化,中间可有不规则的低密度区,代表肿瘤的囊变和脂肪变。约有80%的病例可出现瘤周的水肿带。在CT的骨窗位可显示双侧内听道宽度,并了解有无骨质破坏,51%~85%的病例可见内听道扩大,呈漏斗状(图3)。高分辨率CT做岩骨的连续断层,可显示内听道内的微小肿瘤。大型前庭神经瘤可伴有脑室系统的扩大。
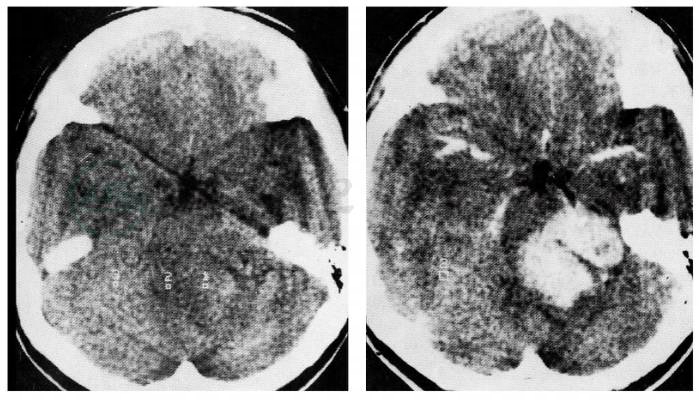
图2 前庭神经鞘瘤
CT平扫示第四脑室受压向右移位;CT增强示病灶均匀强化,边界清楚,伴轻度脑水肿
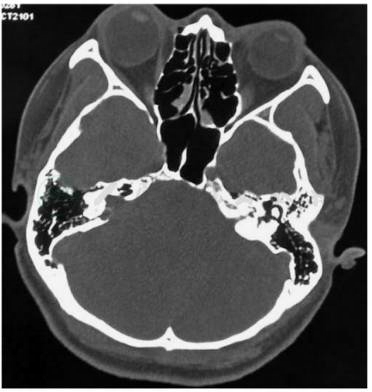
图3 右侧前庭神经瘤,CT骨窗位显示右侧内听道扩大
(3)MRI成像:
由于MRI的高对比度、可三维成像和无颅骨伪影影响的特性,已成为诊断前庭神经瘤最为敏感和可靠的方法之一。前庭神经瘤在T1加权图像上为略低信号或等信号,呈边界清楚的占位病灶;T2加权则为明显高信号,肿瘤边界可与水肿带混淆。肿瘤信号可呈均匀一致,也可以有囊变,其囊变区在T1加权显示为明显低信号。少数肿瘤可伴发出血,在血肿与囊变交界处可形成液平。在静脉注射造影剂后,其实质部分明显出现增强,信号上升,但囊变部分无强化。
MRI可清楚显示听神经瘤的大小,形态及与相邻结构的关系(图4)。当肿瘤较小(10~15mm或更小)时,表现为内听道内软组织块影,尤其在T1加权图像上由于脑脊液为较低信号,与肿瘤信号对比明显,对了解肿瘤的大小、形态极为有利。当肿瘤较大时,表现为扩展至岩尖和桥小脑池的圆形或分叶状、边缘清晰的肿块。在T2加权图像上由于肿瘤和脑脊液均为高信号,与低信号的内听道骨壁对比明显,可清楚显示内听道。当肿瘤增大,常伴周围薄层脑组织水肿带,在T1为低信号,T2为高信号。在较大的听神经瘤可出现明显的脑外占位征象,与CT表现相似,但因MRI无颅骨伪影,显示尤为清楚。
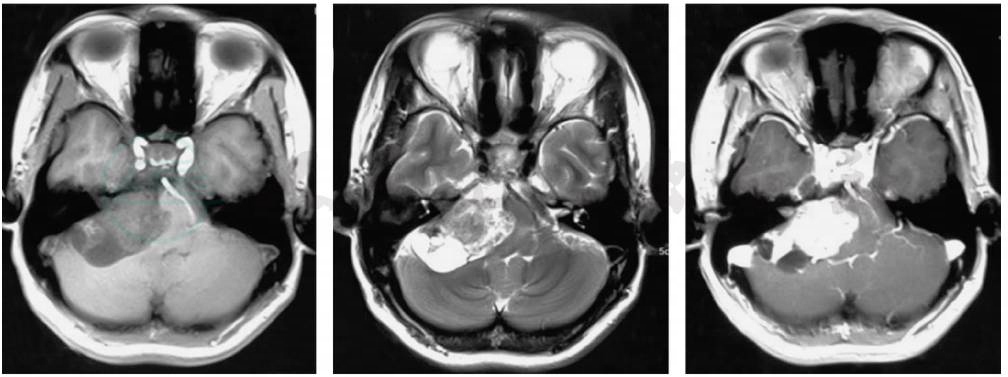
图4 右前庭神经鞘瘤
MRI平扫:在T1加权图像上为略低信号或等信号,呈边界清楚的占位病灶,脑干受压;T2加权则为明显高信号,肿瘤边界可与水肿带混淆;MRI增强,实质部分明显强化,呈边界清楚的高信号病灶
(4)DSA检查:
已少用,仅用于了解不典型前庭神经瘤的血供及相邻的血管情况或用于鉴别诊断。可酌情选用CTA或MRA或DSA。
综上所述,由于目前前庭神经瘤诊断手段的多样化,前庭神经瘤的诊断多不困难,凡单侧耳鸣伴听力进行性下降者,详细的听力检查证明为神经性耳聋且无复聪现象,伴前庭功能减退或消失,则BAEP、内听道摄片及MRI均具有早期诊断价值,且MRI可明确病灶大小、部位及与邻近结构的关系,有利于治疗方法的选择。
前庭听神经瘤是良性肿瘤,治疗原则首选手术治疗,尽可能安全、彻底地切除肿瘤,避免周围组织的损伤。多数学者认为在达到肿瘤全切除后,可获得根治。其次随着γ刀、射波刀等立体定向放射外科技术的临床应用和普及,部分小型前庭神经瘤(直径<2.5 cm)和大型前庭神经瘤术后残留者均使用γ刀或射波刀治疗,在肿瘤控制和神经功能保留等方面获得满意疗效。因此如患者高龄、有系统性严重疾患或肿瘤巨大、与脑干粘连紧密等情况下,不应强求肿瘤的全切除而可做次全切除或囊内切除,残余肿瘤用γ刀照射。随着显微解剖和显微外科手术技术和方法的不断发展,包括面神经术中监护及术中脑干诱发电位监测等技术的使用,前庭神经瘤的手术全切除率和面神经、听神经的保留率均显著提高,因此在手术切除和γ刀治疗、肿瘤全切和神经保留等问题上可以综合考虑,谨慎选择,制订个体化的治疗方案。
值得强调的是,前庭神经瘤属脑外病变,其与周围的脑神经、脑干和血管之间均有蛛网膜间隙,因此在大多数情况下,术中镜下较易分离,可有效避免神经、血管的损伤。故在前庭神经瘤手术中,应重视蛛网膜间隙的辨认和保护。
1.手术入路和方法
(1)枕下-内听道入路
Dandy(1941)创用颅后窝枕下入路治疗前庭神经瘤,并为神经外科医师所普遍应用,成为前庭神经瘤手术的经典入路,但面、听神经常在肿瘤的前下方,故保留面神经较困难。Rand和Kurze(1965)改良该入路,在显露内听道口后即磨开内听道后唇,形成枕下-内听道入路,从而获得较高的面神经保留率。
手术体位有侧卧、仰卧和半坐位,切口可有各种变化,有高颅压者可先于侧脑室枕角穿刺,留置引流管,缓慢放出脑脊液。骨窗一般位于一侧枕下,外缘应暴露乙状窦,上缘暴露横窦,枕大孔后缘和寰椎后弓不必显露。剪开硬膜后,放出小脑延髓池脑脊液,小脑大多能满意塌陷。小肿瘤(直径≤2cm)应先磨除内听道上壁,自内听道内向颅内分离,切除肿瘤。大肿瘤(直径>2cm,图5)则应先分离肿瘤周围的蛛网膜间隙,囊内分块切除肿瘤,达大部切除后,游离囊壁,妥善处理肿瘤周围的神经血管及脑干面,然后处理内听道(同小型前庭神经瘤),在保留面神经的同时,应争取保留听力,因为约10%的大型前庭神经瘤(直径>3cm)患者可有残余听力,术后听力保留率可达3%~22%。
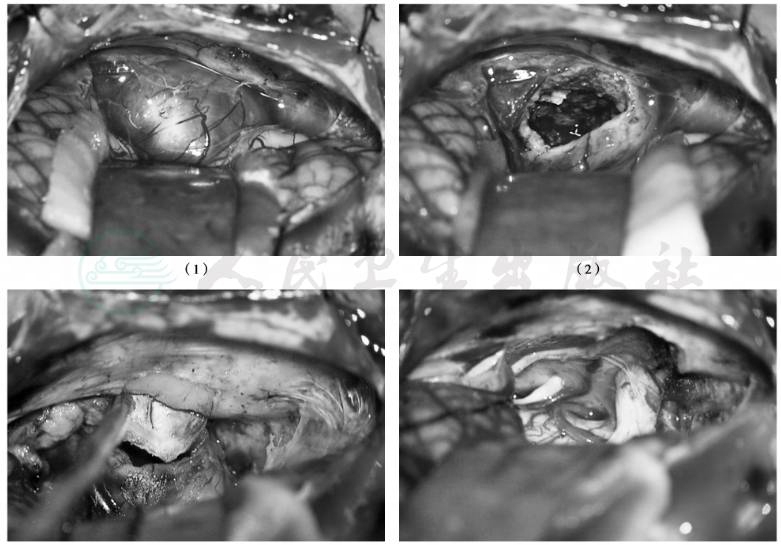
图5 前庭神经鞘瘤:大型听神经瘤的处理
(1)先切开硬膜约2cm,放枕大池脑脊液,脑压下降后向内侧牵开小脑半球,暴露肿瘤;(2)分离肿瘤表面的蛛网膜,囊内切除肿瘤;(3)磨开内听道;(4)肿瘤全部切除后
(2)经颅中窝入路
体位为仰卧位,耳前颧弓上“S”形切口,骨窗2/3位于外耳道前方,1/3在外耳道后方,靠近颅中窝底。磨除内听道上区的骨质,达内听道硬脑膜,向内显露颅后窝硬膜,向内可暴露面神经管口,手术在肿瘤的前面进行,有利于分离保护面神经。但应注意保护小脑前下动脉襻。
(3)经迷路入路
仅限于小型前庭神经瘤。耳后切口,将岩骨磨除达内听道口,切除内听道内的肿瘤,整个手术可清楚看到面神经、耳蜗神经等与肿瘤的关系,面神经的保留率提高,患者反应轻,恢复快。但因迷路破坏,故听力在术后将完全丧失,且脑脊液耳漏机会多,在较大肿瘤易致颅内出血。
前应准备神经电生理监测或面神经监护仪,以确保最大限度地保留面神经功能。电极插入到同侧的眼轮匝肌和口轮匝肌。铺巾前确认监护仪器工作正常。当试图保留听力时,术中的ABR监测是必要的。在前庭神经瘤的手术中,术中的面神经功能保护是最重要的,其次是肿瘤的全切和听力的保留。患者如果术前就出现严重的面瘫,术中面神经的解剖保留意义有限。许多研究表明,肿瘤的大小与术后面神经的功能密切相关,肿瘤越大,面神经越容易损伤。有报道在肿瘤>4cm时,有62.5%的患者术后即刻H-B分级为3级或以上;而肿瘤<2.5cm,仅有35.3%的患者术后即刻H-B分级为3级或以上;然而,约75%的患者在术后6个月后,面神经功能可恢复正常或接近正常。证实即便肿瘤较大,仍然有机会保留面神经功能。常用的面神经功能评价分级系统是House&Brackmann分级。
2.手术并发症
进入20世纪90年代后,虽然手术技术和疗效不断提高,但前庭神经瘤的手术并发症仍无法完全避免,常见的有脑脊液漏:2%~10%,颅内血肿:2%左右,术后脑积水:2%,颅内感染:1.2%~10%。
我们对华山医院神经外科1999~2013年1167例大型前庭神经瘤(T3和T4)的术后并发症进行了统计分析,脑脊液漏发生率为2%;颅内血肿为1.5%;术后脑积水为1.2%;术后感染为9.8%(近3年的术后感染率已经有明显的下降)。但最常见的仍是神经功能的损伤,包括术后面瘫、共济失调、听力丧失和后组脑神经损伤。
术后面瘫仍是大型前庭神经瘤最常见的并发症,如颅内面神经断端可以确认,应及时进行缝合,如两端连接不起来,应行神经移植,一期修复;如面神经断端无法辨认,可于术后2~4周内行颅外的面-副神经、面-舌下神经或面-膈神经吻合,于术后3~6个月可见到面肌的自主活动。术后由于面瘫,眼睑闭合不能,尤其三叉神经也受影响,则极易形成角膜溃疡导致眼内感染而失明,应及时做眼睑缝合,等神经功能恢复后拆开。对于术后共济失调和后组脑神经的损伤,及早进行术后正规的康复训练,大多数患者症状均会好转和恢复。
3.药物治疗
近来,由于分子生物学的深入研究,发现merline在神经鞘瘤发生发展的重要作用以及可干扰的靶点,为神经鞘瘤患者,特别是双侧前庭鞘瘤者,提供药物治疗手段。可是,目前的研究报告多属临床Ⅰ~Ⅱ型,尚缺乏Ⅲ型和长期随访高级别的研究资料。
(1)贝伐单抗(bevacizumab/avastin)
是一种人单克隆IgG1的抗体,抑制VEGF,已用于治疗包括胶质母细胞瘤等。MautnerVF(2010)报告静脉滴注 avastin 5mg/kg,初始90',渐减至30',每2周一次,治疗2例双侧前庭神经瘤,一例治疗6个月后肿瘤缩小40%,听力改善,另例MR示脑干受压明显减轻,空洞变小,但听力不改善,此例因有高血压,同时服用血管紧张素受体阻滞剂。Plotkin SR(2009)等报告治疗10例进展型双侧前庭神经瘤患者,瘤缩小和听力中度改善9例。
(2)PTC299
是VEGF合成上游的抑制剂,通过阻断转录后处理。目前在进行临床二期研究。虽然上述药物有一定效果,但仅部分患者有效。这是由于血管生成仅是肿瘤增生一个方面,还需寻找其他作用靶点和进行大样本验证。
(3)曲妥珠单抗(trastuzumab)
是ERBB2(鸟类verb-b2成红细胞白血病病毒癌基因同源2或神经/同源胶质母细胞瘤衍生癌基因)受体抑制剂,体外研究证实可抑制前庭脑细胞增生。它与 erlotimb(也是ERBB抑制剂)可抑制裸鼠种植前庭施万细胞生长。
(4)厄洛替尼(erlotinib)
是一种口服EGFR酪氨酸激酶抑制剂。目前用于治疗非小细胞肺癌和胰腺癌。它能促使前庭神经膜细胞死亡,但临床治疗11例双侧前庭神经瘤患者,MR未见肿瘤缩小,听力未改善。由于它作用于EGFR各体以外肿瘤增生的分子通路,值得进行临床二期验证。另一优点是没有细胞毒性化疗剂的副作用,可长期服用。
(5)拉帕替尼(lapatinib)
是一种同时抑制EGFR和HER2[百同源E6-AP(UBE3A)羧端域和染色体浓缩调控因子(CHCI)样域(RLD)2]制剂,也能抑制ERBB2磷酸化。2007年美国FDA批准治疗乳腺癌脑转移,效果令人鼓舞。目前正在临床前期研究。
【双侧听神经瘤】
双侧听神经瘤约占听神经瘤总数的1%~2%。多为多发性神经纤维瘤病的一种或部分表现,也将其归入Ⅱ型神经纤维瘤病,为常染色体显性遗传,发病年龄较轻。患者除有双侧听神经瘤外,可伴有皮肤、皮下组织、周围神经和脊髓的多发性神经纤维瘤,有时还伴有颅内其他肿瘤如脑膜瘤、胶质瘤等,或伴各种先天性畸形,皮肤上可有棕褐色斑,称为“牛奶咖啡斑”。
双侧听神经瘤的手术效果很差,术后听力损害和面瘫的发生率较高,手术的关键在于如何保留面神经功能和听力,因双侧永久性面瘫和失聪将是正常生活的重大障碍。因此如双侧听神经瘤导致明显的颅内高压,威胁患者的生命时,可手术切除一侧较大的肿瘤,保留较小的肿瘤,用γ刀控制其生长。如双侧肿瘤均较大,也可双侧同时手术或分期手术,但至少要保留一侧的面神经,如一侧不能保留面神经,则对侧只能做包膜下切除,残余肿瘤进行γ刀治疗,绝不可强求双侧肿瘤的全切除。如双侧肿瘤均在2.5cm以内,可同时手术切除,但应努力保留双侧面神经和听力,也可同时行γ刀治疗。













