英文名称 :viral anterior uveitis
前葡萄膜炎是最常见的葡萄膜炎类型,约占全部葡萄膜炎的75%。虽然多数前葡萄膜炎的病情程度较轻,但是其容易反复发作,并可引起瞳孔后粘连或膜闭、白内障及青光眼等并发症,从而导致严重的视功能损害。
在传统病因学分类中,HLA-B27相关性前葡萄膜炎和特发性前葡萄膜炎是最为常见的前葡萄膜炎亚型,然而近年来,随着分子生物学诊断技术的发展及其临床推广应用,病毒性前葡萄膜炎逐渐被眼科医生所认识。
大量研究显示,在以往诊断为“特发性”前葡萄膜炎、Fuchs葡萄膜炎综合征(也称Fuchs异色性虹膜睫状体炎)、青光眼-睫状体炎综合征(Posner-Schlossmann syndrome),简称青-睫综合征的病人中,有相当一部分是由病毒感染所致,或与病毒感染相关。譬如,一项来自泰国北部的研究显示,在除外了相关系统性疾病和常见非病毒性系统性感染(如梅毒、结核和HIV)的“不明病原”的前葡萄膜炎后,在67%(20/30)的病人房水中,用 PCR和/或Goldmann-Witmer(GW)系数法检测,可以检测出病毒并确定为病毒感染[1]。
1.导致前葡萄膜炎的常见病毒
· 单纯疱疹病毒(HSV-1和HSV-2)
· 水痘-带状疱疹病毒(VZV)
· 巨细胞病毒(CMV)
· 风疹病毒(RV)
其他少见病毒,如EB病毒、腺病毒、人类疱疹病毒6型(human herpes virus6 HHV6)、人类嗜 T 淋巴细胞病毒(human T-cell lymphotropic virus type-1,HTLV-1)等导致的前葡萄膜炎也有报道。在文献报道的引起前葡萄膜炎的病毒中,欧洲及北美发达国家以HSV和VZV较为常见,而亚洲国家以CMV更为多见[2]。
2.临床特征
病毒性前葡萄膜炎的病人多为免疫功能正常者,其前葡萄膜炎具有一些共同的临床表现特征,主要包括:
(1)弥漫性分布的细小KP,或星芒状KP。
(2)常伴有眼压升高。
(3)虹膜萎缩等[3,4]。
但是,不同类型病毒引起的前葡萄膜炎又有各自的临床特点(表1),甚至某些病人可以表现为Fuchs葡萄膜炎综合征,或青-睫综合征等[5,6]。
表1不同病毒所致前葡萄膜炎临床特点及其对应综合征
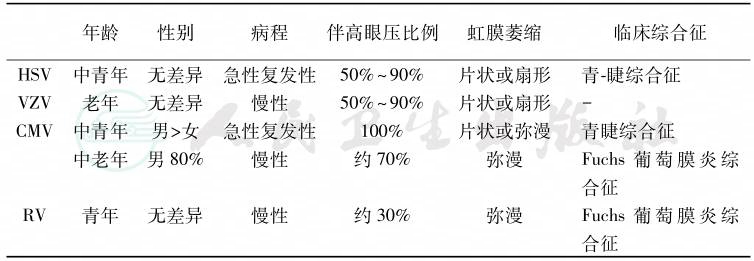
HSV:herpes simplexvirus,单纯疱疹病毒;VZV:varicella-zoster virus,水痘-带状疱疹病毒;
除非合并眼邻近部位或眼其他部位组织感染的特征性表现,如VZV累及三叉神经第一支引起的额面部皮肤疱疹,或单纯疱疹病毒导致的病毒性角膜炎,一般情况下,根据眼前节的临床表现,仅能做出疑似病毒性前葡萄膜炎的临床诊断,而病因学诊断则需要依靠明确的病原学证据。
1.房水抽取方法
目前常用的方法是前房穿刺抽取房水做病毒检测(表2)。
北京协和医院眼科葡萄膜炎专业组推荐的前房穿刺抽液方法如下:取液前准备参照白内障手术前滴用抗生素滴眼液3天(如0.3%左氧氟沙星或0.5%左氧氟沙星等氟喹诺酮类滴眼液,或0.3%妥布霉素等氨基糖苷类滴眼液),4次/天,或术前频繁点眼(6~8次,间隔10分钟以上)[10];之后,用5%聚维酮碘消毒结膜囊30秒;拔掉1ml注射器(25G针头)的活塞,并将其置于无菌巾上,在手术室显微镜下,将连着针筒的针头穿刺进入前房,在眼压作用下房水会缓慢进入针筒,术者应同时观察前房深度,当前房较浅时,拔出针头(一般抽取房水量约为0.1ml),再用注射器活塞将针筒内的房水推入无菌离心管,立即送检病毒检测。
表2诊断性前房穿刺抽液的方法

2.房水病毒检测方法
目前房水检测病毒的方法主要有两大类:病毒核酸检测与GW系数法。
(1)病毒核酸检测:
主要是基于PCR的技术,包括普通PCR、多重PCR、定量实时PCR(quantitative real-time PCR)以及检测PCR产物的基因芯片技术等。
1)DNA病毒核酸检测:
表3中列举了文献中报道[4],并经作者实验重复[11]验证的用于检测玻璃体和房水中HSV-1、HSV-2、VZV及CMV等病毒DNA的引物序列。
表3多重PCR法检测房水中病毒DNA的引物及预测的溶解和退火温度
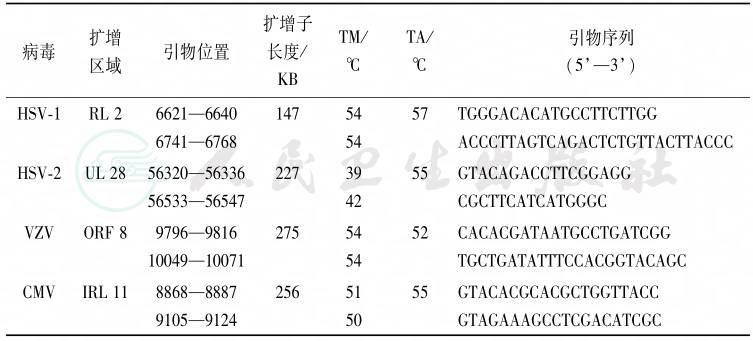
TM:melting temperature,溶解温度;TA:annealing temperature,退火温度。
2)RNA病毒核酸检测:
风疹病毒为RNA病毒,可用以下设计引物及实验条件[12]:
引物 1(ATGGCACACACACCACTGCT)
引物2(CAAGCGAG(CT)AAGCC(AG)GCGAG)
在37°C逆转录50分钟,然后用上述引物行第一轮巢式PCR,接着用:
引物3(ACCACTGCTGTGTCGGAGACCCGG)
引物4(TAAGCCAGAGAGT(AG)GGAGGGCGCA)
行第二轮巢式PCR,温度条件为:95℃变性5分钟,然后30个如下循环(95℃30秒、55℃45秒以及72℃60秒),最后72℃5分钟延长。扩增产物可用琼脂糖凝胶电泳染色法或Southern印迹法,检测相应的扩增片段,以定性判断受检标本中是否存在某种病毒核酸。
(2)GW系数法:
GW系数是另一确诊病毒性前葡萄膜炎的方法,此法通过检测房水中的病毒特异性抗体IgG、房水中总IgG、血清中病毒特异性抗体IgG,以及血清中总IgG含量,再根据公式计算得出系数,据此系数的高低判断是否为病毒感染,其计算公式如下:

目前,多数研究将GW系数的临界值设置为3.0,即针对某一病原的GW系数大于 3.0 时,检测结果判断为阳性[13,14]。
3.房水病毒检测时应注意的问题
(1)病程对两种方法的阳性率均有影响,其中由于急性期和进展期病人存在病毒的活跃复制,因此,PCR法阳性率较高;而慢性期或抗病毒治疗后的患者,其病毒复制活性较低,因此,PCR法阳性率较低。
(2)GW系数法测量的是房水和血清中抗病毒的特异性抗体IgG,由于感染后抗体产生需要一定时间,在病程早期阳性率较低,而慢性期相对较高。
在临床应用中,对于病毒检测结果的诊断意义判断,需要注意以下几点:
1.目前,尚无诊断病毒性前葡萄膜炎的金标准,文献中只报道了疑诊病毒性前葡萄膜炎病人房水中某种病毒核酸检测的阳性率和GW系数的阳性率,并无这些检测方法精确的敏感性和特异性数值的报道。虽然有些研究也比较了不同检测技术之间的差异,比如,用多重PCR和定量实时PCR检测葡萄膜炎眼内液(房水和玻璃体)标本中疱疹病毒家族核酸,发现多重PCR的定性判断比定量PCR方法(临界值为50×103/ml)的阳性率要高[15],但是,由于目前尚无被正式批准用于检测眼内液的定量PCR试剂盒,这一结论仅限于该研究所采用的特定方法,以及解释其所检测病人的结果。
最近,著者利用多重PCR和X-TAG液态芯片技术检测了典型急性视网膜坏死(ARN)病人患眼的玻璃体和房水标本,发现以上两种方法检测结果完全一致,且VZV及HSV的阳性率可达94%(17/18),且特异性达100%(典型ARN的临床表现作为金标准)[11]。但是,这两种方法对病毒性前葡萄膜炎房水标本检测的可靠性尚需要验证。
同样,由于尚无诊断的金标准,GW系数的临界值设置为3.0,也是参考眼弓形虫病等其他眼内感染检测结果判定的标准而定,而不是通过前房液标本的病毒检测数据得到的标准[16],所以,临床应用该法时,仍应密切结合临床表现特征,综合加以判断分析。
2.对于大多数感染性葡萄膜炎,同时行病毒核酸检测和GW系数检测可提高病原的检出率[13,14],因此,建议同时进行这两项检查。对于病毒性前葡萄膜炎(HSV-1、HSV-2、VZV及CMV等)的房水病毒检测来说,一般情况下,PCR核酸检测法比GW系数法阳性率更高[6,16],而且PCR检测设备和技术应用的更为广泛。
但是需要指出的是,多项研究显示,在RNA病毒引起的前葡萄膜炎检测中,核酸检测法的敏感性很低,反而GW系数法要远高于前者[6]。此外,房水中病毒检测的阳性率与病情严重的程度、病程的不同阶段明显相关,另外,抗病毒治疗也可能会降低房水中病毒核酸的检出率[17]。
3.尽管对病毒性前葡萄膜炎的认识日渐加深,但是,迄今为止对诊断性前房穿刺术的适应证尚未达成专家共识,因此,著者认为:
(1)实际临床工作中,应充分认识到临床诊断比房水病原学检测更为重要。
(2)尽管房水的病原学检测是病毒性前葡萄膜炎病原学诊断的唯一方法,但是,由于目前对房水病原学检查方法(包括单一,或两者联合)的敏感性和特异性尚不清楚,因此无法准确得知房水病原学检查的阴性预测值和阳性预测值。
阳性预测值和阴性预测值分别是指阳性和阴性诊断试验结果所估计的受检者患病和不患病的可能性,是最具有临床指导意义的参数,其计算公式如下:

(3)对房水病毒检查的临床意义仍需要进一步研究。美国Bascom Palmer眼科研究所的一项回顾性研究显示,在前葡萄膜炎病人中,仅有约13%(7/53)因房水检测到病毒,而改变了治疗方案[18];而在另一项研究中,只对具有特征性虹膜节段萎缩(但无病毒性角膜炎其他临床表现)的前葡萄膜炎病人房水进行了检测,在96%(23/24)的标本中检测到HSV或VZV(PCR联合GW法),而所有标本的CMV检测均阴性[16]。这两个研究说明,在没有病毒性前葡萄膜炎的特征性临床表现的病人中,房水病原学检测的阳性率很低,而有诊断意义的临床体征甚至比房水检测更为重要。
然而,也有学者认为,在怀疑感染性前葡萄膜炎时,应尽早行房水病原学检测,以尽快给予针对性的抗病毒治疗,从而减少单纯以糖皮质激素治疗所带来的病情容易反复的问题[19]。
1.导致病毒性前葡萄膜炎的主要病毒包括:单纯疱疹病毒、水痘-带状疱疹病毒、巨细胞病毒及风疹病毒。
2.弥漫性分布的细小或星芒状KP、眼压升高、虹膜萎缩为三个常见临床体征。
3.前房水病毒检测方法主要包括病毒核酸检测和GW系数法。
4.在缺乏专家共识的情况下,病毒检测结果要密切结合临床表现进行综合分析。













