心力衰竭(cardiac failure)是新生儿期常见的危急重症,也是围产儿死亡的主要原因之一。新生儿心力衰竭是指新生儿期由于各种原因导致心脏前、后负荷增加或心肌本身病变引起心脏泵血不能满足血液循环和组织代谢需要而出现一系列病理征象。由于新生儿的自身特点,临床表现不典型,易与其他疾病混淆,又受原发病的影响,早期诊断困难,如不能早期识别与及时处理,常可危及生命。
1.心室功能不全
心室功能不全包括收缩性或舒张性功能不全,可发生于CHD患儿和心脏结构正常患儿。心室收缩功能不全,即心室收缩力降低;心室舒张功能不全是指心室充盈受损,心肌顺应性降低引起压力-容积关系差异极大,导致心室充盈压较高。心室功能不全多由CHD所致;此外,心脏结构正常者,由于心脏自身原因(心脏性病因)或外在原因(非心脏病因)也可引起心室功能不全。
(1)CHD:
患儿在就诊时可能有心室功能不全,但更常是在心脏缺损修复术后几年甚至几十年后发生心室功能不全和心力衰竭。
(2)心脏结构正常患儿发生心室功能不全的心脏病因:
①心肌病:如扩张型心肌病、肥厚型心肌病等是心脏结构正常患儿发生心力衰竭最常见的原因。②心肌炎:通常是病毒感染引起,有时也可由非病毒性病原体或非感染性因素引起。③心肌缺血/梗死:新生儿罕见。出生时即有左冠状动脉异常起源于肺动脉的婴儿,常表现为心肌缺血/梗死的症状和体征,通常有心力衰竭。④心律失常:如完全性心脏传导阻滞、室上性和室性心律失常(室上性心动过速、心房扑动、心房颤动、异位性房性心动过速及阵发性交界区折返心动过速、交界性或室性心动过速、心室颤动)可导致心室功能不全和心力衰竭。应用药物或消融方法控制心律失常多能改善心室功能。⑤药物/毒素作用:采用化疗药物(尤其是蒽环类药物)治疗的癌症患儿,终身都有发生心室功能不全和心力衰竭的风险。
(3)心脏结构正常患儿心室功能不全导致心力衰竭的非心脏病因:
①败血症或脓毒症;②呼吸系统疾病,如BPD、囊性纤维化和间质性肺疾病,这类疾病可引起肺动脉高压和右心衰竭;③其他疾病,如新生儿SLE、窒息、贫血、失血等。
2.容量或压力超负荷
许多因素可致心脏长期处于容量或压力超负荷状态,早期心室收缩力正常,但最终导致心力衰竭。
(1)容量超负荷:
①心脏性:由于体循环与肺循环间存在中或大的交通(分流),导致容量超负荷,可发生于以下心脏病变:室间隔缺损、动脉导管未闭、房间隔缺损(罕见)、主-肺动脉窗、房室隔缺损、功能性单心室(肺血流无梗阻型)、主动脉瓣关闭不全、二尖瓣关闭不全、肺动脉瓣关闭不全等。②非心脏性:心室泵功能正常时容量超负荷性心力衰竭也可由动静脉畸形(心外分流)、液体过剩(如少尿型肾衰竭)等非心脏性病因所致。
(2)压力超负荷:
可能是CHD伴重度心室流出道梗阻,妨碍心脏射血,导致心排血量不足和/或充盈压较高所致。根据严重程度和病程长短,压力超负荷可能引起收缩性或舒张性功能障碍,见于主动脉瓣狭窄、主动脉缩窄、肺动脉狭窄等。
3.其他病因
重度高血压时可发生心室功能不全;肺动脉高压引起右心室压力超负荷,可导致右心衰竭。
心力衰竭时血流动力学指标的改变包括按体表面积计算的心排血量的心脏指数(CI)、血压、中心静脉压(CVP)和肺毛细血管楔压(PCWP)等。心力衰竭时,CI减少,血压降低,组织灌注不良,心室舒张末压增高。左心室舒张末压增高,引起右心房压、肺静脉压和PCWP升高,出现肺循环淤血;当出现右心衰竭时,右心室舒张末压和右心房压升高,CVP超过12mmHg(1.6kPa),出现体循环淤血。
1.脑钠肽(BNP)和氨基末端脑钠肽前体(NT-proBNP)水平
BNP和NT-proBNP检测已用于多种儿科心脏疾病(CHD、心肌炎、心肌病、肺动脉高压等)所致心力衰竭严重程度和监测疗效的评估。BNP和NT-proBNP水平出生时较高,出生后几天内迅速下降。BNP和NT-proBNP检测在提示结构性和功能性心脏病方面具有一定意义,BNP测定有助于区分心脏性疾病与非心脏性病因的心力衰竭症状,前者升高明显,后者无明显变化。
2.肌钙蛋白(Tn)
TnI和TnT是心肌损伤的敏感标志物。心肌炎和心肌缺血时,Tn水平升高。有左室功能不全的患儿,Tn水平升高可能提示急性心肌炎。
3.全血细胞计数
中到重度室间隔缺损的患儿贫血可促发心力衰竭;预先存在心力衰竭的患儿贫血可加重心力衰竭症状。对于心力衰竭合并贫血的患儿,应寻找贫血病因并给予处理。
4.血清生化监测
包括电解质、BUN、Cr和肝功能检查。重度心力衰竭患儿可能有低钠血症;肾功能损害可能促发心力衰竭,也可能加重既存的心力衰竭;由于右心衰竭时肝淤血,所以肝功能指标可能升高。
5.胸部X线检查
胸部X线检查有助于评估心脏扩大和肺循环淤血,还可监测心力衰竭治疗效果。心力衰竭时间质性肺水肿和胸腔积液常见。
6.心电图
心电图是评估心力衰竭患儿的重要诊断性工具,最常见的心电图表现是窦性心动过速,但无特异性,这一表现是患儿每搏输出量减少的一种生理性代偿反应。有时心电图可能提示基础病因,例如ST段和T波异常在所有类型的心肌病和心肌炎中均常见;符合心室肥厚标准的QRS波电压增加,可能见于肥厚型或扩张型心肌病;QRS波电压降低,可提示心肌水肿或心包积液,也可能见于心肌炎患儿;限制型心肌病可见双心房肥大;新生儿SLE时,可能有不同程度的心脏传导阻滞;房性、交界性或室性心动过速或频繁的心房或心室异位起搏可能提示心律失常,是心室功能不全的基础病因,也可能是其并发症。
7.超声心动图
在有心力衰竭症状和体征的患儿中,超声心动图是评估心室大小和功能的主要影像学检查。其还可明确患儿的心脏结构是正常的还是有先天性心脏病。提示心室功能不全的表现有:心室收缩功能受损,如射血分数(ejection fraction,EF)<56%或缩短率(fractional shortening,FS)<29%;心室容积Z值评估为心室增大或扩张。提示容量超负荷的表现有:心房和/或心室增大;较大的间隔缺损伴大量分流;重度瓣膜关闭不全。提示压力超负荷的表现有:心室肥厚,如左室壁增厚;重度流出道梗阻,如主动脉瓣或肺动脉瓣瓣膜、瓣下或瓣上狭窄。
8.磁共振成像
心脏MRI可提供关于心脏解剖结构、心室功能、心肌炎症及脂肪和纤维组织浸润的准确和详细信息。由于行心脏MRI需要镇静、检测时间较长,在新生儿中应用受限。
9.心导管术
以下情况时,心导管术可有一定帮助:超声心动图和/或MRI无创检查后仍不清楚心力衰竭的基础病因;超声心动图上冠状动脉解剖显示不清楚或不确定但临床仍考虑冠状动脉异常;评估疑似心肌炎或鉴别限制型心肌病与缩窄性心包炎,可能行心导管术心内膜心肌活检;患儿有明确的或疑似肺动脉高压时,可行心导管术来评估PVR和血管舒张反应;心导管术还可评估心力衰竭患儿的血流动力学状态(心内压力、肺动脉压、PVR和心排血量)。
10.其他检查
根据不同临床发现,可能还需要其他检查:如有心肌病时,可能需要甲状腺功能检查、代谢性疾病筛查或基因检测等检查来明确病因;有心肌炎临床证据时,应行诊断性评估来明确其基础感染病因。
心力衰竭的治疗取决于心力衰竭的病因和严重程度,心力衰竭患儿的治疗目标是缓解症状、延缓心力衰竭进展、降低并发症和住院风险、改善患者生存和生活质量。
对于结构性心脏缺陷因容量超负荷(间隔缺损和动脉导管未闭等)或压力超负荷(肺动脉瓣狭窄、主动脉瓣狭窄、其他右室或左室流出道梗阻等)出现心力衰竭症状但心室功能保留患儿,主要治疗是采用手术或以导管为基础的干预来纠正这些基础缺陷。在等待更为确定的干预时机期间,可能需要内科干预来稳定病情或缓解症状。心室泵功能障碍患儿在实施手术或以导管为基础的纠正措施之前,应根据心力衰竭分期给予治疗以稳定病情(表3)。
表3婴儿和儿童心力衰竭分期及治疗推荐

引自:实用新生儿重症医学.第1版.ISBN:978-7-117-36408-9.主编:
1.治疗原发病
原发病及诱因的治疗是解除心力衰竭的重要措施。如复杂心脏畸形应及时手术;如有低血钙、低血糖或贫血应及时纠正;心律失常应尽快用抗心律失常药物控制;肺炎、败血症引起的心力衰竭选择适当抗生素控制感染。
2.一般监护和治疗
包括生命体征监护、适当体位、镇静、氧疗和营养支持等。
(1)监护:
严密监护心电、呼吸、血压及周围循环,必要时可进行无创心排血量监测;保持合适的环境温度及适当体位,将头抬高15°~30°(头高倾斜位);安抚患儿,避免过度哭闹和烦躁,必要时给予镇静;控制液量和输液速度。
(2)氧疗:
心力衰竭患儿均需供氧。但对依赖动脉导管未闭生存的先天性心脏病(主动脉闭锁、主动脉缩窄、主动脉弓离断、大动脉转位、左心发育不良综合征、三尖瓣闭锁等)患儿供氧应慎重,氧疗时使氧饱和度达到75%~85%即可。监测血气,纠正酸碱紊乱。必要时给予无创或有创机械辅助通气。
(3)营养支持:
心力衰竭患儿通常存在进食疲劳,摄入量可能有限,但由于代谢需求增加,需尽最大努力提供营养支持。对于某些心力衰竭患儿,每日可能需要摄取120kcal/kg以上热量才能保证最佳生长。为了保证热量摄取充足,需间断或连续进行鼻胃管或胃造口术管饲。此外,推荐重度心力衰竭患儿限盐、限液以减少容量超负荷,一般患儿液体量较正常需要量减少1/4~1/3,保持水、电解质平衡;对于严重心力衰竭患儿,应限制液体量为每日65ml/kg,并及时纠正低血糖。
3.药物治疗
药物治疗主要用于心室泵功能障碍患者,但由于新生儿数据有限,新生儿心力衰竭的药物治疗主要是基于成人研究的间接证据。对于容量超负荷或压力超负荷但心室功能保留患儿,在等待纠正基础缺陷期间,初始也可使用药物治疗来稳定病情和缓解症状。出现不明原因休克的新生儿,应开始输注前列腺素,并应持续至超声心动图检查排除导管依赖性先天性心脏病。对于心室功能降低的患儿,持续的房性和室性快速性心律失常可迅速损伤血流动力学,若纠正电解质异常和其他可能诱因后并未缓解或耐受性差,则需要抗心律失常治疗;若患儿病情极其不稳定,则可能要行心脏复律或除颤。
(1)血管紧张素转化酶抑制剂(angiotensin-converting enzyme inhibitor,ACEI):
ACEI可抑制血管紧张素Ⅱ生成,血管紧张素Ⅱ是一种强效的血管收缩剂,也能促进心肌细胞肥大、纤维化和醛固酮分泌。B期和C期心力衰竭患儿的一线治疗可采用ACEI,用药期间应密切监测血压和肾功能。ACEI使心力衰竭患儿首先获益的是降低后负荷,提高心排血量,长期使用时可介导左室重构逆转。
1)卡托普利:
早产儿起始剂量每次0.01mg/kg,每8~12小时1次。≤7天的足月儿,起始剂量每次0.01mg/kg,每8~12小时1次;>7天者,起始剂量每次0.05~0.1mg/kg,每8~24小时1次,最大剂量每次0.5mg/kg,每6~24小时1次。
2)依那普利:
起始剂量 0.04~0.1mg/(kg•d),每天1次,最大量可增至0.5mg/(kg•d)。
(2)利尿剂:
利尿剂通过促进尿钠排泄而降低前负荷,并可缓解肺水肿及外周性水肿等容量超负荷的症状。可用于治疗C期或D期心力衰竭患儿。
1)袢利尿剂:
袢利尿剂可抑制Henle袢升支粗段对钠和氯的重吸收,最常采用呋塞米,剂量每次1mg/kg,静脉或口服给予,一天2~3次。袢利尿剂的副作用包括:电解质紊乱(低钠血症、低氯血症和低钾血症)、代谢性碱中毒和肾功能不全。长期应用袢利尿剂治疗可导致肾钙沉着症和耳毒性(通常发生于大剂量静脉给药时)。
2)噻嗪类利尿剂:
噻嗪类利尿剂可抑制肾远曲小管对钠和氯离子的重吸收,一般作为二线药物使用,常与袢利尿剂合用。常用的噻嗪类利尿剂为氯噻嗪、氢氯噻嗪及美托拉宗,目前已较少应用。
3)醛固酮拮抗剂:
醛固酮拮抗剂可减弱肾集合管的保钠排钾作用。常用螺内酯,每天3mg/kg,分2~3次口服。由于有保钾利尿作用,所以其特别适合与袢利尿剂和噻嗪类利尿剂联用。副作用包括高钾血症。
(3)洋地黄类:
具有正性肌力作用,由抑制Na+/K+-ATP酶活性以及提高胞内Ca2+浓度来介导;负变时作用,能延缓心房传导;以及迷走神经紧张作用,可减少心力衰竭时交感神经系统激活所介导的症状和体征。不推荐无症状心室功能障碍患儿使用洋地黄类药物,常用于治疗C期心力衰竭患儿,特别是利尿剂和ACEI等其他药物治疗后症状仍持续者,可改善生理状况和缓解症状。
1)地高辛:
地高辛的有效剂量安全窗较窄,个体耐受性不同,使用时应监测地高辛药物浓度和治疗效果。低剂量用药时(谷浓度为0.5~0.9ng/ml)即可获益,且潜在不良反应心律失常罕见。地高辛口服剂量:早产儿饱和量24小时20μg/kg,维持量24小时5μg/kg,分2次口服;足月儿饱和量24小时30μg/kg,维持量24小时8μg/kg,分2次口服;若静脉用药,剂量为口服剂量的3/4。
2)西地兰:
主要用于急、慢性心力衰竭、心房颤动和阵发性室上性心动过速。西地兰的洋地黄化量为0.02mg/kg,首剂给予洋地黄化量的1/2~1/3,其余分2~3次间隔6~8小时给予。
(4)β受体拮抗剂:
β受体拮抗剂可抵消心肌长期交感神经激活引起的适应不良作用。通常在利尿剂、地高辛和ACEI治疗方案基础上加用β受体拮抗剂治疗,如卡维地洛或美托洛尔,有频繁心室异位起搏的患者可首选美托洛尔。β受体拮抗剂用于经其他心力衰竭药物治疗病情稳定、具有收缩功能障碍的C期心力衰竭,也可能在B期心力衰竭的单纯ACEI或ARB治疗基础上加用这类药物。失代偿性心力衰竭患者应停用β受体拮抗剂。
1)卡维地洛:
开始采用低剂量,约为最终目标剂量的1/8,通常为 1次0.05mg/kg,每日2次,口服,每2周增加1次剂量(即剂量翻倍),从而尽量减少副作用。一般来说,每次增量的首剂在诊室服用,观察无不良反应可按计划继续此剂量,逐渐增加到最大剂量0.4mg/kg,每日2次。副作用包括疲劳、低血压、心动过缓、支气管痉挛及低血糖,这些可能会影响剂量增加。
2)美托洛尔:
初始剂量为每次0.1mg/kg,每日2次,口服给药,并按需缓慢增量,通常每2周增量1次,最多1mg/(kg•d)。副作用与卡维地洛类似。
(5)肺血管扩张剂:
肺血管扩张剂用于肺动脉高压所致右心衰竭患儿。
(6)正性肌力药:
正性肌力药用于低心排血量时,如心力衰竭急性加重时用来改善心排血量,以及用于稳定等待心脏移植患者的病情。这些药物的作用机制是保持较高的细胞内cAMP水平,其中儿茶酚胺类(如多巴胺、多巴酚丁胺)可通过增加cAMP的生成,磷酸二酯酶Ⅲ抑制剂(如米力农)则通过减少cAMP降解来实现。常用正性肌力药物的作用特征见表4。
表4常用正性肌力药物的作用特征
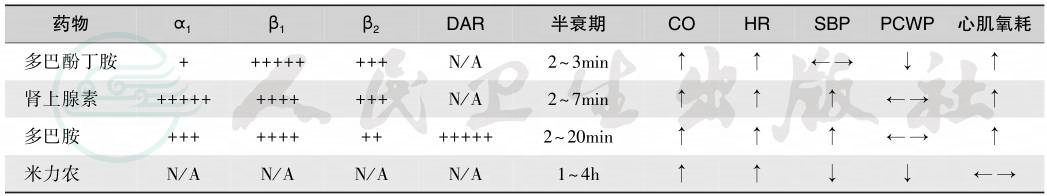
注:DAR.多巴胺受体;CO.心排血量;HR.心率;SBP.收缩压;PCWP.肺毛细血管楔压。
引自:实用新生儿重症医学.第1版.ISBN:978-7-117-36408-9.主编:
1)多巴胺(dopamine):
是失代偿性心力衰竭优选的药物,通常联合静脉用米力农。小剂量2~5μg/(kg•min)主要作用于多巴胺受体,对心脏β1受体和外周血管α1受体也有轻度作用,对血流动力学的影响因人而异;中等剂量 5~10μg/(kg•min)主要作用于心脏β1受体,对外周血管α1受体有轻度作用,可增加心排血量和外周血管阻力,提高平均动脉压;大剂量>10μg/(kg•min)主要作用于外周血管 α1受体,增加外周血管阻力,同时也作用于心脏β1受体增加心排血量。 当>20μg/(kg•min)时,由于心脏 β1受体作用易诱发快速性心律失常。
2)多巴酚丁胺(dobutamine):
强力作用于心脏β1受体增加心排血量减少左心室充盈,对外周血管α1受体作用较弱,且有中等强度的β2扩血管作用,整体表现为反射性扩张血管,对血压无明显影响。新生儿剂量范围为 2~20μg/(kg•min),静脉滴注,根据临床反应调整用量。
3)肾上腺素(adrenalin):
低剂量肾上腺素持续静脉滴注用于难治性低血压和/或终末器官灌注不良时。强力作用于心脏β1受体,对外周血管α1和β2受体也有中等强度作用。可增加心肌收缩力和心排血量,对外周血管阻力的作用有剂量依赖性。小剂量时β2受体占主导,可降低外周阻力。大剂量时α1占主导,增加外周阻力。新生儿初始剂量0.05~0.2μg/(kg•min),根据平均动脉压反应可上调至0.5~1μg/(kg•min)。
4)去甲肾上腺素(norepinephrine):
是各种原因休克伴低血压的首选血管收缩剂。强力作用于外周血管α1受体,中等强度作用于心脏β1受体。提高平均动脉压作用强于多巴胺,且对心率影响小。新生儿起始剂量 0.05~0.1μg/(kg•min),根据临床反应可上调至 2μg/(kg•min)。
5)异丙肾上腺素(isoprenaline):
主要用于心动过缓导致的低血压。强力作用于心脏β1受体和外周血管β2受体。与多巴酚丁胺不同的是,具有明显的增加心率和心肌收缩力作用,提高心排血量,同时有扩张外周血管的作用,并降低平均动脉压。新生儿剂量范围 0.05~2μg/(kg•min),静脉滴注,根据临床反应调整用量。
6)米力农(milrinone):
米力农为大多数医疗机构中,用于失代偿性心力衰竭首选的磷酸二酯酶Ⅲ抑制剂,静脉注射。米力农可增加心肌收缩性,并降低后负荷,而不会显著增加心肌耗氧量。为了避免发生低血压,米力农初始输注速率为 0.25μg/(kg•min),前期无须快速推注,随后按需逐渐缓慢增加剂量,最大剂量为 1μg/(kg•min)。
(7)奈西立肽:
不推荐急性心力衰竭时常规应用奈西立肽。奈西立肽是一种重组B型利钠肽,能通过促进排尿、尿钠排泄以及动静脉扩张来降低心脏前、后负荷,从而PCWP,改善心排血量,对心肌无直接正性肌力作用。在副作用方面,奈西立肽有增加低血压风险。用法:先给负荷量1.5μg/kg,缓慢静脉注射,继之 0.007 5~0.015μg/(kg•min),静脉滴注;也可不用负荷量而直接静脉滴注,疗程一般3天。
4.心脏再同步化治疗
最佳药物治疗疗效不充分的部分C期和D期心力衰竭患儿可选择心脏再同步治疗(cardiac resynchronization therapy,CRT),尤其是伴射血分数(ejection fraction,EF)降低(即 EF<35%)和心电图显示有左束支传导阻滞的患者。由于先天性心脏病的解剖基础复杂、多次心脏手术引起瘢痕形成,以及右束支传导阻滞和右心室衰竭比例比成人高,所以很难评估CRT对新生儿科/儿科人群的疗效。目前尚无随机对照试验评估CRT在心力衰竭儿童中的应用。
5.ECMO
ECMO是全心肺旁路装置,可用于即将发生或已经发生的心搏骤停,如心脏手术后休克和急性心肌炎。ECMO可提供数日至数周的充分心肺支持。一项纳入3 416例新生儿及4 181例儿科心脏病性ECMO病例的多中心注册研究显示,出院生存率分别为38%和45%。如果心肌未恢复或预期在2~3周内不能恢复,则ECMO可用作更耐用心室辅助装置(ventricular assist device,VAD)的过渡,随后进行心脏移植。
6.心脏移植
心脏移植推荐用于内科难治性终末期心力衰竭(D期)。伴严重活动受限、明显生长障碍、难治性心律失常或限制型心肌病的C期HF患者,也可考虑心脏移植。此类患儿应考虑早期转至儿科移植中心,优化内科治疗和列入心脏移植等待名单的时机。是否行心脏移植,取决于内科治疗的预期生存、生活质量、其他治疗选择,以及移植后估计生存期。













