英文名称 :tumor-like inflammatory demyelinating diseases
中文别名 :瘤块状脱髓鞘病变;炎性脱髓鞘假瘤
瘤样炎性脱髓鞘疾病(tumor-like inflammatory demyelinating diseases,TIDD)又称为瘤块状脱髓鞘病变(tumefactive demyelinating lesions,TDLs)或炎性脱髓鞘假瘤(inflammatory demyelinating pseudotumor),是中枢神经系统的一种特殊类型的炎性脱髓鞘疾病,通常以头痛、言语不清、肢体力弱等起病多见。
1993年,Kepes等报道了31例经病理证实的脑内TIDD,当时推测是介于MS与感染或疫苗接种后播散性脑脊髓炎(disseminated encephalomyelitis,DEM)之间的一种独立的疾病。近年来,国内外大量临床研究发现,大多数TIDD患者是单相病程,少数患者可以向复发-缓解型MS(RRMS)转化,极少数可再次以TIDD形式复发,还有极少数可与视神经脊髓炎谱系疾病(NMOSD)重叠。
TIDD的发病率和患病率等流行病学资料缺如。男女患者的比例基本相当,各年龄段均可以发病,但以中青年较多。国内报道的平均年龄约为35岁,国外有报道发病年龄稍大,如Kim报道15例TIDD平均年龄为42岁。
1.病因
目前尚不清楚。早期曾认为,TIDD是MS与ADEM 的中间类型(Kepes et al,1993);Poser等(2004)提出,TIDD是 MS的一种变异型。TIDD多为单时相病程,少数呈复发-缓解,可转变为MS或NMOSD。
2.病理
TIDD病变以影响白质为主,可累及皮质和皮质下白质。TIDD的病理学特征是:
(1)HE和髓鞘染色显示,病变区域组织结构破坏,髓鞘脱失。
(2)轴索染色和免疫组织化学标记神经丝蛋白可显示,髓鞘脱失区域轴索相对保留。
(3)HE和CD68染色可显示,病变区域内有大量吞噬髓鞘碎片的格子细胞;急性期固蓝(Luxol fast blue)髓鞘染色可见胞质内充满蓝染的髓鞘碎片。
(4)病变及周围区域组织内可见血管周围“套袖样”淋巴细胞浸润(图1),以T淋巴细胞为主。
(5)HE和GFAP染色,病变组织内不同程度反应性增生的星形胶质细胞。
(6)多数可见散在分布的Creutzfeuldt细胞(怪异的肥胖型星形细胞)(图2),其特征为:胞质丰富、淡染,核膜消失,染色质变为不规则染色体形式,称为“流产型核分裂”,易误诊为胶质瘤,该细胞对TIDD诊断虽不具有特异性,但结合其他改变高度提示该诊断。
(7)TIDD病理学改变也会随病程而发生相应变化(孙辰婧等,2015)。病程急性期(起病≤3周)病理表现符合急性活动期改变:病灶处于激烈的炎症反应中,髓鞘大量脱失,轴索也可见不同程度肿胀损伤。亚急性期(起病4~6周)病理符合慢性活动期改变:病灶边缘清晰,轴索相对保留,含有髓鞘降解物的巨噬细胞呈放射状聚集在病灶边缘。病程慢性期(起病≥7周)病理以阴燃性活动期或非活动期表现为主:显示病灶髓鞘部分再生。病灶中心为非活动性的,炎细胞数较少,周围散在巨噬细胞和小胶质细胞,但这些细胞内几乎不含有髓鞘降解物。非活动期主要表现为病灶中髓鞘脱失区逐渐修复。
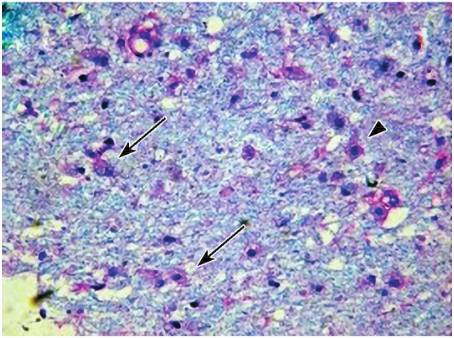
图1TIDD的白质脱髓鞘病变和炎细胞浸润,吞噬细胞内含有大量脱髓鞘的碎片,泡沫样吞噬细胞(箭头)和星形胶质细胞(三角)(HE+LFB,×200)
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
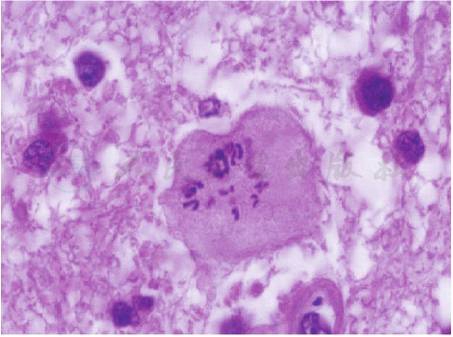
图2显示 TIDD的Creutzfeldt细胞(HE,×400)
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
1.影像学检查
TIDD以白质受累为主,还可累及皮质和皮质下白质。病灶可为单发或多发,病变双侧受累较为常见,极少数可同时累及脊髓。累及额叶最为多见,其次为颞叶、顶叶,基底节区与胼胝体及半卵圆中心受累也较常见(戚晓昆等,2010)。
TIDD的影像学形态可见:①弥漫浸润样病灶(diffuse infiltrating lesions)较多见,病灶较大,T2WI显示病变边界较清,可呈不均匀强化,犹如弥漫浸润样生长;②环样病灶(ring-like lesions)病灶中等大小,形态为类圆形,可呈现开环形强化(多见)和闭环强化(少见);③囊样病灶(megacystic lesion)较少见,病灶较小,T1WI、T2WI均显示病灶呈高信号,边界很清楚,可呈环形强化(图3)。
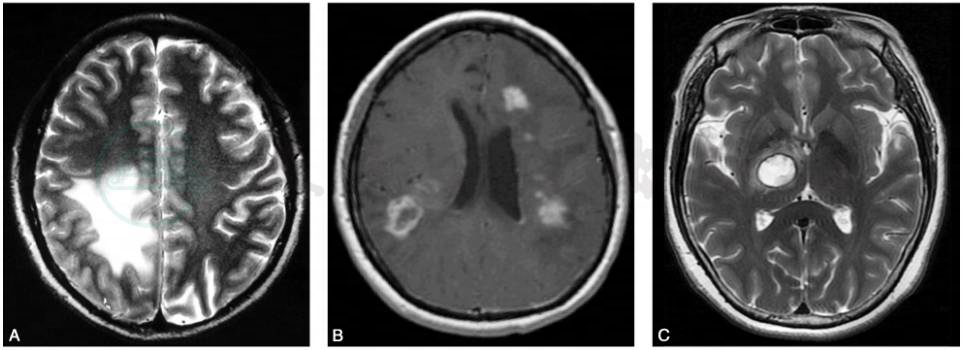
图3三种不同形态学类型的TIDD
A.弥漫浸润样病灶;B.环样病灶;C.囊样病灶
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
(1)脑CT检查:
TIDD在CT平扫时绝大多数为边界较清楚的低密度影(图4A),个别可为等密度(图4B),CT强化多不显著。脑CT显示高密度病灶或周围有高密度环基本可除外TIDD诊断(Kim et al,2009)。
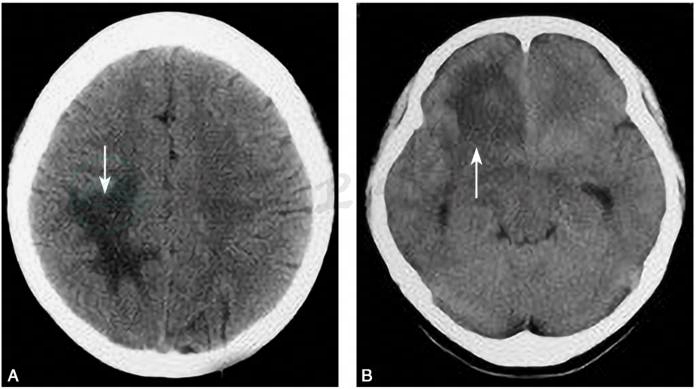
图4TIDD病灶密度
A.低密度病灶(箭头);B.等密度病灶(箭头)
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
(2)脑 MRI检查
1)脑MRI平扫:
TIDD在脑MRI显示的病灶常比CT的范围要大,水肿也更明显,T1WI、T2WI多为高信号,其中,70%~100%的患者T2WI为高信号,边界较清楚,部分伴T2低信号边缘(图5A)。TIDD多有占位效应(图6A),但其程度多不及脑肿瘤,病灶周围多可见水肿带。急性或亚急性期,以细胞源性水肿为主,弥散加权成像(diffusion weighted imaging,DWI)多为高信号(图5C、D),经激素规范治疗后,病灶多在数周内逐渐缩小或消散。
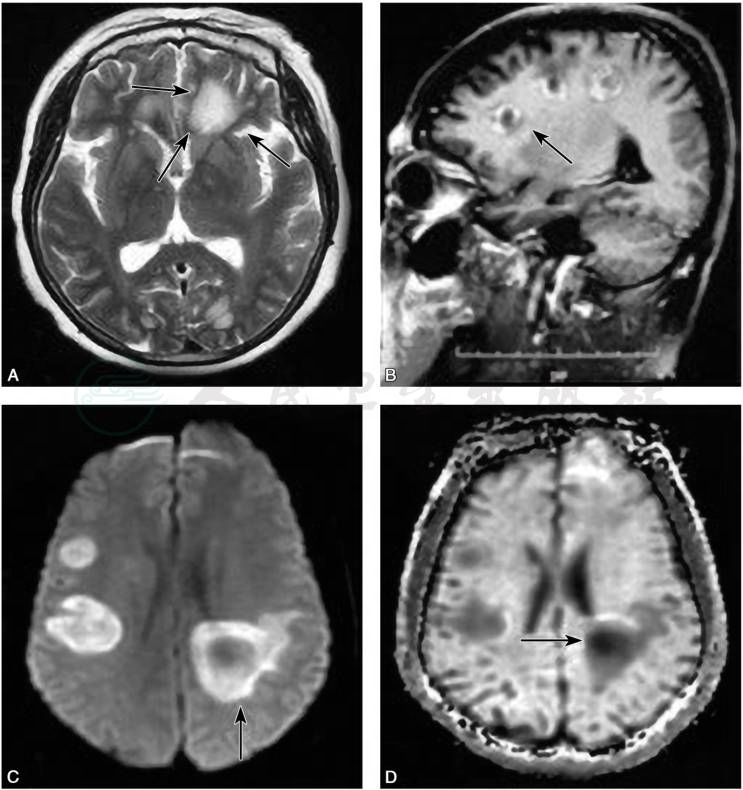
图5TIDD“云片状”病灶及环形强化
A.病灶周边低信号边缘(箭头所指);B.病灶呈“C”形强化(箭头所指)。双侧侧脑室旁病灶弥散受限,表现为C.DWI高信号;D.ADC低信号
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
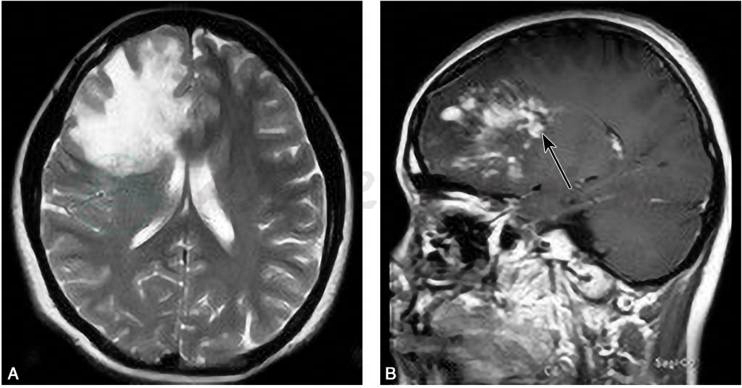
图6TIDD病灶占位效应
A.右侧额叶皮质下团块状长T2异常信号,占位效应明显,病灶周围指压状水肿显著;B.矢状位T1WI增强示:右侧病灶呈多发线状以及结节样强化,病灶内扩张的静脉血管呈长轴垂直于侧脑室的“梳齿状”强化(箭头所指)
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
2)MRI增强:
因血脑屏障的破坏,TIDD急性期与亚急性期在钆喷酸葡胺(Gd-DTPA)增强时,表现为结节样、开环样、闭环样、火焰状等不同形式的强化。其中,“开环样”强化(也有称“C”形强化,图5B)最具特征,即断“C”或开环形强化。另外,部分TIDD MRI增强扫描可见垂直于脑室的扩张的静脉影,呈“梳齿样”结构(刘建国等,2014)(图6B),急性期与亚急性期多见,该特点对于TIDD的诊断具有一定特异性,脑肿瘤无此特点。
3)磁共振波谱(magnetic resonance spectroscopy,MRS):
可反映病变组织的代谢情况,对TIDD与脑胶质瘤与PCNSL的鉴别具有一定的临床价值。TIDD的MRS主要表现为胆碱(Cho)峰升高,N-乙酰天门冬氨酸(NAA)峰降低,多数还伴有一定程度乳酸(Lac)峰升高(图7)。
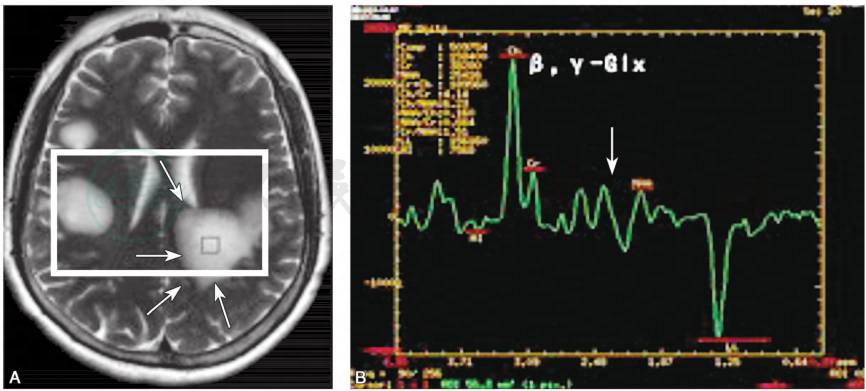
图7TIDD“云片状”病灶
A.双侧额叶皮质下云片状长T2异常信号,边缘呈短T2信号;B.1H-MRS显示,定位区域为左侧顶叶角回侧脑室旁病灶区(图3-12-24A),Cho峰显著升高,Cho/Cr=2.93,NAA 峰轻度降低,NAA/Cr=0.62,Lac峰显著升高(TE=144),β,γ-Glx峰升高
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
4)灌注加权成像(perfusion weighted imaging,PWI):
可用来评价病灶内的血流灌注情况,主要有两种方法:①需静脉团注外源性对比剂(如Gd-DTPA)的动态磁敏感对比增强(dynamic susceptibility contrast-enhanced,DSC)方法;②完全无创的动脉自旋标记(arterial spin labeling,ASL)方法。胶质瘤新生血管多,往往呈高灌注,而TIDD一般不出现高灌注表现(图8)。
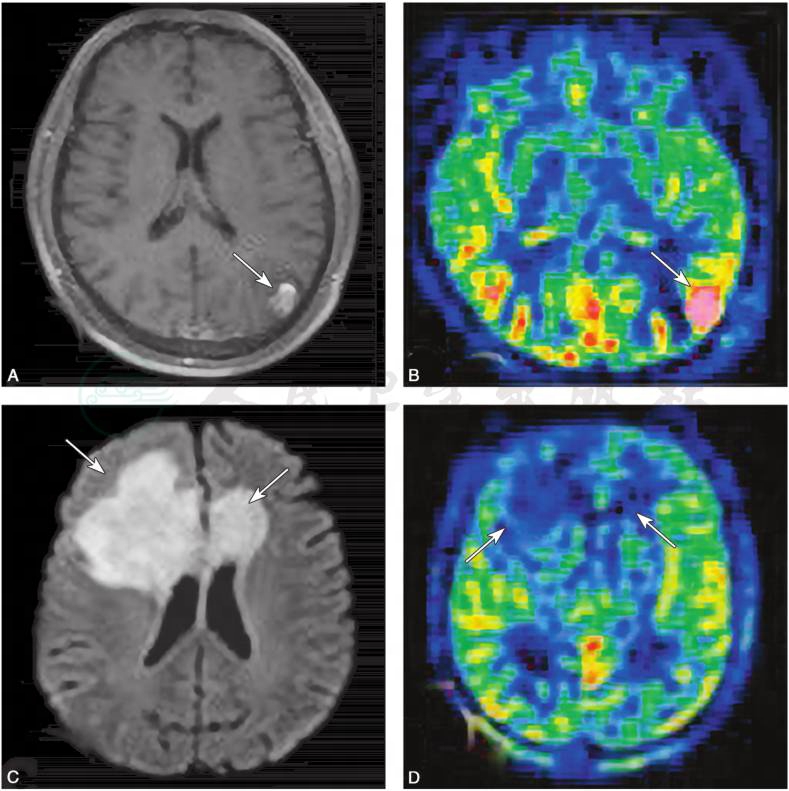
图8灌注加权成像
病例1,女性,50岁,主因“癫痫1天”入院,胶质母细胞瘤,轴位T1WI增强示:左侧顶枕交界皮质可见结节样强化病灶(A),在 ASL像呈高灌注(B);病例2,男性,44岁,主因“意识障碍3天”入院,急性起病,TIDD,轴位DWI(C)示:双侧额叶皮质下及侧脑室旁白质可见大片融合蝶形病灶,累及胼胝体膝部,ASL显示双侧病灶处灌注无明显增高(D)
引自:神经病学:全2册.第3版.ISBN:978-7-117-31406-0.主编:
2.脑脊液检查
颅压多数正常,少数轻度增高,多数CSF蛋白水平正常,少数轻、中度增高,细胞数多为正常。个别患者CSF的寡克隆带(OB)呈弱阳性或阳性。部分患者的髓鞘碱性蛋白(myelin basic protein,MBP)或IgG合成率有不同程度增高。动态观察若OB持续呈阳性,要注意其向MS转化的可能。
血清学免疫相关检查:极少数TIDD与NMOSD重叠,其血清水通道蛋白4(aquaporin4,AQP4)抗体阳性;伴有可提取核抗原(extractable nuclear antigen,ENA)部分抗体阳性者更易复发。
根据TIDD诊断标准中的诊断级别,分别推荐相应处置:①病理确诊与临床确诊的TIDD:可直接启动TIDD相关治疗;②临床可能的TIDD:根据受累部位,充分评估手术风险后,推荐组织活检,若病理学表现缺乏特异性,无法确诊,分析原因后可行再次活检,根据病理结果进行相应诊疗决策;③对组织活检仍无法确诊且暂无再次活检计划的,或因各种原因无法行活检术的,除外禁忌后,均推荐激素试验性治疗(Puri et al,2005),治疗后行增强MRI扫描进行影像学评估,对于增强完全消失或大部分消退的可基本除外胶质瘤的可能,应进行密切随访,若于半年内复发或病情再次加重的,应注意淋巴瘤的可能性。
TIDD多为单时相病程,少数可复发。治疗方面主要可分:急性期治疗、缓解期治疗(疾病修正治疗)、神经营养治疗、对症治疗、康复治疗及生活指导。因绝大多数TIDD为单时相病程,复发较少,且病灶体积相对较大,故激素的治疗方法则既不同于NMOSD的“小剂量长期维持”,也不同于 MS的“短疗程”,而是有其自身特点(戚晓昆,2012)。对于TIDD复发的患者,需首先检测血清AQP4抗体,结果阳性高度提示患者存在向NMOSD方向转变的可能、且复发率可能较高、神经功能残障相对显著,急性期和/或缓解期治疗均可参考2016年《中国视神经脊髓炎谱系疾病诊断与治疗指南》进行规范治疗;若血清AQP4抗体阴性,则仍按TIDD相关推荐治疗建议如下:
1.急性期治疗
减轻急性期临床症状、缩短病程、改善神经功能缺损程度,使颅内占位病灶体积缩小至消退,达到影像学缓解或治愈,预防并发症。
(1)激素治疗:
可作为首选,TIDD对激素治疗多数较敏感,但因TIDD的病灶体积相对较大,病情多较MS为重,故其激素冲击治疗之后的阶梯减量往往应较MS为慢,以免病情反复或加重。对于在激素减量过程中,若出现新发症状或症状反弹,可再次激素冲击治疗或给予1个疗程静脉大剂量免疫球蛋白治疗(具体方法见下文)。
(2)激素联合免疫抑制剂:
适用于激素冲击效果不佳者,主要包括硫唑嘌呤、环磷酰胺、吗替麦考酚酯、甲氨蝶呤、他克莫司等,尚缺乏TIDD相关的循证医学证据,具体使用方法及注意事项可参考2016年《中国视神经脊髓炎谱系疾病诊断与治疗指南》。
(3)静脉注射大剂量免疫球蛋白(intravenous immunoglobulin,IVIG):
尚缺乏有效证据,适用于血清AQP4抗体阳性的患者,也可用于不适合激素治疗或激素治疗无效的,且又不适合使用免疫抑制剂的特殊人群,如:妊娠或哺乳期妇女、儿童。推荐用法:免疫球蛋白用量为0.4g/(kg•d),静脉滴注,连用5天为1个疗程。
2.复发型TIDD缓解期的治疗
控制疾病进展,预防复发。对于符合MS时间与空间多发特点的TIDD可按MS进行免疫抑制剂或疾病缓和治疗(DMT)(多发性硬化诊断和治疗中国专家共识,2014),对于不符合MS及NMOSD诊断的,亦可予免疫抑制剂治疗,尚缺乏循证医学证据。
3.免疫抑制治疗
对于不符合MS与NMOSD的TIDD可作为一线药物进行选择使用,常用的有硫唑嘌呤、环磷酰胺、吗替麦考酚酯等,具体使用方法及注意事项,可参考2016年《中国视神经脊髓炎谱系疾病诊断与治疗指南》。
4.神经修复治疗
推荐使用多种B族维生素,如维生素B1、甲钴胺、复合维生素B、叶酸等,常规剂量即可。另外,还可使用神经生长因子、单唾液酸四己糖神经节苷脂钠、胞磷胆碱等。
5.康复治疗及生活指导
TIDD在急性期后往往遗留一些功能障碍,因此,后期康复锻炼较为重要。应早期在康复师的指导下,对伴有肢体、语言、吞咽等功能障碍的患者,进行相应功能康复训练。













