英文名称 :complete transposition of the great arteries
完全性大动脉错位(complete transposition of the great arteries,TGA)是婴儿期最常见的发绀型先天性心脏畸形之一,占先天性心脏病发病率的7%~9%。大动脉错位是指心房与心室连接一致,而大动脉与心室连接不一致,主动脉发自右心室,肺动脉发自左心室。主动脉内接受体循环的静脉血,而肺动脉接受的是肺静脉的动脉血,因而形成了两个隔绝的循环系统。
主动脉发自解剖右心室,肺动脉发自解剖左心室。其房室连接一致,即解剖右心房连接解剖右心室,解剖左心房连接左心室。绝大部分心脏位置正常,右位心少见。
根据有无合并室间隔缺损分为室间隔完整型TGA和室间隔缺损型TGA。室隔完整型TGA,常伴卵圆孔或动脉导管未闭。生后数周随着肺血管阻力下降,左心室压力降低,而右室压力相对升高,室间隔可凸向左室侧,严重时可导致左室流出道梗阻。随着病程的进展,左心室室壁会逐渐变薄,1个月后出现不同程度退化。
约50%的TGA伴有室间隔缺损,称为室间隔缺损型的TGA。室间隔缺损多位于膜周和漏斗部,合并其他心脏畸形比室间隔完整型TGA更多见,包括肺动脉狭窄、肺动脉闭锁、房室间隔缺损、主动脉弓缩窄或主动脉弓离断等。
5%~10%TGA患者中存在冠状动脉异常开口和走行,包括左冠状动脉回旋支起源于右冠状动脉,单根冠状动脉,肌壁内冠状动脉等。目前最常用的命名方法是LEIDEN分型(图1)。
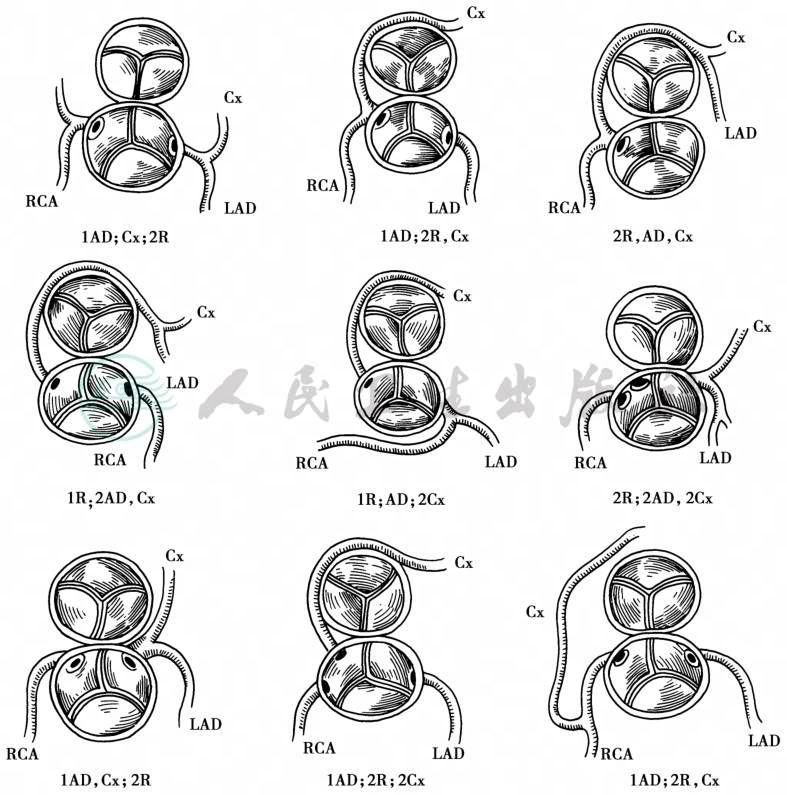
图1 LEIDEN分型
Sinus 1:位于观察者右侧 Sinus 2:位于观察者左侧RCA:右冠状动脉 LAD:左冠状动脉前降支 Cx:回旋支
在胚胎发育第5~7周,正常的发育过程中,左侧的肺动脉瓣下圆锥继续发育,使肺动脉瓣向左上生长连接右室流出道,右侧主动脉瓣下圆锥渐渐消失,使主动脉瓣向后与左心室连接。而大动脉错位与正常相反,主动脉下圆锥持续存在,而肺动脉下圆锥隔吸收并与二尖瓣间纤维连续,结果导致主动脉瓣位于肺动脉瓣前方,连接右心室,肺动脉连接左心室。而两组半月瓣未经正常的变换分别与远端大血管连接,这些演变最终形成大动脉错位。
大动脉错位的特征是两个独立的平行循环,使回流到右室的体静脉血泵入体循环,回流到左室的肺静脉血泵到肺循环。如果两个循环之间互不沟通,患儿将不能存活。因此多数伴有动脉导管、房间隔缺损或室间隔缺损。
室间隔完整型TGA只能依靠动脉导管或者房间隔缺损进行血流交通,仅能满足氧合的低限。随着出生后肺阻力的下降,左心室压力也相应下降。生后4~6个月,左心室将不能适应急剧增加的体循环压力负荷。同时肺阻力下降也引起肺血流增加,造成左心室扩张,最终导致左心衰竭。
室间隔缺损型TGA,根据室缺的大小以及有无合并肺动脉流出道狭窄,存在不同的表现。小型室间隔缺损的TGA类似于室间隔完整型,较早存在发绀。大型的室间隔缺损混合多,临床发绀轻,如果不伴有肺动脉流出道的狭窄,随着肺阻力的下降,引起严重的肺充血,导致肺动脉高压,很快引起不可逆的肺血管病变,在生后6个月时就可能失去手术机会。如果伴有肺动脉流出道狭窄,临床上则会较早出现发绀,发绀的程度与肺动脉流出道狭窄的轻重有关,但在一定程度上限制了肺血流。一部分患者处于生理平衡,延迟了心功能衰竭的发生。
不论是否存在室间隔缺损,TGA患者均可发生肺血管病变,但室间隔缺损型TGA要早于室间隔完整型TGA,这可能与氧饱和度、二氧化碳浓度以及肺动脉pH变异有关。
听诊可有柔和的收缩期杂音,第二心音响亮单一。肝脏增大。胸片示肺血管纹影增多增粗,心影呈斜置蛋形,右心室扩大。因肺动脉与主动脉前后重叠,上纵隔变窄。如伴肺动脉流出道狭窄,肺血管纹影减少。心电图示窦性节律,电轴右偏,右心室肥大。ST段和T波可出现缺血性表现。
超声心动图可明确诊断。肺动脉主干出自左心室,并发出左右肺动脉分支,升主动脉出自右心室。通过超声心动图可以明确主动脉和肺动脉主干之间的位置关系和瓣膜的大小以及功能;明确左、右冠状动脉开口的位置和主干的走行;明确体-肺循环交通(ASD、VSD或PDA)的大小位置和分流量;明确左心室后壁的心肌厚度以及心肌质量的测定,以判断可否做大动脉转换术;明确有无合并其他心脏畸形,如主动脉弓离断、主动脉弓缩窄、完全性肺静脉异位引流等。
心导管造影可进一步明确冠状动脉的起源和行径,两大动脉的位置关系,测定左心室压力了解左室功能,明确有无合并肺动脉流出道狭窄和主动脉弓病变。目前作为检查手段已经很少应用,较多地应用在房间隔球囊撕裂术中。
1.内科治疗
诊断明确,存在临床症状,禁止吸氧,应用前列腺素E1[保达欣5~50ng/(kg·min)]保持动脉导管开放,同时应用多巴胺或多巴酚丁胺改善心功能,纠正酸中毒、低血糖,为手术创造条件。
2.手术治疗
(1)姑息性手术
当患儿存在严重青紫,代谢性酸中毒,全身基础状况差,或者伴有严重肺动脉发育不良等而无法行一期根治手术时,需要先接受姑息性手术。
1)心导管球囊撕裂房隔术(Rashkind)(图2)
主要应用于室间隔完整型的TGA。由于心房交通小,生后可出现严重发绀,低氧血症,酸中毒和心力衰竭。术后能改善低氧,为施行大动脉调转术作准备。

图2 球囊囊管撕裂房隔术
(1)导管从右心房进入左心房;(2)气囊充气后拉回右房,扩大房间隔缺损
2)房间隔部分切除(Blalock-Hanlon)
目前很少采用,以往主要应用于心导管球囊撕裂房隔术后低氧和心力衰竭改善不明显的患者。
3)体-肺动脉分流术
主要采用改良Blalock-Taussig分流术,应用于不具备早期根治条件同时伴有肺动脉流出道狭窄的TGA。如心房内分流少,同时行房间隔扩大术,以改善低氧血症。
4)肺动脉环缩术
巨大室间隔缺损或多发性室间隔缺损,早期先行肺动脉环缩,防止肺动脉高压。或者左心室已退化,肺动脉环缩可增加后负荷,锻炼左室功能。
(2)完全纠治性手术方法
1)心房内调转术
即Mustard或Senning术,通过心房内板障使体静脉血回流入左心室至肺动脉,氧合血回流入右心室至主动脉,供全身循环,达到血流动力学的纠治。早期死亡率低(<5%),但远期并发症多,包括心律失常,板障漏,腔静脉、肺静脉回流梗阻,解剖右心室不能长期承受体循环压力,导致右心衰竭,瓣膜反流等,目前临床上已少用。
Mustard手术步骤:(图3)
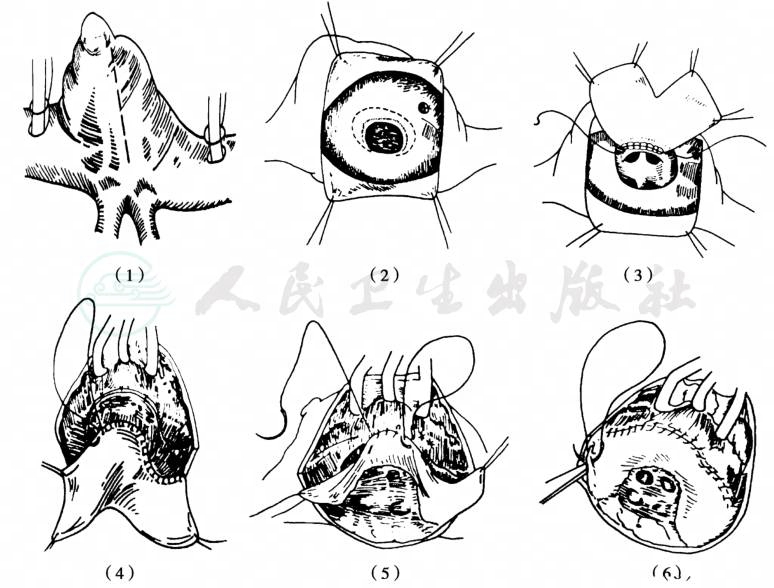
图3 Mustard术
(1)右心房斜切口;(2)切除部分房间隔组织;(3)裤形心包边与左肺静脉开口左侧壁缝合;(4)~(6)建立心内板障,最终将腔静脉血通过房间隔缺损引入左心室至肺动脉,肺静脉血引入右心室至主动脉
Senning手术步骤(图4)
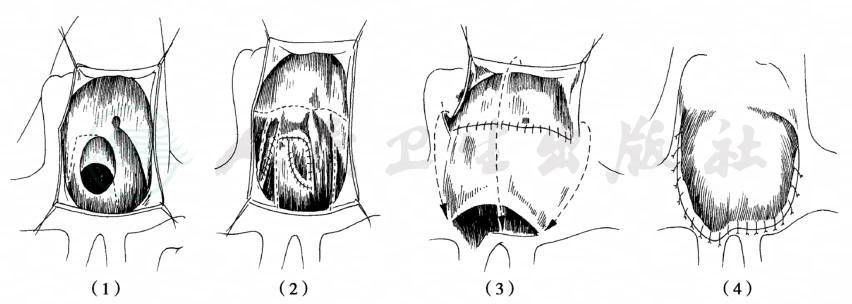
图4 Senning术
(1)近三尖瓣处切开房间隔;(2)缝合房间隔组织至左肺静脉开口前缘,使肺、体静脉分隔;(3)缝合右心房切口后缘至残留房间隔组织,使腔静脉血流入左心室;(4)右心房前缘沿着腔静脉上下端缝合至左心房切口侧面,使肺静脉血流入右心室
2)Rastelli术(图5)
应用于室间隔缺损型的TGA伴有肺动脉流出道狭窄。建立室间隔缺损与主动脉之间的心内隧道,使左心室血流入主动脉,采用心外管道建立右心室至肺动脉的连接,使右心室血流入肺动脉。纠治手术年龄在3~4岁以上,术后并发症包括心外管道梗阻、左室流出道梗阻和心律失常等。由于心外人工管道不能随着年龄的增长而生长,需多次手术置换。同时,心内隧道致左心室流出道梗阻的发生率较高。对室缺远离主动脉开口和室缺至主动脉开口之间有三尖瓣腱索或乳头肌阻挡,不易行Rastelli手术。
手术步骤:胸骨正中切口,建立体外循环。右心室切口,探查室间隔缺损位置、大小,确定室缺足够大,室缺至主动脉开口之间无多余心肌和三尖瓣组织阻挡,必要时可扩大室缺,采用补片或者1/3~1/2周径的人造血管补片建立室缺至主动脉瓣口的心内隧道。横断肺动脉,近心端连续缝合关闭。采用同种带瓣管道连接右心室切口至远心端肺动脉。
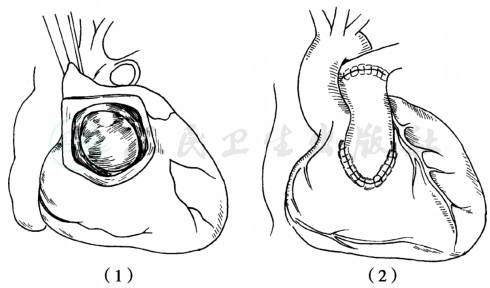
图5 Rastelli手术
(1)室间隔缺损至升主动脉开口间建立心内隧道;(2)同种带瓣管道连接右心室切口至肺动脉
3)大动脉调转术(Arterial Switch术)(图6)
进行主动脉和肺动脉的换位使得主动脉与左心室连接,肺动脉与右心室连接。室间隔完整型TGA最佳手术年龄在出生后2周内。如果超过1个月,左心室功能可能退化,需进一步行心脏超声和心导管检查评价左心室功能,以决定能否行一期大动脉调转术。如果室间隔位置居中或者测得左心室压力大于右心室压力的60%,可考虑行决定一期大动脉调转术。室间隔缺损型TGA的左心室压力能较长时间维持在体循环压力的2/3以上,因此纠治时间可相对晚,但对于不伴有肺动脉流出道狭窄的患者最好不要超过3个月。6个月后可能出现肺血管阻塞性病变,失去手术机会。
手术步骤:胸骨正中切口。上下腔静脉插管建立体外循环,在转流降温时,解剖游离并缝扎离断动脉导管,彻底游离升主动脉、肺动脉干和左右肺动脉。一般肛温降至32℃,主动脉根部注入心肌保护液。右心房切口,通过房间隔缺损或卵圆孔未闭放置左心引流,可先行室间隔缺损修补,然后行大动脉转换术。在升主动脉距瓣上1cm处横断,探查左右冠状动脉开口,沿冠状动脉开口1~2mm外缘剪下主动脉壁,并游离冠状动脉近端约5mm。此过程中要不断探测冠状动脉行径,勿损伤冠状动脉的各分支。肺动脉干位于左右肺动脉分叉处横断,检查肺动脉瓣,在肺动脉根部相应位置剪去直径约5mm的圆形肺动脉壁,将左右冠状动脉向后与肺动脉吻合,注意冠状动脉不能扭曲,保持通畅,缝合严密,避免补针。将左、右肺动脉提至主动脉前方,将主动脉阻断钳换至肺动脉前方再阻断,将升主动脉与肺动脉根部连续缝合,形成新的主动脉。采用自体心包片应用0.6%的戊二醛处理后修补原主动脉根部取冠状动脉后的缺损,最后与肺动脉干吻合形成新的肺动脉干。关闭房间隔缺损后松开主动脉阻断钳,冠状血管灌注充盈和心肌颜色转红。
大动脉调转术的生存率明显升高,术后并发症少见。早期死亡原因主要是冠状动脉功能不全,出血。远期并发症主要为右室流出道梗阻,新主动脉瓣反流和瓣上狭窄。
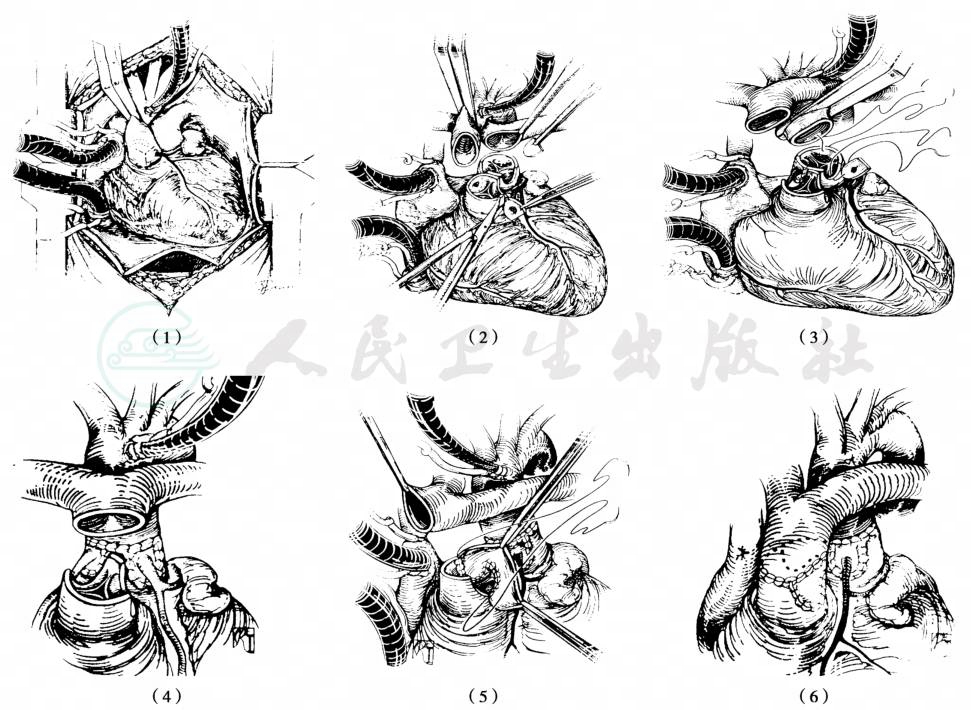
图6 大动脉调转术
(1)上下腔静脉插管(也可采用单根右心房插管);(2)横断主、肺动脉,取下带有主动脉壁的冠状动脉开口,适当游离;(3)将冠状动脉开口吻合于新主动脉根部,并将肺动脉远端提于主动脉前面;(4)吻合新主动脉;(5)取心包片重建新肺动脉;(6)完成后
4)Damus-Kaye-Stansel术
适合右室流出道或主动脉瓣下严重狭窄,因冠状动脉畸形或大血管侧-侧位或二次手术粘连冠状动脉移植困难的患者。该手术不需要移植冠状动脉,左心室到主动脉的血流是通过近心端肺动脉与升主动脉端-侧连接而成,带瓣管道连接右心室和远端肺动脉。缺点是主动脉瓣位于静态关闭的右心室,容易瓣膜漏和形成凝块,同时需定期更换心外管道。
5)大动脉移位术(Nikaidoh术)(图7)
采用连同自体冠状动脉一起进行主动脉换位以及双心室流出道重建。适用于室间隔缺损型的TGA并伴有严重的左室流出道狭窄。
手术步骤:从右心室取下自体主动脉瓣,勿损伤冠状动脉。横断狭窄的肺动脉,剪除狭窄的瓣叶,切开左心室流出道至室间隔缺损,将主动脉瓣移植至肺动脉瓣环处。然后取补片关闭室间隔缺损至主动脉瓣环处,形成左心室流出道。肺动脉远端与右心室切口吻合。
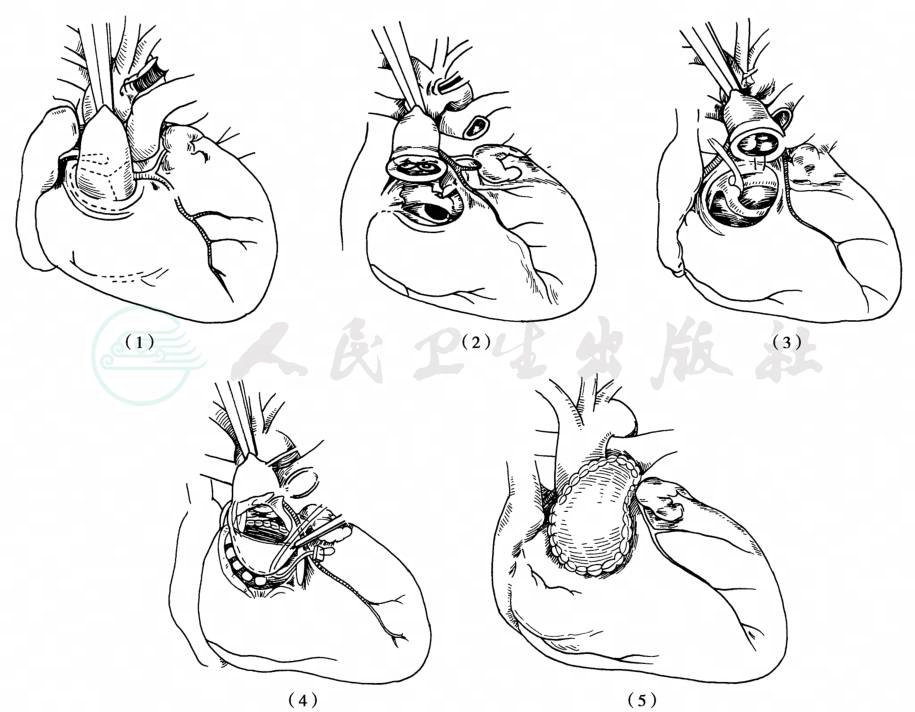
图7 大动脉移位术(Nikaidoh术)
(1)主动脉瓣叶下5mm处切开右室流出道,探查冠状动脉开口及走向;(2)小心游离冠状动脉,完整取下带着左右冠状动脉的主动脉瓣;(3)肺动脉干横断,剪开肺动脉瓣环至室间隔缺损贯通,将取下的主动脉瓣向后移植于原肺动脉瓣环;(4)补片关闭室间隔缺损至主动脉瓣环处,形成左心室流出道;(5)远端肺动脉后壁与右心室切口上缘直接缝合,前面采用心包补片覆盖,重建右室流出道
3.二期大动脉调转手术
适用4周龄到8周龄以上的患者。因为左心功能的退化不能行Ⅰ期手术纠治,先行肺动脉环缩术进行短暂的左室功能锻炼,如果左室功能达到完全纠治的要求并且患者耐受,则进行大动脉调转术。通常应用于左心室压力低于体循环压力的60%和心房内转换矫治术后体循环功能衰竭的患者。
手术步骤:一期手术胸骨正中切口下行右侧改良B-T分流和肺动脉环缩术,肺动脉环缩同时检测左心室压力,使左心室压力达到右心室压力的80%左右。如果房间交通小,术中行房间隔切除扩大术。术后机械辅助通气,心脏超声了解左心室功能和质量,7~10天后行二期大动脉调转术,术中需拆除肺动脉环缩和右侧B-T。













